


2. 重庆市妇幼保健院药剂科, 重庆 400010;
3. 吉首大学医学院药理教研室, 湖南 吉首 416000
2. Dept of Pharmacy, Chongqing Health Center for Women and Children, Chongqing 400010, China;
3. Dept of Pharmacology, Jishou University School of Medicine, Jishou Hunan 416000, China
结直肠癌(colorectal cancer,CRC)是世界第3大肿瘤,约占全球所有肿瘤的10%,男性的发病率高于女性,每年约有60万人死于该疾病[1, 2]。当前CRC主要的治疗手段包括外科手术、放射治疗以及辅助化疗(临床评估为Ⅲ、Ⅳ期或高风险的Ⅱ期CRC患者)[3]。在5年生存期方面,I期患者的生存率可达90%以上,而IV期患者则低至10%[3]。
现有的研究结果表明,癌症的发生与一系列基因结构和功能的改变相关(包括癌基因和抑癌基因的突变)[1]。本文的研究对象PTEN(phosphatase and tensin homolog),又被称为第10号染色体缺失的磷酸酶和张力蛋白同系物,是公认的恶性肿瘤抑制基因,它是细胞的重要调控因子,影响细胞的增殖、凋亡、迁移和代谢[3]。PTEN基因的表达变化能对人类肿瘤的发生和发展产生一定的影响[4],是结直肠癌的潜在治疗靶点。
美洛昔康(meloxicam,Mel)是一种环氧合酶-2(COX-2)选择性抑制剂,具有选择性高、副作用小和半衰期较长的优点[5]。本实验室前期研究结果提示,Mel可能具有一定的抗肿瘤作用[6]。为了进一步证实上述发现和揭示Mel的抗癌作用机制,本文以人结肠癌LoVo细胞和PTEN基因为研究对象,探索Mel对结直肠癌细胞增殖和迁移的影响及其相关机制。
本研究结果,将有助于诠释Mel对人结直肠癌LoVo细胞的作用和机制,可为Mel作为抗癌候选药物的进一步深度研发提供实验证据和相关理论基础。
1 材料与方法 1.1 试剂及细胞培养人结直肠癌LoVo细胞、293细胞(American Type Culture Collection,ATCC);Mel(西安昊轩生物科技有限公司);试验所用抗体(Santa Cruz Biotechnology公司);重组腺病毒(芝加哥大学何通川教授惠赠);采用DMEM培养基(高糖)培养细胞(含10%胎牛血清,100 kU ·L-1青霉素和0.1 g ·L-1链霉素),DMEM培养基、胎牛血清(Hyclone);细胞培养条件为5% CO2和37℃;逆转录试剂盒(日本TaKaRa公司)。其它常用生物化学和分子生物学试剂均为分析纯。
1.2 试验设计及分组试验分为对照组和试验组。试验组使用Mel处理细胞,Mel用DMSO溶解作为工作液,设20、40和80 μmol·L-1 3个浓度梯度试验组;对照组的处理是使用相同体积的DMSO。
1.3 集落形成试验将处于对数生长期的LoVo细胞接种于6孔板,每孔细胞数量约为1×104,接种4h后确认细胞贴壁,分别使用20、40和80 μmol·L-1Mel干预。加药24 h后弃去药液,用预冷(4℃)PBS洗3次以除去残留药液,使用0.25%的胰蛋白酶消化后收集细胞。将细胞吹散成为单细胞悬液,细胞计数后每组分为50、100、200个细胞铺于12孔板,每孔加入不含药物的完全培养基2 mL,置于5% CO2、37℃孵箱中孵育。孵育14 d后,弃培养基,用预冷(4℃)PBS洗3次后,每孔加入用PBS缓冲、用10%甲醛配制的饱和结晶紫溶液0.2 mL,室温下染色25 min后移去结晶紫染液,用PBS清洗3次以除去未与细胞结合结晶紫,将孔板于室温晾干后进行扫描。每组试验重复3次。
1.4 划痕试验将处于对数生长期的LoVo细胞接种于6孔板,每孔细胞数量约为1×105,于孵箱中培养至细胞长满,弃去完全培养基,用10 μL移液器枪头划出均匀的划痕,每孔划3条,用marker笔在6孔板底部标记定位,作为后续观察的定位点。划出均匀划痕后,用预冷(4℃)PBS洗去划痕时刮下的细胞,洗净后,每孔中加入无血清DMEM培养基2 ml,以试验设计浓度的Mel干预(0、20、40和80 μmol·L-1),加药处理0、6、24 h后,将6孔板置于倒置显微镜下(100倍)照相,以分析细胞迁移的现象。每组试验重复3次。
1.5 RT-PCR试验将处于对数生长期的LoVo细胞接种于T25培养瓶,每瓶细胞数为1×106。待细胞贴壁后,分别加入20、40和80 μmol·L-1的Mel进行干预或加入DMSO作为对照。24、48 h后,采用常规TRIzol法提取细胞总RNA,于-80℃下保存。逆转录方法参照逆转录试剂盒(日本TaKaRa公司)说明书,RT-PCR测定PTEN基因表达水平,凝胶成像仪(美国BIO-RAD公司)成像并用Image Lab 3.0软件分析结果。每组试验重复3次。
| Gene | Strand | Primer sequences |
| GAPDH | Fwd | 5′-CAACGAATTTGGCTACAGCA-3′ |
| Rev | 5′-AGGGGAGATTCAGTGTGGTG-3′ | |
| PTEN | Fwd | 5′-ACCAGGACCAGAGGAAACCT-3′ |
| Rev | 5′-GCTAGCCTCTGGATTTGACG-3′ |
将对数生长期的LoVo细胞接种于6孔板中,每孔细胞数为1×105,分别使用20、40、80 μmol·L-1的Mel处理,相同条件下培养24、48 h后收集细胞提取各组总蛋白,细胞裂解和溶胞产物通过煮沸10 min变性,采用BCA法进行总蛋白定量;总蛋白用10%的变性聚丙烯酰胺不连续凝胶(SDS-PAGE)进行电泳,将目标蛋白从凝胶电转至PVDF 膜后,按Western blot常规方法进行操作,化学发光法ECL显影,凝胶成像仪(美国BIO-RAD公司)成像并用Image Lab 3.0软件分析结果。每组试验重复3次。
1.7 重组腺病毒的扩增取对数生长期的293细胞接种于T75,孵育至镜下观察到T75中长至约80% 293细胞时,加入2 μL重组腺病毒Ad-si.PTEN原液并迅速混匀,于孵箱中继续培养。加入重组腺病毒24、48、72 h后,在荧光下观察病毒感染率,当293细胞出现50%漂浮时,用吸管吹下细胞终止培养。于3 000 r·min-1,4℃下离心10 min,收集293细胞于EP管,储存于-80℃过夜;次日从-80℃冰箱取出EP管在37℃下快速解冻,解冻后用涡旋混匀器充分振荡,按此方法反复冻融4次以充分从细胞中释放病毒;最后,于8 000 r·min-1,4℃下离心15 min所收集上清液即为扩增所得重组腺病毒,储存于-20℃备用。
1.8 重组腺病毒的滴度测定取相同浓度的对数生长期LoVo细胞悬液接种于24孔板,每孔细胞数量约为2×103,接种4 h后于镜下观察到细胞贴壁,将重组腺病毒分为6组(0.25、0.5、1 、2、4、8 μL)依次加入各孔,每组设3个复孔,置于孵箱中孵育24、48、72 h后,在荧光下观察病毒感染率,在白光下观察细胞的生长情况,选取LoVo细胞生长状态良好且病毒感染率较高的病毒浓度,作为后续试验中重组腺病毒组的浓度。
1.9 Annexin-V检测24孔板中接种对数生长期LoVo细胞,每孔细胞数为1×103,按试验设计加入Mel(40 μmol·L-1)、Ad-si.PTEN干预细胞。干预24 h后,弃培养基,用预冷PBS(4℃)洗3次,加入100 μL Binding Buffer和FITC标记的10 μL Annexin-V(20 mg·L-1),在室温下避光孵育30 min后,加入400 μL Binding Buffer,立即用荧光显微镜进行观察并在100倍倒置显微镜下拍照。每个试验组设3个复孔。
1.10 统计学分析采用SPSS 19.0软件进行统计分析,试验数据以  ± s表示,t检验用于组间比较。
± s表示,t检验用于组间比较。
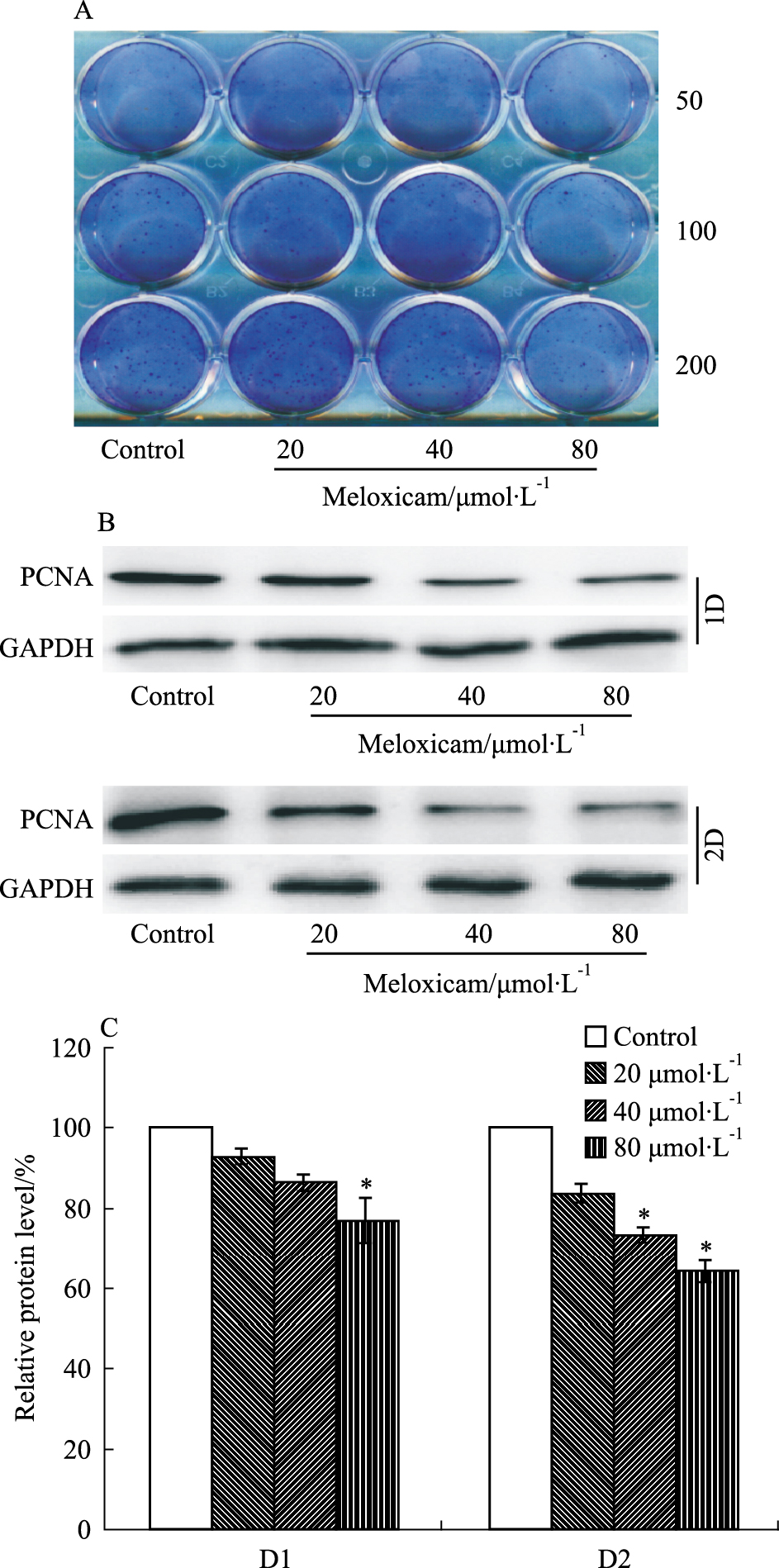
集落形成试验结果显示(Fig1A),Mel对LoVo细胞的集落形成能力具有明显抑制作用。细胞核增殖抗原PCNA是细胞增殖相关基因,其表达水平与细胞增殖状态成正比。Western blot试验结果显示(Fig1B、C),Mel能下调LoVo细胞中的细胞核增殖抗原PCNA蛋白表达水平。与对照组相比,80 μmol·L-1Mel干预48 h,可将LoVo细胞中PCNA的蛋白表达水平抑制到61.57%±2.81%(t=7.086,P=0.019)。结果表明,Mel具有抑制LoVo细胞增殖的能力。
|
| Fig 1 Effects of meloxicam on proliferation of LoVo cells LoVo cells were treated with different concentrations of meloxicam for 24, 48 h, followed by colony formation assay and Western blot. A: The crystal violet staining results; B: The results of Western blot assay; C: The quantification of the western-blot results.*P<0.05 vs control group |
细胞划痕试验结果显示(Fig2),Mel能够明显抑制LoVo细胞的迁移,并且其抑制作用强度与药物浓度的高低成正相关。因此,Mel能降低LoVo细胞的活性。

|
| Fig 2 Effects of meloxicam on migration in LoVo cells LoVo cells were treated with different concentrations of meloxicam for 0, 6 and 24 h, followed by Wound healing assay |
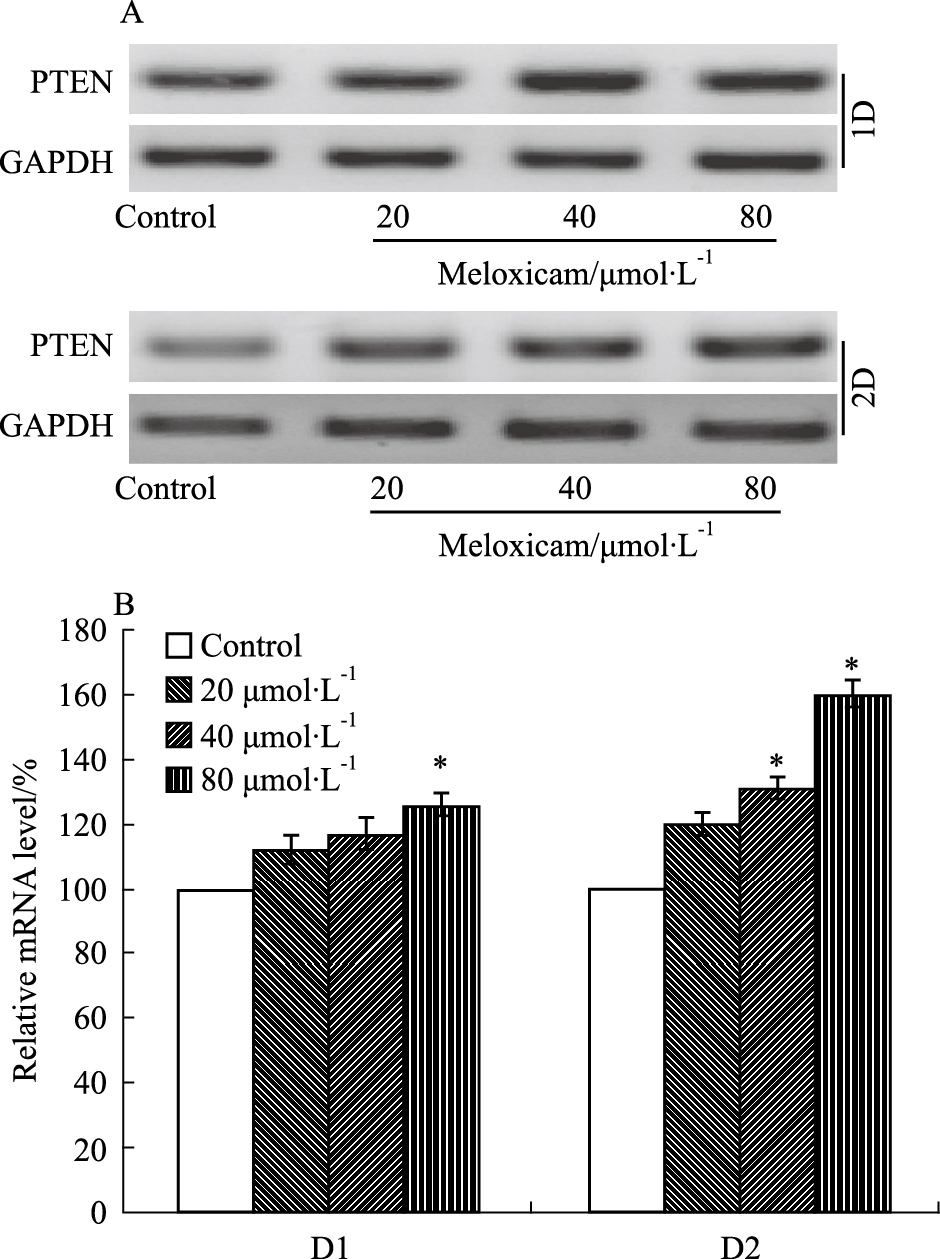
RT-PCR结果显示(Fig3),与对照组相比,80 μmol·L-1Mel干预48 h后PTEN的mRNA表达水平上调至160.43%±4.71%(t=24.244,P=0.002)。结果提示,Mel可上调LoVo细胞中PTEN的mRNA表达。
|
| Fig 3 Effects of meloxicam on mRNA level of PTEN in LoVo cells LoVo cells were treated with different concentrations of meloxicam for 24 and 48 h. followed by RT-PCR assay. A: The results of RT-PCR assay; B: The quantification of the RT-PCR results.*P <0.05 vs control group |
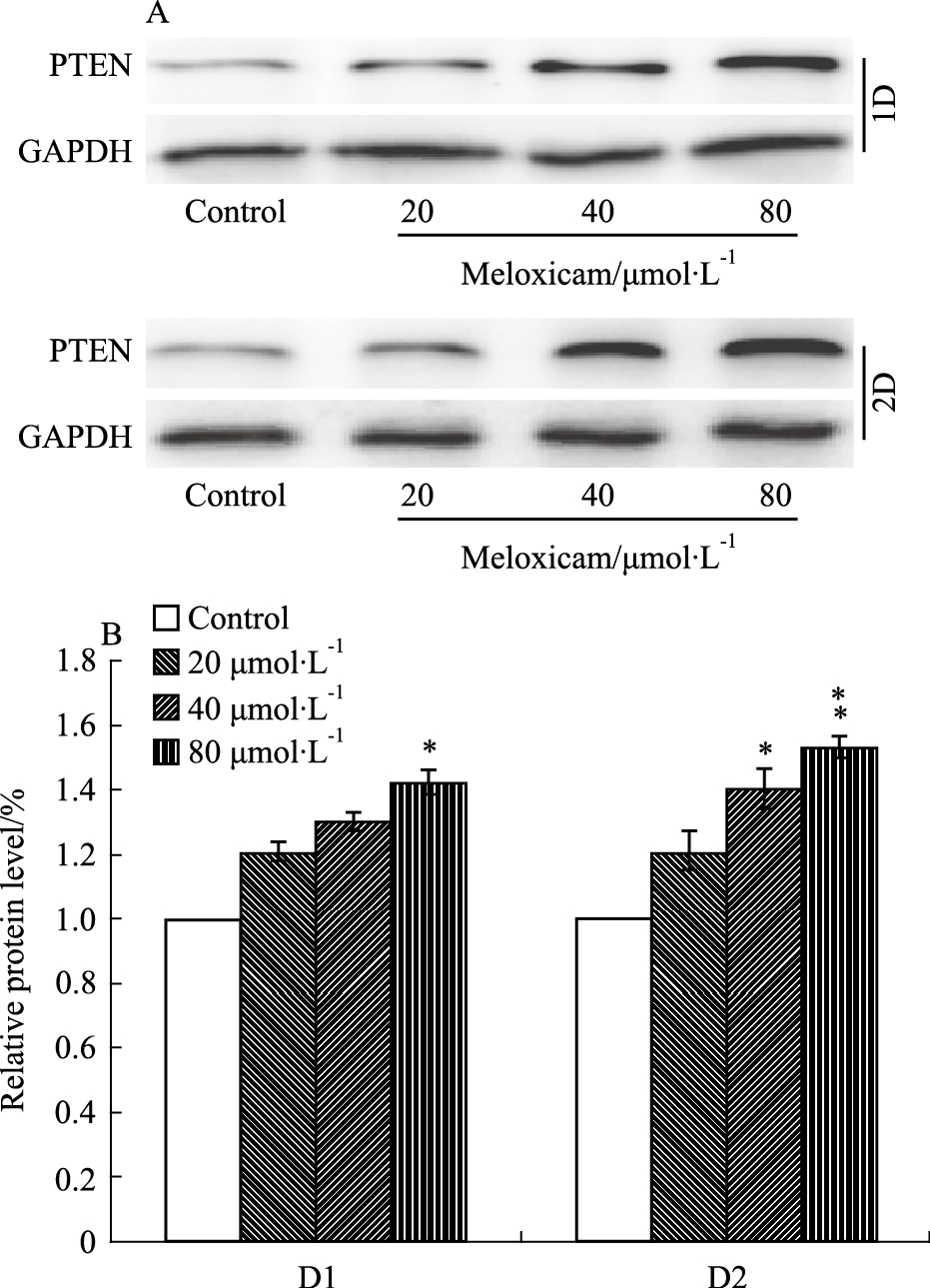
Western blot试验结果显示(Fig4),与对照组相比,80 μmol·L-1Mel干预48 h后PTEN的蛋白表达水平上调至152.63%±3.33%(t=27.359,P=0.001),Mel能上调LoVo细胞内PTEN的蛋白表达水平。
|
| Fig 4 Effects of meloxicam on protein level of PTEN in LoVo cells LoVo cells were treated with different concentrations of meloxicam for 24 and 48 h. followed by Western-blot assay. A: The results of Western-blot assay; B: The quantification of the western-blot results.*P<0.05,**P < 0.01 vs control group |
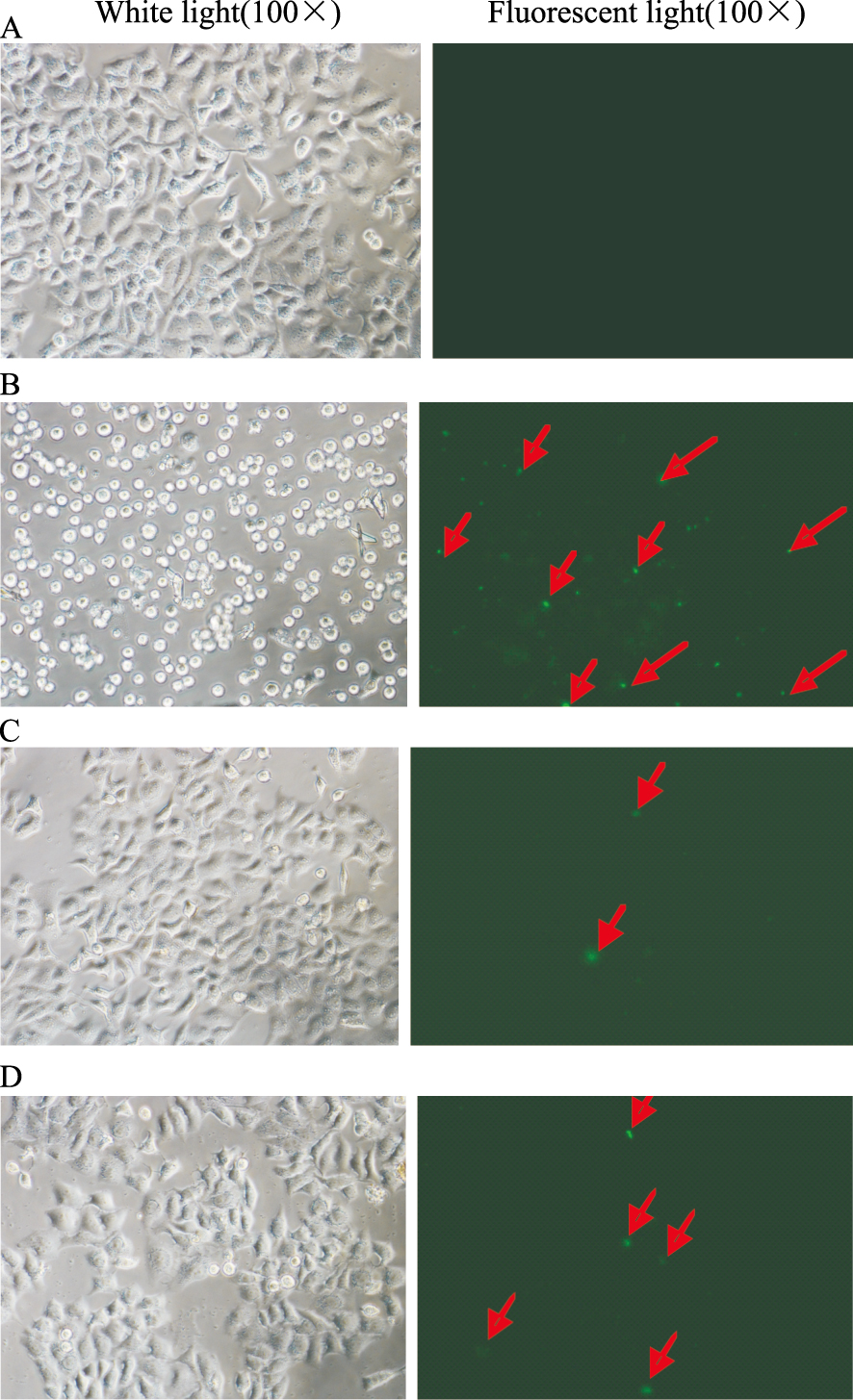
Annexin-V 试验结果显示(Fig5),与对照组相比,Mel(40 μmol·L-1)能明显诱导LoVo细胞凋亡;单独使用Ad-si.PTEN 重组腺病毒组的细胞凋亡现象并不明显;而合用Mel(40 μmol·L-1)与Ad-si.PTEN 腺病毒组,则能一定程度上逆转Mel对LoVo细胞的凋亡促进作用。Ad-si.PTEN重组腺病毒能部分逆转Mel对LoVo细胞的凋亡作用。
|
| Fig 5 Effects of Ad-si.PTEN on apoptosis in LoVo cells LoVo cells were treated with meloxicam(40 μmol·L-1)or Ad-si.PTEN for 24 h, followed by Annexin-V analysis. A: control group analysis results; B: treated with meloxicam(40 μmol·L-1) group analysis results; C: treated with Ad-si.PTEN group analysis results; D: treated with meloxicam(40 μmol·L-1) and Ad-si.PTEN group analysis results |
临床证据表明,免疫反应增强是结直肠癌发展过程中一个公认的危险因素,约80%~90%结直肠癌中存在着COX-2的高表达[7]。根据与炎症反应关系的差异,可以将结直肠癌分为两类:① 散发性结直肠癌(sporadic CRC,SCRC),一种源于内在遗传不稳定性的肿瘤,炎症反应滞后于肿瘤发生;② 炎症诱导性结直肠癌(colitis associated cancer,CAC),一种由慢性炎症性肠道疾病诱发的肿瘤。值得注意的是,人类最常见的慢性炎症性肠道疾病是溃疡性结肠炎和Chron′s疾病,它们均与结直肠癌发生相关[8]。COX-2的高表达可以促进上皮细胞增殖,抑制上皮细胞凋亡,以及触发血管新生[7];关于阿司匹林抑制结直肠癌发生发展的研究证据已比较充分[9]。本研究结果提示,COX-2抑制剂Mel能抑制LoVo细胞的增殖和活性,其机制可能与PTEN的表达上调有关;为免疫反应参与癌症的发生与发展假说提供了新的实验证据。
集落形成试验能够检验单个细胞的增殖能力,孵箱中培养14 d后,1个细胞增殖分化成为50个以上的细胞,即形成肉眼可见的集落,证明该细胞处于较好的增殖状态,否则表明细胞增殖状态受到抑制;细胞核增殖抗原PCNA是细胞增殖相关基因,其表达水平与细胞增殖状态成正比[10];本文的集落形成试验和PCNA蛋白表达实验结果,分别从细胞和分子水平印证了Mel能抑制人结直肠癌LoVo细胞增殖。划痕试验能对细胞的迁移能力进行直观评价[11],本实验结果显示,Mel能明显降低人结直肠癌LoVo细胞的迁移能力,可能有助于控制晚期结直肠癌的远处转移。RT-PCR和Western blot实验结果表明,Mel能上调LoVo细胞中抑癌基因PTEN 的mRNA和蛋白表达水平;Annexin-V试验中,Ad-si.PTEN腺病毒能够部分逆转Mel促进 LoVo细胞的凋亡作用;可见,PTEN基因的表达可能与Mel的抗LoVo细胞作用有关。
流行病学研究结果表明[4, 12, 13],第10号染色体缺失的磷酸酶和张力蛋白同系物(PTEN)是最常见的恶性肿瘤抑制基因,它是PI3K/Akt信号通路的负性调节物,影响细胞的增殖、凋亡、迁移,肿瘤细胞的PTEN水平下调与预后不良关系密切。Mel对LoVo细胞增殖、迁移的影响可能就是通过调节PI3K/Akt信号通路发挥作用,本课题组将在后续的实验中进一步验证。因此,根据前人的研究成果和本试验结果,作者推测Mel可能有利于延缓结直肠癌病理进程、改善结直肠癌患者的预后,值得做深入研究。期望本文的结果和结论,能够为结直肠癌新药研发及新治疗靶点的发现,提供出新的、有益的线索和思考。
(致谢:本文实验在重庆市生物化学与分子药理学重点实验室完成,重庆市生物化学与分子药理学重点实验室何百成教授给予技术指导和部分经费资助,特致衷心感谢!)
| [1] | Lin J T, Wang J Y, Chen M K, et al. Colon cancer mesenchymal stem cells modulate the tumorigenicity of colon cancer through interleukin 6[J]. Exper Cell Res, 2013,319(14):2216-29. |
| [2] | 吕会增,陈图锋,郑宗珩,等. 全反式维甲酸提高人结肠癌LoVo细胞对奥沙利铂敏感性[J].中国药理学通报,2009, 25(6):773-7. Lyu H Z, Chen T F, Zheng Z H, et al. All-trans retinoic acid-induced drug sensitivity of oxaliplatin in human colorecta lcancer cell line LoVo[J].Chin Pharmacol Bull, 2009,25(6):773-7. |
| [3] | Qi L, Sun B, Liu Z, et al. Dickkopf-1 inhibits epithelial-mesenchymal transition of colon cancer cells and contributes to colon cancer suppression[J].Cancer Sci, 2012, 103(4):828-35. |
| [4] | Jhawer M, Goel S, Wilson A J, et al. PIK3CA mutation/PTEN expression status predicts response of colon cancer cells to the epidermal growth factor receptor inhibitor cetuximab[J].Cancer Res, 2008, 68(6):1953-61. |
| [5] | Xin B, Yokoyama Y, Shigeto T, et al. Inhibitory effect of meloxicam, a selective cyclooxygenase-2inhibitor,and ciglitazone, a peroxisome proliferator-activated receptor gamma ligand, on the growth of human ovarian cancers[J].Cancer, 2007, 110(4):791-800. |
| [6] | 周 密,何百成,秧茂盛. Mel抑制人结直肠癌细胞增殖与Wnt/β-catenin 信号的关系研究[J].中国药理学通报,2015,31(3):396-400. Zhou M, He B C, Yang M S. Anti-proliferative effect of meloxicam and Wnt/β-catenin signal in colon cancer cells[J].Chin Pharmacol Bull, 2015,31(3),396-400. |
| [7] | Konturek P C, Rembiasz K, Burnat G, et al. Effects of cyclooxygenase-2 inhibition on serum and tumor gastrins and expression of apoptosis-related proteins in colorectal cancer[J].Digest Dise Sci,2006, 51(4):779-87. |
| [8] | Barry E L, Sansbury L B, Grau M V, et al. Cyclooxygenase-2 polymorphisms, aspirin treatment, and risk for colorectal adenoma recurrence-data from a randomized clinical trial[J].Cancer Epidemiol Biomarkers Prev, 2009, 18(10):2726-33. |
| [9] | Huang K, Gutierrez L P, Bülow S, et al. Clinical characteristics and outcomes in familial adenomatous polyposis patients with a long-term treatment of celecoxib:a matched cohort study[J].Fam Cancer, 2011,10(2):303-8. |
| [10] | Poosarla C, Ramesh M, Ramesh K, et al. Proliferating cell nuclear antigen in premalignancy and oral squamous cell carcinoma[J]. J Clin Diagn Res,2015, 9(6):ZC39-41. |
| [11] | 凌光辉, 朱雪婧, 夏运成, 等. 葡萄糖PDS对单层人腹膜间皮跨细胞电阻及迁移修复能力的影响[J]. 中南大学学报(医学版), 2008, 34(05):418-24. Ling G H, Zhu X J, Xia Y C, et al. Effect of glucose peritoneal dialysates on the trans mesothelial electrical resistance and cellular migration of monolayer human peritoneal mesothelial cell[J].J Cent South Univ(Med Sci), 2008, 34(05):418-24. |
| [12] | Atreya C E, Sangale Z, Xu N, et al. PTEN expression is consistent in colorectal cancer primaries and metastases and associates with patient survival[J].Cancer Med, 2013, 2(4):496-506. |
| [13] | 沈存思,范方田,陶 丽,等. 抑癌基因 PTEN 与肿瘤血管生成研究进展[J]. 中国药理学通报,2013, 29(5):597-600. Shen C S, Fan F T, Tao L, et al. Review of PTEN in tumor angiogenesis[J].Chin Pharmacol Bull, 2013, 29(5), 597-600. |

