


2. 大连理工大学生命与医药学院, 辽宁 盘锦 124221
2. School of Life Science and Medicine, Dalian University of Technology, Panjin Liaoning 124221, China
帕金森病(Parkinson′s disease,PD)是一种中枢神经系统退行性疾病,主要发病特征是中脑黑质致密部内多巴胺神经元的凋亡/死亡,进而导致纹状体内多巴胺的丢失[1]。在PD病人或PD动物模型的发病过程中,抗氧化剂及氧化应激可能直接或间接地对其机制产生影响。目前,临床治疗PD的药物和非药物治疗都只能缓解病人的症状,并且大部分药物长期服用对神经系统有一定的毒副作用,会引起神经系统功能障碍。因此寻求能通过血脑屏障并且毒副作用小的PD治疗药物有重要的现实意义。
药用茯苓是茯苓的干燥菌核,具有抗氧化、抗肿瘤的活性,起到利水渗湿、健脾、安神的功效[2]。茯苓多糖是一种目前研究最广泛的真菌多糖,具有抗肿瘤、抗氧化以及免疫调节等多种生物活性,在多种药物和功能性食品添加剂方面均有所应用[3, 4]。硫酸化茯苓多糖(sulfation pachymaran,SP)是一种人工改造的,由硫酸根取代了茯苓多糖链单糖分子上某些羟基而形成的多糖衍生物,研究表明其在抗病毒、增强机体免疫力、抗凝血等方面的活性较茯苓多糖都有所增强[5, 6]。本课题组前期也开展了SP急性毒性试验、体内代谢以及其对慢性肾功能衰竭的防治作用等方面研究,但有关SP抗氧化性、对神经保护作用等鲜见报道。
1-甲基-4-苯基-1,2,3,6-四氢吡啶(MPTP)是一种潜在的、可选择性损伤黑质纹状体多巴胺神经元的毒素,将其一定量给予啮齿类动物时可引发PD。线粒体功能障碍和多巴胺氧化代谢引起的氧化应激在PD的发病过程中起到非常重要的作用[7]。随着人或动物年龄的增长,氧化应激容易导致各种神经退行性疾病的发生。MPTP作为一种神经毒素能够透过血脑屏障,在脑内经单胺氧化酶B转变为活性MPP+,而MPP+在多巴胺神经元中选择性地通过高通量多巴胺转运体积累,从而诱导多巴胺神经元凋亡/死亡。在大脑中增加的多巴胺转运体及MDA的代谢,导致内源性的谷胱甘肽(GSH)和抗氧化酶(SOD)水平的降低均能对神经元的死亡产生影响。因此,本课题拟从氧化应激的角度来探讨SP对MPTP诱导的小鼠帕金森模型的影响,进而探讨SP对MPTP诱导的神经元损伤的保护作用,揭示其潜在的帕金森治疗效应,为神经保护药物开发提供理论依据。
1 材料与方法 1.1 主要仪器与试剂扫描酶标仪(型号:Multiskan go 1510,美国Thermo Scientific);倒置荧光显微镜(型号:Olympus IX71,日本Olympus);超低温冰箱(型号:DW-HW138,中科美菱);冷冻研磨机(CryoMill,德国Retsch);高速冷冻离心机(型号:Neofuge 23R,香港力康);台式高速低温离心机(型号:1-15PK,德国Sigma );纯水机(型号:Simplicity 美国Millipore)。
SP由合肥学院馈赠;MPTP购于Sigma公司;SOD、谷胱甘肽过氧化物酶(GSH-Px)、过氧化氢酶(CAT)、MDA、超氧阴离子、过氧化氢检测试剂盒均购自南京建成生物工程研究所;其他试剂均为国产分析纯。
1.2 实验动物的处理 1.2.1 动物模型构建ICR小鼠,♂,体质量25~30 g,40只,均购于徐州医学院动物部。将ICR小鼠随机分成对照组、模型组(MPTP组)、治疗组(SP 50、100、150 mg·kg-1),每组8只。根据小鼠体重计算每次腹腔注射用量,连续注射17 d,对照组d 1~17均注射生理盐水;模型组d 1~7注射MPTP,d 8~17注射生理盐水;治疗组d 1~7注射MPTP,d 8~17注射SP。
1.2.2 处死与匀浆保存动物在给药d 18,乙醚深度麻醉,安乐处死,分离中脑和脑皮层,按照重量体积比1 ∶9加入生理盐水,剪碎组织,置于冷冻研磨机中振速为2 500~3 000 r·min-1,震动1 min,5 000 r·min-1离心5 min,得匀浆上清备用。
1.3 氧化相关指标的测定分别测定小鼠中脑和脑皮层GSH-Px、CAT、SOD酶活性、抗超氧阴离子的活力、MDA及过氧化氢的含量,按试剂盒方法进行,利用酶标仪测定OD值,根据公式计算各指标。
1.4 统计学分析数据采用One-way ANOVA 检验进行组间显著性分析比较。
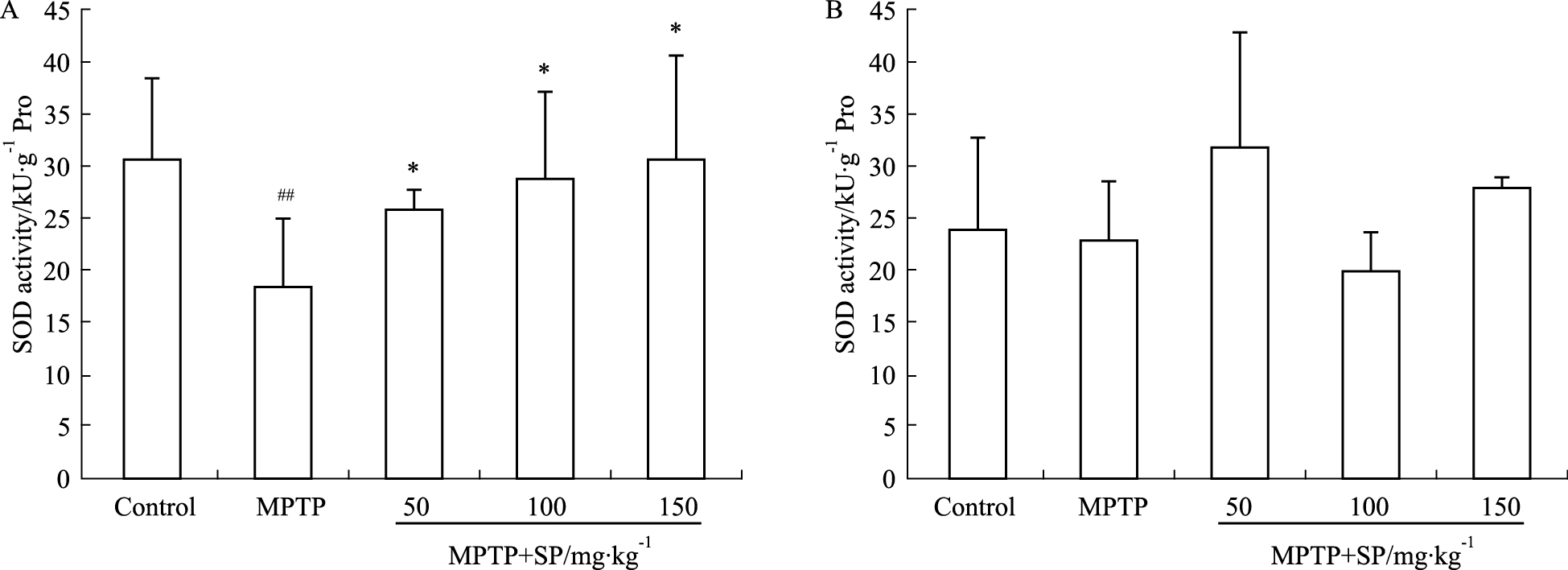
2 结果 2.1 SP对小鼠中脑和脑皮层SOD、GSH-Px、CAT酶活性影响 2.1.1 SP对SOD活性影响Fig1A为SP对MPTP诱导小鼠中脑SOD酶活性的影响。从图可见,小鼠注射MPTP后,中脑的SOD酶活性(18.5±6.5)与对照组(30.6±7.8)相比有明显下降。SP治疗后,中脑的SOD酶活性呈现升高的趋势,并随着SP浓度的增加,SOD酶活性也不断升高,当SP浓度达到150 mg·kg-1时,SOD酶活性(30.6±10.1)最高。Fig1B为SP对MPTP诱导小鼠脑皮层SOD酶活性的影响。由图可知,MPTP组的SOD酶活性(22.9±5.5)相对于对照组(23.7±9.0)呈现下降趋势,但差异无显著性,而治疗组与MPTP组相比,在一定浓度范围内,随着SP浓度的升高,SOD酶活性有所升高,但差异无显著性。
|
| Fig.1 Effects of SP on superoxide dismutase (SOD) activity in midbrain and cortex of MPTP-induced mice A: The SOD activity in the midbrain of the MPTP-induced mice; B: The SOD activity in the cortex of the MPTP-induced mice. ##P < 0.01 vs control group; *P < 0.05 vs MPTP group. |
Fig2A、2B分别为SP对MPTP诱导小鼠中脑和脑皮层GSH-Px酶活性的影响。无论在中脑或是皮层中,MPTP组(中脑143.6±41.2,皮层79.3±47.5)与对照组(中脑168.9±25.4,皮层123.2±9.6)相比,GSH-Px的酶活性有所下降,具有统计学意义。SP治疗后,与MPTP组相比,在一定范围内,治疗组的GSH-Px酶活性相对有所提高,但低于对照组的酶活性。当SP浓度为100 mg·kg-1时酶活性(中脑160.5±20.4,皮层90.7±11.0)最高,但随着SP浓度的增加,酶活性降低,且低于MPTP组,可见高浓度SP具有一定的毒性。

|
| Fig.2 Effects of SP on GSH-Px activity in midbrain and cortex of MPTP-induced mice A: The GSH-Px activity in the midbrain of the MPTP-induced mice; B: The GSH-Px activity in the cortex of the MPTP-induced mice. #P < 0.05,##P < 0.01 vs control group; *P < 0.05 vs MPTP group. |
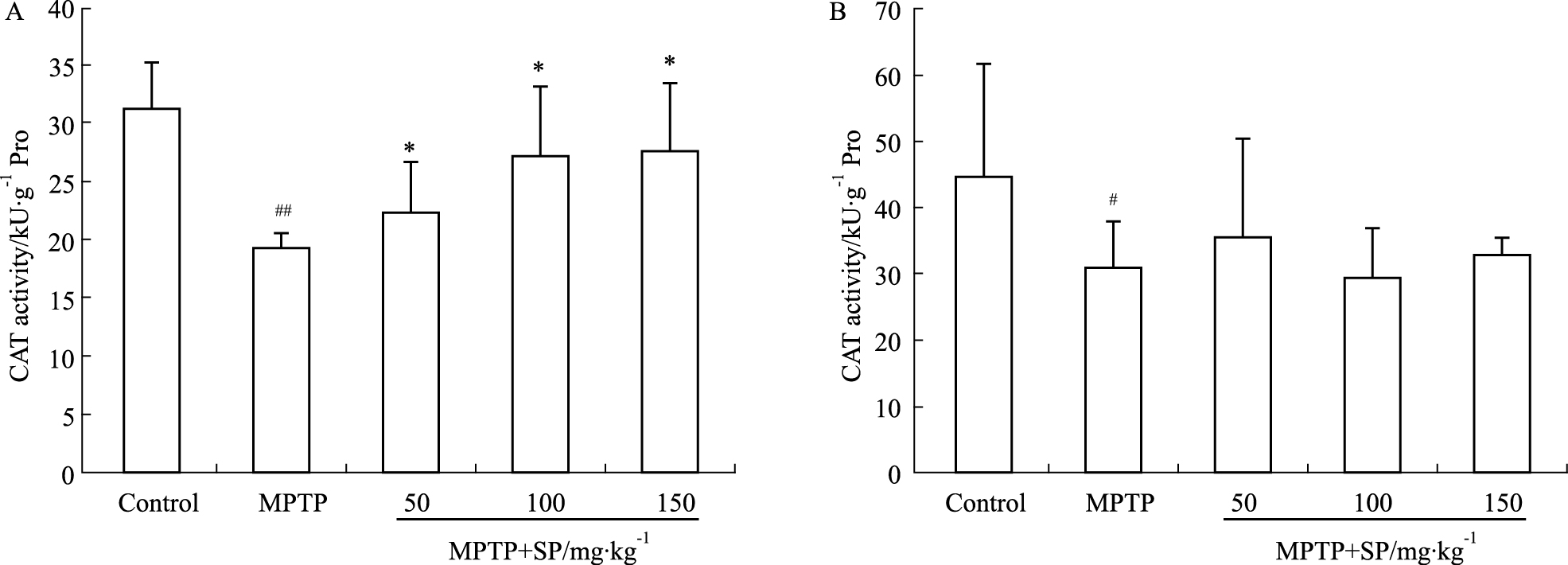
从Fig3A可看出,MPTP组(19.5±1.1)与对照组(31.2±3.9)相比较,中脑CAT酶活性明显降低;Fig3B可看出,MPTP组(30.2±6.7)与对照组(44.6±17.2)相比,脑皮层CAT酶活性明显降低。所有剂量SP治疗后,中脑中CAT酶活性(22.3±4.4、27.1±5.8、27.6±5.8)均有明显的提高,并随着SP的不断增加呈现上升趋势,但脑皮层CAT酶活性变化不明显。
|
| Fig.3 Effects of SP on the CAT activity in midbrain and cortex of MPTP-induced mice A: The CAT activity in the midbrain of the MPTP-induced mice; B: The CAT activity in the cortex of the MPTP-induced mice. #P < 0.05,##P < 0.01 vs control group; *P < 0.05 vs MPTP group. |
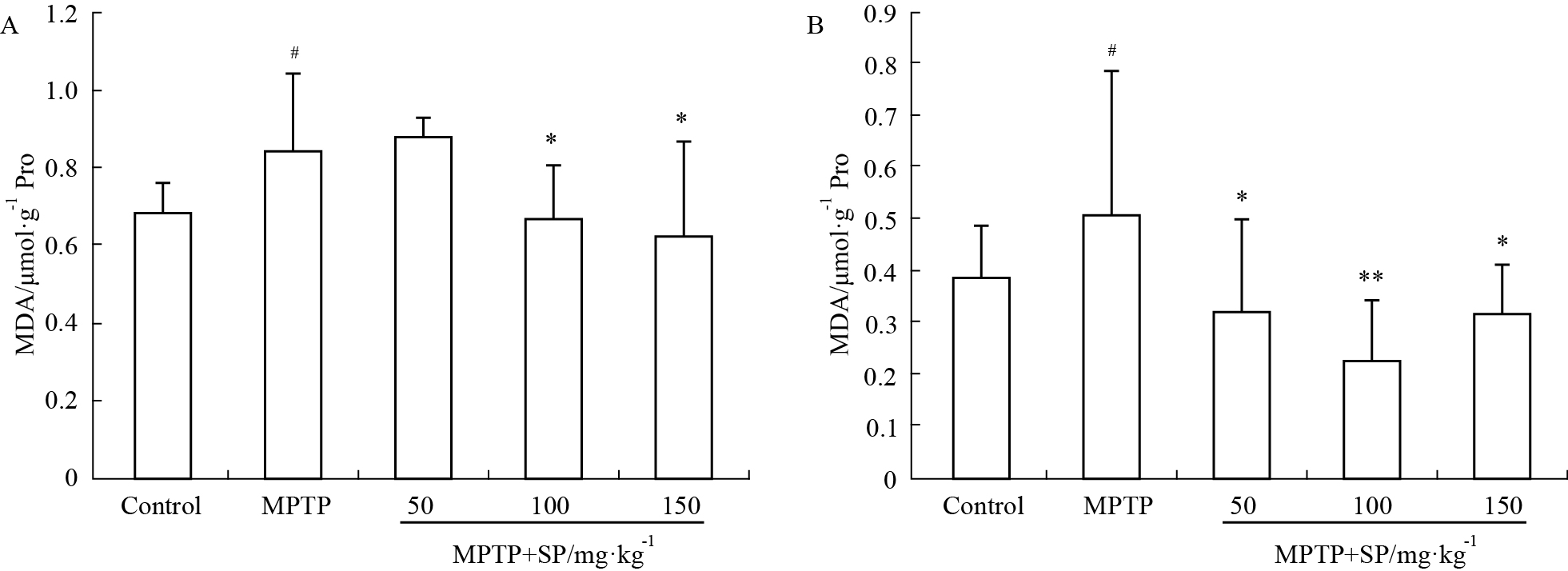
由Fig4A、B可知,MPTP组(中脑0.84±0.20,皮层0.51±0.27)与对照组(中脑0.69±0.07,皮层0.38±0.10)相比MDA含量有了明显的提高;SP治疗后,中脑的MDA含量在SP浓度为100 mg·kg-1(0.64±0.15)、150 mg·kg-1(0.62±0.27)时,MDA含量都明显低于MPTP组,脑皮层中MDA含量都低于MPTP组,SP浓度为100 mg·kg-1(0.23±0.11)时最低,差异有显著性。
|
| Fig.4 Effects of SP on concentration of MDA in midbrain and cortex of MPTP-induced mice A: The concentration of MDA in the midbrain of the MPTP-induced mice; B: The concentration of MDA in the cortex of the MPTP-induced mice. #P < 0.05 vs control group; *P < 0.05,**P < 0.01 vs MPTP group. |
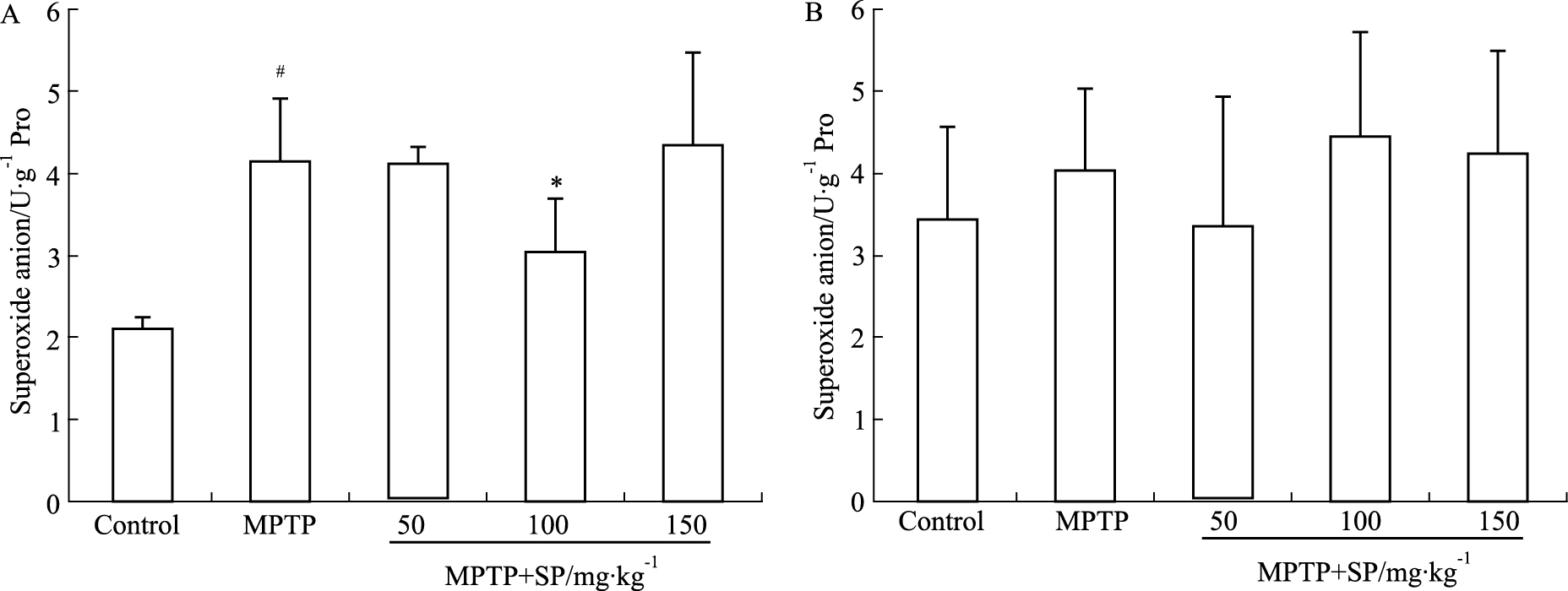
由Fig5A、B可知,MPTP组(中脑4.17±0.74,皮层4.00±1.01)与对照组中脑(2.10±0.13)和脑皮层(3.42±1.11)相比,小鼠的抗超氧阴离子能力都有明显的降低。SP治疗后,与MPTP组相比,在一定浓度范围内,治疗组中抗超氧阴离子能力出现不同程度的提高,当SP浓度为100 mg·kg-1(3.04±0.65)时中脑组织抗超氧阴离子能力最高,而SP浓度为50 mg·kg-1(4.10±0.18)和150 mg·kg-1(4.36±1.10)无统计学意义。脑皮层中各浓度SP治疗均无统计学意义。
|
| Fig.5 Effects of SP on antisuperoxide anion activity in midbrain and cortex of MPTP-induced mice A: The antisuperoxide anion activity in the midbrain of the MPTP-induced mice; B: The antisuperoxide anion activity in the cortex of the MPTP-induced mice. #P < 0.05 vs control group; *P < 0.05 vs MPTP group. |
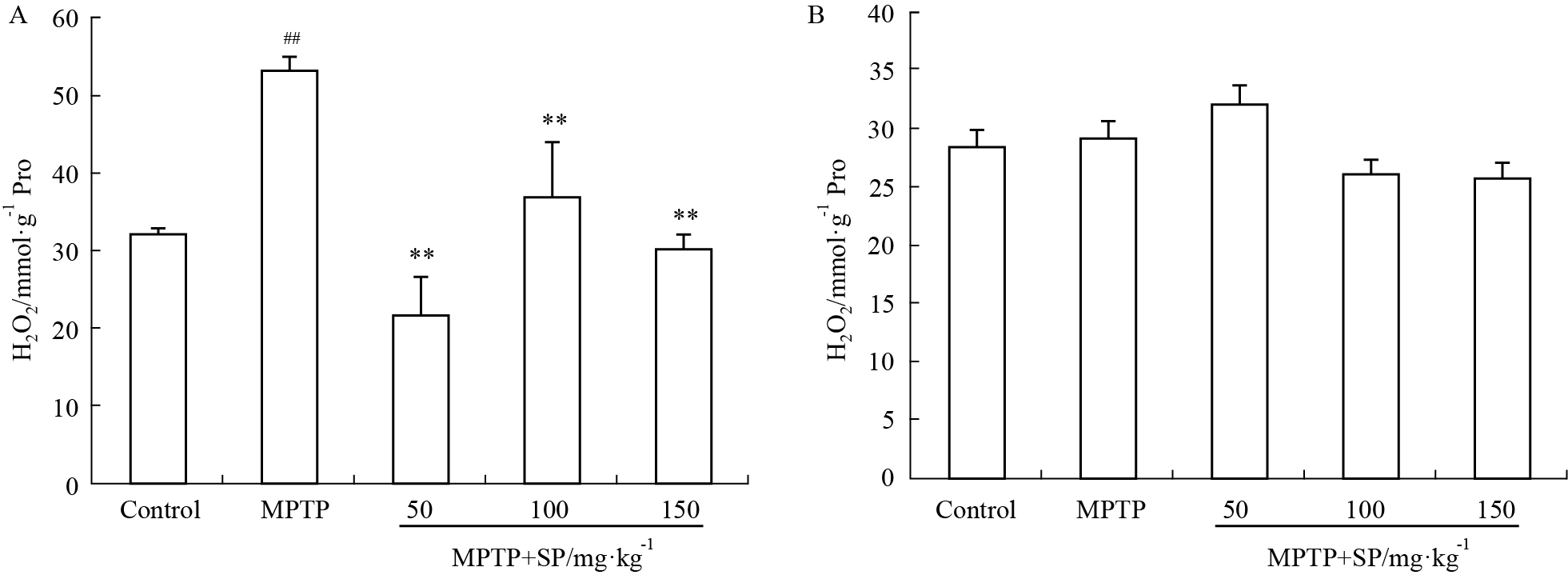
由Fig6A可知,中脑中MPTP组(53.22±1.71)与对照组(32.26±0.55)相比过氧化氢含量有了明显的提高,而脑皮层有不明显的提高。SP治疗后,中脑中过氧化氢含量(25.23±2.30、36.81±7.19、30.27±1.8)都低于MPTP组,且差异有显著性。脑皮层中,当SP浓度为50 mg·kg-1(32.00±7.15)时高于对照组;当SP浓度为100 mg·kg-1(26.08±2.35)和150 mg·kg-1(25.77±7.93)时过氧化氢含量略低于MPTP组和对照组,无统计学意义。
|
| Fig.6 Effects of SP on concentration of H2O2 in midbrain and cortex of MPTP-induced mice A: The concentration of H2O2 in the midbrain of the MPTP-induced mice; B: The concentration of H2O2 in the cortex of the MPTP-induced mice. ##P < 0.01 vs control group; **P < 0.01 vs MPTP group. |
PD是一种由于脑内多巴胺(DA)减少而导致的神经性功能疾病,导致PD中脑黑质纹状体系统多巴胺能神经元死亡的机制主要是由于氧化应激产生了大量的氧自由基,从而诱导神经元细胞死亡。氧化应激的特征在于氧化还原产生的自由基或其他活性物质和抗氧化能力的失衡,并且它可以改变有关的线粒体功能和蛋白质之间的间隙[8]。有研究从患者或尸体的大脑样本中的组织氧化分析指标中,得到了PD存在氧化应激损伤的直接证据[9]。降低多不饱和脂肪酸和增加MDA的含量被认为可以使黑质中血脂水平升高,随着氧化损伤作用,PD患者黑质中抗氧化剂谷胱甘肽的含量也有所下降。有报道已经阐述茯苓多糖能不同程度增加血清中SOD的活性,降低MDA含量,具有较好的抗衰老作用[10]。本研究利用神经毒素MPTP诱导PD小鼠模型,MPTP组小鼠中脑和脑皮层的MDA、过氧化氢含量升高,差异具有统计学意义。说明MPTP诱导下小鼠中脑和脑皮层受到损伤,脑内的氧化应激性减弱,PD造模成功。注射SP,考察小鼠中脑和脑皮层中SOD、GSH-Px、CAT三种抗氧化酶的活性、超氧阴离子活力单位以及MDA、过氧化氢含量,探究SP对MPTP诱导PD小鼠的作用。抗氧化剂对于MPTP诱导的多巴胺能神经元丢失具有保护作用,有研究人员研究茯苓多糖对大鼠血清抗氧化酶活性的影响,对于添加茯苓多糖7周后的几组大鼠的抗氧化酶(GSH-Px、SOD、CAT)活性与其他对照组相比有明显差异,其血清的抗氧化酶活性明显增加[11]。本实验动物模型经SP治疗后,小鼠中脑和脑皮层中3种抗氧化酶的活性、抗超氧阴离子的能力有所升高,MDA和过氧化氢的含量出现不同程度的降低。说明SP作为一种氧化保护剂,对MPTP处理的小鼠GSH-Px、SOD、CAT和抗超氧阴离子能力的降低具有明显的抑制作用,能够提高小鼠脑内的抗氧化酶活性,降低机体内的自由基含量,减少MDA和过氧化氢的产生,保护脑神经元细胞。综上所述,我们认为SP对MPTP诱导帕金森小鼠的神经元细胞具有一定的保护作用。
| [1] | Mosley R L, Benner E J, Kadiu I, et al. Neuroinflammation, oxidative stress and the pathogenesis of Parkinson's disease[J]. Clin Neurosci Res, 2006, 6(5):261-81. |
| [2] | 程水明, 桂 元, 沈 思, 黄 文. 茯苓皮三萜类物质抗氧化活性研究[J]. 食品科学, 2011, 32(9):27-30. Cheng S M, Gui Y, Shen S, Huang W. Antioxidant properties of triterpenes from Poria cocos Peel[J]. Food Sci, 2011, 32(9):27-30. |
| [3] | 张 竞,潘 琢,赵宝华. 真菌多糖抗肿瘤机制研究进展[J]. 生命科学仪器, 2011, 32(18):2988-9. Zhang J, Pan Z, Zhao B H. Recent studies on anti-tumor effect of fungal polysaccharides[J].Life Sci Instrum, 2011, 32(18):2988-9. |
| [4] | 牛 爽, 郝利民, 赵树欣, 陈 强. 茯苓多糖的研究进展[J]. 食品科学, 2012, 33(13):348-53. Niu S,Hao L M,Zhao S X,Chen Q. Research progress in polysaccharides from Poria cocos[J]. Food Sci, 2012, 33(13):348-53. |
| [5] | 梅天笑,王小莺,万 根,聂海静. 多糖的修饰及其抗凝血活性研究进展[J]. 江西农业大学学报, 2013, 35(5):1108-13. Mei T X,Wang X Y,Wan G,Nie H J.Progress in modifications polysaccharide and its auticoagalant activity[J]. Acta Agric Univ Jiangxi, 2013, 35(5):1108-13. |
| [6] | Wang X F, Wang J L, Zhang J, et al. Structure-antioxidant relationships of sulfated galactomannan from guar gum[J]. Int J Biol Macromol, 2010, 46(1):59-66. |
| [7] | Mancuso C, Scapagnini G, Curro D, et al. Mitochondrial dysfunction, free radical generation and cellular stress response in neurodegenerative disorders[J]. Front Biosci, 2007, 12(3):1107-23. |
| [8] | Seet R C, Lee C Y, Lim E C, et al. Oxidative damage in Parkinson disease:measurement using accurate biomarkers[J]. Free Radic Biol Med, 2010, 48(4):560-6. |
| [9] | Dexter D T, Carter C J, Wells F R, et al. Basal lipid peroxidation in substantia nigra is increased in Parkinson's disease[J]. J Neurochem, 1989, 52(2):381-9. |
| [10] | 侯安继, 陈腾云, 彭施萍, 等. 茯苓多糖抗衰老作用研究[J]. 中药药理与临床,2004,20(3):10-1. Hou A J, Chen T Y, Peng S P, et al. Anti-aging effect of polysaccharides from Poria cocos[J]. Pharmacol Clin Chin Mat Med, 2004,20(3):10-1. |
| [11] | Ke R D, Lin S F, Chen Y, et al. Analysis of chemical composition of polysaccharides from Poria cocos Wolf and its anti-tumor activity by NMR spectroscopy[J]. Carbohydr Polym, 2010, 80(1):31-4. |
