


类风湿性关节炎(rheumatoid arthritis,RA)是一种发病原因不明,累及全身关节的慢性自身免疫疾病,RA以滑膜炎症、滑膜组织增生、骨及软骨的破坏为主要病理特征[1]。滑膜成纤维细胞(synovial fibroblasts,FLS)参与了RA发展进程中的免疫应答、血管新生和关节破坏等病理过程[2, 3]。临床研究表明,RA患者的RA-FLS与正常的FLS细胞相比,具有增殖活跃、凋亡抑制,分泌高水平促炎性细胞因子等特征,是类风湿药物研究及治疗的重要靶细胞。由于RA患者FLS来源较少,建立与RA -FLS 相似特征的动物细胞模型AA大鼠滑膜成纤维细胞(AA-FLS)对抗RA 药物筛选及开发是非常必要的。本项研究在前期RA动物模型成功复制的基础上,成功建立了AA-FLS体外原代培养方法,并对AA-FLS的细胞状态、增殖活性、细胞凋亡水平及细胞因子分泌水平及线粒体通路调控蛋白Bcl-2和Bax及Pro-caspase-3和Cleave-caspase-3表达水平进行分析,综合评价AA-FLS的生物特性,探讨AA-FLS作为抗RA的体外研究细胞模型的可行性。
1 材料与方法 1.1 动物及分组SPF级SD大鼠20只,♂,体质量(160±20) g,由南方医科大学实验动物中心提供,动物合格证号:SCXK(粤)2011-0015。适应性喂养3d后随机分为2组,正常对照组10只,AA模型组10只。
1.2 试剂热杀死结核分枝杆菌H37Ra,由Difco实验室提供(Detroit,MI,USA);矿物油,美国Sigma;Ⅰ型胶原酶,美国Sigma;0.25% EDTA胰蛋白酶,美国Gibco;胎牛血清,中国四季青;双抗,美国Gibco;DMEM培养液,美国Hyclone;TNF-α;DMSO;生物素-链霉卵白素免疫组化检测试剂盒(SP-9000)、DAB显色试剂盒,北京中杉金桥公司产品;苏木精伊红(HE)染色试剂盒,碧云天公司产品;Cell Counting Kit-8(CCK-8),日本同仁;Hochest 33258试剂盒,凯基生物技术有限公司;Anti-Bcl-2 antibody、 Anti-Bax antibody、Anti-Caspase-3 antibody、Anti- vimentin antibody、Anti-CD68 antibody,美国Abcam;TNF-α、IL-1β ELISA试剂盒,北京达科为公司产品。
1.3 主要仪器电子天平,德国Sartorius公司;超净工作台,波兰shel-Lab;IX51倒置显微镜,日本Olympus株式会社;二氧化碳恒温培养箱,新加坡Esco公司;MK3型酶标仪,芬兰TECAN GENios公司。
1.4 AA-FLS原代培养Mtb诱导SD大鼠建立类风湿关节炎大鼠模型见课题组前期研究[4, 5]。大鼠免疫Mtb 后18 d,腹腔注射100 g·L-1水合氯醛麻醉,处死后固定在超净工作台内,取双侧后膝关节滑膜组织,PBS缓冲液冲洗3次,加入4 g·L-1胶原酶Ⅰ浸没组织,用眼科剪快速剪碎组织1~2 min,于37℃,5% CO2的培养箱中孵育4 h。2 800 r·min-1,4℃离心10 min,用含10% FBS的DMEM培养基与沉淀混匀,均匀铺于培养皿中,放入37℃,5% CO2培养箱中培养,d 2换液。
1.5 AA-FLS细胞传代弃去旧培养基,用PBS缓冲液洗2次,加入含EDTA胰酶消化细胞,轻轻晃动培养皿使胰酶消化液覆盖细胞。消化完全后加入DMEM完全培养基终止消化,吹打培养皿收集细胞,800 r·min-1离心5 min,弃上清液,用DMEM完全培养基重悬细胞,混匀后均匀铺于培养皿中,37℃、5% CO2培养箱中培养。
1.6 AA-FLS细胞鉴定 1.6.1 细胞形态观察在倒置显微镜下观察各代滑膜成纤维细胞的形态,生长状态和细胞纯度。显微镜下观察到的呈梭形细胞为滑膜成纤维细胞,圆形、椭圆形为巨噬样滑膜细胞。观察每次传代后滑膜成纤维细胞形态和细胞所占比例的变化情况。
1.6.2 HE染色将指数生长期的AA-FLS接种于置有10 mm×10 mm盖玻片的6孔板内,加入DMEM完全培养基,37℃、5% CO2培养箱中培养24 h,倒置显微镜下观察细胞爬片良好时,将爬片取出,按以下步骤进行HE染色:多聚甲醛固定15 min,PBS洗2 min,苏木精染10 min,蒸馏水冲洗多余染色液,PBS洗数秒,体积分数0.95的乙醇5 s,伊红染2 min,体积分数0.70乙醇洗2次,显微镜下观察。
1.6.3 免疫细胞化学将传代至第3代的AA-FLS铺于96孔板内,细胞同期化后,冷PBS洗3次,多聚甲醛固定15min,Triton-X-100室温孵育20 min,H2O2孵育15 min灭活内源性过氧化物酶活性,正常山羊血清工作液室温封闭15 min,倒去。抗大鼠vimentin抗体和抗大鼠CD68抗体(1 ∶200稀释)4℃孵育过夜,阴性对照用PBS代替一抗。PBS洗3次,滴加生物素标记山羊抗兔IgG室温孵育15 min,PBS洗3次后,SP室温孵育15min,DAB显色,苏木精复染,倒置显微镜下观察滑膜成纤维细胞vimentin的表达情况。
1.7 CCK-8法检测AA-FLS增殖活性取对数生长期的AA-FLS和正常大鼠FLS细胞,以DMEM完全培养基制备成2×107个·L-1的细胞悬液,以每孔200 μL分别接种于96孔板中,细胞同期化后AA-FLS组和正常大鼠FLS组换同体积新鲜的DMEM完全培养基,每组5个复孔,分别培养1~7 d。培养结束后每孔加入10 μL的CCK-8溶液,在培养箱中孵育4 h,用酶标仪测定450 nm处的吸光度,绘制AA-FLS和正常大鼠FLS的生长曲线,比较两种细胞的增殖活性。
1.8 Hoechst 33258法检测AA-FLS凋亡特性收集生长状态良好的对数生长期的AA-FLS和正常大鼠FLS(培养液中漂浮细胞800 r·min-1,离心5 min收集;贴壁细胞以胰蛋白酶消化,离心收集),收集好的细胞用PBS缓冲液洗2次,去上清,用甲醛溶液4℃固定15 min,PBS洗2次,离心去上清后用PBS缓冲液调整细胞浓度为1×108个·L-1,吸取50 μL细胞悬液,以盖玻片均匀涂片,自然风干,滴加50 μL的Hoechst 33258溶液在细胞涂片上,室温避光染色10 min,用流水冲洗多余染料,UV显微镜下观察细胞并拍照记录。每组细胞取10个视野,每个视野内计数不少于20个细胞核,计数凋亡细胞核数量,并计算各组细胞凋亡率。
1.9 ELISA法检测TNF-α和IL-1β水平分别收集AA-FLS和正常大鼠FLS的培养基,4℃,6 000 r·min-1离心5 min,取上清液备用。设置空白组、标准品组和实验组,每组3个复孔,按ELISA检测试剂盒说明书操作,绘制标准曲线并计算出数据。
1.10 Western blot 测定Bcl-2、Bax、Pro-Caspase-3和Cleave-Caspase-3蛋白表达收集对数生长期的细胞,提取细胞总蛋白,取40 μg以SDS-PAGE电泳分离。低温条件下以恒定电流250Ma转膜90 min。转膜结束后,将PVDF膜用封闭液室温封闭2 h,用TBS-T洗膜3次×5 min。Bcl-2、Bax和Caspase-3一抗以1 ∶1 000比例稀释,将PVDF膜放入相应的蛋白一抗液体中,4℃孵育过夜,TBS-T洗膜3次×5 min,加入辣根过氧化物酶标记的二抗室温孵育2 h,用TBS-T洗膜后,ECL法曝光显影。
1.11 统计学分析实验结果以±s表示,数据采用SPSS 19.0统计软件处理,采用完全随机设计的方差分析和t检验法进行统计学分析。
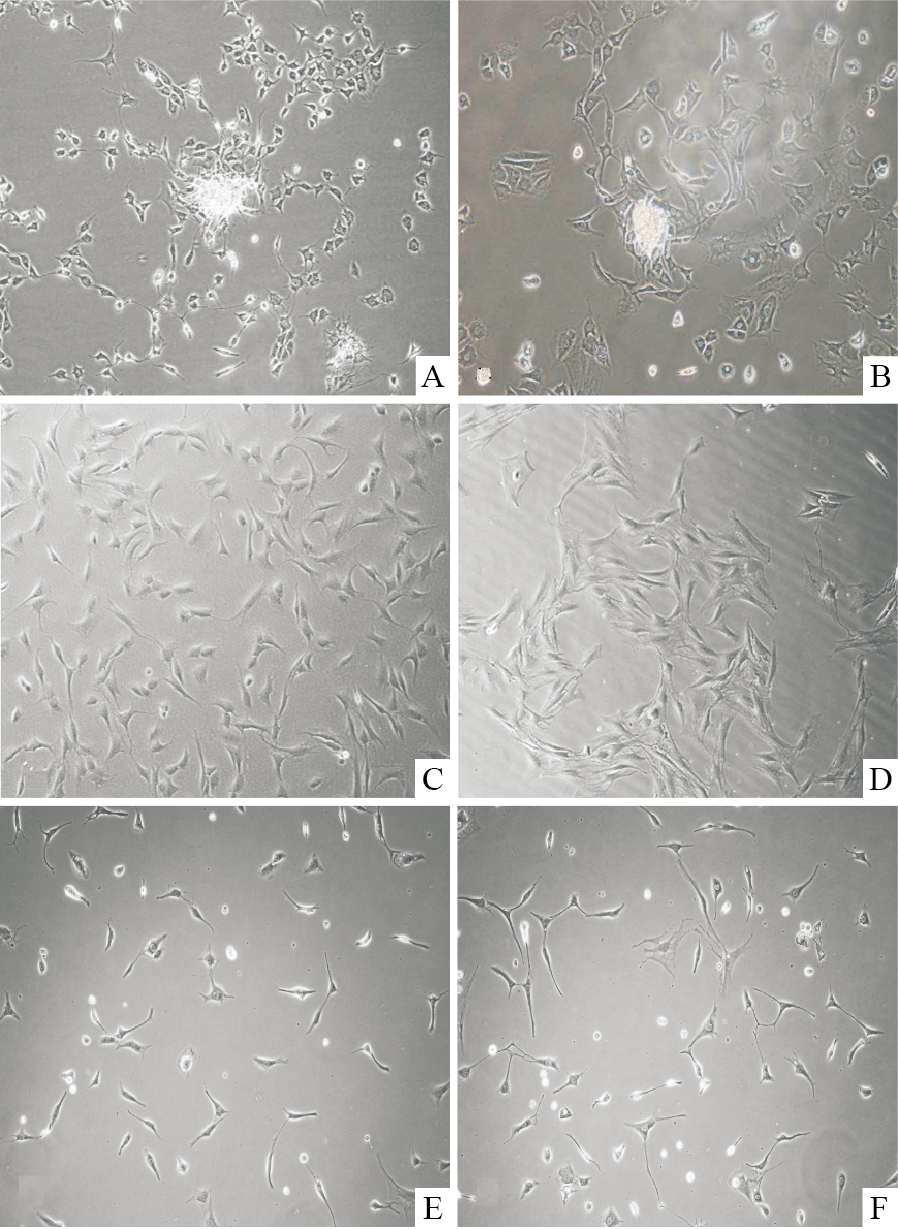
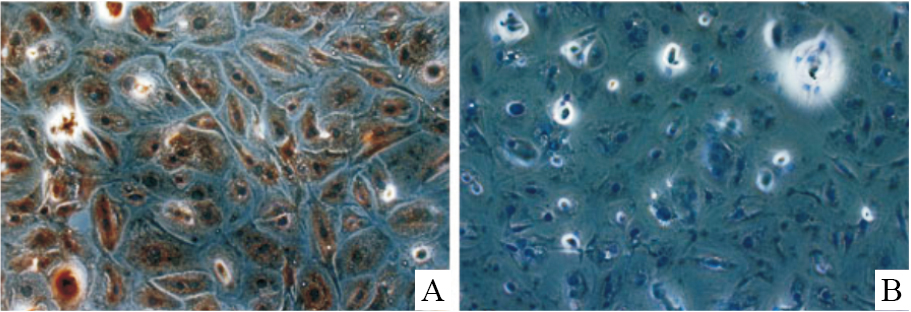
2 结果 2.1 AA-FLS细胞形态及鉴定通过胶原酶法分离获得的原代AA-FLS多为扁圆形或不规则多边形,围绕一些细小的组织块呈辐射状生长,其中混有大量的圆形巨噬样滑膜细胞;经传代后细胞渐伸展为梭形,混杂的巨噬样滑膜细胞数量渐渐减少;传代至第3代之后的细胞,典型梭形形态的细胞占0.95以上且鲜有巨噬样滑膜细胞;第5代以后的细胞开始老化,细胞形态发生变化,有的细胞开始皱缩为类圆形,细胞内出现空泡,细胞间隙增大(Fig1)。HE染色结果显示,AA-FLS形态规则,呈梭形,其细胞核为卵圆形位于细胞中央(Fig2)。免疫细胞化学结果显示,AA-FLS的vimentin表达为阳性,细胞内分布棕黄色颗粒,而CD68细胞几乎不着色为阴性表达(Fig3)。根据细胞来源、形态和免疫细胞化学检测结果可知,分离所得细胞为滑膜成纤维细胞。
|
| Fig.1 Morphology of primary AA-FLSs(×100) A~D:the 1st generation to the 4th generation of AA-FLSs;E~F: the 6th generation to the 7th generation of AA-FLSs |

|
| Fig.2 Morphological observation of AA-FLSs(×400,HE stain) |
|
| Fig.3 Immunocytochemical identification of levels of AA-FLSs characteristic maker A: Vimentin (+) (×200); B: CD68(-) (×200) |
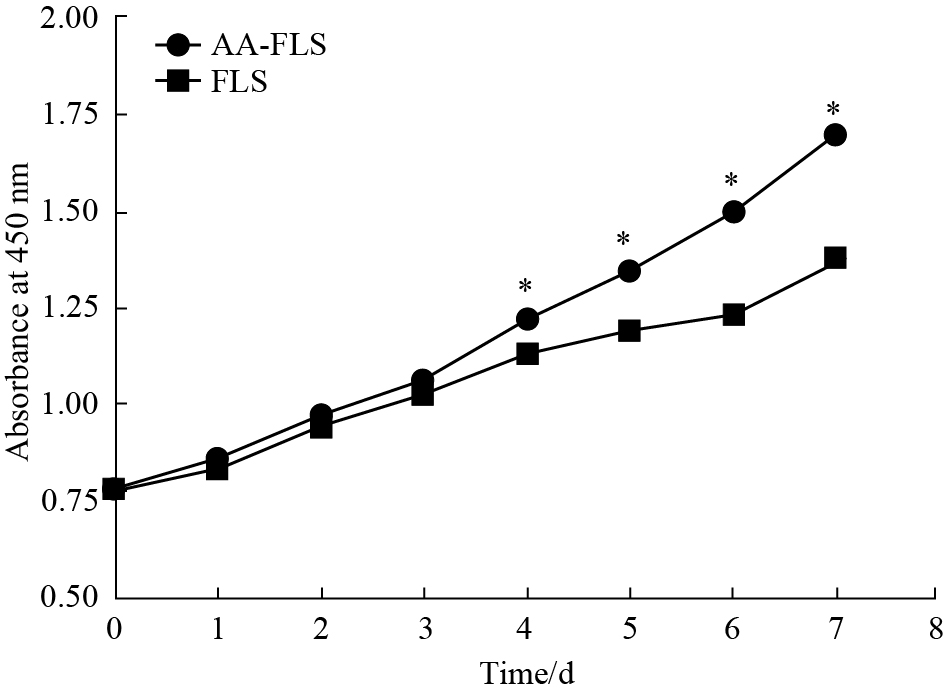
细胞经传代后1~3 d增殖较缓慢,两种细胞的生长曲线均呈平缓上升趋势;d 4~7细胞的增殖速度加快,从d 4开始AA-FLS的增殖速度明显高于正常大鼠的FLS细胞,差异有统计学意义(P < 0.05)(Fig4)。
|
| Fig.4 Proliferation curve of AA-FLS and FLS *P < 0.05 vs FLS group |
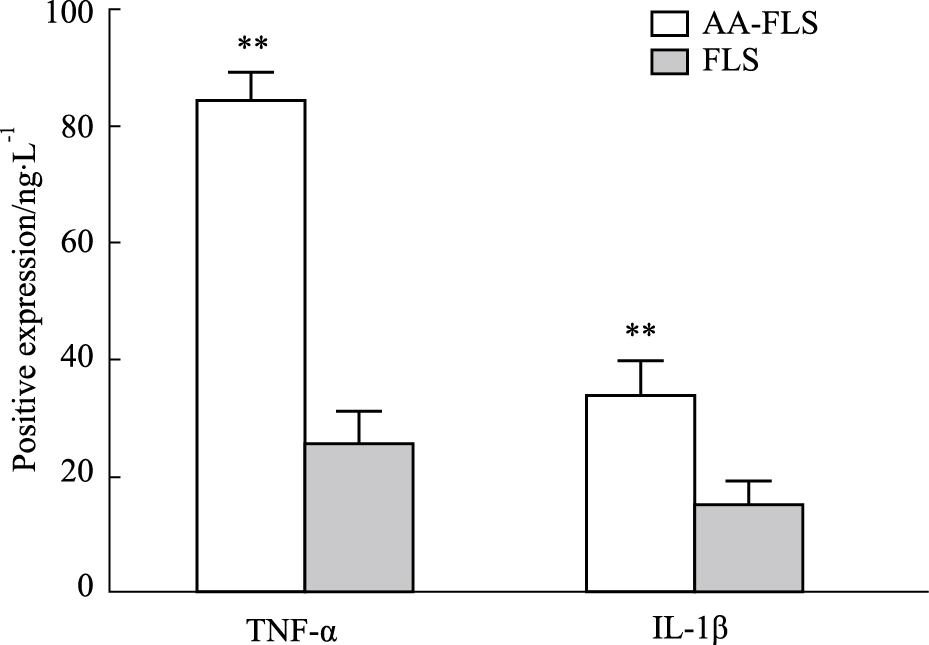
用ELISA法对AA-FLS和正常大鼠FLS细胞上清液中的TNF-α及IL-1β水平进行测定。测定结果显示,AA-FLS的TNF-α、IL-1β的表达水平与正常FLS比较升高,差异有统计学意义(P < 0.01)(Fig5)。
|
| Fig.5 Expression of TNF-α and IL-1β in AA-FLSs **P < 0.01 vs FLS group |
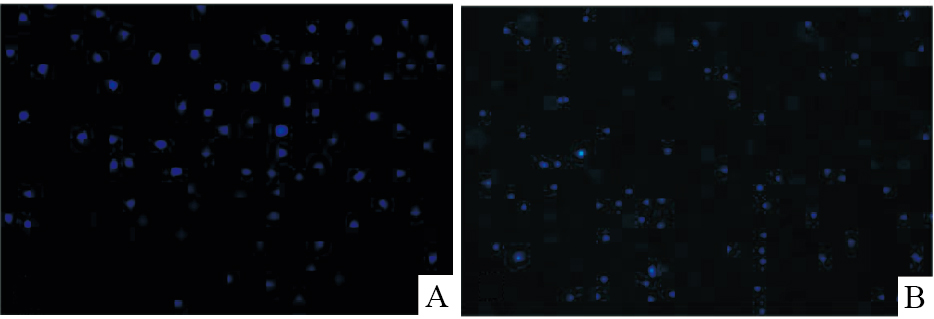
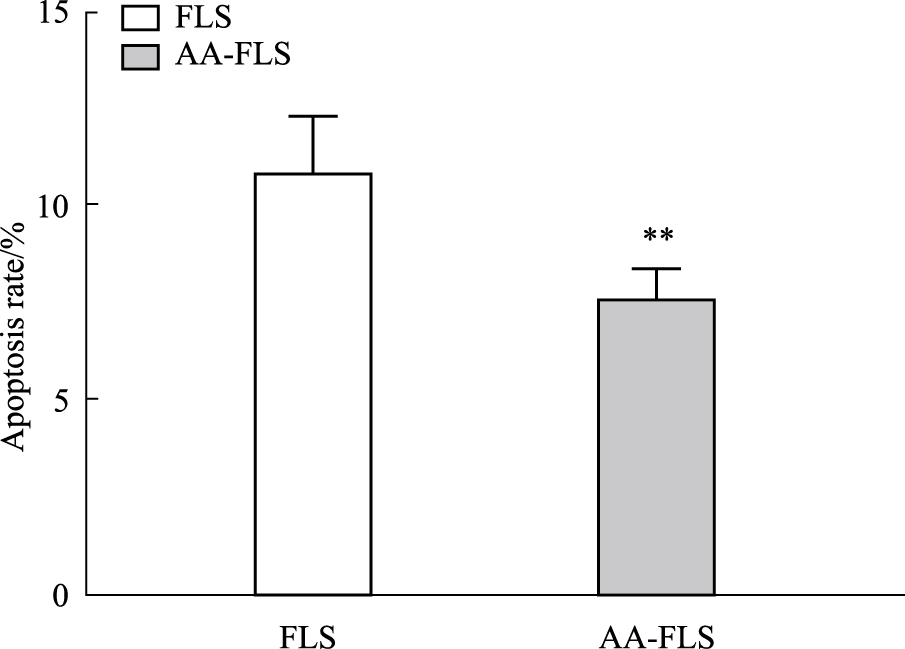
采用Hoechst 33258法分别对正常大鼠FLS和AA-FLS细胞进行染色,在荧光显微镜下观察拍照并记录试验结果。Hoechst 33258为非嵌入型荧光染料,能够在活细胞中DNA聚AT序列富集区域小沟处与DNA结合,从而使细胞核着色。未发生凋亡的活细胞因核DNA结构相对保持完整,与Hoechst 33258染料结合较少,在荧光显微镜下呈现弥散、微弱的淡蓝色荧光。凋亡状态的细胞,由于DNA发生断裂,能够充分与Hoechst 33258染料结合,在荧光显微镜下呈亮蓝色荧光。根据实验结果显示(Fig6、7),正常大鼠FLS细胞在UV显微镜下多数细胞核呈淡蓝色荧光,少量细胞核呈明显亮蓝色荧光,细胞凋亡率为(11.828±1.445)%;AA-FLS细胞呈凋亡抑制趋势,显微镜下观察细胞核呈现弥散状的微弱蓝荧光,极少细胞出现亮蓝色荧光,细胞凋亡率为(7.512±0.824)%,与正常FLS细胞组相比较差异具有统计学意义(P < 0.01)。
|
| Fig.6 Hoechst 33258 stain assay (×200) A:FLS; B:AA-FLS. |
|
| Fig.7 Apoptotic rate in AA-FLS **P < 0.01 vs FLS group |
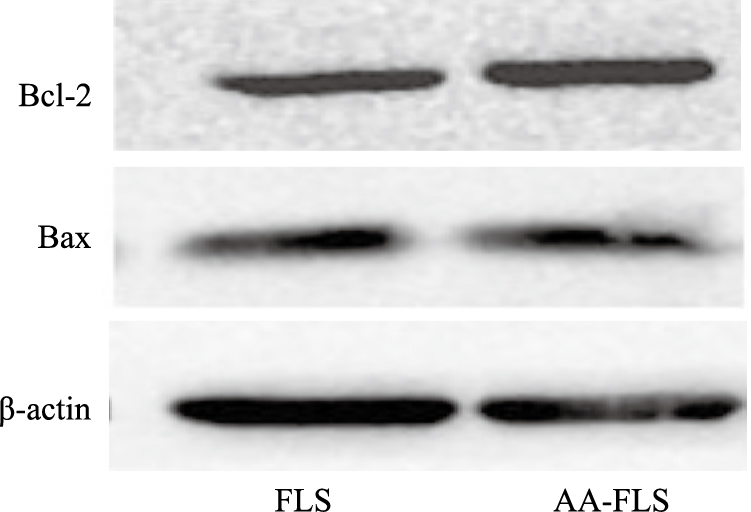
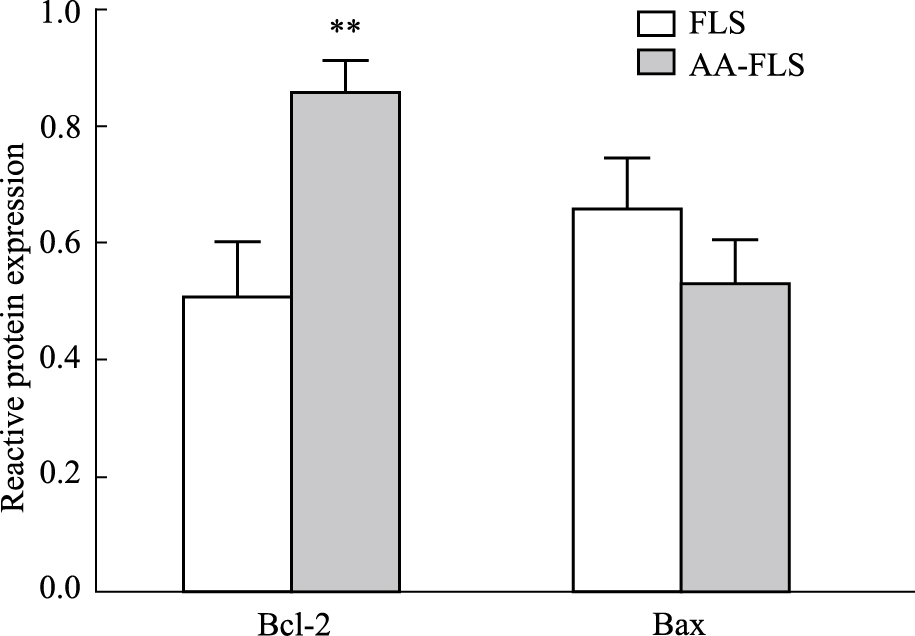
通过Western blot方法,检测AA-FLS和FLS中的线粒体凋亡通路调控蛋白Bcl-2和Bax的表达差异。实验结果显示(Fig8、9),与正常组大鼠FLS比较,AA-FLS中的Bcl-2相对表达量增高,差异有显著性(P < 0.01);Bax的相对表达量呈下降趋势,但结果差异不具有统计学意义(P=0.050 4)。
|
| Fig.8 Expressions of Bcl-2 and Bax in AA-FLS |
|
| Fig.9 Reactive protein expressions of Bcl-2 and Bax in AA-FLS and FLS(±s) **P < |
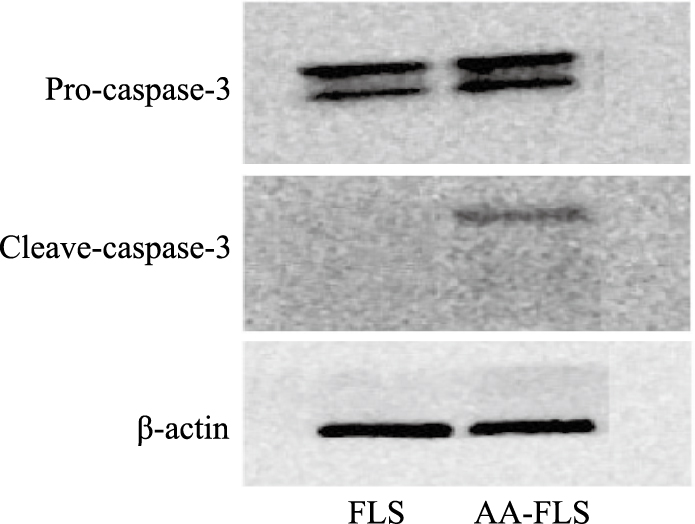
Western blot结果显示,AA-FLS中的Pro-caspase-3蛋白的表达量与正常FLS相比较出现增高现象,但差异无统计学意义;本实验中发现,正常FLS细胞中未表达Cleave-caspase-3蛋白(Fig10)。
|
| Fig.10 Reactive protein expression of Caspase-3 in AA-FLS and FLS |
目前对FLS细胞的原代培养主要有组织块法和胶原酶法[6]。在用组织块法进行原代培养时,由于组织块与培养皿的贴附不牢,容易脱落;组织块大小不易控制,细胞不易从组织块中爬出,大量的细胞间物质会使培养周期延长,极易污染,成功率不高。本实验中采用胶原酶法分离获取原代FLS细胞,需注意分离剪取大鼠滑膜组织时,用PBS缓冲液洗去滑膜组织上的血和油脂,尽量剪碎滑膜物质,胶原酶消化细胞间物质,使FLS细胞释出。使用胶原酶消化滑膜组织,不使用胰酶与胶原酶的混合溶液,因胰酶对细胞损伤较大,使细胞爬出较慢,且爬出后细胞状态不佳。
原代培养初期,FLS细胞增殖缓慢且混有大量巨噬样滑膜细胞,可利用巨噬样滑膜细胞与FLS细胞的贴壁性差异、消化时间不同以及巨噬样滑膜细胞在体外的增殖速度极慢等特性,通过传代纯化FLS细胞。经过传代至第3代之后的FLS细胞增殖速度明显加快,由原代至第2代的5~7 d周期缩短为1~2 d的周期。第5代之后的FLS细胞增殖变慢,细胞出现老化、空泡,变形等现象,贴壁性变差,细胞活性逐渐降低,因此宜使用第3~5代的FLS细胞进行实验。我们通过免疫细胞化学的方法测定细胞对Vimentin和CD68的表达,结合细胞来自于滑膜组织以及细胞形态学的观察,从而鉴别细胞类型。Vimentin为成纤维细胞的特殊标志物,本实验中免疫细胞化学的结果显示,通过胶原酶法分离获得的细胞Vimentin表达阳性,而CD68几乎不表达,证实所培养细胞为滑膜成纤维细胞。
RA是一种多系统的慢性疾病,发病原因至今尚未明确。该病好发于手、腕、足等小关节,对称分布,RA患者会出现不同程度的畸形,是人类致残的主要原因之一[7]。FLS参与了RA病程的各个阶段[8]。异常活化的RA-FLS增殖活跃并且具有抗凋亡的特性,是导致滑膜组织增生的主要原因;各种抗原通过识别结合RA-FLS表面的Toll样受体,触发免疫应答,激活下游信号通路;活化的RA-FLS释放趋化因子,趋化白细胞进入滑膜组织;分泌大量促炎性细胞因子,诱发滑膜炎症;RA-FLS对软骨进行黏附,释放基质金属蛋白酶MMPs降解细胞外基质;诱导破骨细胞的激活与分化,最终骨侵蚀和骨关节的破坏[9]。对RA-FLS的细胞周期测定发现,细胞G2期很短,在无刺激因子干预的条件下呈良性增殖特点[10]。体外培养RA、骨关节炎(osteoarthritis,OA)和创伤性关节炎患者的FLS细胞并比较3种细胞的增殖活性,RA-FLS的增殖程度较OA组和创伤性关节炎组增高[11]。Perlman等[12]取RA和OA患者的滑膜组织进行抗凋亡蛋白Bcl-2的表达测定,Bcl-2在RA患者的滑膜组织中呈高表达,尤其是在CD68阴性表达的位置,即RA患者成纤维样滑膜细胞的Bcl-2表达水平升高,出现凋亡抑制的特性。TNF-α和IL-1β是RA发病过程中的重要细胞因子,不仅能引起和加重炎症反应,还能激活细胞通路刺激FLS细胞增殖,参与了软骨及骨的破坏过程[13, 14]。临床研究表明[15],RA患者血清中的TNF-α和IL-1β含量高于正常人的水平。有实验证明,用RA患者的滑液与正常的FLS细胞共同培养,细胞所分泌的TNF-α和IL-1β水平明显升高,提示活化的RA-FLS细胞可分泌高水平的促炎性细胞因子。因此,在临床病理上RA病人的FLS表现为类肿瘤样异常增殖、抗凋亡、释放高水平的促炎性细胞因子的特性。
佐剂型关节炎(adjuvant arthritis,AA)大鼠与RA患者在临床表现和病理上有相似或相近的特征,该模型复制方法简便、可重复性强、成模率高,经济实用,是RA的理想动物模型。AA大鼠的FLS较RA患者的FLS更易获取,因此,我们对AA-FLS作为体外研究RA发病机制以及抗RA药物筛选的细胞模型可行性进行探讨。本实验通过AA大鼠模型获取的AA-FLS细胞状态良好,具有典型的成纤维细胞形态特征;由CCK-8实验结果可知,AA-FLS在传代培养d 6细胞数量能达到倍增,而正常大鼠FLS细胞数量倍增的时间在7 d以上,AA-FLS增殖活性明显高于正常大鼠FLS;AA-FLS细胞上清液中的TNF-α和IL-β水平高于正常大鼠FLS,提示AA-FLS可分泌高水平的促炎性细胞因子,介导炎症反应和对骨的破坏作用,同时这也是AA-FLS异常增殖的原因之一;对AA-FLS的凋亡状态分析发现,与正常大鼠FLS相比AA-FLS的细胞凋亡率明显降低,同时AA-FLS中抗凋亡蛋白Bcl-2的表达水平明显上调,而Bax的相对表达量有下降的趋势,提示AA-FLS的线粒体凋亡通路受到抑制而呈现抗凋亡的特性。通过实验结果发现,AA-FLS在细胞增殖、细胞因子释放和细胞凋亡等方面均表现出与RA-FLS相似相近的生物特性,因此,AA-FLS可作为体外筛选抗RA药物的细胞模型。
(致谢:本实验在南方医科大学中医药学院中药药理实验室完成,感谢邓秋狄和白殊同对文章相关工作的支持。)
| [1] | Escalante A,Del Rincon I.The disablement process in rheumatoid arthritis[J]. Arthr Rheumat,2002,47(3):333-42. |
| [2] | Lee Y A,Choi H M,Lee S H,et al.Synergy between adiponectin and interleukin-1β on the expression of interleukin-6,interleukin-8,and cyclooxygenase-2 in fibroblast-like synoviocytes[J]. Exp Mol Med,2012,44(7):440-7. |
| [3] | Bartok B,Firestein G S.Fibroblast-like synoviocytes:Key effector cellsin rheumatoid arthritis[J]. Immunol Rev,2010,233(1):233-55. |
| [4] | 佟 丽,辛增辉,陈育尧,等.Mtb诱导的SD大鼠佐剂性关节炎模型的建立及评价[J].中国药理学通报,2009,25(2):259-63. Tong L,Xin Z H,Chen Y Y,et al.Establishment and evaluation of adjuvant-induced arthritis animal model by Mtb in Sprague-Dawley rats[J].Chin Pharmaclo Bull,2009,25(2):259-63. |
| [5] | 陈佩虹,陈育尧,林晓春,等.热杀死结合分支杆菌H37Ra诱导的SD大鼠佐剂性关节炎模型研究[J].中国药理学通报,2011,27(1):129-33. Chen P H,Chen Y Y,Lin X C,et al.Study of adjuvant-induced arthritis animal model by Mtb in Sprague-Dawley rats[J].Chin Pharmaclo Bull,2011,27(1):129-33. |
| [6] | 丁 娟,王志军,董晓薇,等.RA滑膜成纤维细胞的原代培养及鉴定[J].现代生物医学进展, 2012,36:7008-11. Ding J,Wang Z J,Dong X W,et al.Primary culture and identification about fibroblast-like synoviocytes of RA[J].Prog Mod Biomed,2012,36:7008-11. |
| [7] | Moroin L,Bianchi I,Lieo A.Ceoepidemiology,gender and autoimmune diseas[J].Autoimmun Rev, 2012,11(6-7):A386-A92. |
| [8] | Jie L,Du H,Huang Q,et al.Tanshinone IIA induces apoptosis in fibroblast-like synoviocyte in rheumatoid arthritis via blockade of the cell cycle in th G2/M phase and a mitochondrial pathway[J]. Biol Pharm Bull,2014,37(8):1366-72. |
| [9] | Yamanishi Y,Firestein G S.Pathogenesis of rheumatoid arthritis:the role of synoviocytes[J].Rheum Dis Clin North Am,2001,27(2):355-71. |
| [10] | 舒 强,李兴福,刘花香,李 栋.类风湿性关节炎成纤维样滑膜细胞增殖特性的体外研究[J].山东大学学报(医学版),2006,44(11):1095-9. Shu Q,Lin X F,Liu H X,Li D.Proliferation of fibroblast-like synovial cells in patients with rheumatoid arthritis in vitro[J].J Shangdong Univ (Health Sci),2006,44(11):1095-9. |
| [11] | 肖楚吟,潘云峰,吴玉琼,等.类风湿性关节炎成纤维样滑膜细胞体外增殖活性的研究[J].中华关节外科杂志(电子版),2010,5:631-6. Xiao C Y,Pan Y F,Wu Y Q,et al.Cell proliferation activity of rheumatoid arthritis fibroblast-like synoviocytes in vitro[J].Chin J Surg(Electronic Edit), 2010,5:631-6. |
| [12] | Perlman H,Georganas C,Pagliari L J,et al.Bcl-2 expression in synovial fibroblasts is essential for maintaining mitochondrial homeostasis and cell viability[J].J Immunol,2000,164(10):5227-35. |
| [13] | Vuolteenaho K,Moilanen T,Hamalainen M,Moilanen E.Regulation of nitric oxide production in osteoarthritic and rheumatoid cartilage. Role of endogenous IL-1 inhibitors[J]. Scand J Rheumatol,2003,32(1):19-24. |
| [14] | Jagetia G C,Aggarwal B B.Spicing up of the immune system by curcumin[J]. J Clin Immunol,2007,27(1):19-35. |
| [15] | Casnici C,Lattuada D,Tonna N,et al.Optimized "in vitro" culture conditions for human rheumatoid arthritis synovial fibroblastis[J].Mediators Inflamm,2014:702057. |

