


2. 河北省人民医院内分泌科, 河北 石家庄 050051
2. Dept of Endocrinology, Hebei General Hospital, Shijiazhuang 050051, China
长期高脂饮食可引发Ⅱ型糖尿病、肥胖、高血压、高血脂、心脏病等一系列胰岛素抵抗综合征,目前认为,高脂环境是诱发胰岛素抵抗的独立危险因素之一。肝脏是脂类代谢的重要靶器官,也是胰岛素作用的主要器官,肝脂代谢失调是引起机体代谢异常,导致胰岛素抵抗的重要原因之一[1, 2]。氧化苦参碱是豆科植物苦参的主要生物碱之一,主要用于乙肝、脂肪肝的治疗。本实验采用高脂喂养ApoE-/-小鼠建立胰岛素抵抗模型,研究高脂喂养后对肝脂质代谢相关蛋白(脂质转运、脂质氧化和脂质合成蛋白)基因表达的变化,探讨氧化苦参碱干预对胰岛素抵抗小鼠脂代谢的作用机制。
1 材料与方法 1.1 药品与试剂氧化苦参碱(苦参素胶囊)购于正大天晴药业股份有限公司;胰岛素放射免疫试剂盒购自上海研晶生物公司;脂蛋白酯酶(LPL)、脂肪酸转位酶(FAT/CD36)、肉毒碱棕榈酰基转移酶1(CPT1)、解偶联蛋白2(UCP2)、胆固醇调节元件结合蛋白-1c(SREBP-1c)、脂肪酸合成酶 (FAS)、乙酰辅酶A羧化酶(ACC)抗体均购自Abcam公司;引物由上海生工生物公司合成。
1.2 仪器DFM-96型放射免疫γ计数器购自众成机电技术公司;7300荧光定量PCR仪购自ABI公司;凝胶成像分析仪,购自美国Biorad公司。
1.3 实验动物SPF级C57BL/6J小鼠17只、SPF级ApoE-/-小鼠68只,均为♂,18~20 g,由北京大学医学部提供,许可证号SCXK(京)2011-0012。饲养于屏障系统,光照12 h/d,温度20~26℃,相对湿度40%~70%。
1.4 实验饲料基础饲料热量: 脂肪10.3%,蛋白质24.2%,碳水化合物65.5%;高脂饲料热量:脂肪59.8%,蛋白质20.1%,碳水化合物20.1%。
1.5 方法 1.5.1 实验分组及给药17只C57BL/6J小鼠设为正常组(NC),给予基础饲料;68只ApoE-/-小鼠设为高脂组,给予高脂饲料,每周测定小鼠体重,喂养16周后,随机分为4组:模型组(IR)、氧化苦参碱低剂量组(OXYL、25 mg·kg-1·d-1)、中剂量组(OXYM、50 mg·kg-1·d-1)、高剂量组(OXYH、100 mg·kg-1·d-1),连续给药8周,模型组和正常组给以纯水。给药结束后,各组随机取7只小鼠进行高胰岛素-正葡萄糖钳夹试验[3],计算葡萄糖输注率(GIR),评价胰岛素敏感性。剩余10只小鼠采集血清、肝,-80℃保存备用。
1.5.2 检测血清生化指标采用全自动生化分析仪检测空腹血糖(FBG)、甘油三酯(TG)、胆固醇(TC)、脂肪酸(FFA),放射免疫法检测空腹胰岛素(FINS),计算胰岛素抵抗指数(HOMA-IR)=空腹血糖×空腹胰岛素/22.5。
1.5.3 实时荧光定量PCR技术检测肝组织LPL、FAT/CD36、CPT1、UCP2、SREBP-1c、FAS、ACC mRNA表达肝组织匀浆后,TRIzol法提取总RNA,按照说明书进行反转录,荧光定量PCR仪进行扩增。引物序列:
LPL引物:上游:5′-AACTGCCACTTCAACCACAG-3′,下游:5′-CCAACTCTCATACATTCCCGT-3′,产物片段 78 bp;FAT/CD36引物:上游:5′-ACCAGAAATAGACCCTTGTGA-3′,下游:5′-ATGTGTGTGAGAGTTGAAACG-3′,产物片段145 bp;CPT1引物:上游:5′-TTATCGTGGTGGTGGGTGT -3′,下游:5′-CGCTCACAATGTTCTTCGTCT-3′,产物片段132 bp; UCP2引物:上游:5′-GATACTCTCCTGAAAGCCAACC-3′,下游:5′-CGAAGGCAGAAGTGAAGTGG-3′,产物片段64 bp;SREBP-1c引物:上游:5′-CAAAGAGGAGATTGGCATTG-3′,下游:5′-TGCGTGTGGAGAAGTAGATGT-3′,产物片段86 bp;FAS引物:上游:5′-TCGCCTATGGTTGTTGACC-3′,下游:5′-ATGGTTTCACGACTGGAGG-3′,产物片段132 bp; ACC引物:上游:5′-CAGGTTCTTTGTTCGTGCG-3′,下游:5′-CTTCCAGGAGCAGTCGTTC-3′,产物片段101 bp; GAPDH引物:上游:5′-GACCCCTTCATTGACCTCAAC-3′,下游:5′-CGCTCCTGGAAGATGGTGAT-3′,产物片段138 bp;以GAPDH为内参基因,采用2-△△Ct 法计算目的基因相对表达量。
1.5.4 Western blot方法检测肝组织LPL、FAT/CD36、CPT1、UCP2、SREBP-1c、FAS、ACC蛋白表达肝组织匀浆后,提取总蛋白,10% SDS聚丙烯酰胺凝胶电泳,采用半干转膜法转膜至PVDF膜,洗膜,加入一抗孵育,洗膜,加入相应的二抗反应,发光。对条带进行扫描,软件分析条带的吸光度值,以目的条带和内参照吸光度值的比值用于统计分析。
1.5.5 统计学处理用SPSS 13.0统计软件分析数据,各项数据以x±s表示,组间比较采用单因素方差分析,两组间各指标比较采用t检验。
2 结果 2.1 各组小鼠体重及血清生化指标比较与正常组相比,模型组小鼠体重(BW)、FBG、TC、TG、FFA、FINS、HOMA-IR均明显升高(P < 0.05)。与模型组相比,氧化苦参碱组TC、TG、FFA、HOMA-IR均明显降低(P < 0.05),中、高剂量组BW、FBG、FINS明显降低(P < 0.05)。见Tab1。
| Group | BW/g | FBG/mmol·L -1 | TC/mmol·L -1 | TG/mmol·L -1 | FFA/mmol·L -1 | FINS/mU·L -1 | HOMA-IR |
| NC | 33.4±2.76 | 5.10±0.38 | 2.02±0.24 | 0.65±0.08 | 1.90±0.31 | 25.86±3.27 | 5.89±1.00 |
| IR | 46.07±3.34 * | 7.41±0.88 * | 12.16±8.37 * | 1.69±0.78 * | 3.17±0.46 * | 96.05±9.85 * | 31.5±4.3 * |
| OXYL | 44.2±3.18 | 6.91±0.97 | 10.41±1.26 # | 1.26±0.15 # | 2. 65±0.41 # | 88.57±8.78 | 27.05±3.52 # |
| OXYM | 42.58±3.82 # | 5.96±0.41 # | 9.87±1.04 # | 1.18±0.20 # | 2.45±0.29 # | 82.72±8.27 # | 21.84±1.87 # |
| OXYH | 41.14±3.12 # | 5.75±0.77 # | 8.81±0.72 # | 1.00±0.16 # | 2.23±0.29 # | 67.48±9.33 # | 17.27±3.59 # |
| * P <0.05 vs NC group; # P <0.05 vs IR group | |||||||
与正常组相比,模型组小鼠GIR明显降低(P < 0.05),与模型组比较,氧化苦参碱组GIR明显升高(P < 0.05)。见Tab2。
| Group | GIR |
| NC | 26.65±2.88 |
| IR | 16.46±1.62 * |
| OXYL | 18.53±1.62 # |
| OXYM | 20.13±1.84 # |
| OXYH | 21.33±2.26 # |
| * P <0.05 vs NC group; # P <0.05 vs IR group | |
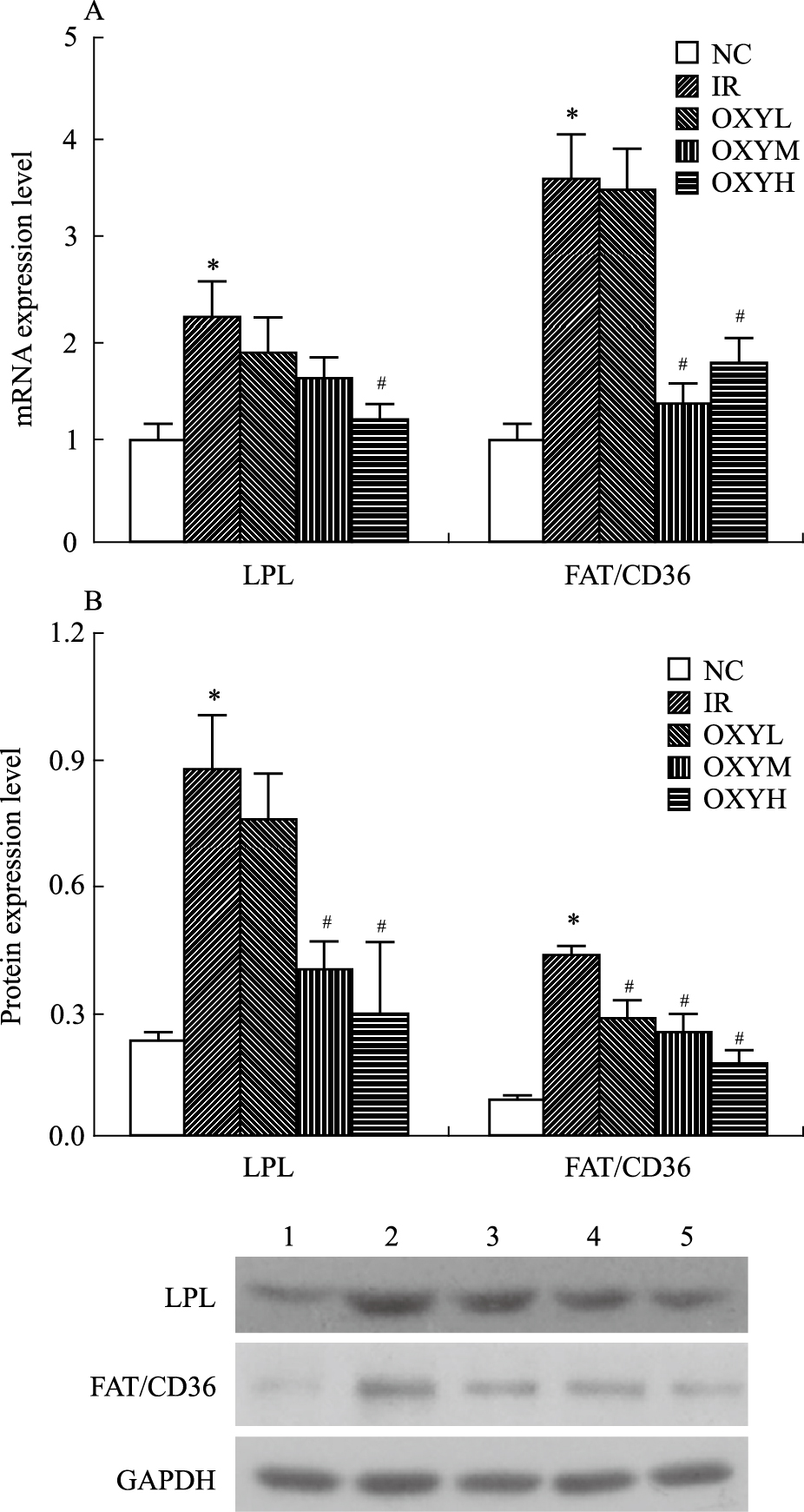
与正常组相比,模型组小鼠肝LPL、FAT/CD36 mRNA和蛋白表达均明显升高(P < 0.05)。与模型组相比,高剂量组 LPL、FAT/CD36 mRNA和蛋白表达均明显降低(P < 0.05)。中剂量组LPL、FAT/CD36蛋白表达均明显降低(P < 0.05)。见Fig1。
|
| Fig.1 mRNA(A) and protein expression(B)of LPL,FAT/CD36 among groups 1.NC;2.IR;3.OXYL;4.OXYM;5.OXYH.*P < 0.05 vs NC group;#P < 0.05 vs IR group |
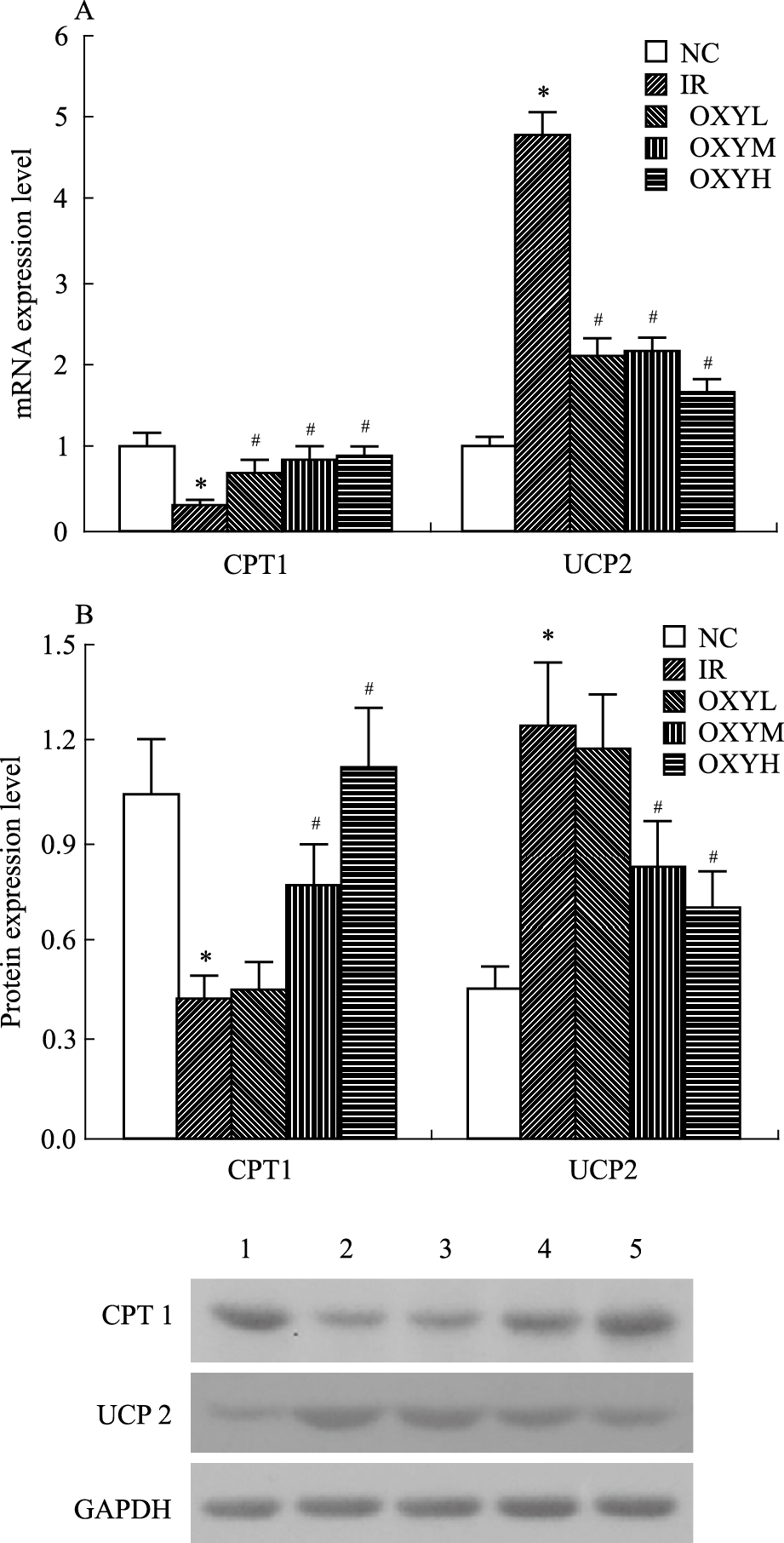
与正常组相比,模型组小鼠肝CPT1 mRNA和蛋白表达明显降低、UCP2 mRNA和蛋白表达明显升高(P < 0.05)。与模型组相比,氧化苦参碱组CPT1 mRNA表达明显上升、UCP2 mRNA表达明显降低(P < 0.05)。中、高剂量组CPT1蛋白表达上升,UCP2蛋白表达下降(P < 0.05)。见Fig2。
|
| Fig.2 mRNA(A) and protein expression(B)of CPT1,UCP2 among groups 1.NC;2.IR;3.OXYL;4.OXYM;5.OXYH. *P < 0.05 vs NC group;#P < 0.05 vs IR group |
与正常组相比,模型组小鼠肝SREBP-1c、FAS、ACC mRNA和蛋白表达均明显升高(P < 0.05)。与模型组相比,氧化苦参碱组SREBP-1c mRNA和蛋白表达均明显降低(P < 0.05),氧化苦参碱组FAS mRNA表达均明显降低(P < 0.05),中、高剂量组FAS蛋白表达均明显降低(P < 0.05),高剂量组ACC mRNA和蛋白表达均明显降低(P < 0.05)。见Fig3。

|
| Fig.3 mRNA(A) and protein expression(B)of SREBP-1c,FAS,ACC among groups 1.NC;2.IR;3.OXYL;4.OXYM;5.OXYH;*P < 0.05 vs NC group;#P < 0.05 vs IR group |
胰岛素抵抗是高血脂、2型糖尿病、肥胖、高血压等代谢疾病的共同病理基础。因此,如能在早期对胰岛素抵抗进行干预和治疗,则可有效延缓或降低多种代谢性疾病的发生、发展。ApoE-/-小鼠为载脂蛋白E(ApoE)基因敲除小鼠,具有高胆固醇的特性,常被用于动脉粥样硬化的研究。本研究采用高脂喂养ApoE-/-小鼠,发现小鼠具备了高血糖、高血脂、高胰岛素血症等明显的胰岛素抵抗特征,同时钳夹试验也证实了高脂喂养的ApoE-/-小鼠产生了明显的胰岛素抵抗,与金鑫等[4]报道一致。氧化苦参碱治疗糖尿病并发症、脂肪肝、乙肝等已有大量报道[5, 6],给予氧化苦参碱干预8周后,可使小鼠体重降低,同时明显降低血糖、血脂、胰岛素,改善ApoE-/-小鼠的胰岛素抵抗,提示了氧化苦参碱具有治疗糖尿病、心血管病等代谢性疾病的潜力。
肝脏是表现胰岛素抵抗的主要器官,也是合成、释放各种脂蛋白及脂代谢酶类的重要靶器官。脂代谢主要包括甘油三酯代谢、胆固醇及其酯的代谢、糖脂代谢等,其在肝中代谢主要过程为:(1)转运:含甘油三酯的脂蛋白在脂蛋白酯酶(LPL)作用下分解为游离脂肪酸,长链游离脂肪酸进一步在脂肪酸转位酶 (FAT/CD36)作用下进入肝细胞,转变为活性形式;如果发生紊乱,将导致脂肪酸代谢异常[7, 8]。(2)氧化:在肉毒碱棕榈酰基转移酶1(CPT1)作用下长链脂酰辅酶转运进入线粒体,在肝线粒体内氧化利用;(3)合成:肝细胞内亦可以合成一部分脂质。上述过程中每个环节的异常均可引起甘油三酯,继而诱导胰岛素抵抗引起多种代谢综合征疾病。
对肝细胞脂转运、氧化、合成3个方面对高脂喂养的ApoE-/-小鼠导致胰岛素抵抗进行了机制探讨:(1)研究结果显示,肝组织中转运关键酶LPL、FAT/CD36在高脂喂养的ApoE-/-小鼠中表达升高,表明血中的脂类在上调的转运蛋白酶作用下更多的进入肝组织,在胰岛素抵抗中发挥重要作用;(2)CPT1是线粒体β氧化的限速关键酶[9]。其中CPT1在肝组织高表达,结果显示高脂喂养的ApoE-/-小鼠肝组织中CPT1表达下降,表明下调的CPT1破坏了线粒体氧化脂肪酸能力,致使脂质沉积;UCP2是解偶联蛋白(UCPs)家族蛋白之一,是位于线粒体内膜的一类保守的家族蛋白,在激活剂如游离脂肪酸作用下,UCP2被活化,导致线粒体解偶联,降低ATP产生[10]。本实验结果显示了胰岛素抵抗小鼠肝组织UCP2表达上升;(3)肝组织内脂质合成增加是促进肝细胞脂质沉积的重要机制之一。SREBP-1c是肝细胞内调控脂肪酸合成的转录因子,参与调控下游脂肪酸合成酶、乙酰辅酶A羧化酶等,控制脂肪酸的合成[11]。研究表明高脂喂养的ApoE-/-小鼠肝SREBP-1c及下游的FAS、ACC基因均表达升高,提示了高脂喂养可使ApoE-/-小鼠肝脂质合成增加。
氧化苦参碱可以抑制肝脂转运蛋白LPL、FAT/CD36表达,调节线粒体氧化关键蛋白CPT1、UCP2表达,抑制合成蛋白SREBP-1c、FAS、ACC表达,从脂转运、氧化、合成3个环节相关基因的表达较全面的调节肝脂质代谢,改善胰岛素抵抗,具有重要的临床价值及社会意义,也为治疗代谢性疾病提供了新的思路。
(致谢:本研究课题主要在河北省人民医院老年医学重点实验室完成,衷心感谢实验室人员和同学的帮助,尤其感谢宋光耀教授和王超副研究员的支持与指导!)
| [1] | McGarry J D. Banting lecture 2001:dysregulation of fatty acid metabolism in the etiology of type2 diabetes[J]. Diabetes, 2002, 51(1):7-18. |
| [2] | 李秋云, 王彩宁, 史丽萍,郭智慧.2型糖尿病及前期患者胰岛素抵抗与脂代谢紊乱的关系[J].中国全科医学,2011,14(8C):2716-9. Li Q Y,Wang C N,Shi L P,et al. Relationship between insulin resistance and dyslipidemia in patients with prediabetes and type 2 diabetes mellitus[J]. Chin General Practice, 2011,14(8C):2716-9. |
| [3] | 臧莎莎,刘颐轩,宋光耀,王 超.津力达对胰岛素抵抗大鼠骨骼肌脂质沉积及线粒体功能的影响[J].中成药,2014,36(7):1371-76. Zang S S,Liu Y X,Song G Y, Wang C.Effect of Jinlida granules on accumulation in skeletal muscle and mitochondrial function in insulin resistant rats[J].Chin Tradit Patent Med, 2014,36(7):1371-76. |
| [4] | 金 鑫,张彦芬,秘 尧,等.津力达对高脂诱导的胰岛素抵抗ApoE-/-小鼠骨骼肌胆固醇相关基因的影响[J].中国药理学通报,2014,30(11):1600-4. Jin X,Zhang Y F,Mi Y,He Q L,et al.Effect of Jinlida on cholesterol related genes genes in the skeletal muscle of fat-induced insulin-resistant ApoE-/- mice[J].Chin Pharmacol Bull,2014,30(11):1600-4. |
| [5] | 杨中林.氧化苦参碱在制备防治糖尿病肾病药物中的应用:中国,CN103432124A[P], 2013-12-11. Yang Z L, The effect of Oxymatrine on the prevention and treatment of diabetic nephropathy:Chinese Patent, CN103432124A[P], 2013-12-11. |
| [6] | 梁建新,屈杏芬,曾文铤,等.氧化苦参碱治疗慢性乙型肝炎肝纤维化的作用机制[J].中国老年学杂志,2010,30(11):1505-8. Liang J X,Qu X F,Zeng W T,et al. The mechanism of Oxymatrine treated chronic hepatic fibrosis[J].Chin J Gerontol, 2010,30(11):1505-8. |
| [7] | Kersten S.Physiological regulation of lipoprotein lipase[J].Biochim Biophys Acta,2014,1841(7):919-33. |
| [8] | Miquilena-Colina M E, Lima-Cabello E, Sánchez-Campos S, et al.Hepatic fatty acid translocase CD36 upregulation is associated with insulin resistance, hyperinsulinaemia and increased steatosis in non-alcoholic steatohepatitis and chronic hepatitis C[J].Gut,2011,60(10):1394-402. |
| [9] | Townsend K L, An D, Lynes M D, et al. Increased mitochondrial activity in BMP7-treated brown adipocytes, due to increased CPT1-and CD36-mediated fatty acid uptake[J].Antioxid Redox Signal. 2013,19(3):243-57. |
| [10] | Souza B M, Assmann T S, Kliemann L M,et al. The role of uncoupling protein 2(UCP2) on the development of type 2 diabetes mellitus and its chronic complications[J].Arq Bras Endocrinol Metabol,2011,55(4):239-48. |
| [11] | Choi Y J,Shin H S, Choi H S,et al. Uric acid induces fat accumulation via generation of endoplasmic reticulum stress and SREBP-1c activation in hepatocytes[J].Lab Invest,2014,94(10):1114-25. |

