


2. 遵义医学院药理教研室, 基础药理省部共建教育部重点实验室, 贵州 遵义 563000;
3. 重庆科瑞制药(集团)有限公司, 重庆 400060
2. Dept of Pharmacology and the Key Laboratory for Basic Pharmacology of Ministry of Education, Zunyi Medical College, Zunyi Guizhou 563000, China;
3. Chongqing Kerui Pharmaceutical(Group) Co. Ltd., Chongqing 400060, China
血管病变是糖尿病的主要并发症之一。糖尿病导致的微血管病变与糖尿病视网膜病、糖尿病肾病、糖尿病心肌病以及糖尿病神经病变等的发生关系密切[1];大血管病变则可引起高血压、动脉粥样硬化及外周动脉疾病[2]。糖尿病血管病变的发生受多种因素影响,持续高血糖水平所致的血管内皮损伤和功能紊乱是其发生的最主要病理生理基础[3]。内皮损伤的初始表现之一为乙酰胆碱(acetylcholine,ACh)诱导的内皮依赖性舒张作用改变,该作用主要由内皮依赖性松弛因子(EDRF),即一氧化氮(nitric oxide,NO)介导。NO对维持正常内皮结构和功能具有重要意义。另有研究发现,过氧化物酶增殖物激活受体β(peroxisome proliferator-activated receptor β,PPAR β)特异性激动剂GW0742能够抑制血管紧张素II诱导的动脉粥样硬化[4],改善自发性高血压大鼠内皮功能[5];在糖尿病及其并发症中,GW0742对糖尿病肾病具有保护作用[6],可促进糖尿病大鼠缺血后肢的骨骼肌血管生成[7],但对于GW0742在高糖损伤内皮的作用及可能机制目前国内外研究较少。本研究拟采用高糖孵育大鼠胸主动脉建立糖尿病血管内皮损伤模型[8],对GW0742的相关作用及可能机制进行初步探索。
1 材料与方法 1.1 材料 1.1.1 实验动物SPF级♂ SD大鼠,体质量240~260 g,由重庆医科大学实验动物中心提供[许可证号:SYXK(渝)2010-0001]。
1.1.2 仪器及试剂GW0742购自Cayman公司,用0.1% DMSO溶解后,双蒸水稀释至所需浓度;苯肾上腺素(phenylephrine,PE)购自上海禾丰制药有限公司;ACh、 DMSO、 BCA 蛋白浓度测定试剂盒和RIPA裂解液均购自江苏碧云天生物技术公司;NO含量测定试剂盒购自南京建成生物技术公司;TRIzol、逆转录试剂盒和SYBR Green Supermix购自TaKaRa生物试剂公司;兔抗PPAR β多克隆抗体购自Santa Cruz;兔抗Phospho-NF-κB p65抗体购自Cell Signaling;内皮型一氧化氮合酶(endothelial nitric oxide synthase,eNOS)多克隆抗体购自Abcam公司。其余试剂均为国产分析纯。
BL-420S生物机能实验系统、HW-400恒温平滑肌槽(成都泰盟科技有限公司);肌张力换能器(5 g)(中国北京航天医学工程研究所);CFX ConnectTN定量PCR检测系统和凝胶成像图像分析系统(Bio-Rad公司)。
1.2 方法 1.2.1 血管条制备将SD大鼠脱颈椎处死,取出胸主动脉,剥离周围结缔组织,制成长3~5 mm的血管环,置于含Krebs液[成分(mmol ·L-1):NaCl 119,KH2PO4 1.2,CaCl2 2.5,KCl 4.7,MgSO4 1.2,NaHCO3 25.0,Glucose 11,pH 7.4] 20 mL 的水浴槽中,恒温(37.0±0.5)℃,持续通以0.95 O2+0.05 CO2混合气体。
1.2.2 内皮依赖性舒张功能测定血管张力经张力换能器连接于BL-420S生物信息采集处理系统,前负荷1 g,平衡1 h(每隔15 min更换 Krebs液一次)后,给予PE 10 μmol·L-1预收缩血管,达到坪值并稳定后,加入ACh 10 μmol·L-1验证内皮完整性(舒张率达到60%~90%认定内皮功能完整)[9]。本实验中ACh舒张率为79.4%±5.4%。Krebs液反复冲洗移去药物,平衡30 min后,再次用PE预收缩血管。换液,然后将血管条分别置于含不同药物的Krebs液中孵育6 h,再次给予PE收缩血管,达到孵育前相似的收缩坪值并稳定后,以累积浓度法给予ACh(按0.5对数单位递增,0.001~30 μmol·L-1),观察血管的舒张反应,计算血管最大舒张作用与PE收缩力的百分比(血管的最大舒张效应,即Emax)和ACh产生50%最大舒张效应浓度的负对数(-log IC50)。
1.2.3 实验分组分为5组:① 正常对照组(NG):正常Krebs液(含葡萄糖11 mmol·L-1)+甘露醇44 mmol·L-1;② 高糖模型组(HG):Krebs液中含葡萄糖55 mmol·L-1;③、④、⑤不同浓度GW0742(0.01、0.1、1 μmol·L-1)给药组:HG条件下加入不同浓度GW0742。每组重复6次。
1.2.4 组织病理学检测血管条孵育6 h后,用4%的多聚甲醛浸泡固定,石蜡包埋,作4 μm冠状切片,HE染色,于高倍镜下观察血管形态学变化。
1.2.5 qRT-PCR法检测血管PPAR β、NF-κB p65、eNOS的mRNA表达参照GenBank中大鼠的基因序列合成引物(由TaKaRa生物技术公司合成)(引物序列见Tab1)。用TRIzol提取组织总RNA,测定RNA浓度,按照1 g/20 L反应体系进行逆转录合成cDNA,利用SYBR Green荧光技术,在定量PCR仪器上按如下条件进行扩增:95℃ 30 s;95℃ 5 s;60℃ 30 s,40个循环。以β-actin作为内参,对Ct值进行统计,根据相对定量计算公式分析结果。每组重复3次。
| Name | Primer sequence | Product/bp |
| PPAR β | Forward 5′-CTGGCAGAACCCAGTACCAG-3′ | |
| Reverse 3′-GTGAGCCGGTGTCATGGTTA-5′ | 130 | |
| NF-κB p65 | Forward 5′-AACGCGTCCAACCTGAAGAT-3′ | |
| Reverse 3′- TGTCTGTGAACATCCGTGGG-5′ | 128 | |
| eNOS | Forward 5′-GATTCTGCCAGTGGGAGCC -3′ | |
| Reverse 3′-CACATTGGTGGCATCCTTCC -5′ | 93 | |
| β-actin | Forward 5′-GCAGGAGTACGATGAGTCCG-3′ | |
| Reverse 3′-ACGCAGCTCAGTAACAGTCC-5′ | 74 |
血管组织液氮冷冻后匀浆提取总蛋白,用BCA蛋白浓度检测试剂盒检测蛋白浓度。取30 μg蛋白进行SDS-聚丙烯酰胺电泳分离,转移至PDVF膜上,5% BSA封闭2 h,加入一抗(β-actin按1:1 000稀释,其余均按1:500稀释),4℃摇床过夜,加入辣根过氧化物酶标记的二抗(1:3 000稀释)。用发光液(Advanstor 公司)显色,凝胶成像仪成像后用Image Lab软件(Bio-Rad)分析结果。每组重复3次。
1.2.7 NO含量测定按试剂盒说明书操作,于550 nm波长下,用硝酸还原法测定血管组织匀浆上清液NO含量。NO含量计算:NO含量(μmol·g-1 Pro)=(测定OD值-空白OD值)/(标准OD值-空白OD值)× 20(μmol·L-1)/待测样本蛋白浓度(g Pro·L-1)。
1.3 统计学处理所有实验数据均用x±s表示,用SPSS 20.0统计软件进行分析,组间比较采用单因素方差分析。
2 结果 2.1 GW0742对高糖损伤胸主动脉内皮依赖性舒张作用的影响大鼠胸主动脉在高糖环境下孵育6 h后,PE的收缩力为(0.66±0.12)g,与NG组(0.63±0.10)g比较差异无显著性(P>0.05),提示本实验条件下,高糖对PE诱导的血管收缩可能没有影响;高糖环境使ACh诱导的内皮依赖性舒张作用明显减弱(P<0.01),Emax和-lg IC50分别降低了78.3%和214.5%;低浓度GW0742(0.01 μmol·L-1)对高糖损伤的ACh舒张作用改善无显著性(P>0.05);但0.1和1 μmol·L-1的GW0742使ACh的Emax分别增加了98.2%、347.6%(P<0.01),-lg IC50分别增加了106.2%、191.8%(P<0.05),1 μmol·L-1 的GW0742甚至使ACh的作用基本恢复到正常对照组水平(Fig1,Tab2)。

|
| Fig.1 Effects of GW0742 on endothelium-dependentrelaxation of acetylcholine under HG(x±s, n=6) A: the typical traces of the dose-response relationship for acetylcholine (ACh) on rat aorta; B: the dose-response curve of ACh on aortic rings. PE: phenylephrine; NG: glucose at 11 mmol· L-1+mannitol 44 mmol·L-1; HG: glucose at 55 mmol·L-1.*P<0.05,**P<0.01 vs NG;#P<0.05,##P<0.01 vs HG. |
| Group | Emax/% | -log IC 50 |
| NG | 77.22±4.56 | 5.88±0.08 |
| HG | 16.73±5.59 ** | -6.73±5.43 ** |
| HG+GW0742/0.01 μmol·L -1 | 22.25±3.45 | -1.74±2.28 |
| HG+GW0742/0.1 μmol·L -1 | 33.17±4.38 ## | 0.42±2.26 # |
| HG+GW0742/1 μmol·L -1 | 74.88±7.88 ## | 6.18±0.5 ## |
| E max: the maximal relaxation effect of acetylcholine; -log IC 50: the negative log molar concentration of acetylcholine for inducing 50% of Emax; NG: glucose at 11 mmol· L -1+mannitol 44 mmol·L -1; HG: glucose at 55 mmol·L -1. ** P<0.01 vs NG; # P<0.05, ## P<0.01 vs HG | ||
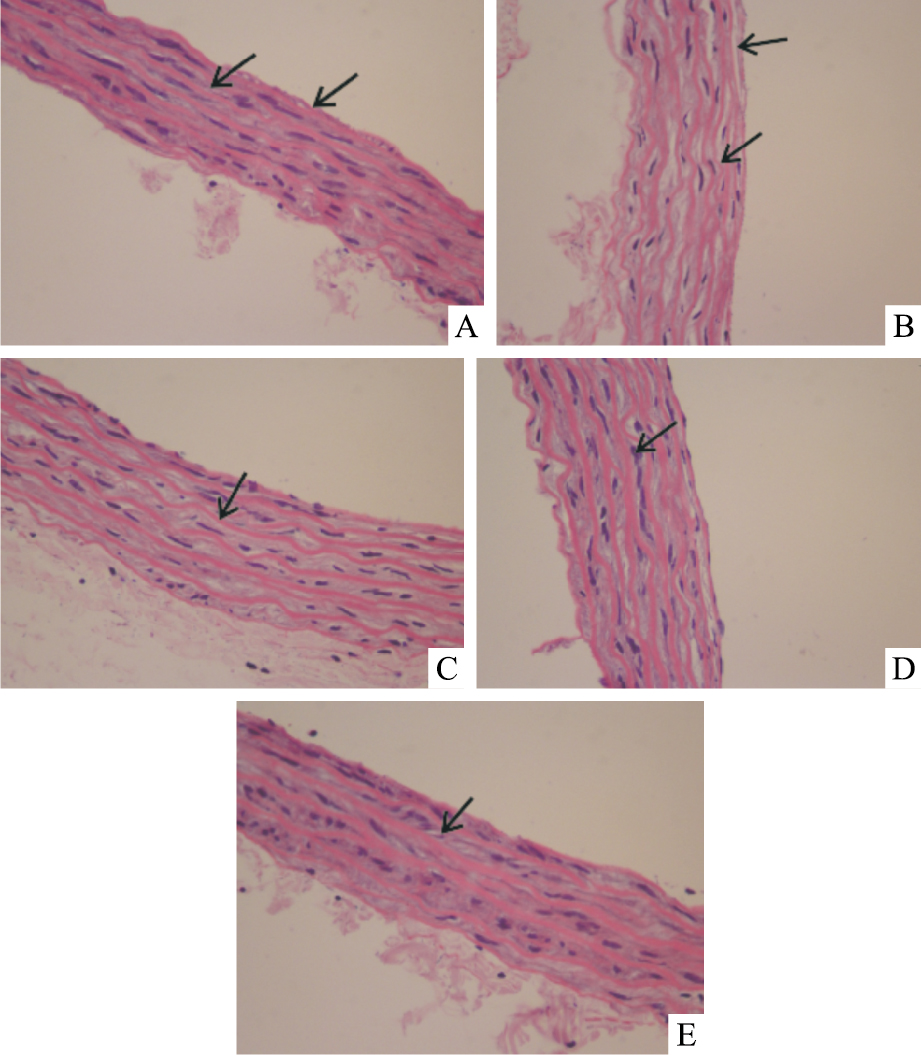
正常血管内皮细胞完整平坦,内外弹力层连 接紧密,血管平滑肌细胞排列整齐,血管结构清晰完整(Fig2A);高糖孵育后的血管内皮细胞受损,内弹性膜断裂,内层平滑肌细胞排列疏松紊乱(Fig2B);给予GW0742后,血管形态学结构较HG组明显改善,内皮细胞损伤改善,内弹性膜断裂减少,平滑肌排列较整齐,高剂量GW0742(1 μmol·L-1)干预后血管形态与正常血管基本相似(Fig2C,D,E)。
|
| Fig.2 Effects of GW0742 on morphologicalchanges of aortic rings under HG(HE, 400×) A: NG (glucose at 11 mmol·L-1+mannitol 44 mmol·L-1); B: HG (glucose at 55 mmol·L-1); C: HG+GW0742 (0.01 μmol·L-1); D: HG+GW0742 (0.1 μmol·L-1); E: HG+GW0742 (1 μmol·L-1) |
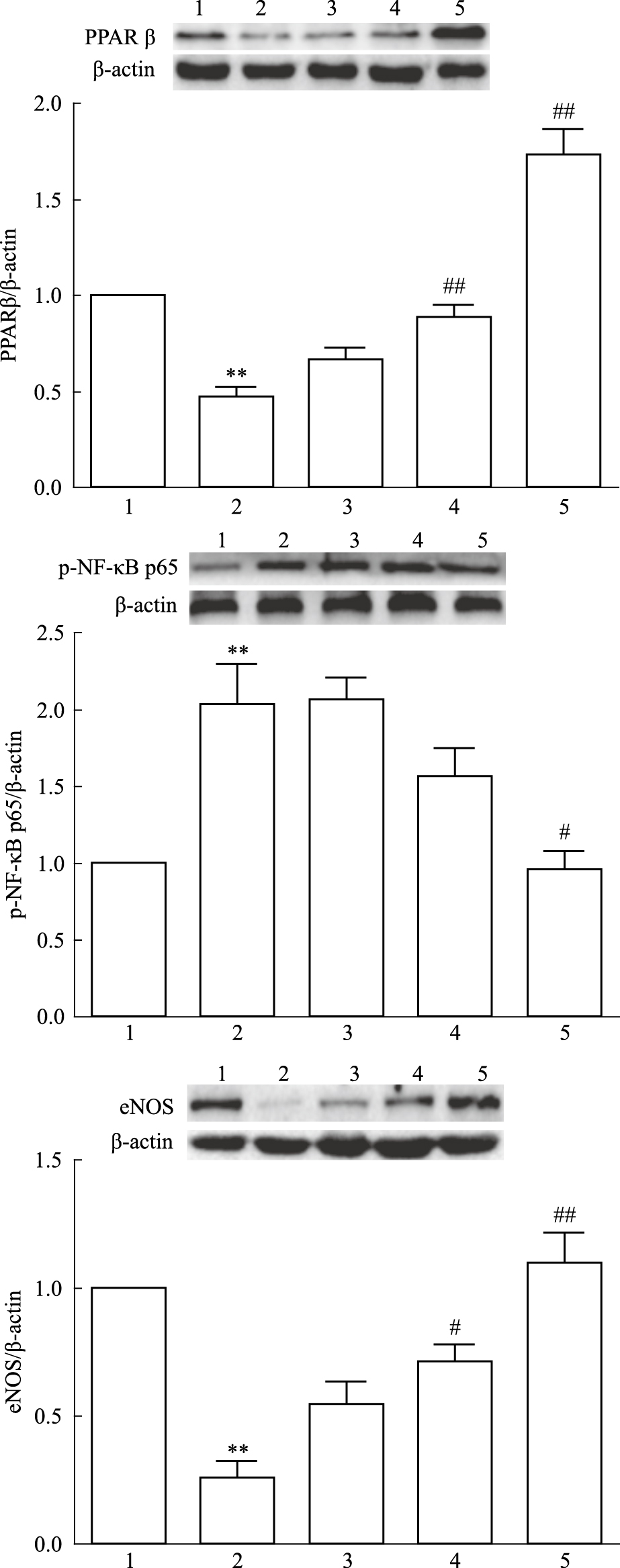
与正常组相比,高糖组PPAR β mRNA和蛋白表达明显降低(P<0.01),NF-κB p65 的表达则明显升高(P<0.01),同时eNOS的表达减少(P<0.01)。GW0742明显上调高糖减少的PPAR β表达(P<0.05),降低NF-κB p65的表达(P<0.05),增加eNOS表达(Fig3,Fig4)。

|
| Fig.3 Effects of GW0742 on mRNA expression of PPAR β,NF-κB p65, eNOS under HG condition(x±s,n=3) 1:NG;2:HG;3:HG+GW0742 (0.01 μmol·L-1); 4:HG+GW0742 (0.1 μmol·L-1); 5:HG+GW0742 (1 μmol·L-1); NG: glucose at 11 mmol·L-1+mannitol 44 mmol·L-1; HG: glucose at 55 mmol·L-1.**P<0.01 vs NG; #P<0.05,##P<0.01 vs HG. |
|
| Fig.4 Effects of GW0742 on protein expressions of PPAR β,p-NF-κB p65, eNOS under HG condition(x±s, n=3) 1:NG;2:HG;3:HG+GW0742 (0.01 μmol·L-1);4:HG+GW0742 (0.1 μmol·L-1); 5:HG+GW0742 (1 μmol·L-1);NG: glucose at 11 mmol·L-1+mannitol 44 mmol·L-1; HG: glucose at 55 mmol·L-1.**P<0.01 vs NG;#P<0.05,##P<0.01 vs HG. |
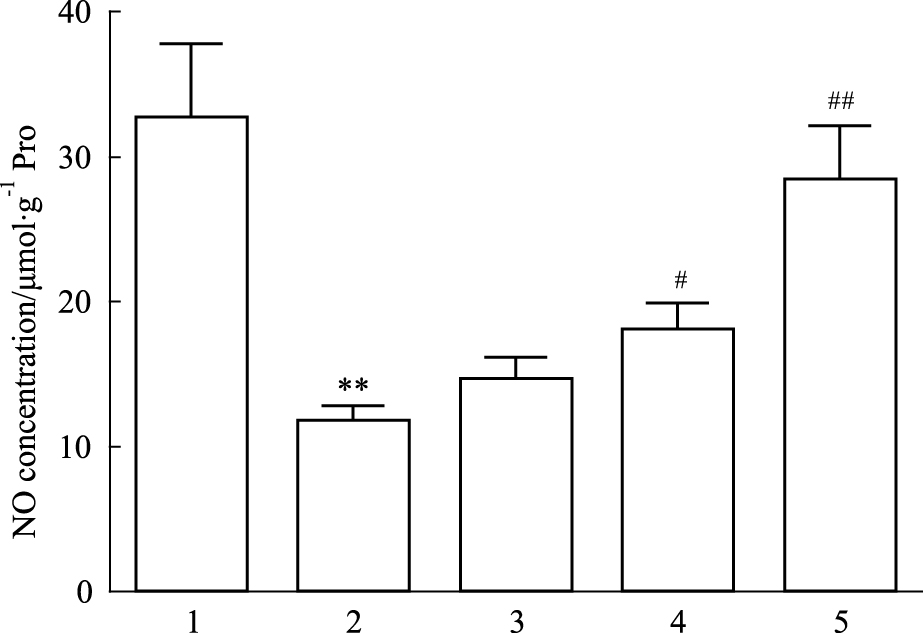
与正常组相比,高糖孵育后血管NO浓度降低了63.7%(P<0.01),GW0742 0.1和1 μmol·L-1分别使NO含量增加了52.5%(P<0.05)和150.5%(P<0.01)。1 μmol·L-1的GW0742使NO的含量基本恢复至正常组水平(Fig5)。
|
| Fig.5 Effects of GW0742 on NO contentsin aortas under HG conditions(x±s, n=3) 1:NG;2:HG;3:HG+GW0742 (0.01 μmol·L-1); 4:HG+GW0742 (0.1 μmol·L-1); 5:HG+GW0742 (1 μmol·L-1); NG: glucose at 11 mmol·L-1+mannitol 44 mmol·L-1; HG: glucose at 55 mmol·L-1.**P<0.01 vs NG;#P<0.05,## P<0.01 vs HG. |
血管病变在糖尿病及其并发症的发生发展中具有重要作用,但相关机制仍未完全阐明。临床和体外研究表明,由于糖尿病患者糖代谢异常,体内血糖水平持续性升高,导致血管内皮损伤,引发内皮功能紊乱[10, 11, 12]。本研究中,与相同渗透压的正常葡萄糖(11 mmol·L-1)对照组比较,55 mmol·L-1葡萄糖使ACh诱导的血管内皮依赖性舒张作用明显降低,提示高糖可能导致血管的内皮功能受损,且这种损伤作用并不是由于渗透压的增加引起的。同时,组织形态学检测证实高糖也破坏了血管内皮细胞和血管平滑肌细胞结构完整性。大量研究认为,内皮功能紊乱和缺失是糖尿病血管病变的主要危险因素[13],但遗憾的是,目前对于高糖损伤的内皮功能并没有特别有效的干预措施。研究发现,GW0742对高糖损伤人脐静脉内皮细胞和I型糖尿病大鼠内皮功能障碍有保护作用[14, 15]。本实验结果亦表明,GW0742能改善高糖环境下ACh血管内皮依赖性舒张功能,保护高糖条件下血管内皮和平滑肌细胞的结构。上述结果提示,GW0742对高糖损伤的内皮具有保护作用,对糖尿病血管病变可能有良好的干预作用。GW0742是选择性的PPAR β激动剂。PPAR β是过氧化物酶增殖物激活受体3个亚型之一,主要在体内代谢活跃的组织表达,调控脂肪酸代谢和葡萄糖平衡等相关基因,在糖、脂代谢、炎症反应中发挥重要作用。在糖尿病db/db小鼠,长期激动PPAR β可以改善胰岛素敏感性和胰岛功能,同时改善脂质代谢,提示PPAR β可能是糖尿病治疗的一个重要作用靶点[16]。本实验结果显示,高糖孵育后PPAR β在mRNA和蛋白水平表达均明显降低,而给予GW0742后,PPAR β表达明显升高,提示高糖损伤血管内皮细胞结构和功能与PPAR β相关信号通路受损有关,而GW0742对内皮的保护作用可能是其激动PPAR β的结果。
脂肪细胞中,PPAR β激活后可通过调节ERK1/2的活化,减少NF-κB激活,从而抑制脂多糖诱导的细胞因子的产生[17];在EA. hy926内皮细胞,激活PPAR β可抑制细胞因子诱导的NF-κB核转录过程[18]。这些结果提示,NF-κB可能是PPAR β的下游因子之一。作为重要的核转录调控因子,NF-κB几乎存在于所有细胞中,参与细胞凋亡、肿瘤发生、炎症和免疫反应等多种生物进程。NF-κB通路的激活亦参与了糖尿病的发生发展。NF-κB抑制剂Celastrol可改善胰岛素抵抗,减轻糖尿病肾损伤[19];干扰NF-κB表达,阻断NF-κB的作用对Ⅱ型糖尿病大鼠的内皮细胞有保护作用[20]。本实验结果显示,高糖孵育胸主动脉的NF-κB在mRNA和蛋白水平的表达均明显上升,而GW0742则使其表达下降,提示NF-κB的激活亦参与了高糖对内皮的损伤,GW0742通过激活PPAR β,降低NF-κB的活性产生内皮保护作用。
Liu等[21]发现,糖尿病引发的内皮功能紊乱与NF-κB信号通路激活后,eNOS活性被抑制,最终细胞NO释放减少有关。NO是NF-κB信号通路的重要下游因子,也是内皮细胞释放的重要血管活性物质。在eNOS作用下,内皮释放NO,激活血管壁平滑肌细胞的鸟苷酸环化酶,促进环磷酸鸟苷生成,从而产生血管舒张作用,增加血管eNOS的表达,有助于改善高脂饮食引起的内皮损伤[22]。本研究显示,高糖孵育后,由NO介导的ACh内皮依赖性舒张作用降低,大鼠胸主动脉eNOS mRNA和蛋白表达亦减少,NO释放明显减少。该结果再次证实,eNOS-NO通路受损在高糖对内皮的损伤作用中具有重要意义。GW0742在改善高糖损伤ACh内皮依赖性舒张的同时,上调血管内eNOS mRNA和蛋白表达,增加NO释放,提示eNOS-NO系统的激活在GW0742保护高糖损伤血管内皮中亦有重要作用。综上所述,GW0742对高糖损伤血管内皮功能具有保护作用,该作用可能是GW0742激活PPAR β表达,降低NF-κB活性,改善eNOS-NO系统的结果。但GW0742的上述作用是否还有其余信号通路或血管活性物质参与,需要进行更多深入研究。
(致谢:本实验于重庆医科大学生物化学与分子药理学重点实验室完成,感谢实验室各位老师和同学在实验过程中给予的帮助)
| [1] | Triggle C R. The early effects of elevated glucose on endothelial function as a target in the treatment of type 2 diabetes[J].Drugs Today(Barc), 2007, 43(11):815-26. |
| [2] | Ojima A, Ishibashi Y, Matsui T, et al. Glucagon-like peptide-1 receptor agonist inhibits asymmetric dimethylarginine generation in the kidney of streptozotocin-induced diabetic rats by blocking advanced glycation end product-induced protein arginine methyltranferase-1 expression[J].Am J Pathol, 2013, 182(1):132-41. |
| [3] | Hadi H A, Suwaidi J A. Endothelial dysfunction in diabetes mellitus[J].Vasc Health Risk Manag, 2007, 4(2):853-76. |
| [4] | Takata Y, Liu I, Yin F, et al. PPAR-δ mediated anti-inflammatory mechanisms inhibit angiotensin II accelerated atherosclerosis[J].Proc Natl Acad Sci USA, 2008, 105(110):4277-82. |
| [5] | Zarzuelo M J, Jime/nez R, Galindo P, et al. Antihypertensive effects of peroxisome proliferator-activated receptor-β activation in spontaneously hypertensive rats[J].Hypertension, 2011, 58(4):733-43. |
| [6] | Matsushita Y, Ogawa D, Wada J, et al. Activation of peroxisome proliferator-activated receptor delta inhibits streptozotocin-induced diabetic nephropathy through anti-inflammatory mechanisms in mice[J].Diabetes, 2011, 60(3):960-8. |
| [7] | Khazaei M, Salehi E, Rashidi B, et al. Role of peroxisome proliferator-activated receptor β agonist on angiogenesis in hindlimb ischemic diabetic rats[J].J Diabetes Complicat, 2012,26(2):137-40. |
| [8] | Wu Y, Xue L, Du W, et al. Polydatin restores endothelium-dependent relaxation in rat aorta rings impaired by high glucose:a novel insight into the PPARβ-NO signaling pathway[J].Plos One, 2015, 10(5):e0126249. |
| [9] | 茹筱晨, 钱令波, 崔 洁.乙醇对离体大鼠胸主动脉环的舒张作用及其机制[J].中国应用生理学杂志, 2008, 24(3):269-73. Ru X C, Qian L B, Cui J, et al. Vasodilating effect and its mechamism of ethanol on isolated rat thoracic aorta at different resting tension[J].Chin J Appl Physiol, 2008, 24(3):269-73. |
| [10] | Campos C. Chronic hyperglycemia and glucose toxicity:pathology and clinical sequelae[J].Postgrad Med, 2012, 124(6):90-7. |
| [11] | Kobayashi T, Matsumoto T, Kamata K. Mechanisms underlying the chronic pravastatin treatment-induced improvement in the impaired endothelium-dependent aortic relaxation seen in streptozotocin-induced diabetic rats[J].Br J Pharmacol, 2000, 131(2):231-8. |
| [12] | Caballero A E. Endothelial dysfunction, inflammation, and insulin resistance:a focus on subjects at risk for type 2 diabetes[J].Curr Diab Rep, 2004, 4(4):237-46. |
| [13] | Xu J, Zou M H. Molecular insights and therapeutic targets for diabetic endothelial dysfunction[J].Circulation, 2009, 120(13):1266-86. |
| [14] | Quintela A M, Jiménez R, Piqueras L, et al. PPARβ activation restores the high glucose-induced impairment of insulin signaling in endothelial cells[J].Br J Pharmacol, 2014,171(12):3089-102. |
| [15] | Quintela A M, Jiménez R, Gomez-Guzman M, et al. Activation of peroxisome proliferator-activated receptor-β/-δ(PPARβ/δ) prevents endothelial dysfunction in type 1 diabetic rats[J].Free Radic Biol Med, 2012, 53(4):730-41. |
| [16] | Winzell M S, Wulff E M, Olsen G S, et al. Improved insulin sensitivity and islet function after PPARdelta activation in diabetic db/db mice[J].Eur J Pharmacol, 2010, 626(2-3):297-305. |
| [17] | Rodríguez-Calvo R, Serrano L, Coll T, et al. Activation of peroxisome proliferator-activated receptor beta/delta inhibits lipopolysaccharide-induced cytokine production in adipocytes by lowering nuclear factor-kappa B activity via extracellular signal-related kinase 1/2[J].Diabetes, 2008, 57(8):2149-57. |
| [18] | Rival Y, Benéteau N, Taillandier T, et al. PPARalpha and PPARdelta activators inhibit cytokine-induced nuclear translocation of NF-kappa B and expression of VCAM-1 in EA.hy 926 endothelial cells[J].Eur J Pharmacol, 2002, 435(2-3):143-51. |
| [19] | Kim J E, Lee M H, Nam D H, et al. Celastrol, an NF-κB inhibitor, improves insulin resistance and attenuates renal injury in db/db mice[J].Plos One, 2013, 8(4):62-8. |
| [20] | Zheng X, Zhu S, Chang S, et al. Protective effects of chronic resveratrol treatment on vascular inflammatory injury in streptozotocin-induced type 2 diabetic rats:role of NF-kappa B signaling[J].Eur J Pharmacol, 2013, 720(13):147-57. |
| [21] | Liu C, Sun J, Xue F, et al. Effect of 3, 4-dihydroxyacetophenone on endothelial dysfunction in streptozotocin-induced rats with type 2 diabetes[J].J Cardiovasc Pharmacol, 2015, 65(1):22-7. |
| [22] | 程静静, 陈 莉, 李朝飞, 等.白藜芦醇通过减缓内质网应激及增加eNOS的表达改善高热量高胆固醇饮食引起的内皮损伤[J].中国药理学通报, 2014,30(12):1756-62 Cheng J J, Chen L, Li C F, et al. Resveratrol improves vascular endothelial injury induced by high-calorie and high-cholestrol diet through reduced ERS and increased eNOS expression[J].Chin Pharmacol Bull, 2014, 30(12):1756-62. |

