


RAGE是一种多配体受体,可与晚期糖基化终末产物(advanced glycation end-products,AGEs)、高迁移率蛋白B1(high mobility group B1,HMGB1/Amphoterin)、S100/钙粒蛋白和β淀粉样肽(β-amyloid protein,Aβ)等配体相互作用,促使细胞内多条信号通路的激活,产生氧化应激和炎症反应,最终引起细胞或组织功能紊乱。RAGE分布在多种细胞的表面,1993年,研究者发现[1],在CD4+ T细胞表面存在能够结合AGEs的受体RAGE,该受体不仅利于体内多余AGEs的清除,而且与免疫因子的产生有关,能够调节免疫应答。近年来大量研究发现,RAGE与不同的配体结合后,可对CD4+ T细胞的增殖、分化和迁移等产生多种不同的影响。本文就近年来关于RAGE及其配体对CD4+ T细胞作用的研究进展作一综述。
1 RAGE及其信号通路1992年,Neeper首次从牛肺组织中分离出可以识别并结合晚期糖基化终末产物(AGEs)的蛋白质,将其命名为RAGE[2]。RAGE由胞外区、单次跨膜区和胞内区三部分组成,其中胞外区有3个免疫球蛋白样区。在成年人体内,RAGE主要分布在免疫细胞、神经元细胞、内皮细胞、血管平滑肌细胞和癌细胞中。RAGE一般低表达于这些细胞中,但当细胞或组织局部出现RAGE配体或炎症因子聚集时,可诱导RAGE的表达[3]。
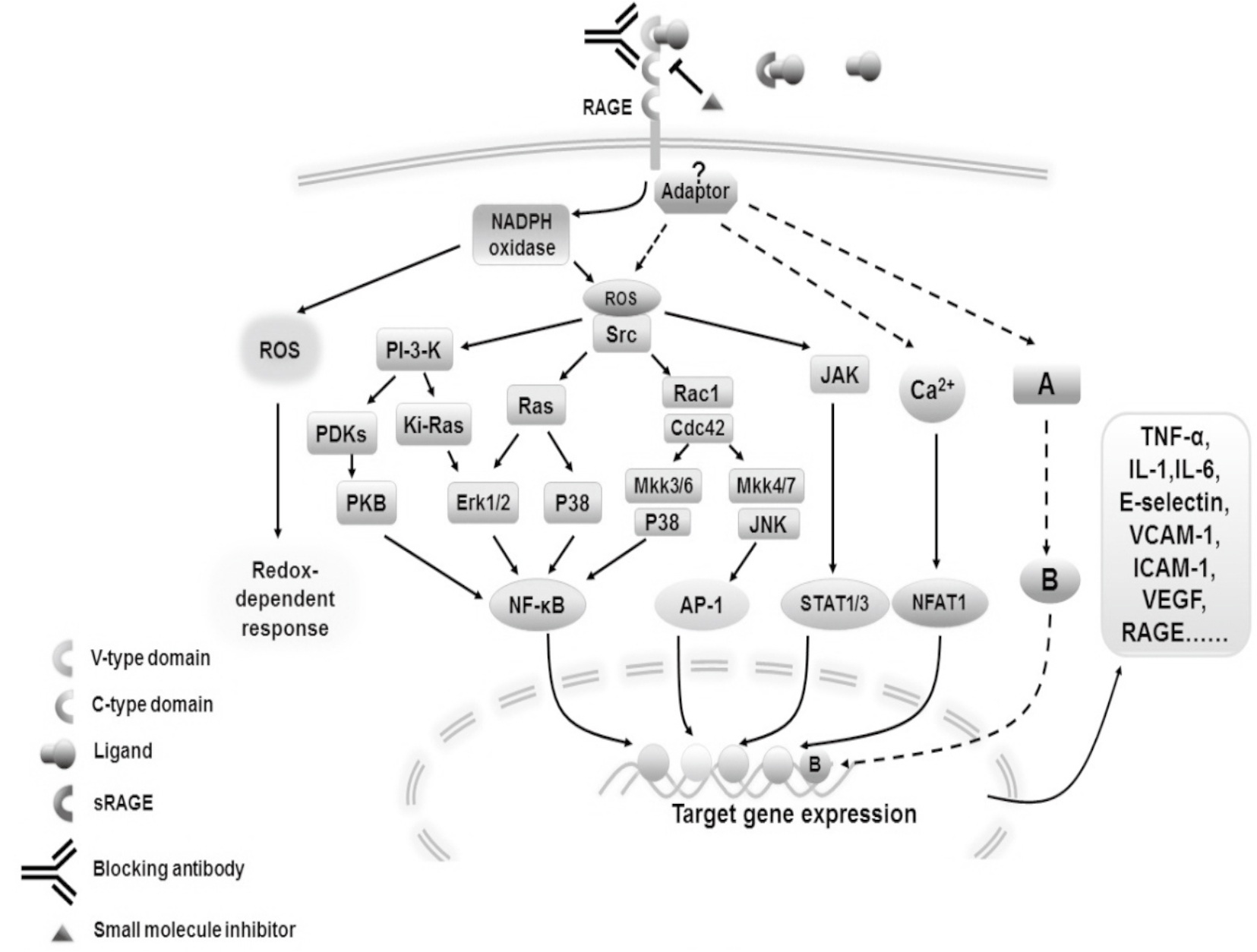
RAGE可与多种配体结合,包括AGEs、HMGB1/Amphoterin、S100/钙粒蛋白和Aβ等,两者结合后可促使信号通路的激活,最终引起炎症反应和氧化应激,造成细胞和组织损伤。RAGE与不同配体结合后激活细胞内不同的信号通路,因此,RAGE—配体激活的信号通路具有特异性和复杂性,如Fig1中所示[3]。多数信号通路激活后最终促使核转录因子-κB(nuclear factor kappa B,NF-κB)入核,调节重要的目的基因的表达,如:肿瘤坏死因子(TNF-α)、白介素-1(IL-1)、白介素-6(IL-6)等,这些细胞因子可促进炎症和肿瘤的发生。同时NF-κB也是RAGE基因的核转录因子,可上调RAGE基因如:肿瘤坏死因子(TNF-α)、白介素-1(IL-1)、白介素-6(IL-6)等,这些细胞因子可促进炎症和肿瘤的发生。同时NF-κB也是RAGE基因的核转录因子,可上调RAGE基因的表达,因此,RAGE—配体结合后可通过正反馈调节使信号级联反应持续发生。
|
| Fig.1 Signalling pathways activated by RAGE-ligand A:Other signalling molecules; B:Other transcription factors. |
近年来研究发现,RAGE与其配体在体内免疫应答过程中发挥重要的作用,阻断RAGE的作用可以抑制迟发型超敏反应[4]、佐剂性关节炎[5]、实验性自身免疫性脑脊髓炎[6]和自身免疫性糖尿病[7]等多种免疫相关疾病的炎症反应。研究发现,RAGE表达于多种免疫细胞中,比如单核细胞、巨噬细胞、CD4+ T细胞和CD8+ T细胞等,并可以调节这些细胞的活化和功能,进而调节体内的免疫应答。其中,RAGE对于CD4+ T细胞起着重要的作用。
2 CD4+ T细胞及其功能人体的T细胞来源于骨髓,在胸腺中分化成熟,进入外周,经历活化、增生和分化后形成成熟的效应T细胞。T细胞在胸腺中经过阳性选择和阴性选择后,根据膜表面标记和功能差异可分为CD4+ T细胞和CD8+ T细胞。多数CD8+ T细胞以直接细胞毒性作用为功能特点;CD4+ T细胞主要是发挥辅助或者调节性作用,既参与对细胞免疫的调节,也参与对体液免疫的调节。CD4+ T细胞可以通过分泌细胞因子或活化并招募巨噬细胞、嗜中性粒细胞和嗜酸性粒细胞等细胞来清除体内的病毒、细菌和寄生虫等;同时,CD4+ T细胞也能辅助B细胞产生抗体。但当其错误的识别自身抗原产生免疫反应时,机体就会产生自身免疫性疾病。
在免疫应答过程中,CD4+ T细胞的分化是很重要的一步。成熟的CD4+ T细胞经过表面受体(T cell receptor,TCR)可与抗原呈递细胞表面的MHCII抗原复合体的相互作用,以及分泌的细胞因子的刺激,会促使T细胞激活进而逐步分化为功能各异的细胞群,包括辅助性T细胞(T helper cell)和调节性T细胞(regulatory T cells,Treg)。前者主要包括4个亚群,分别为1型辅助性T细胞(T helper cell 1,Th1)、2型辅助性T细胞(T helper cell 2,Th2)、17型辅助性T细胞(T helper cell 17,Th17)和滤泡辅助性T细胞(follicular helper T cells,Tfh)。Th1细胞的保护效应主要针对肿瘤和细胞内微生物,参与I型糖尿病、迟发型高敏反应、甲状腺炎和类风湿性关节炎等病理过程和疾病;Th2细胞针对细胞外寄生虫,分泌的细胞因子主要调节体液免疫反应,在诱发过敏反应中(比如过敏性疾病、哮喘等)起着决定性的作用;Th17细胞则通过分泌IL-17参与固有免疫、抗细菌感染和介导自身免疫性疾病;Tfh是近年来发现的另一种特殊的辅助性T细胞亚群,主要功能为辅助B细胞参与体液免疫。调节性T细胞主要负责调节机体免疫反应,在免疫应答的负调节及维持自身免疫耐受中发挥重要的作用[8]。
3 RAGE及其配体对CD4+ T细胞的作用大量研究发现,RAGE及其配体对于CD4+ T细胞的激活、增殖、迁移和分化均起着重要的作用。
RAGE能够促进CD4+ T细胞的增殖。Chen等[9]从野生型小鼠(C57BL/6)和 RAGE-/-小鼠脾脏中提取T细胞与去T细胞的野生小鼠脾细胞进行混合淋巴细胞实验,发现来源于RAGE-/- 小鼠的T细胞增殖能力明显低于野生型T细胞。Moser等[10]把来源于RAGE+/+或RAGE-/-小鼠的CD4+ T细胞转入同种异体RAGE-/-或RAGE+/+ C57BL/6小鼠(宿主)体内,给小鼠腹腔注射鸡卵清蛋白,发现接受来源于RAGE+/+小鼠的CD4+ T细胞与RAGE+/+宿主都有利于T细胞的激活与增殖,而接受来源于RAGE-/-小鼠的CD4+ T细胞与RAGE-/-宿主无明显T 细胞激活与增殖。这些结果表明表达于CD4+ T细胞的RAGE参与了细胞免疫反应。
RAGE在CD4+ T细胞分化的过程中也起着重要的调节作用。Moser等 [10]对RAGE缺失的T细胞研究发现,RAGE阴性T细胞中Th2细胞因子(包括IL-4和IL-5)水平升高,但Th1型细胞因子(包括IL-2和IFN-γ)减少;而接受来源于RAGE+/+小鼠的 CD4+ T细胞与RAGE+/+ 宿主中Th1型细胞因子明显增多。Chen等 [9]的实验也发现RAGE促进CD4+ T细胞向Th1细胞方向分化,而且在Th1细胞中RAGE的mRNA水平明显高于Th2细胞。这一现象说明RAGE参与了免疫反应中Th1和Th2细胞之间平衡调节。
3.1 AGEs-RAGE对CD4+T细胞的影响AGEs是一组在蛋白质、脂肪酸或核酸的氨基基团与还原糖的醛基之间发生非酶性糖基化反应所形成的一系列具有高度活性终产物的总称。AGEs与RAGE结合后,引起氧化应激并激活多条细胞信号转导通路[11],诱发一系列促炎、促凝血反应等,参与糖尿病、肾功能衰竭、动脉粥样硬化、神经退行性病变、慢性肝病、HIV等多种自身免疫功能紊乱相关性疾病的发生发展。最近研究发现,AGEs-RAGE相互作用参与并影响了CD4+ T细胞的分化和功能。
用AGEs处理初始CD4+ T细胞后[12],CD4+ T细胞群内Th1型细胞因子IFN-γ和Th17型细胞因子IL-17α细胞因子水平较均明显增高。而Th2型细胞因子IL-4和Treg型特异性因子Foxp3水平在各组之间无明显差异。Th1细胞特异性转录因子T-bet和Th17细胞特异性转录因子RORγt表达水平亦明显增高。而Th2细胞及Treg细胞特异性转录因子GATA3和Foxp3表达水平在各组间无明显差异。因此,AGEs诱导了初始CD4+ T细胞向Th1和Th17细胞转换。利用RAGE shRNA沉默CD4+ T细胞中的RAGE基因后发现,在AGEs诱导的初始CD4+ T细胞分化成Th1和Th17细胞表型的过程中,RAGE介导了细胞的转化。
同时也发现,将AGEs处理的Treg细胞与初始CD4+T细胞共培养时,随着AGEs剂量的增加,初始CD4+T细胞增生率逐渐升高,表明AGEs也干预了Treg细胞的抑制功能。
3.2 S100b-RAGE对CD4+ T细胞的影响S100b蛋白是RAGE的配体之一,属于酸性钙结合蛋白-S100蛋白家族的成员,具有钙离子结合区,因而被认为是一种钙传感器蛋白,可通过钙离子信号转导途径在细胞增殖、分化、基因表达及细胞凋亡中发挥广泛的生物学活性 [13]。
Yan等 [6]发现在多发性硬化(MS)患者和其经典模型动物即实验性自身免疫性脑脊髓炎(EAE)小鼠的脊髓,尤其是在炎症病灶周围的CD4+ T细胞中高表达RAGE及其配体S100b蛋白,且两者相互作用可以促使抗原特异性CD4+ T细胞向中枢神经系统的迁移。在利用鞘原蛋白诱导EAE小鼠模型过程中,通过给予小鼠sRAGE或抗RAGE抗体阻断RAGE的功能,可以明显减少小鼠脊髓中RAGE及其配体S100b的表达以及中枢神经系统(CNS)中炎症细胞的入侵,并使病情明显减轻。进一步研究发现,EAE小鼠模型中CD4+ T细胞表面存在大量的黏附分子受体,而给予sRAGE的小鼠中黏附分子受体的水平明显降低;而且S100b-RAGE相互作用产生大量的趋化因子和黏附分子,诱导了鞘原蛋白特异性CD4+ T细胞向CNS的迁移,促使了脑脊髓炎的产生。因此,S100b-RAGE相互作用在MS发病的早期参与了CD4+ T细胞向CNS内迁移的过程;在发病后期,加剧了CNS中的炎症反应。但S100b-RAGE相互作用对CD4+ T细胞增殖和分化的影响尚不清楚。
3.3 HMGB1-RAGE对CD4+T细胞的影响高迁移率蛋白 B1(high mobility group B1,HMGB1/Amphoterin)是RAGE的配体之一,在哺乳动物体内分布广泛。HMGBl与RAGE有较高的亲和力[14],两者结合后可促进细胞因子活化,介导炎症反应。近年来研究发现,其与脓毒症、肿瘤、风湿免疫、动脉粥样硬化、缺血/再灌注损伤等多种疾病密切相关。
树突状细胞(DC)是T细胞重要的抗原递呈细胞,可以产生并释放HMGB1,分泌的HMGB1促进DC细胞的成熟并调节其功能;同时对于CD4+ T细胞的存活、增殖和分化起着重要的作用。Dumitriu等 [15]用抗-CD3和(或)抗-CD28 抗体刺激CD3和CD28分子受体的同时,用HMGB1刺激CD4+ T细胞,可使其大量增殖,同时向Th1细胞的方向分化,表达更多的IFN-γ;但对于Th2细胞的分化没有影响。而利用RAGE抗体阻断RAGE的功能,可使T细胞增殖和向Th1细胞分化的能力明显降低。
4 总结与展望RAGE及其配体在多种疾病中起着重要作用,大量研究证实利用RAGE抑制剂阻断RAGE与配体的结合在预防和治疗相关疾病中有重要的意义[16, 17, 18, 19],并且不会影响机体正常的生理功能[17, 20]。因此,RAGE已成为治疗疾病的新靶点[21]。综上所述,RAGE及其配体相互作用可以促进CD4+ T细胞的激活、增殖和迁移,并能够调节其向促炎方向(包括Th1细胞和Th17细胞)分化。由于CD4+ T细胞是体内的细胞免疫的重要参与者,CD4+ T细胞及其各亚群在迟发型超敏反应、佐剂性关节炎和自身免疫性糖尿病等免疫性疾病中起着关键性作用,因此,利用sRAGE、anti-RAGE或其他RAGE抑制剂阻断RAGE的功能可以调节这些疾病的进程。所以,RAGE对于成为这些疾病的治疗靶点具有较大的潜力。
对于RAGE在CD4+ T细胞中作用的研究为相关疾病的发病机制提供了重要的理论支持。但目前关于RAGE对CD4+ T细胞作用的具体机制尚未得到充分解释,并且有些配体(如S100b蛋白)对CD4+ T细胞作用的研究仍不全面。因此,对于RAGE在CD4+T细胞中的作用有待进一步全面和深入的研究。
| [1] | Imani F, Horii Y, Suthanthiran M, et al. Advanced glycosylation endproduct-specific receptors on human and rat T-lymphocytes mediate synthesis of interferon gamma:role in tissue remodeling[J]. J Exp Med, 1993, 178(6):2165-72. |
| [2] | Neeper M, Schmidt A M, Brett J, et al. Cloning and expression of a cell surface receptor for advanced glycosylation end products of proteins[J]. J Biol Chem, 1992, 267(21):14998-5004. |
| [3] | 吕 翠,刘洪娟,刘晓丽,张文生. 晚期糖基化终末产物受体及其抑制剂的研究进展[J]. 中国药理学通报, 2013, 29(4):452-6. Lyu C, Liu H J, Liu X L, Zhang W S. The research progress on RAGE and RAGE inhibitor[J]. Chin Pharmacol Bull, 2013, 29(4):452-6. |
| [4] | Hofmann M A, Drury S, Fu C, et al. RAGE mediates a novel proinflammatory axis:a central cell surface receptor for S100/calgranulin polypeptides[J]. Cell, 1999, 97(7):889-901. |
| [5] | Hofmann M A, Drury S, Hudson B I, et al. RAGE and arthritis:the G82S polymorphism amplifies the inflammatory response[J]. Genes Immun, 2002, 3(3):123-35. |
| [6] | Yan S S, Wu Z Y, Zhang H P, et al. Suppression of experimental autoimmune encephalomyelitis by selective blockade of encephalitogenic T-cell infiltration of the central nervous system[J]. Nat Med, 2003, 9(3):287-93. |
| [7] | Chen Y, Yan S S, Colgan J, et al. Blockade of late stages of autoimmune diabetes by inhibition of the receptor for advanced glycation end products[J]. J Immunol, 2004, 173(2):1399-405. |
| [8] | Jiang S, Dong C. A complex issue on CD4(+) T-cell subsets[J]. Immunol Rev, 2013, 252(1):5-11. |
| [9] | Chen Y, Akirav E M, Chen W, et al. RAGE ligation affects T cell activation and controls T cell differentiation[J]. J Immunol, 2008, 181(6):4272-8. |
| [10] | Moser B, Desai D D, Downie M P, et al. Receptor for advanced glycation end products expression on T cells contributes to antigen-specific cellular expansion in vivo[J]. J Immunol, 2007, 179(12):8051-8. |
| [11] | Haslbeck K M, Schleicher E, Bierhaus A, et al. The AGE/RAGE/NF-(kappa)B pathway may contribute to the pathogenesis of polyneuropathy in impaired glucose tolerance (IGT)[J]. Exp Clin Endocrinol Diabetes, 2005, 113(5):288-91. |
| [12] | Han X Q, Gong Z J, Xu S Q, et al. Advanced glycation end products promote differentiation of CD4(+) T helper cells toward pro-inflammatory response[J]. J Huazhong Univ Sci Technolog Med Sci, 2014, 34(1):10-7. |
| [13] | da Rocha A B, Schneider R F, de Freitas G R, et al. Role of serum S100B as a predictive marker of fatal outcome following isolated severe head injury or multitrauma in males[J]. Clin Chem Lab Med, 2006, 44(10):1234-42. |
| [14] | Rauvala H, Rouhiainen A. RAGE as a receptor of HMGB1 (Amphoterin):roles in health and disease[J]. Curr Mol Med, 2007, 7(8):725-34. |
| [15] | Dumitriu I E, Baruah P, Valentinis B, et al. Release of high mobility group box 1 by dendritic cells controls T cell activation via the receptor for advanced glycation end products[J]. J Immunol, 2005, 174(12):7506-15. |
| [16] | Taguchi A, Blood D C, del Toro G, et al. Blockade of RAGE-amphoterin signalling suppresses tumour growth and metastases[J]. Nature, 2000, 405(6784):354-60. |
| [17] | Deane R, Singh I, Sagare A P, et al. A multimodal RAGE-specific inhibitor reduces amyloid beta-mediated brain disorder in a mouse model of Alzheimer disease[J]. J Clin Invest, 2012, 122(4):1377-92. |
| [18] | Lyu C, Wang L, Liu X, et al. Geniposide attenuates oligomeric Abeta(1-42)-induced inflammatory response by targeting RAGE-dependent signaling in BV2 cells[J]. Curr Alzheimer Res, 2014, 11(5):430-40. |
| [19] | Lyu C, Wang L, Liu X, et al. Multi-faced neuroprotective effects of geniposide depending on the RAGE-mediated signaling in an Alzheimer mouse model[J]. Neuropharmacology, 2015, 89:175-84. |
| [20] | Sabbagh M N, Agro A, Bell J, et al. PF-04494700, an oral inhibitor of receptor for advanced glycation end products (RAGE), in Alzheimer disease[J]. Alzheimer Dis Assoc Disord, 2011, 25(3):206-12. |
| [21] | Sukkar M B, Ullah M A, Gan W J, et al. RAGE:a new frontier in chronic airways disease[J]. Br J Pharmacol, 2012, 167(6):1161-76. |

