


1 JNK蛋白激酶
c-Jun氨基末端激酶(c-Jun N-terminal kinase,JNK),是高等动物体内进化保守的MAPKs超家族中的一员[1]。蛋白激酶JNK包括3种蛋白质——JNK1、JNK2和JNK3,分子质量为46×103或55×103,它们分别由基因MAPK8、MAPK9和MAPK10所编码。研究表明虽然3种JNK的亚型在氨基酸序列上有高度的同源性,但它们在组织器官中的分布和生理功能上存在着明显的差异,高等动物中几乎所有组织器官中的细胞中都有JNK1和JNK2表达,而JNK3只存在于神经组织(如大脑、脊髓)、心脏、睾丸中[2]。这可能是由于它们分别参与了不同底物的调节或者是结构相似的蛋白质之间也存在着功能性的差异。在细胞没有受到刺激的情况下,JNK2优先与c-jun结合有助于c-jun的退化;在细胞受到外部的刺激下,JNK1首先能磷酸化c-jun来提高它的转录活性。
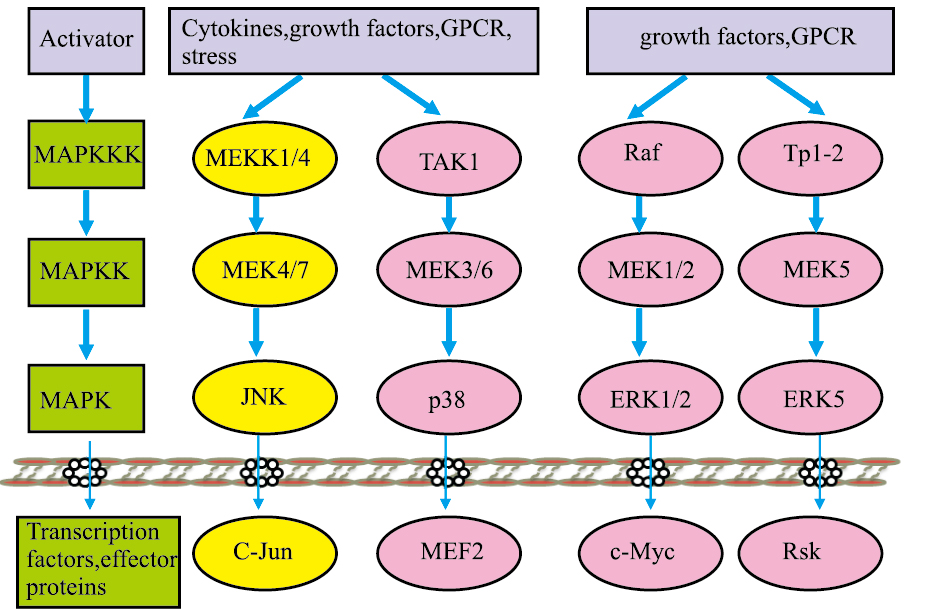
2 MAPKs信号通路丝裂原活化蛋白激酶(mitogen activated protein kinases,MAPKs)是哺乳动物体内普遍存在的一类丝氨酸、苏氨酸蛋白激酶,它在细胞的增殖、分化、转化和凋亡中发挥着非常重要的作用。许多胞外刺激物或物理化学刺激,如细胞因子,生长因子,pH,氧化还原,应激等都可以激活MAPKs信号通路(Fig1),并且每种MAPKs通路可作用于特定的下游底物并对相关刺激做出反应。典型的MAPKs信号转导是通过三级酶促级联的形式进行的(Fig1):首先有丝分裂原刺激MAPKKK使之磷酸化并被激活,活化的MAPKKK通过双特异性磷酸化激活MAPKK,进一步将MAPK的两个位点Thr和Tyr磷酸化使之激活,通过这种方式,将细胞外信号放大并传递到细胞中完成一系列的生理活动。
|
| Fig.1 MAPKs signaling pathway Activator:激活物;Cytokines: 细胞因子;Growth factors:生长因子;GPCR:G蛋白偶联受体;Stress:应激;Transcription factors:转录因子;Effector proteins:效应蛋白 |
目前发现MAPK有4种亚型:c-Jun氨基末端激酶(JNK)、p38丝裂原活化蛋白激酶(p38MAPK)、细胞外信号调节激酶1/2(ERK1/2)和细胞外信号调节激酶5(ERK5),它们能够被不同的刺激物激活,通过不同的信号转导通路使转录因子活化,在细胞的生长、分化和凋亡等一系列生理过程中发扮演着关键性的角色[3]。在大多数情况下,ERK1/2和ERK5对细胞具有保护作用,而JNK和p38则对细胞凋亡、炎症具有促进作用。
3 JNK信号通路细胞外激活因子(细胞因子、生长因子、病毒细菌)以及物理化学刺激(如电离辐射、热休克、渗透压)等都可以使JNK信号通路激活(Fig2)。当受到外界刺激后,JNK残基上的Thr183和Thr185位点可以直接被它的上游激酶MEK4和MEK7双磷酸化而活化并具有酶催化活性[4],但在JNK信号通路中MEK4和MEK7的功能却是不同的,Tyr185位点首先被MEK4磷酸化,而Thr183位点却被MEK7优先磷酸化。除此之外JNK也可以被蛋白磷酸酶(MAPKKK,MAPKK)或者支架蛋白(JIPs)磷酸化并激活。

|
| Fig.2 JNK signaling pathway Cytokines:细胞因子;Growth factors:生长因子;Viral bacteria:病毒细菌;Anticancer drugs:抗癌药物;Radiation:辐射;Heat shock:热休克;Small GTPases:小G蛋白;Other signal collecting proteins:其它信号募集蛋白;Cell shape changes:细胞形状改变;Cell differentiation:细胞分化;Cell survival:细胞存活;Cell proliferation:细胞增殖;Cell apoptosis:细胞凋亡 |
通常情况下JNK主要存在于细胞质中,当它被上游信号或刺激因子激活后,就会迅速地转位到细胞核内并与核内转录因子c-jun结合,使c-jun的氨基末端第63和73位上的丝氨酸残基磷酸化从而使c-jun活化并增加其转录活性和稳定性,除此之外JNK还能激活核内的其它转录因子,如Elk-1、ATF2、P53、c-Myc等,进一步的研究发现细胞质中的非转录因子,如Bcl-2、BAD、Bcl-xl和Bim等也可以被JNK激活[5]。JNK信号转导通路的形式可大致概括为: 生长因子、病毒细菌等→小G蛋白→MAPKKK→MAPKK(MEK4/7)→MAPK(JNK)→核内转录因子(c-jun、Elk-1等)→细胞存活、分化、增殖、凋亡等。
4 JNK的生理功能大量的生化知识研究和敲出JNK基因后的老鼠实验证实,JNK激酶介导的细胞增殖和细胞凋亡参与了人类多种疾病(癌症、神经退行性疾病和心肌/肝脏缺血再灌注损伤)的发生发展过程。所以,JNK是细胞由正常状态向病理状态转变过程中的一个重要的调节激酶,而JNK信号通路能够成为治疗由细胞增殖、凋亡所引起的疾病的重要分子靶标,并且JNK的多肽分子抑制剂对于由缺血和应激引起的细胞死亡的预防有着更为重要的治疗潜能。
4.1 JNK信号通路与细胞增殖细胞是以有丝分裂的方式进行增殖的,JNK激酶也参与了这个过程,Makino等[6]研究发现:成纤维细胞生长因子(bFGF)能够诱导人皮肤的成纤维细胞(HDFs)增殖,而加入JNK的抑制剂SP600125后其增殖会被明显地抑制,这说明JNK能够促进bFGF诱导人皮肤的成纤维细胞的增殖。除此之外,与正常细胞相比,在霍奇金淋巴瘤细胞中JNK的活性会明显的升高,表明JNK可能与该肿瘤的形成有很大的关系,其机制可能是JNK能够促进肿瘤细胞增殖[7]。Sakurai等[8]研究后发现,持续激活的JNK信号通路会使肝细胞中NF-κB失活从而促进肝癌的发生,因此,肿瘤的形成可能与JNK的激活促进细胞的增殖有关。Nateri等[9]通过对小鼠肠道模型的研究发现,敲除小鼠的c-Jun基因或者改变JNK磷酸化的位点,可使其肠道肿瘤减小,肿瘤细胞数量减少,从而使小鼠的寿命得到延长。Chang等[10]在研究人类肝癌时发现,JNK1能增加激酶活性和肿瘤细胞的数量从而促进肿瘤发生。Ras或Raf的激活能够诱导果蝇的肿瘤细胞增生,进一步的研究发现,其肿瘤细胞的异常增生是由JNK和Raf共同决定的[11]。在哺乳动物中对JNK的作用进行研究后也发现其能促进癌细胞的增殖。
有学者提出:细胞内的JNK活化既是一种生长信号,也是一种促凋亡信号(Tab1),细胞种类的不同、刺激因素的差异以及JNK的不同亚型都会使JNK信号通路在细胞中具有不同的作用,它既能促进细胞增殖也能促进细胞凋亡。候炳旭等[12]对此的解释可能是:人体内可能具有不同种JNK的同工酶,它们在不同的细胞类型中或者是同种细胞的不同发育阶段的表达具有差异,对刺激因素的反应方式不同,担负的生理功能也不同。
| Role of JNK | Cell types | JNKisoforms |
| Hepatic carcinoma | JNK1 | |
| Lung cancer | JNK1 | |
| Colorectal cacer | JNK1 | |
| Prostate cancer | JNK2 | |
| Esophageal | JNK2 | |
| Promoting proliferation of cancer cells | Castrointestinal tumors | JNK2 |
| Brain tumors | JNK2 | |
| Embryoma | JNK2 | |
| Ovarian cancer | JNK | |
| Nasopharyngeal carcinoma | JNK | |
| Esophageal squamous cellcarcinoma | JNK | |
| Breast cancer | JNK1 | |
| Skin papilloma | JNK1 | |
| Gastric | JNK2 | |
| Brain tumors | JNK3 | |
| Promoting apoptosis of cancer cells | Lung cancer | JNK |
| Hepatic carcinoma | JNK | |
| Lymphoma | JNK | |
| Cervical cancer | JNK | |
| Gastrointestinal tumors | JNK |
细胞凋亡是一种由基因控制的细胞程序性死亡,它在生物体的进化、胚胎发育、免疫应答、代谢和调节等生理过程中都具有重要意义。JNK信号通路在细胞凋亡中也发挥重要的调节功能,使其与多种疾病有着直接和间接的联系。
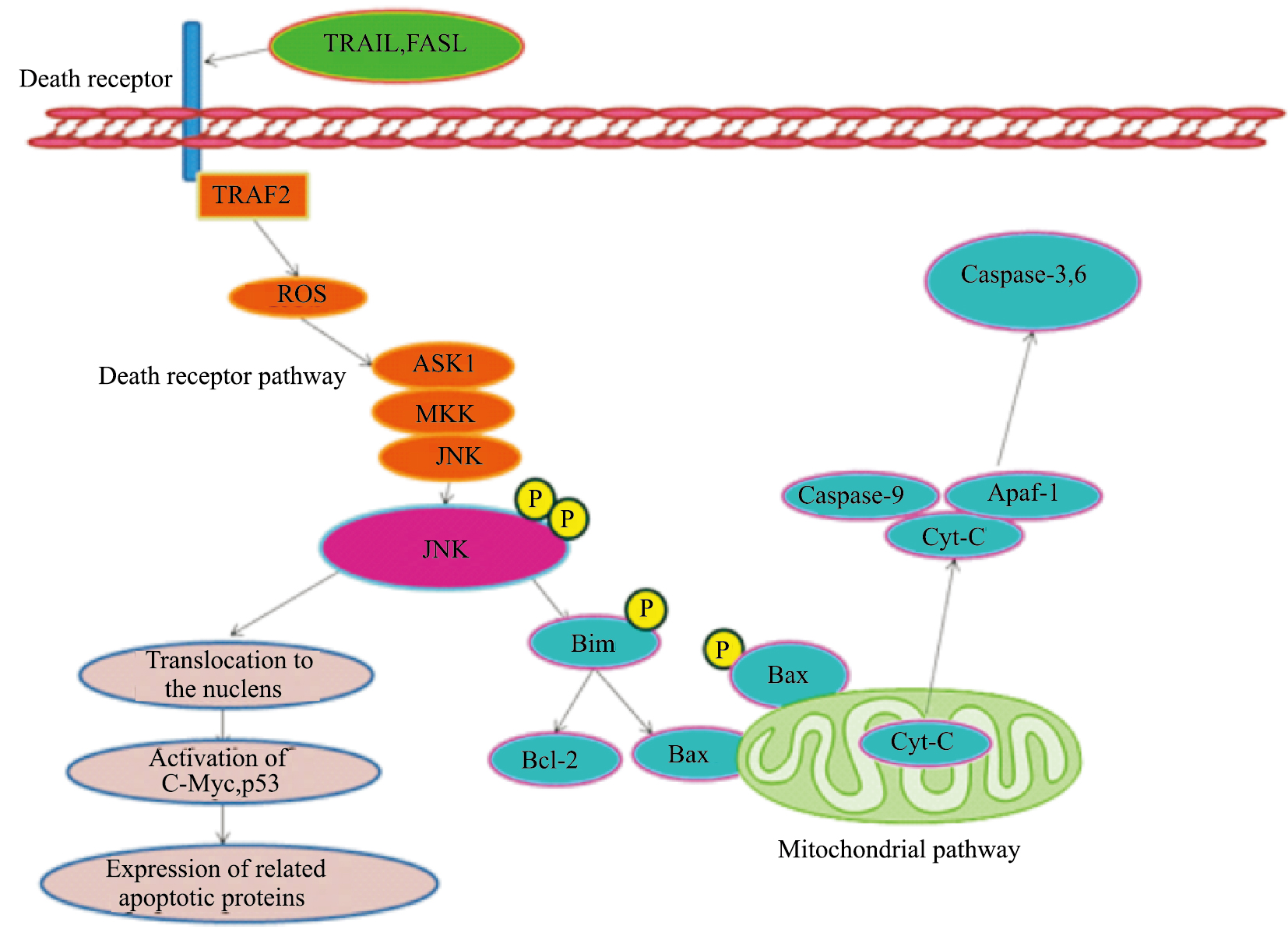
4.2.1 JNK诱导细胞凋亡的信号通路许多国内外的实验已经表明,JNK促凋亡的机制主要有两种(Fig3):一是通过死亡受体途径上调促凋亡蛋白的表达。一部分活化的JNK会迅速地从细胞质进入到细胞核中,被磷酸化后能够激活c-jun、c-Fos、Elk-1等转录因子,这些核内转录因子能够调节处于下游的凋亡靶基因转录以及凋亡蛋白的表达[13],如细胞核中被磷酸化的JNK能激活相关的转录因子来诱导FasL、TRAIL、TNF等死亡配体的表达,这些死亡配体与死亡受体(Fas、TNFR)相结合形成死亡诱导信号复合物并激活caspase,从而启动死亡受体途径来促进细胞凋亡[14, 15]。二是作用于线粒体途径。活化的JNK可以进入到细胞核内,也可以留在细胞质中,进入到细胞核内的JNK可以通过调节Bim、Bid、DP5等蛋白的表达来激活Bax等促凋亡蛋白,而留在细胞质中的JNK能通过磷酸化Thr167位点从而直接激活促凋亡蛋白Bax[16],除此之外,活化的JNK还会直接调节BH3-only等促凋亡蛋白的表达,从而使Bax等促凋亡蛋白活化。当然,活化的JNK也会调节Bcl-2、Bcl-XL等抗凋亡蛋白的表达,而抗凋亡蛋白Bcl-2和促凋亡蛋白Bax的比率与细胞的存活或凋亡有很大的联系,当Bcl-2和Bax的表达量处于动态平衡时细胞正常,当Bcl-2的表达大于Bax表达时,Bcl-2会首先形成同源二聚体从而阻止细胞凋亡,当Bax的表达量比Bcl-2大时,Bax能迅速形成同源二聚体来诱导细胞凋亡[17],被刺激后的Bax从细胞质转入到线粒体上从而使线粒体膜的通透性转变孔过度开放,使细胞色素C、Smac等促凋亡因子释放至细胞质激活caspase酶,通过线粒体途径来促进细胞的凋亡,其凋亡途径为:JNK→Bim→Bax→Cyt-C→Caspase-9→Caspase-3/6。
|
| Fig.3 JNK mediated apoptosis pathway Death receptor:死亡受体;Death receptor pathway:死亡受体途径;Translocation to the nucleus:转位至细胞核;Activation of C-Myc, p53:激活P53,C-Myc;Expression of related apoptotic proteins:相关凋亡蛋白的表达;Mitochondrial pathway:线粒体途径 |
神经退行性疾病是大脑或脊髓的细胞神经元异常凋亡和萎缩而导致运动、记忆等功能障碍。如,阿尔茨海默病(Alzheimer’s disease,AD)、帕金森病(Parkinson disease’s,PD)和脑缺血(cerebralischemia)等。然而,JNK信号通路的活化会使神经细胞凋亡,由此,它与神经退行性疾病有很大的联系。
AD的典型病理特征是脑内出现了大量的老年斑,其主要成分是β淀粉样蛋白(β-amyloid,Aβ)。β淀粉样蛋白的异常聚集等因素能够激活JNK并诱导神经细胞死亡[18]。丛伟红等[19]研究发现,在大鼠的海马神经元注射Aβ后,与对照组相比磷酸化的JNK阳性细胞大量增加,进一步观察后发现海马神经元也明显的增多并伴有胶质细胞的产生。在AD小鼠模型和AD死者的脑中都能够检测到大量磷酸化JNK及其底物c-Jun[20]。PD是由多巴胺能神经元的选择性丢失或凋亡而引起的另外一种神经退行性疾病。研究发现JNK通路的激活也会导致PD。在对患有PD的小鼠模型进行神经毒素MPTP诱导后以及PD病人死后的尸检中,均能检测到活化的JNK,而活化的JNK能促进多巴胺能神经元凋亡,当注射JNK抑制剂SP00125后,多巴胺能神经元凋亡会明显减少[21]。
4.2.3 对癌细胞凋亡的影响许多研究报道,JNK信号通路与肿癌的发生有紧密的联系,在不同类型的肿癌中发挥着非常重要的作用,其可以促进肿瘤细胞的凋亡,抑制肿瘤的形成(Tab1)。从紫色秃马勃中分离出的一种新型蛋白质提取物大马勃,它可以激活JNK信号通路使结肠癌细胞凋亡,可以用这种方法来治疗结肠癌患者,然而,使用JNK抑制剂SP600125后,发现大马勃对SW480细胞的促凋亡作用明显减弱[22]。活化的JNK可以抑制肺癌细胞的形成或变异细胞的生长,维持上皮细胞的分化[23]。除此之外,Kennedy等[24]研究发现,敲除小鼠的JNK基因后既会导致其肿瘤数量迅速增加又会加快肿瘤的生长速度,这表明JNK通路可能抑制肿瘤细胞的生成或诱导肿瘤细胞凋亡,防止肿瘤的发生。JNK之所以能够抑制肿瘤的发生,这跟它的促凋亡机制有关或者它能通过对CD8+ T淋巴细胞免疫系统的影响来加强对肿瘤的监护[25]。
4.2.4 对心肌细胞凋亡的影响心肌缺血/再灌注损伤(myocardium ischemia/reperfusion injury,MI/RI)是心肌器官在缺血较长时间后再提供血液,不仅不能保护机体的恢复功能,反而会比灌注前加重机体的损伤,并且出现一些功能性障碍。JNK是一种促凋亡激酶,它能够介导两种促凋亡途径,然而在心肌细胞的凋亡过程中主要是由线粒体途径介导的[26]。Jeong等[27]研究发现,在大鼠的心肌缺血/再灌注模型中加入姜黄素后,观察到凋亡激酶JNK以及心肌梗死面积都会减少。同时,Ghosh等[28]也证实,As2O3可以激活心肌细胞内的JNK信号,而JNK抑制剂SP600125能够降低NF-κB和IKK的磷酸化从而抑制JNK信号通路的活化,由此减少心肌细胞的凋亡。在氧化损伤的心肌细胞中,磷酸化的JNK会增加,加入人参皂苷Rb1和JNK抑制剂后,心肌细胞的凋亡得到抑制其活性会提高[29]。
4.2.5 对肝细胞凋亡的影响JNK信号通路在缺血诱导的肝细胞中的损伤作用远远大于对中枢神经系统的损伤,肝损伤主要发生在肝移植、肿瘤切除和循环性休克等条件下,JNK信号通路是在再灌注期活性氧产生之后被激活的。研究发现,在肝脏缺血/再注灌的早期,JNK磷酸化的程度会有明显的提高,JNK在肝脏缺血/再灌注中对其具有损伤作用,然而JNK的潜在抑制剂人参皂苷Rg1可以减小其损害[30]。Takamura等[31]用GalN/LPS诱导正常小鼠后发现其肝脏会立刻衰竭,当加入JNK特异性抑制剂sp600125后,发现其能够抑制肝细胞的凋亡,表明JNK可能与GalN/LPS诱导的小鼠肝细胞凋亡有关。Uehara等[32]以大鼠的肝为研究对象证实:JNK信号通路是肝脏缺血/再灌损伤的主要调节因素,JNK可以通过线粒体途径和死亡受体途径共同介导由肝脏缺血/再灌损伤引起的肝细胞凋亡,而具有高选择性、可逆性竞争ATP的JNK抑制剂(CC0209766、CC0223105以及信号药物CC-401)都可以抑制Bak的激活和Bid的降解过程,从而降低肝细胞和肝窦内皮胞坏死及凋亡。
5 结语与展望近几年来,随着越来越多的JNK下游底物和调节因子的发现,这为研究JNK信号通路在细胞增殖和细胞凋亡过程中的病理生理功能打下了良好的基础,然而JNK对细胞最终命运的影响取决于它被何种上游信号激活以及以何种蛋白作为底物。与JNK结合受其调控或影响的蛋白质非常多,有些是促进细胞凋亡,而另一些则是抑制凋亡过程促进细胞存活或增殖,即使在细胞凋亡中,它们的凋亡机制和途径也是不一样的,如在调控神经、癌、心肌、肝细胞凋亡中,有的是通过死亡受体途径,还有的是通过线粒体途径来促进细胞的凋亡。
在不同的细胞类型和不同的抗癌药物作用下,JNK的激活状态和与之相结合的蛋白质存在极大的差异,激活的信号通路也不尽相同,产生的生物效应大相径庭。而直接以JNK为作用靶点的抗癌药物很容易同时影响到细胞的多条信号通路的激活与关闭,药物选择性差、副作用大,因此需要更加透彻的理解JNK信号通路参与各种细胞凋亡及疾病发生的具体机制,从而提供更多的由细胞凋亡引起的疾病的治疗方法。相信在不久的将来,人们对JNK信号通路将会有更清晰、更明确的认识,从而为人类的健康做出巨大的贡献。
| [1] | Owen G R, Achilonu I, Dirr H W. High yield purification of JNK1β1 and activation by in vitro reconstitution of the MEKK1→MKK4→JNK MAPK phosphorylation cascade[J]. Protein Expres Purif, 2013, 87(2):87-99. |
| [2] | Seki E, Brenner D, Karin M. A Liver full of JNK:Signaling in regulation of cell function and disease pathogenesis, and clinical approaches[J]. Gastroenterology, 2012, 143(2):307-20. |
| [3] | Cargnello M, Roux P P. Activation and function of the MAPKs and their substrates, the MAPK-activated protein kinases[J]. Mcrobiol Mol Biol Rev, 2011, 75(1):50-83. |
| [4] | Plotnikov A, Zehorai E, Procaccia S, Seger R. The MAPK cascades:Signaling components, nuclear roles and mechanisms of nuclear translocation[J]. Biochim Biophys Acta, 2011, 1813(9):1619-33. |
| [5] | Bubici C,Papa S.JNK signaling in cancer:in need of new, smarter therapeutic targets[J].Br J Pharmacol,2014,171(1):24-37. |
| [6] | Makino T, Jinnin F C, Muchemwa S, et al. Basic fibroblast growth factor stimulates the proliferation of human dermal fibroblasts via the ERK1/2 and JNK pathways[J]. Brit J Dermatol, 2010, 162(4):717-23. |
| [7] | Leventaki V, Drakos E, Karanikou M, et al. C-JUN N-terminal kinase (JNK) is activated and contributes to tumor cell proliferation in classical Hodgkin lymphoma[J]. Human Pathol, 2014, 45(3):565-72. |
| [8] | Sakurai T, Maeda S, Chang L, Karin M. Loss of hepatic NF-κB activity enhances chemical hepatocarcinogenesis through sustained c-Jun N-terminal kinase 1 activation[J]. Proc Natl Acad Sci USA, 2011,103(28):10544-51. |
| [9] | Nateri A S, Spencer-Dene B, Behrens A. Interaction of phosphorylated c-Jun with TCF4 regulates intestinal cancer development[J]. Nature, 2005, 437(7056):281-5. |
| [10] | Chang Q, Zhang Y, Beezhold K J, et al. Sustained JNK1 activation is associated with altered histone H3 methylations in human liver cance[J]. Hepatol, 2009, 50(2):323-33. |
| [11] | Uhlirova M, Jasper H, Bohmann D. Non-cell-autonomous induction of tissue overgrowth by JNK/Ras cooperation in a Drosophila tumor model[J]. Proc Natl Acad Sci USA, 2005, 102(37):13123-8. |
| [12] | 候炳旭,冯丽英.JNK信号通路介导的凋亡在疾病中的作用[J].世界华人消化杂志, 2011,19(17):1819-25. Hou B X, Feng L Y. Role of JNK signaling pathway-mediated apoptosis in diseases[J]. Shijie Huaren Xiaohua Zazhi, 2011, 19(17):1819-25. |
| [13] | Raman M, Chen W, Cobb M H. Differential regulation and properties of MAPKs[J]. Oncogene, 2007, 26:3100-12. |
| [14] | Carboni S, Antonsson B, Caillard P, et al. Control of death receptor and mitochondrial-dependent apoptosis by c-jun N-terminal kinase in hippocampal CA1 neurones following global transient ischeamia[J]. J Neurochem, 2005, 92(5):1054-60. |
| [15] | Eferl R, Wagner E F. AP-1:a double-edged sword in tumorigenesis[J].Nat Rev Cancer, 2003, 3(11):859-68. |
| [16] | Bogoyevitch M A, Kobe B. Uses for JNK:the many and varied substrates of the c-Jun N-terminal kinases[J]. Microbiol Mol Biol Rev, 2006, 70(4):1061-95. |
| [17] | Renault T T, Teijido O, Antonsson B, et al. Regulation of Bax mitochondrial localization by Bcl-2 and Bcl-XL:keep your friends close but your enemies closer[J]. Int J Biochem Cell B, 2013, 45(1):64-7. |
| [18] | Smith W W, Gorospe M, Kusiak J W. Signaling mechanisms underlying Aβ toxicity:potential therapeutic targets for Alzheimer's disease[J].CNS Neurol Disord-DR, 2006, 5(3):355-61. |
| [19] | 丛伟红, 刘建勋, 杨 斌, 董小霞. JNK信号通路参与Aβ毒性对大鼠海马神经元的损伤[J]. 中国药理学通报, 2010, 26(8):1034-7. Cong W H, Liu J X, Yang B, Dong X X. JNK signal transduction pathway participated Aβ-induced neuronal injury in rat hippocampus[J]. Chin Pharmacol Bull, 2010, 26(8):1034-7. |
| [20] | Resnick L, Fennell M. Targeting JNK3 for the treatment of neurodegenerative disorders[J]. Drug Discov Today, 2004, 9(21):932-9. |
| [21] | Pan J, Zhao Y X, Wang Z Q, et al. Expression of FasL and its interaction with Fas are mediated by c-Jun N-terminal kinase (JNK) pathway in 6-OHDA-induced rat model of Parkinson disease[J]. Neurosci Lett, 2007, 428(2):82-7. |
| [22] | Tsay J G, Chung K T, Yeh C H, et al. Calvatia lilacina protein-extract induces apoptosis through glutathione depletion in human colorectal carcinoma cells[J]. J Agric Food Chem, 2009, 57(4):1579-88. |
| [23] | Winn R A,Marek L,Han S Y, et al. Restoration of Wnt-7a expression reverses non-small cell lung cancer cellular transformation through frizzled-9-mediated growth inhibition and promotion of cell differ entiation[J]. J Biol Chem, 2005, 280(20):19625-34. |
| [24] | Kennedy N J, Sluss H K, Jones S N, et al. Suppression of Ras-stimulated transformation by the JNK signal transduction pathway[J]. Genes Dev, 2003, 17(5):629-37. |
| [25] | Gao Y, Tao J, Li M O, et al. JNK1 is essential for CD8+ T cell-mediated tumor immune surveillance[J]. J Immunol, 2005, 175(9):5783-9. |
| [26] | Aoki H, Kang P M, Hampe J, et al. Direct activation of mitochondrial apoptosis machinery by c-Jun N-terminal kinase in adult cardiac myocytes[J]. J Biol Chem, 2002, 277(12):10244-50. |
| [27] | Jeong C W, Yoo K Y, Lee S H, et al. Curcumin protects against regional myocardial ischemia/reperfusion injury through activation of RISK/GSK-3β and inhibition of p38 MAPK and JNK[J]. JCPT, 2012, 17(4):387-94. |
| [28] | Ghosh J, Das J, Manna P, Sil P C. Taurine prevents arsenic-induced cardiac oxidative stress and apoptotic damage:Role of NF-κB, p38 and JNK, MAPK pathway[J].Toxicol Appl Pharmacol, 2009, 240(1):73-87. |
| [29] | Li J, Shao Z H, Xie J T, et al. The effects of ginsenoside Rb1 on JNK in oxidative injury in cardiomyocytes[J]. Arch Pharm Res, 2012, 35(7):1259-67. |
| [30] | Zhang X J, He C W, Li P, et al, Ginsenoside Rg1, a potential JNK inhibitor, protects against ischemia/reperfusion-induced liver damage[J]. J Funct Foods, 2015, 15:580-92. |
| [31] | Takamura M, Matsuda Y, Yamagiwa S, et al. An inhibitor of c-Jun NH2-terminal kinase, SP600125, protects mice from D-galactosamine/lipopolysaccharide-induced hepatic failure by modulating BH3-only proteins[J]. Life Sci, 2007, 80(4):1335-44. |
| [32] | Uehara T, Benett B, Sakata S T, et al. JNK mediates hepatic ischemia reperfusion injury[J]. J Hepatol, 2005, 42(6):850-9. |

