


2. 复旦大学遗传与发育协同创新中心, 上海 200433;
3. 湖南省分子靶标新药研究协同创新中心, 湖南 衡阳 421001
2. Collaborative Innovation Center for Genetics and Development, Fudan University, Shanghai 200433, China;
3. Hunan Province Cooperative Innovation Center for Molecular Target New Drug Study, Hengyang Hunan 421001, China
人类基因组计划的完成使得人类得以从基因的角度透析疾病。而后分子和细胞生物学的多层次的表观基因组、转录组、蛋白质组、脂质组、微生物组、代谢组以及暴露组的研究使得能够从分子和细胞水平解读疾病发生和发展[1]。同时,大量临床试验数据及经验的积累,为实施大规模队列研究和人类表型组计划打下基础。测序技术的迅猛发展以及超级计算机对生物大数据的处理能力也使得精确分析表型与遗传因素之间关系成为可能。
组学研究、大规模队列试验和数据处理是精准医学的核心。精准医学是综合个体遗传因素及环境因素信息与表型关联的个体化医学模式,是在大数据驱动下的一门多学科交叉学科。鉴于我国巨大的医疗资源需求的现状,研究和实施适合我国国情的精准医学计划旨在解决以“群体”为对象的传统医学诊断误差大、用药非精准以及医疗资源浪费大的难题,具有积极的社会意义和经济意义。
本文就精准医学的提出和发展基础,以及国内相关研究进展进行综述。
1 从循证医学到精准医学循证医学时代强调“群体”的临床证据,而忽视了“个体”的复杂性以及“个体”的遗传特性和环境因素的差异性。循证医学过分关注群体统计学差异,忽视了临床实践的真正意义;而精准医学正是关注于“个体”:这便决定未来的医学模式将从循证医学转变为精准医学。
“精准医学(precision medicine)”一词最早是由哈佛大学商学院商业战略家Clayton Christensen在2008年提出以表述分子诊断使得医生不用依赖于直觉和经验便可以明确诊断[2]。但是,当时这个描述并没有引起太多的关注。
2011年美国国立研究委员会下属的“发展新疾病分类法框架委员会”发表的《迈向精准医学:建立一个生物医学知识网络和一个新疾病分类法框架》蓝图,作为“个体化医学”的新表述形式,“精准医学”才开始被广泛重视。精准医学是指为每位病患的个体特征制定医疗方案,根据对某种疾病的易感性或特定治疗方案的反应将患者个体分成亚群;然后将预防或治疗措施集中于有效病患,而免去给无效患者带来费用和副作用。[3]“精准”包括“准确(accurate)”和“精密(precise)”两重含义。精准医学根据病人个体特异性制定个性化精准预防、精准诊断和精准治疗方案,是具有颠覆性的医学新模式[4]。
2015年初,奥巴马政府在国情咨文中提出美国的“精准医学计划(precision medicine initiative,PMI)”[5, 6],并为精准医学计划的5个具体内容在2016财年预算案中提出2.15亿美元预算。“精准医学计划”是以遗传信息的发现和人类基因组计划的实施为基础,依靠百万志愿者的基因组信息和临床信息的大数据来支撑癌症与其它多基因病研究,转变相关管理部门的监管方式,寻求公立机构和私立机构良好合作的大型全国性乃至全球性前瞻性项目[7]。
从循证医学到精准医学是一个粗放到精确的过程:循证医学关注于“群体”统计学差异,精准医学则关注于“个体”组学特征;循证医学强调随机对照数据,精准医学强调分子生物学证据。
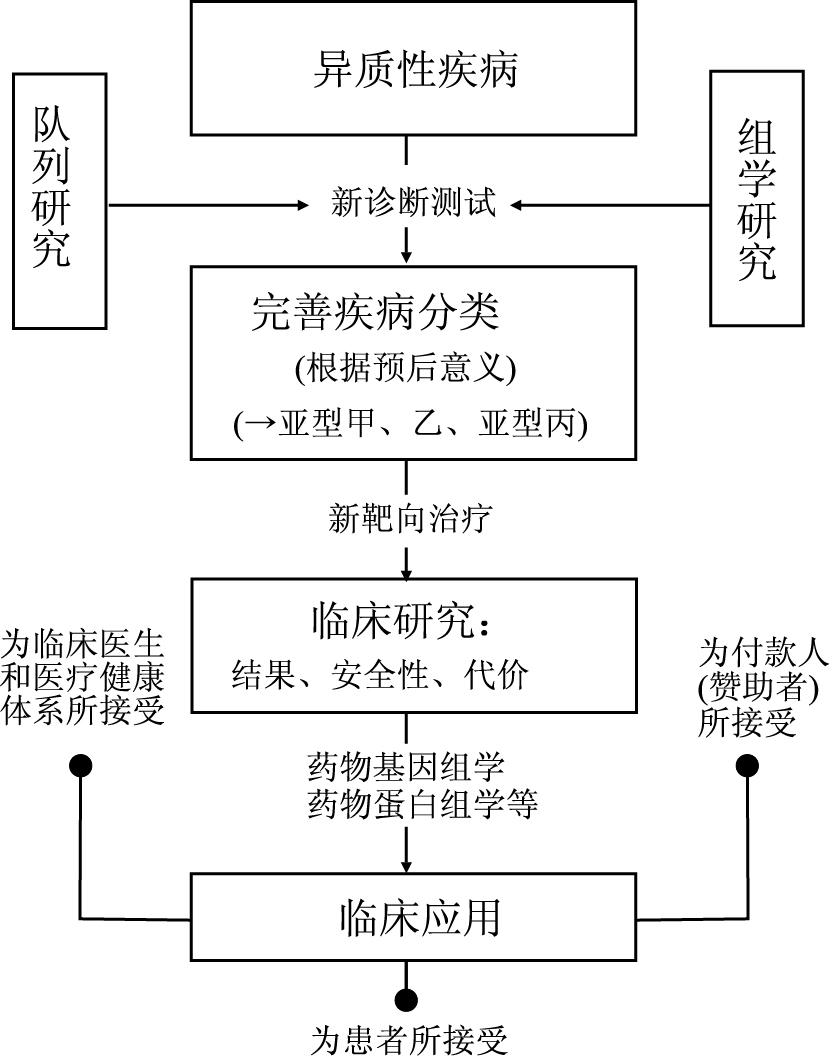
2 精准医学研究的核心和基础精准医学研究的主要目的是通过标准化的各种大型的队列研究和多种组学研究,寻找疾病的新的生物标志物以完善疾病分类;完善后的新疾病分型通过药物基因组学等手段进行临床转化,达到个体化的精准医疗(Fig2)。其中大型队列研究是精准医学的核心;多种组学研究是精准医学的基础,其中药物基因组学、药物表观基因组学以及药物蛋白组学等是精准医疗临床转化的桥梁;大数据的标准化处理与发掘是精准医学的重要凭据。
|
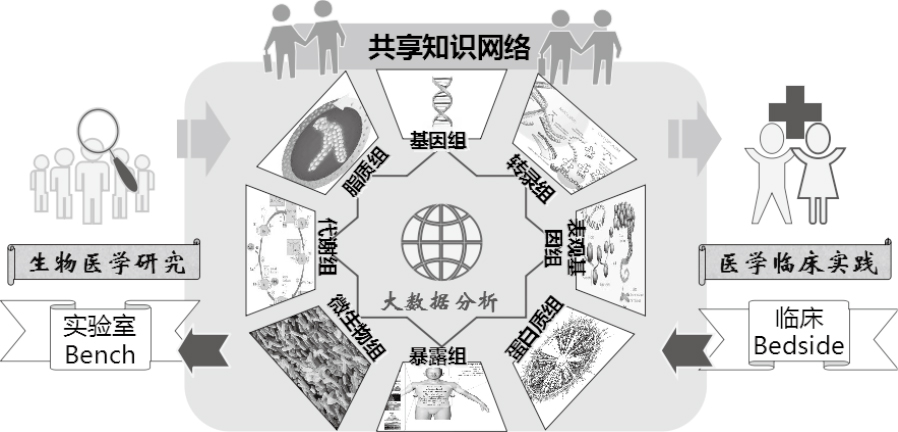
| Fig.1 Common knowledge network of precision medicine |
|
| Fig.2 Scope of precision medicine |
作为精准医学研究的核心,大规模队列研究通过对大规模健康和疾病人群的随访信息和临床样本的收集,进行多层次综合性的组学研究,有利于发现疾病早期诊疗的生物标志物。其中新药临床试验由于规范度高、标准化好等优势,是精准医学大规模队列研究中规范样本和表型数据的重要来源。医院生物样本和临床信息是精准医学的宝贵资源和重要前提,由于其复杂的多样性,其可靠性成为决定精准医学成败的关键。
欧洲癌症与营养关系的前瞻研究计划(european prospective investigation into cancer and nutrition,EPIC)自二十世纪末起开始调查膳食、代谢及遗传因素与癌症发病之间的关系。EPIC通过对10个欧洲国家的50万余人群的长期随访(其中2.6万人后期发展为癌症),以及对900万例样本的收集和分析,研究了不同膳食类型、遗传多态性等与癌症发生发展的关系。其研究结果对降低癌症发病率、减轻癌症患者的痛苦并延长患者的生存期具有积极的意义[8]。
欧洲遗传和基因组流行病学网络(european network for genetic and genomic epidemiology,ENGAGE)荟萃了13 个国家的 39 份队列研究中超过60万的研究对象。其目的是通过将欧洲及其他种群队列遗传和基因组研究中新产生的流行病学数据转换为与未来临床应用相关的信息。ENGAGE使得研究人员能够确定大量的影响代谢、行为和心血管性状的新易感基因,并研究基因和生活方式的因素之间的相互作用。
电子医疗记录(electric medicine record,EMR)作为数字化的临床信息记录,具有标准统一、可读性强等特点。电子医疗记录基因组学网络(eMERGE网络)是EMR的发展。自2007年成立以来,eMERGE网络已经在基因组学和生物信息学领域取得了长足的进步,是基因组学研究的一个强大且非常具有成本效益的工具[9]。
2.2 组学研究疾病的成因是复杂的,基因无法单独解释全部现象,因而综合性、多层次、跨尺度的组学研究是必要的(Fig1)[10]。一项研究表明,基因组只能解释弥漫性大B细胞淋巴瘤患者治疗一度起效后但又最终失效原因的40%。而癌细胞表观基因组的整体改变开启了应当关闭的正常基因,或是反过来关闭了应当开启的正常基因,很大程度上决定了疾病进展[10]。
基因组学是多组学研究的基础。从1990年“人类基因组计划”被提出和实施开始,新一代测序技术的发明与应用大大缩短了全基因组测序所需时间和成本。成本的降低和速度的提升使得针对普通个人的基因组应用成为可能,个体基因组为精准医学的临床应用(个体化医疗)提供基础。HapMap计划、千人基因组计划以及ENCODE计划等重大基础性国际研究计划的完成也推动基因组学的持续向前发展。
药物基因组学是实现药物精准治疗的基础;药物基因组学完美诠释了精准医学的accuracy和precise,前者体现为治疗靶点的精准和靶向治疗,如吉非替尼针对突变型的EGFR受体;后者体现为治疗剂量的精准,如TPMT突变纯合子基因型患者使用6-巯基嘌呤剂量应减少为10%。药物基因组学是精准医学临床转化的基础和关键环节:通过对患者遗传特性的研究和分型,能够将药物应用于特定的有效患者,从而改善用药的安全性和有效性,达到精准医学的完美临床转化[12, 13, 14]。例如,研究表明PD-1(programed death-1)抗癌免疫疗法治疗非小细胞肺癌时会出现个体化差异:高突变患者对PD-1疗法敏感,低突变患者敏感度低,患者整体应答水平只有17%~21%;通过药物基因组学可以使其在特定亚型(高突变)患者的有效性和安全性大幅提升[15]。此外,药物基因组学能够加速新药靶点的发现,加速靶向新药的研发和上市[16]。在我国原创抗癌新药西达本胺(组蛋白去乙酰化酶抑制剂)的研发和上市过程中,药物基因组学便起到了极大的促进作用。
| 医疗领域 | 疾病名称 | 生物标志物 | 干预 |
| 肿瘤 | 慢性粒细胞白血病 | BCR-ABL | 伊马替尼 |
| 肺癌 | EML4-ALK | 克唑替尼 | |
| 黑色素瘤/甲状腺癌 | BRAF V600E | 威罗菲尼 | |
| 乳腺癌 | HER2 | 曲妥珠单抗 | |
| 血液病 | 血栓 | 凝血因子V | 避免使用成血栓药物 |
| 传染病 | HIV/AIDS | CD4 + T细胞、HIV病毒载量 | 高活性抗逆转录病毒治疗 |
| 心血管疾病 | 冠状动脉疾病 | CYP2C19 | 氯吡格雷 |
| 肺病 | 囊性纤维化 | G551D | 依伐卡托 |
| 肾脏疾病 | 移植排斥反应 | 尿液中的基因标记 | 抗排斥药物 |
| 肝脏疾病 | 丙型肝炎 | 丙型肝炎病毒载量 | 直接作用的抗病毒药物 |
| 内分泌疾病 | 2型多发性内分泌腺瘤 | RET | 预防性甲状腺切除术 |
| 代谢性疾病 | 高脂血症 | 低密度脂蛋白胆固醇 | 他汀类药物 |
| 神经内科疾病 | 自身免疫性脑炎 | CXCL13 | 免疫治疗 |
| 精神疾病 | 酒精利用障碍 | GRIK1 | 托吡酯 |
| 药物基因组学 | 戒烟 | CYP2A6 | 伐尼克兰 |
| 眼科疾病 | Leber先天性黑蒙 | RPE65 | 基因治疗 |
对癌症、糖尿病等复杂疾病的大规模基因组学研究有助于人类更好地治疗这些疾病。2007年成立的国际肿瘤基因组协作联盟(ICGC)启动了全球范围的肿瘤基因组研究工作,提出对50种癌症绘制体细胞基因突变谱的任务。其成果将推动癌症基因组学向肿瘤生物学的转化研究,促进癌症的个体化精准治疗[17]。
“人类蛋白质组计划(human proteome project,HPP)”是对“人类基因组计划”的延续。HPP对人体内蛋白质的丰度、分布、细胞亚定位、相互作用和细胞功能等进行研究,为基因组学研究提供补充[18]。
表型组学研究是将基础组学研究与临床表型相联系的重要环节。2003年开始进行的“人类表型组计划”在一系列不同水平(分子,细胞,组织和机体水平)收集特定患者表型信息(包括行为、对药物的敏感性等)[19]。通过生物信息分析融合得到组学信息-临床表型联系(Fig3),进而根据患者组学信息指导个体化精准医疗。

|
| Fig.3 Correlation between genomic information and phenotype of precision medicine |
组学技术的质量和标准是精准医学的关键之一。生物大数据来源具有多样性:临床上的成像数据、不同检测标准检测出的健康指标数据,以及无统一标准的组学数据都是生物大数据来源。目前组学研究成果的重复性差、可靠性低、缺乏标准化的数据发掘流程。由于缺乏标准化的数据发掘流程,导致开发的许多生物标志物流程可靠性、适用性差且难以重复,进而使得许多临床试验被迫中止。因而,开发相应的组学技术质量控制标准是十分必要而迫切的。Shi等[20]领导的基因芯片质量控制(microarray quality control,MAQC)项目制定的质量控制标准有利于推动精准医学生物大数据收集标准化。
大数据分析对大样本的临床试验数据和临床表型数据的分析综合、组学数据与表型数据的联系的发现、潜在分子标志物的发现均有积极作用。组学研究会产生海量数据,巨大的数据量,单靠人工进行分析解读几乎是不可能办到的。通过超级计算机进行生物信息学大数据分析(二次分析),全基因组测序产生的TB级原始数据能够被缩减至GB级:数据量的减少,为组学信息的快速解读提供可能[21]。
3 结语“精准医学”一词是对完美临床结果的一种期待,其带有的理想主义色彩使得其潜力可能被高估[22]。基因组数据对临床治疗方案选择的影响是确切的,但是病人的治疗结果不可能单独地为基因所决定。病人还受到生活经验、文化背景、教育程度、成长环境以及其他诸多因素的影响,使得“精准”地实施困难重重。精准医学最终目是临床精准治疗——从基础研究成果到针对病人实际情况的个体化医疗。如何将精准医学基础研究成果转化,服务于临床实践,将是精准医学相关人员需要思考的转化医学问题。正如“现代医学之父”威廉·奥斯勒爵士所言:“合格的医生着眼于病情,而优秀的医生则关注于病人”。
| [1] | 于军."人类基因组计划"回顾与展望:从基因组生物学到精准医学[J].自然杂志, 2013,35(5):326-31. Yu J. Ten years after the Human Genome Project:from genome biology to precision medicine[J]. Chin J Nat, 2013,35(5):326-31. |
| [2] | Katsnelson A.Momentum grows to make 'personalized' medicine more 'precise'[J].Nat Med, 2013,19(3):249. |
| [3] | New NRCU, Disease TO.Toward precision medicine:building a knowledge network for biomedical research and a new taxonomy of disease[M]. Washington (DC):National Academies Press (US), 2011:7-62. |
| [4] | Dolsten M, Sogaard M.Precision medicine:an approach to R&D for delivering superior medicines to patients[J].Clin Transl Med, 2012,1(1):7. |
| [5] | Reardon S.Precision-medicine plan raises hopes[J].Nature, 2015,517(7536):540. |
| [6] | Collins F S, Varmus H.A new initiative on precision medicine[J].N Engl J Med, 2015, 372(9):793-95. |
| [7] | 杨焕明.奥巴马版"精准医学"的"精准"解读[J].中国医药生物技术, 2015(03):193-5. Yang H M.A precise interpretation to 'precision medicine'of president Obama[J].Chin Med Biotechnol, 2015(03):193-5. |
| [8] | Bingham S, Riboli E.Diet and cancer-the European Prospective Investigation into Cancer and Nutrition[J].Nat Rev Cancer, 2004,4(3):206-15. |
| [9] | Gottesman O, Kuivaniemi H, Tromp G, et al.The Electronic Medical Records and Genomics (eMERGE) network:past, present, and future[J].Genet Med, 2013,15(10):761-71. |
| [10] | Garay J P, Gray J W.Omics and therapy-A basis for precision medicine[J].Mol Oncol, 2012,6(2):128-39. |
| [11] | Pan H, Jiang Y, Boi M, Tabbo F,et al.Epigenomic evolution in diffuse large B-cell lymphomas[J].Nat Commun, 2015,6:6921. |
| [12] | 张月丽, 周宏灏, 张伟.维生素的药物基因组学研究进展[J].中国药理学通报, 2014,30(11):1503-7. Zhang Y L, Zhou H H, Zhang W. Advance in research on pharmacogenomics of vitamin[J]. Chin Pharmacol Bull, 2014,30(11):1503-7. |
| [13] | 曾媚姿, 张伟.矿物质的药物基因组学研究进展[J].中国药理学通报, 2014,30(10):1338-42. Zeng M Z, Zhang W. Proress in research on pharmacogenomics of minerals and trace elements[J]. Chine Pharmacol Bull, 2014,30(10):1338-42. |
| [14] | 呼晓雷, 周继朋, 陈小平.AGXT2与ADMA代谢及心脑血管疾病的研究进展[J].中国药理学通报, 2015,31(5):601-5. Hu X L, Zhou J P, Chen X P. Role of AGXT2 in ADMA metabolism and the development of cardiovascular and cerebrovascular diseases[J]. Chin Pharmacol Bull, 2015,31(5):601-5. |
| [15] | Rizvi N A, Hellmann M D, Snyder A, et al.Cancer immunology. Mutational landscape determines sensitivity to PD-1 blockade in non-small cell lung cancer[J].Science, 2015,348(6230):124-8. |
| [16] | 温家根, 周宏灏, 张伟.药物基因组学在药物研发中的转化与应用[J].中国药理学通报, 2013,29(4):445-9. Wen J G,Zhou H H,Zhang W. Transformation and application of pharmacogenomics in drug development[J]. Chin Pharmacol Bull, 2013,29(4):445-9. |
| [17] | 胡学达, 杨焕明, 赫捷, 等.肿瘤基因组学与全球肿瘤基因组计划[J].科学通报,2015,(09):792-804. Hu X D, Yang H M, He J,et al. The cancer genomics and global cancer genome collaboration (in Chinese)[J]. Chin Sci Bull, 2015(09):792-804. |
| [18] | Legrain P, Aebersold R, Archakov A, et al.The human proteome project:current state and future direction[J].Mol Cell Proteomics, 2011,10(7):M111-9993. |
| [19] | Nelson F, Chiara S.The human phenome project[J].Nat Genet, 2003,34(1):15-21. |
| [20] | Shi L, Campbell G, Jones W D, et al.The MicroArray Quality Control (MAQC)-Ⅱ study of common practices for the development and validation of microarray-based predictive models[J].Nat Biotechnol, 2010,28(8):827-38. |
| [21] | Topol E J.Individualized medicine from prewomb to tomb[J].Cell, 2014,157(1):241-53. |
| [22] | Roden D M, Tyndale R F.Genomic medicine, precision medicine, personalized medicine:What's in a name[J]? Clin Pharmacol Ther, 2013,94(2):169-72. |

