


动脉粥样硬化(atherosclerosis,AS)病变是一种复杂的慢性血管炎症性疾病,血管壁的内皮细胞、平滑肌细胞、炎症细胞和血小板功能均有改变[1]。机体的增龄变化、有害代谢产物的堆积以及氧化应激产物增加,均是导致动脉粥样硬化的危险因素。大量研究显示ox-LDL能够损伤血管内皮细胞,促进与动脉粥样硬化的发生[2, 3]。ox-LDL能够刺激血小板活化,促进血栓形成。活化的血小板通过释放细胞因子等炎症蛋白,促进动脉粥样硬化的血管炎症反应。
白藜芦醇(resveratrol,RSV)是多酚类物质,在葡萄籽和红酒中有较高的含量。研究发现[4, 5],RSV是天然的抗氧化剂,具有增加细胞内保护分子Sirt1表达,抗炎和抑制血栓形成的作用。Sirt1是近年来医学研究十分关注的细胞内源性保护性分子,在调节细胞能量代谢与长寿中起十分重要的作用[6]。动物实验研究表明,限制小鼠热量摄取,能够降低小鼠的能量代谢水平,增加Sirt1的表达,延长小鼠寿命[7]。很多研究已经确认Sirt1与机体长寿相关,是一个长寿基因[8, 9]。研究也证实RSV是Sirt1的激动剂,RSV能够增加细胞内Sirt1表达,减轻有害刺激对细胞的损伤,具有多种生物学保护作用。然而,RSV是否能够抑制ox-LDL刺激的血小板活化尚不清楚。本研究重点观察了RSV对ox-LDL诱导的血小板聚集、ROS产生、以及PECAM-1表达的影响,并对相关的分子机制进行了探讨。
1 材料与方法 1.1 药品与试剂白藜芦醇购自Sigma 公司,纯度为99% (货号:R5010)。抗PECAM-1、抗β-actin 抗体购自Santa Cruz 公司;抗Sirt1抗体购自Millipore公司;抗p38MAPK 和抗phospho-p38MAPK 抗体购自Cell Signaling 公司。辣根过氧化酶标记的山羊抗兔二抗、山羊抗小鼠二抗、兔抗山羊二抗购自北京中杉金桥公司。活性氧检测试剂盒(S0033)购自碧云天生物技术有限公司。
1.2 ox-LDL的制备收集新鲜人血清,用梯度超速离心法分离低密度脂蛋白。使用5 μmol·L-1硫酸铜氧化低密度脂蛋白,37℃,10 h,加入1 mmol·L-1 EDTA终止氧化反应。然后用PBS(pH 7.3)4 ℃透析24 h。用0.22 μm的Millex滤器过滤,用BCA法测定LDL蛋白浓度,4℃储存。
1.3 制备洗涤血小板取健康正常人血液,1 200 r·min-1离心10 min,分离上清,得到富血小板血浆。加入TYRODE Buffer (138 mmol·L-1 NaCl,3.3 mmol·L-1 NaH2PO4,2.9 mmol·L-1 KCl,1 mmol·L-1 MgCl2,5.5 mmol ·L-1 glucose,20 mmol ·L-1 HEPES,pH 7.2)和 9 ∶1的ACD (2.5% trisodium citrate,2.0% glucose,1.5% citric acid),2 mmol·L-1 EDTA,混匀,1 400 r·min-1离心10 min。弃上清,悬浮细胞。再次离心,获得洗涤血小板。将血小板悬浮液室温静置30 min后,进行实验。
1.4 血小板聚集测定使用Chrono-Log血小板聚集分析仪测定血小板聚集,血小板聚集率由血小板聚集分析仪的软件计算。取血小板悬浮液300 μL置于测定通道内,搅拌1 min,加入ox-LDL (0.1 g·L-1) 刺激血小板10 min; 药物干预组将100 μmol·L-1 RSV孵育血小板10 min,放入测定通道。搅拌1 min,再加入 ox-LDL (0.1 g·L-1)刺激血小板10 min,终止反应,获得血小板聚集曲线。
1.5 活性氧(ROS)测定使用活性氧检测试剂盒,将荧光探针DCFH-DA(1: 1 000)孵育血小板,37℃,30min,洗涤血小板3次。血小板细胞内的荧光强度用CARY Eclipse荧光分光光度计测定,激发波长为488 nm,发射波长为525 nm。阳性对照组用ox-LDL (0.1 g·L-1) 刺激细胞10 min,药物处理组用100 μmol·L-1 RSV孵育血小板10 min,再加入ox-LDL (0.1 g·L-1) 刺激细胞10 min,开始测定荧光强度。
1.6 Western blot方法检测蛋白表达分别用各种浓度的RSV(1、10、100 μmol·L-1)、p38MAPK 抑制剂SB203580(0.1、0.3、1 μmol·L-1)以及Sirt1抑制剂EX527(10、30、100 nmol·L-1)预孵育血小板10 min,加入ox-LDL(0.1 g·L-1)刺激血小板10 min,终止反应。采用BCA法测定蛋白浓度。取20 μg蛋白样品进行SDS-PAGE电泳后,转至PVDF膜上。用5%脱脂牛奶室温下封闭PVDF膜2 h,洗膜3次。分别加入特异性抗体(PECAM-1、Sirt1、p38MAPK、phospho-p38MAPK、β-actin),4℃,过夜。用TBS-T(100 mmol·L-1 Tris,150 mmol·L-1 NaCl,0.1% Tween,pH 7.2)洗膜3次,每次5 min。加入相应二抗(1 ∶10 000),室温孵育2 h。用TBS-T洗膜4次,每次5 min。最后,加入ECL发光液,用凝胶成像仪成像。
1.7 统计学方法所有数据来源于至少4次独立的实验,数据以x±s表示,采用双尾单因素方差分析以及Student t检验。
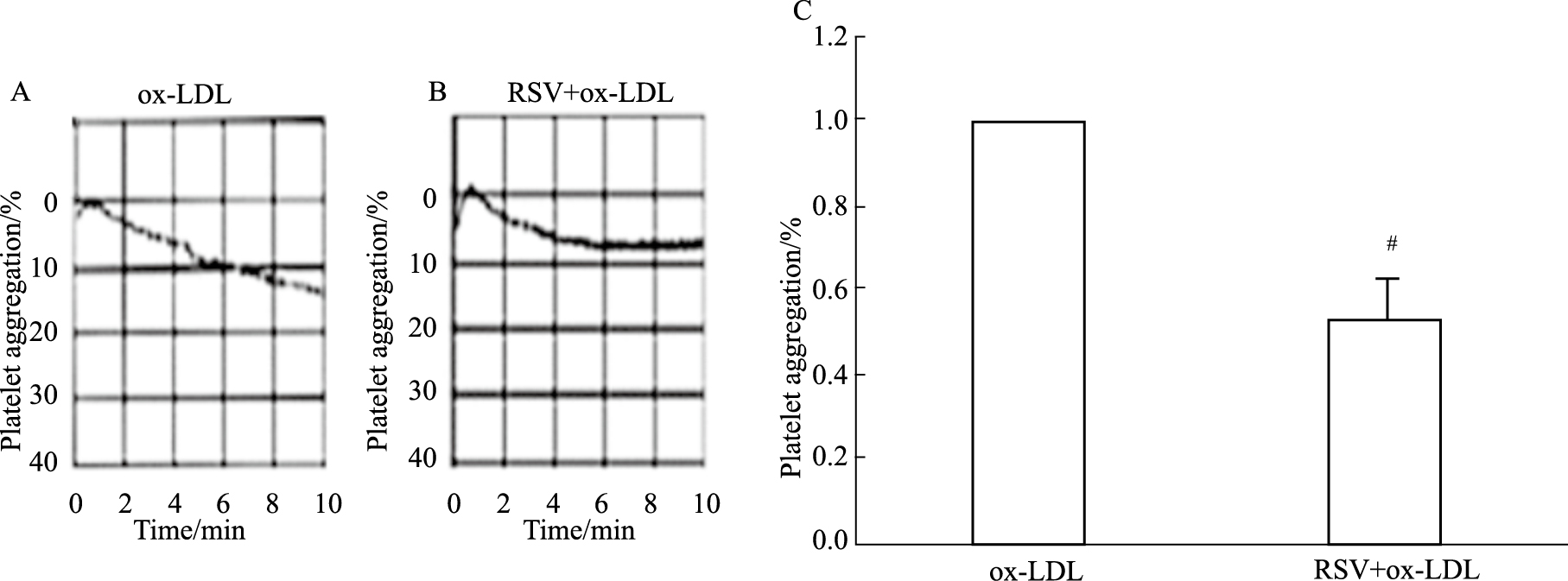
2 结果 2.1 白藜芦醇对血小板聚集的影响血小板聚集分析显示,ox-LDL(0.1 g·L-1)刺激血小板诱导了轻度的血小板聚集,聚集率为14%(Fig1A),而使用100 μmol·L-1白藜芦醇孵育10 min血小板后,血小板聚集受到抑制,聚集率为7%(Fig1B)。白藜芦醇的血小板聚集抑制率为50%,两组之间存在明显差异,差异具有统计学意义(P < 0.05)(Fig1C)。
|
| Fig.1 Effect of RSV on platelet aggregation induced by ox-LDL A: ox-LDL induced platelet aggregation; B: RSV inhibited platelet aggregation induced by ox-LDL; C: Statistical analysis of platelet aggregation. Data were representatives of three independent experiments. #P<0.05 vs ox-LDL-treated group. |
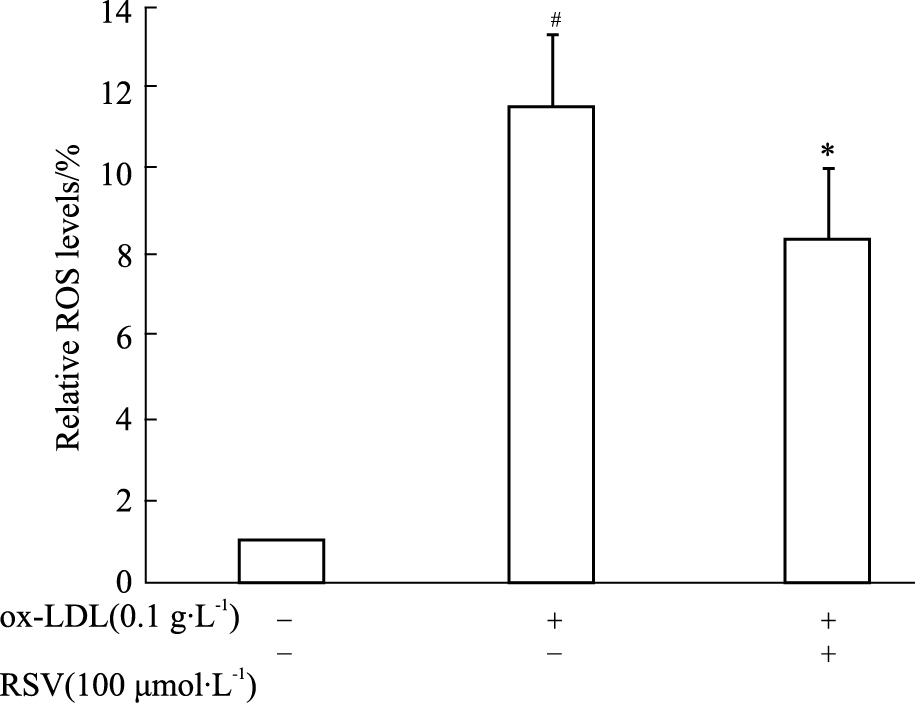
ox-LDL 为氧化型脂质产物,能够诱导细胞的氧化应激及炎症反应。结果显示,ox-LDL (0.1 g·L-1) 刺激血小板ROS产生增加了11.5倍,与正常对照组比较,两组之间差异具有统计学意义,P < 0.05。白藜芦醇处理的血小板与ox-LDL组比较,ROS产生减少了3.2倍,两组之间差异具有统计学意义,P < 0.05(Fig2)。
|
| Fig.2 Effects of RSV on ROS production in ox-LDL-stimulated platelets ROS product was measured by fluorescence spectrophotometer in RSV-treated and ox-LDL-stimulated platelets. Data were representatives of four independent experiments. ox-LDL increased ROS level in platelets. RSV significantly decreased ROS level in ox-LDL-stimulated platelets.#P < 0.05 vs non-ox-LDL-treated group; *P < 0.05 vs ox-LDL-treated group. |
Platelet endothelial cell adhesion molecule-1(PECAM-1)是血小板内皮细胞黏附分子,在血管内皮细胞损伤时促进血小板与内皮细胞的黏附反应。结果显示,ox-LDL刺激血小板后PECAM-1表达增加,而白藜芦醇以剂量依赖的方式抑制了PECAM-1表达,与ox-LDL组比较,二者差异具有统计学意义(Fig3)。

|
| Fig.3 Effects of RSV on PECAM-1 expression in ox-LDL-stimulated platelets A: RSV suppressed PECAM-1 expression in ox-LDL-stimulated platelets; B: Densitometry analysis of PECAM-1 expression. Data were representatives of four independent experiments. #P<0.05 vs non-ox-LDL-treated group; *P<0.05 vs ox-LDL-treated group. |
研究已经提示白藜芦醇是Sirt1的激活剂,本研究观察了白藜芦醇对ox-LDL刺激血小板活化时Sirt1的变化。当ox-LDL (0.1 g·L-1)刺激血小板时Sirt1的表达下降了18%,与对照组比较,两组之间差异具有统计学意义,P < 0.05。与ox-LDL组比较,白藜芦醇(1、10、100 μmol·L-1)以浓度依赖的方式恢复了Sirt1的表达(Fig4A)。此外,我们观察白藜芦醇单独处理对血小板Sirt1表达的影响。结果显示,各种浓度的白藜芦醇(1、10、100 μmol·L-1)孵育血小板 10 mim,各组细胞Sirt1的表达没有明显变化(Fig4B)。这一结果提示,ox-LDL刺激血小板时保护性分子Sirt1受到损伤,出现了表达降低的变化,而白藜芦醇能够逆转这一现象。

|
| Fig.4 Effects of RSV on Sirt1 expression in platelets A, B: RSV recovered Sirt1 expression in ox-LDL-stimulated platelets and densitometry analysis. C, D: RSV along had no effect on Sirt1 expression in non-ox-LDL-stimulated platelets and density analysis. Data were representatives of four independent experiments. #P < 0.05, statistically significant differences from without ox-LDL-treated platelets; *P < 0.05, statistically significant differences from platelets treated with ox-LDL alone. |
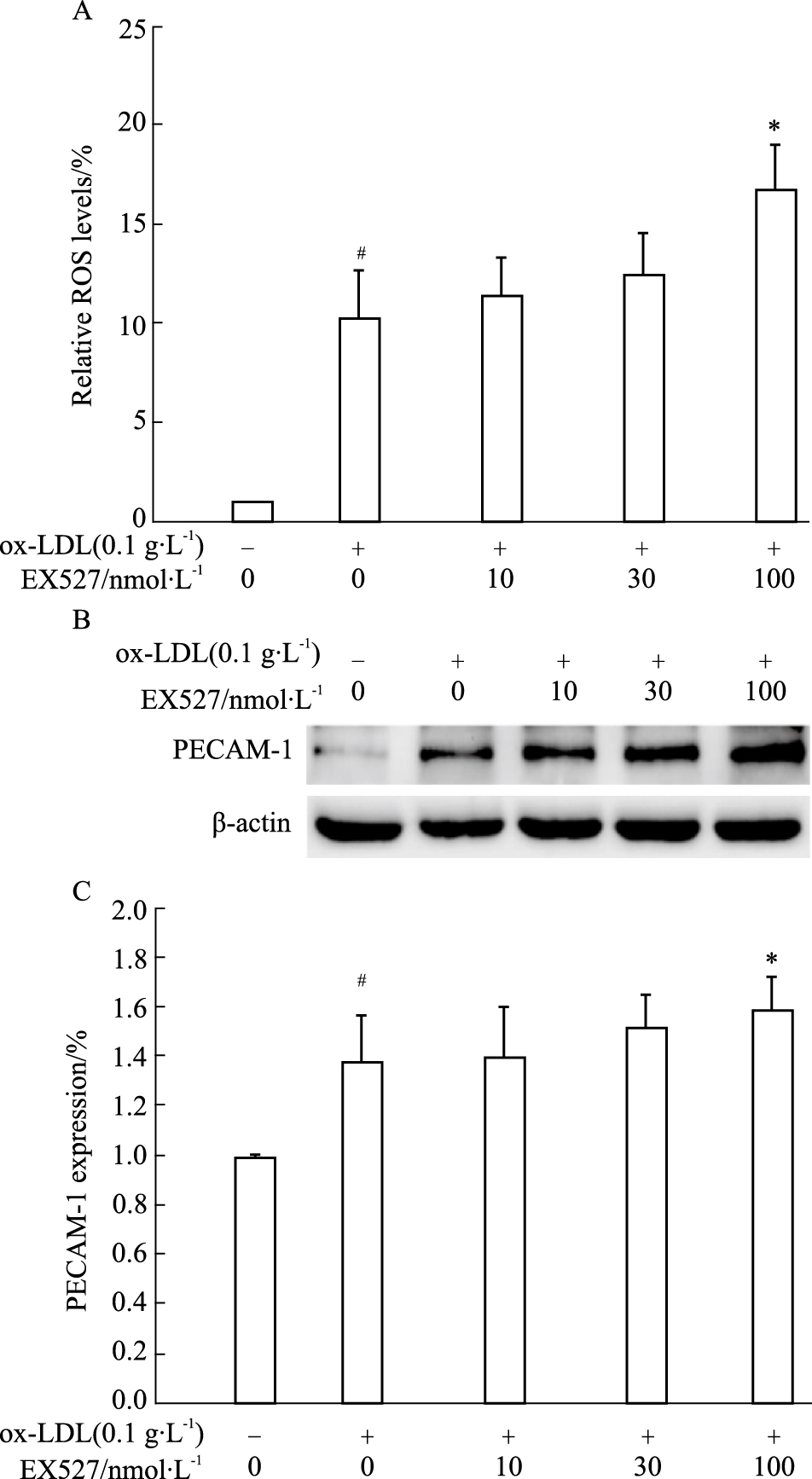
EX527是Sirt1特异性抑制剂,为了分析白藜芦醇抑制ox-LDL刺激血小板ROS产生及PECAM-1表达是否与Sirt1相关,以及Sirt1是否调控ROS产生及PECAM-1表达。我们使用了不同浓度的EX527(10、30、100 nmol·L-1)处理血小板。结果显示,在一个高浓度100 nmol·L-1 EX527处理的血小板ROS产生明显增加,与ox-LDL刺激组比较,二组之间差异具有统计学意义(P < 0.05)(Fig5A)。同样EX527处理的血小板PECAM-1表达也明显增加(P < 0.05)(Fig5B,C)。这一结果提示,病理条件下增加的ROS产生以及PECAM-1表达可能与Sirt1表达/活性降低相关联。
|
| Fig.5 Effects of EX527 on ROS level and PECAM-1 expression in ox-LDL-stimulated platelets A: EX527 increased ROS level in ox-LDL-stimulated platelets; B: EX527 increased PECAM-1 expression in ox-LDL-stimulated platelets; C: Densitometry analysis of PECAM-1 expression. Data were representatives of four independent experiments. #P < 0.05, statistically significant differences from non-ox-LDL-treated platelets; *P < 0.05, statistically significant differences from platelets treated with ox-LDL alone. |
先前的研究表明,p38MAPK参与多种血小板诱导剂刺激的血小板活化,如胶原(collagen)、凝血酶(thrombin)和ADP [10]。本研究我们观察了ox-LDL刺激血小板后p38MAPK的影响。结果显示,ox-LDL刺激血小板后p38MAPK磷酸化水平增加了2.4倍,与对照组比较有明显差异(P < 0.01)。白藜芦醇(100 μmol·L-1)明显抑制了p38MAPK的磷酸化(P < 0.05)(Fig6)。

|
| Fig.6 Effects of RSV on p38MAPK phosphorylation in ox-LDL-stimulated platelets A: RSV suppressed p38MAPK phosphorylation in ox-LDL-stimulated platelets; B: Densitometry analysis of p38MAPK phosphorylation. Data were representatives of four independent experiments. ##P<0.01 vs non-ox-LDL-treated group; *P<0.05 vs ox-LDL-treated group. |
为了确认白藜芦醇降低ROS产生以及PECAM-1表达的药理作用是否与抑制p38MAPK相关,我们使用p38MAPK的抑制剂SB203580,分析其对ox-LDL刺激血小板ROS产生和PECAM-1表达的影响。我们在预实验中确认1 μmol·L-1 SB203580能够完全抑制p38MAPK磷酸化。结果显示,1 μmol·L-1 SB203580不能抑制ox-LDL刺激的血小板ROS产生(Fig7A)。进一步,我们观察了SB203580对PECAM-1的影响。结果显示,与ox-LDL组比较,SB203580(0.1、0.3、1 μmol·L-1)明显抑制了ox-LDL刺激血小板PECAM-1的表达,两组之间差异具有统计学意义(P < 0.05)(Fig7B,C)。这一结果提示,p38MAPK参与调控PECAM-1表达,但对ROS产生无明显影响。白藜芦醇抑制ox-LDL诱导血小板过表达PECAM-1可能与抑制p38MAPK磷酸化相联系。

|
| Fig.7 Effects of SB203580 on ROS level and PECAM-1 expression in ox-LDL-stimulated platelets A: Statistical analysis of relative ROS level; B: SB203580 inhibited PECAM-1 expression in ox-LDL-stimulated platelets; C: Densitometry analysis of PECAM-1 expression. Data were representatives of four independent experiments. #P < 0.05, statistically significant differences from without ox-LDL-treated platelets; *P < 0.05, statistically significant differences from platelets treated with ox-LDL alone. |
血小板活化在动脉粥样硬化血栓形成中是一个关键的环节,然而,近年大量研究显示,血小板在动脉粥样硬化的早期炎症过程中通过释放炎症介质,促进动脉粥样硬化的血管炎症。机体脂质代谢失调导致血脂成分增加,循环中的ox-LDL增加,不仅损伤内皮细胞,同时也能影响血小板功能。最近,我们以及其他的研究均证实,ox-LDL能够使内皮细胞炎症蛋白表达增高,也能促进血小板的聚集。因此,抑制ox-LDL损伤内皮细胞和血小板活化,对于防治动脉粥样硬化血管炎症和血栓形成具有重要意义。血小板是由骨髓巨核细胞脱落而成的无核细胞,近年研究发现,血小板有丰富的mRNA存在,具有合成蛋白的能力。最近,Denis等[11]报告,血小板含有剪接体和小核RNA以及mRNA前体,在血小板活化时能够转化为成熟mRNA,促进血小板炎症蛋白表达。我们的结果也证实血小板活化时炎症蛋白表达增加。
白藜芦醇又称为芪三酚,主要来源于葡萄、虎杖、桑椹等植物,具有抗氧化及抗炎的作用。动物实验提示[12],白藜芦醇能够改善高热量高胆固醇饮食引起的内皮损伤。白藜芦醇的抗氧化作用可能与增加细胞内Sirt1表达相关[13, 14]。在体实验研究表明,通过热量限制和运动等方式可以促进Sirt1表达[15]。然而,Sirt1对血小板功能的调控尚不清楚。我们的结果提示,白藜芦醇能够抑制ox-LDL刺激的血小板聚集,降低血小板ROS产生和PECAM-1表达,这些药理作用与增加血小板Sirt1表达相关。
p38MAPK为MAPK家族的重要成员,不仅参与细胞的生存、分化和凋亡,还在炎症、氧化应激反应中起有重要作用。研究发现[16],白藜芦醇可以抑制巨噬细胞的凋亡,与p38MAPK通路有关。我们的结果显示,抑制p38MAPK磷酸化能够减少ox-LDL刺激血小板炎症蛋白PECAM-1表达,但对ox-LDL诱导的ROS产生无明显抑制作用。在生理条件下,活性氧(reactive oxygen species,ROS)作为第二信使,参与细胞代谢,保持正常的细胞功能。然而,过高水平ROS能够导致细胞发生氧化应激反应。因此,ROS也被认为是氧化应激反应的病理产物和动脉粥样硬化的危险因素[17, 18]。本研究发现,ox-LDL刺激血小板之后,血小板发生聚集,ROS水平随之升高,而白藜芦醇部分地降低了ROS水平。由于细胞内ROS产生的途径较复杂,线粒体代谢、花生四烯酸代谢、nicotinamide adenine dinucleotide phosphate (NADPH)等均是ROS的重要来源。我们的结果提示尽管白藜芦醇减少ROS产生,但抑制效果是不完全的,确切的分子机制还有待于进一步研究。
综上所述,白藜芦醇能够降低ox-LDL诱导的血小板聚集、减少ROS产生,并降低PECAM-1的表达。其分子机制与增加Sirt1的表达相关。此外,白藜芦醇抑制PECAM-1表达与抑制p38 MAPK磷酸化相关。本研究提出了白藜芦醇改善血小板功能的实验依据,对临床预防治疗血栓性疾病,改善血管细胞功能具有重要的参考价值和科学意义。
(致谢:本文在北京老年医学研究所免疫室完成,在此加以致谢!)
| [1] | Ross R. Atherosclerosis is an inflammatory disease[J]. Am Heart, 1999, 138(2):419-20. |
| [2] | Magwenzi S, Woodward C, Wraith K S, et al. Oxidized LDL activates blood platelets through CD36/NOX2-mediated inhibition of the cGMP/protein kinase G signaling cascade[J]. Blood, 2015, 125(17):2693-703. |
| [3] | Carnevale R, Bartimoccia S, Nocella C, et al. LDL oxidation by platelets propagates platelet activation via an oxidative stress-mediated mechanism[J]. Atherosclerosis, 2014, 237(1):108-16. |
| [4] | Wang H, Yang Y J, Qian H Y, et al. Resveratrol in cardiovascular disease: what is known from current research[J]. Heart Fail Rev, 2012, 17:437-48. |
| [5] | Schmitt C A, Heiss E H, Dirsch V M. Effect of resveratrol on endothelial cell function: molecular mechanisms[J]. Biofactors, 2010, 36:342-9. |
| [6] | Kaeberlein M, McVey M, Guarente L. The SIR2/3/4 complex and SIR2 alone promote longevity in Saccharomyces cerevisiae by two different mechanisms[J]. Genes Dev, 1999, 13(19):2570-8010. |
| [7] | Ma L, Dong W, Wang R, et al. Effect of caloric restriction on the SIRT1/mTOR signaling pathways in senile mice[J]. Brain Res Bull, 2015, 116:67-72. |
| [8] | Park S, Mori R, Shimokawa I. Do sirtuins promote mammalian longevity? A critical review on its relevance to the longevity effect induced by calorie restriction[J]. Mol Cells, 2013, 35(6):474-80. |
| [9] | Kilic U, Gok O, Erenberk U, et al. A remarkable age-related increase in SIRT1 protein expression against oxidative stress in elderly: SIRT1 gene variants and longevity in human[J]. PLoS One, 2015, 10(3):e0117954. |
| [10] | Begonja A J, Geiger J, Rukoyatkina N, et al. Thrombin stimulation of p38 MAP kinase in human platelets is mediated by ADP and thromboxane A2 and inhibited by cGMP/cGMP-dependent protein kinase[J]. Blood, 2007, 109(2):616-8. |
| [11] | Denis M M, Tolley N D, Bunting M, et al. Escaping the nuclear confines: signal-dependent pre-mRNA splicing in anucleate platelets[J]. Cell, 2005, 122(3):379-91. |
| [12] | 程静静, 陈 莉, 李朝飞, 等. 白藜芦醇通过减缓内质网应激及增加 eNOS 的表达改善高热量高胆固醇饮食引起的内皮损伤[J].中国药理学通报, 2014, 30(12):1756-62. Cheng J J, Chen L, Li C F, et al. Resveratrol improves vascular endothelial injury induced by high-calorie and high-cholestrol diet through reduced ERS and increased eNOS expression[J]. Chin Pharmacol Bull, 2014, 30(12): 1756-62. |
| [13] | Baur J A, Pearson K J, Price N L, et al. Resveratrol improves health and survival of mice on a high-calorie diet[J]. Nature, 2006, 444:337-42. |
| [14] | Wang Q, Sun X, Li X, et al. Resveratrol attenuates intermittent hypoxia-induced insulin resistance in rats: involvement of Sirtuin 1 and the phosphatidylinositol-4, 5-bisphosphate 3-kinase/AKT pathway[J]. Mol Med Rep, 2015, 11(1):151-8. |
| [15] | Howitz K T, Bitterman K J, Cohen H Y, et al. Small molecule activators of sirtuins extend Saccharomyces cerevisiae lifespan[J]. Nature, 2003, 425(6954):191-6. |
| [16] | Guo R, Su Y, Liu B, et al. Resveratrol suppresses oxidized low-density lipoprotein-induced macrophage apoptosis through inhibition of intracellular reactive oxygen species generation, Lox-1, and the p38 MAPK pathway[J]. Cell Physiol Biochem, 2014, 34(2):603-16. |
| [17] | Lassegue B, San Martin A, Griendling K K. Biochemistry, physiology, and pathophysiology of NADPH oxidases in the cardiovascular system[J]. Circ Res, 2012, 110(10):1364-90. |
| [18] | Gutierrez J, Ballinger S W, Darley-Usmar V M, Landar A. Free radicals, mitochondria, and oxidized lipids:the emerging role in signal transduction in vascular cells[J]. Circ Res, 2006, 99(9):924-32. |

