


2. 福建医科大学附属漳州市医院血液内科, 福建 漳州 363000;
3. 福建医科大学药学院, 福建 福州 350004
2. Dept of Hematology, Zhangzhou Affiliated Hospital of Fujian Medical University, Zhangzhou Fujian 363000, China;
3. School of Pharmacy, Fujian Medical University, Fuzhou 350004, China
赖氨酸特异性组蛋白去甲基化酶1(lysine specific demethylase 1,LSD1)是2004年被人们发现的第1个组蛋白赖氨酸去甲基化酶。LSD1定位于细胞核内,调控着基因转录的激活和抑制,在肿瘤发生和胚胎发育过程中起着重要的作用。它是一个黄素腺嘌呤二核苷酸(flavin adenine dinulcleotide,FAD) 依赖性胺氧化酶,能够特异性地脱去组蛋白H3第4位赖氨酸(H3K4) 和H3K9 位点上的单甲基化和二甲基化甲基基团[1]。有研究发现,LSD1可通过多种途径参与肿瘤的发生,例如 LSD1 可能广泛地调控基因表达并且参与前列腺癌的进展及恶化[2],与乳腺癌、卵巢癌、肝癌的发展也密切相关[3, 4, 5]。
目前H3K4去基化酶LSD1的研究不多,特别是用对RNAi沉默技术研究LSD1后肿瘤细胞的增殖及凋亡以及对组蛋白调控及DNA甲基化影响的报告少见。本研究通过RNAi沉默LSD1基因,探讨LSD1基因对急性T 淋巴母细胞性白血病Molt-4细胞增殖、凋亡及组蛋白甲基化、乙酰化及DNA甲基化的影响,探讨LSD1基因在白血病靶向治疗中的可能性。
1 材料与方法 1.1 试剂 RPMI1640培养基(美国Gibco公司),胎牛血清(杭州四季青生物制品公司),siRNA及PCR引物委托上海吉玛制药技术有限公司合成,LipofectamineTM 2000 转染试剂、Opti-MEM RT-PCR试剂盒、DNA Marker试剂购自美国Invitrogen公司,细胞增殖检测( MTS) 试剂盒(Promega公司),Annexin V-FITC/PI双染试剂盒(BD公司),一抗: p15、Bcl-2、procaspase-3(美国Santa Cruz公司),Anti-acetyl-Histone H3、Anti-acetyl-Histone H4、Anti-trimethyl-Histone H3 (Lys9)、Anti-acetyl-Histone H3(Lys9)、Anti-acetyl-Histone H3(Lys14)、Anti-acetyl-Histone H3(Lys27) 购自美国Upsate公司。羊抗兔、羊抗鼠二抗(Santa Cruz公司)。
1.2 Molt-4细胞培养Molt-4细胞购自中国科学院上海细胞库。Molt-4细胞培养条件:含10%胎牛血清的RPMI 1640细胞培养基(含青霉素105U·L-1+链霉素100 mg·L-1)并在37℃、5%CO2饱和湿度的孵育箱中培养。将Molt-4细胞复苏后,2~3 d规律传代。转染前选择对数生长期细胞,离心收集并接种于6孔培养板中,细胞数为2×106个/孔。
1.3 靶序列的选择siRNA的有关序列由上海吉玛制药技术有限公司设计及合成,为了避免只选择一个序列可能出现无效或低效的情况,我们根据确定序列的原则选择4条靶序列,并用RT-PCR法筛选最佳LSD1基因的siRNA片段为: 上游5′-CCACGAGUCAAACCUUUAUTT-3′; 下 游5′-AUAAAGGU UUGACUCGUGGTT-3′。
1.4 RT-PCR法观察LSD1 siRNA对Molt-4细胞LSD1 mRNA表达的影响设定阴性对照组、0、30、60、120 nmol·L-1 LSD1 siRNA处理组。每孔总体积为2 mL。37℃、5%CO2饱和湿度下培养48 h后,根据TRIzol试剂盒说明书提取总RNA,紫外分光光度法鉴定、定量,A260/A280比值均为1.8~2.0,经逆转录为cDNA。以反应所得cDNA进行PCR扩增。将β-actin(上游引物:5′- GAGACCTTCA AGACCCCAGCC-3′,下游引物:5′-TCGGGGCATCGGAACCGCTCA-3′)与LSD1引物按1 ∶2的比例混合。PCR反应条件: 95℃ 5 min(预变性),95℃ 45 s(变性),61℃ 45 s(退火),72℃ 45 s(延伸),40个循环,最终延伸72℃ 10 min。将PCR产物与上样缓冲液以5 ∶1混合后,16 g·L-1琼脂糖凝胶电泳,于凝胶图像分析仪上自动分析成像,观察效果最佳LSD1 siRNA片段对Molt-4细胞LSD1 mRNA表达的影响。
1.5 MTS法绘制细胞的生长曲线取3个96孔板,每个96孔板中接种Molt-4细胞2×104个/孔,分别加入适量的LSD1 siRNA使终浓度分别为0、30、60、120 nmol·L-1,终体积为100 μL。每组设6个平行孔,转染后置于5%CO2饱和湿度、37℃的孵箱中继续培养。于24、48、72 h分别收获一个板内的4组细胞。将MTS 和PMS按20 ∶1 的体积比混合成混合液,每孔加20 μL的上述混合液,继续培养4 h,震荡10 min,充分溶解结晶物,在酶标仪上测吸光度即OD 值(单波长492 nm),记录试验结果,并计算细胞增殖率。细胞增殖率/%=(OD实验-OD空白)/(OD对照-OD空白)×100%。以细胞增殖率为纵轴、时间为横轴绘制细胞增殖曲线。实验重复3次。
1.6 流式细胞仪检测细胞早期凋亡LSD1 siRNA使终浓度分别为0、30、60、120 nmol·L-1,分别培养48 h后离心收集细胞,在流式细胞仪检测细胞凋亡率,方法及步骤参照BD公司试剂盒说明书进行。实验重复3次。
1.7 Western blot检测干扰后LSD1蛋白、凋亡相关蛋白、p15蛋白、组蛋白H3K4一、二甲基化、H3K9甲基化、H3乙酰化状态及DNA甲基化酶DNMT1的表达用不同浓度的LSD1 siRNA 处理Molt-4细胞48 h后,收集细胞,用PBS洗涤后,调整细胞数为1×106的浓度,加入裂解液与酶抑制剂(100 ∶1)100 μL充分裂解细胞;低温(4℃)12 000 r·min-1离心15 min,吸取中间清亮层,收集蛋白,BCA法进行蛋白定量,-20℃保存备用。取备用蛋白,以12%SDS-PAGE电泳分离,电转移法转膜,室温下摇床封闭1 h;加入用TBS稀释的一抗 4℃过夜,TBS洗涤液洗膜后分别加入二抗,室温下孵育1 h,TBS洗膜后加入化学发光工作液,在X射线胶片(KODAK)上曝光,以β-actin为内参,用AlphaDigiDoc图像分析软件进行分析比较。
1.8 统计学分析采用SPSS 13.5统计学软件进行结果处理,常规进行方差齐性检验、正态性检验。计量资料实验数据采用x±s表示,并进行单因素方差分析。
2 结果 2.1 LSD1 siRNA下调LSD1 mRNA及其蛋白的表达分别将浓度为0、30、60、120 nmol·L-1的LSD1-2045 RNAi片段转染Molt-4细胞,48 h后提取细胞的mRNA进行RT-PCR试验。如Fig1A所示,LSD1 siRNA转染后LSD1 mRNA受到抑制,且与浓度相关。各组LSD1 mRNA条带灰度值与β-actin比值分别为:0.967±0.124、0.302±0.083、0.153±0.082、0.091±0.024,各组与β-actin 比值统计学处理,P < 0.05(Fig1A)。与对照组相比,经LSD1 RNA干扰后,LSD1 蛋白的表达量随着siRNA作用浓度的增加而逐渐减少,其中120 nmol·L-1组减少最明显,下降了67.67% (Fig1B)。

|
| Fig.1 Transfection of LSD1 siRNA in Molt-4 cells A: Reduction of LSD1 mRNA after transfected with indicated concentrations of LSD1 siRNA in Molt-4; B: Reduction of LSD1 protein after transfected with indicated concentrations of LSD1 siRNA in Molt-4 cells |
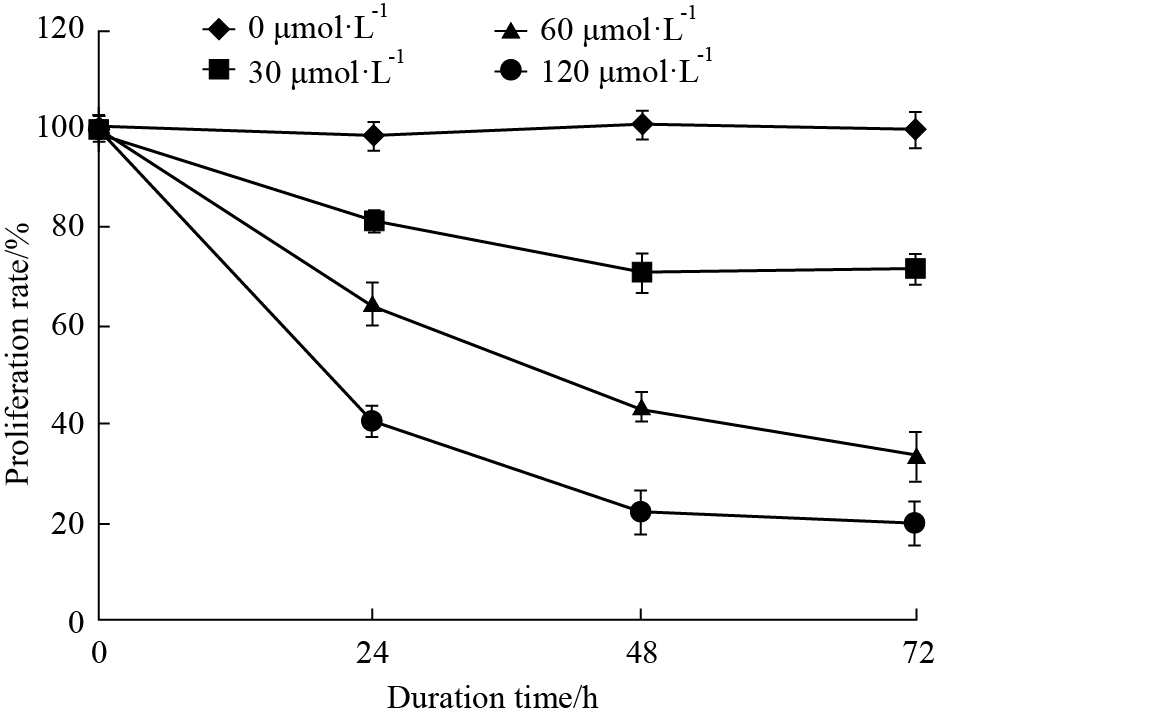
经终浓度分别为0、30、60、120 nmol·L-1的LSD1 siRNA作用24、48、72 h后,Molt-4细胞的增殖率变化见Fig2,随LSD1 siRNA浓度的增加和时间的延长,增殖率逐渐下降,呈现浓度和时间依赖性。
|
| Fig.2 Deceased cell proliferation of Molt-4 cells after transfected with LSD1 siRNA in different concentrations and in different time |
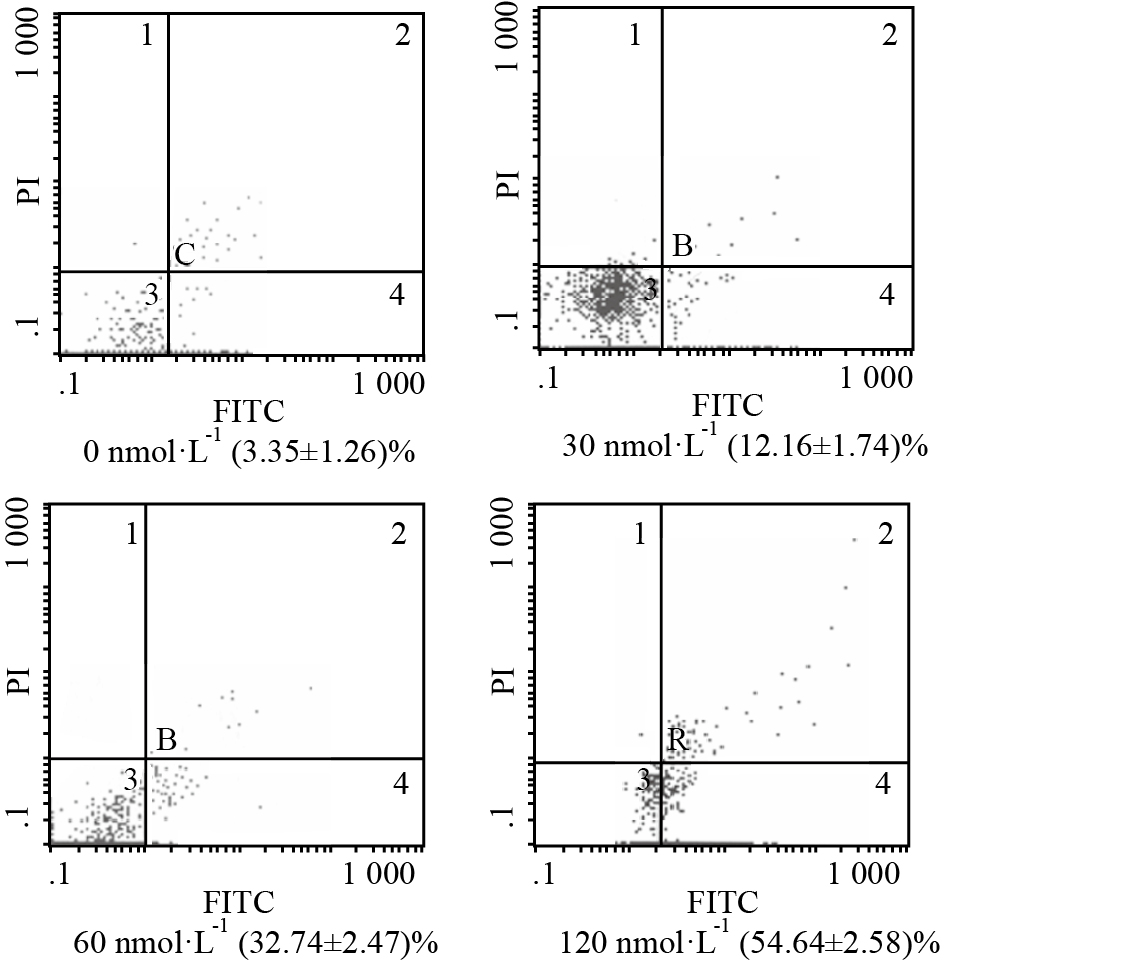
经30、60、120 nmol·L-1的 LSD1 siRNA处理48 h后,Molt-4细胞的凋亡率分别为(12.16±1.74)%、(32.74±2.47)%、(54.64±2.58)%,而对照组为(3.35±1.26)%,细胞的凋亡率随着LSD1 siRNA浓度的增加逐渐上升(P < 0.05)。LSD1 siRNA浓度与凋亡率有明显的量效关系(Fig3)。
|
| Fig.3 Induction of cells apoptosis after transfected with LSD1 siRNA Molt-4 cells for 48 hours |
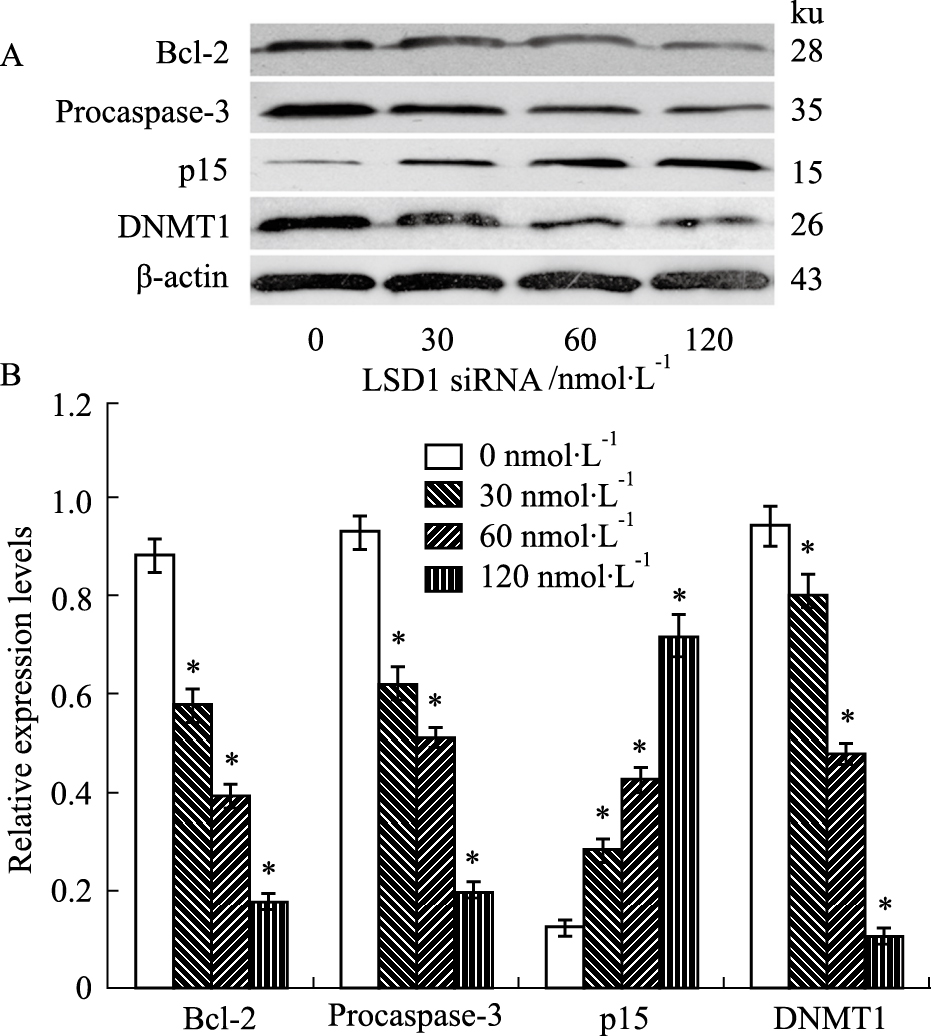
经终浓度分别为0、30、60、120 nmol·L-1的LSD1的siRNA转染Molt-4细胞48 h后,抗凋亡蛋白Bcl-2的表达随着LSD1 siRNA终浓度的增加而逐渐减少,分别比对照组减少33.70%、55.62%、79.78%;procaspase-3随着siRNA处理浓度的增加表达量也逐渐下降,分别比对照组减少33.69%、54.35%、77.17%;同时,随着siRNA处理浓度的增加,抑癌基因p15的表达量逐渐增加,分别比对照组增加1.21倍、2.71倍、4.58倍;而DNMT1蛋白的表达则逐渐减弱,分别比对照组减少22.47%、71.35%、88.76% (P < 0.05)(Fig4)。
|
| Fig.4 Alteration of apoptosis-related protein and DNMT1,p15 protein in Molt-4 cells after transfected with indicated concentrations of LSD1 siRNA for 24 h A:Protein electrophoresis;B:Proteins relative density. *P<0.05 vs 0 nmol·L-1 |
LSD1 siRNA终浓度为 30、60、120 nmol·L-1处理Molt-4细胞48 h后,组蛋白H3K4一甲基化和二甲基化表达随siRNA浓度增加而增强;组蛋白H3K4三甲基化水平不变;组蛋白H3K9一甲基化和二甲基化水平也几乎不变;组蛋白H3乙酰化水平随siRNA浓度增加而表达增强(Fig5)。

|
| Fig.5 Alteration of histone methylation and acetylation modification of Molt-4 cells after transfection with indicated concentrations of LSD1 siRNA for 24 h A: Protein electrophoresis; B: Proteins relative density. *P<0.05 vs 0 nmol·L-1 |
一般认为,肿瘤的发生与癌基因的异常激活或过度表达有关,而抑癌基因的失活也可能使细胞向恶性转化。表观遗传学的改变对肿瘤的发生和发展起了重要的作用。组蛋白H3K4去基化酶LSD1在表观遗传学中发挥了重要作用,其在多种肿瘤表达异常,说明它对肿瘤的发生有关。本研究以RNA干扰技术削减急性淋巴细胞白血病Molt-4细胞的LSD1表达,观察白血病细胞的表观遗传学的变化及增殖、凋亡的影响,探讨LSD1作为抗肿瘤靶点的可能性。
特异性地诱导肿瘤细胞凋亡已经成为治疗恶性肿瘤的主要策略之一。2010年Kontaki等[6]首先报告当DNA损伤时,set和LSD1分别对E2F1-K185me进行去甲基化修饰,使其更远的乙酰化和磷酸化,它主要作用于细胞周期的G1期到S期的过渡,并通过激活p53、p73等辅助因子,即p53依赖和非p53依赖细胞凋亡通路,激活大量凋亡前基因。本研究结果显示,LSD1 siRNA干扰LSD1基因后可促进Molt-4细胞凋亡相关蛋白Bcl-2、procaspase-3裂解,触发细胞凋亡,细胞凋亡率随着LSD1 siRNA浓度的增加逐渐上升(P < 0.05);Wang 等[7]鉴定出DNMT1是LSD1的新底物。DNMT1可被LSD1去甲基化,引起DNA 甲基化的失衡。p15(Ink4b)基因属于抑癌基因中周期蛋白依赖性激酶抑制因子(CKIs)第二大家族,通过抑制CDK4/6,从而抑制Rb蛋白磷酸化,阻止细胞由G1期进入S 期,从而减少细胞的异常生长及变异,阻止肿瘤发生和发展。沉默 LSD1 基因可下调DNA 甲基转移酶1 (DNMT1),使抑癌基因 p15 去甲基化而表达上调,从而抑制肿瘤细胞增殖。
本研究还发现沉默LSD1后,H3K4的一甲基化和二甲基化水平逐渐增强,组蛋白H3乙酰化水平上调,而H3K4的三甲基化及H3K9的一甲基化和二甲基化未发生改变。Shi等[1]和Nicholson等[8]的实验显示在FAD 的参与下,LSD1 在体外可以特异去除组蛋白H3 第4位赖氨酸(H3K4) 的二甲基和一甲基修饰。而三甲基则需要亚胺阳离子中间体才能介导对H3K4三甲基的去甲基化反应。LSD1不是H3K9去甲基化酶,但有文献报告LSD1可在体内才能去除H3K9 的二甲基和一甲基修饰[9]。Miao等[10]研究发现:组蛋白H3-K4Me2、H3-K4Me3、H3-K36Me2和H3-K79Me2与高度乙酰化和基因激活都有关系。因此,可以推导出:当组蛋白H3-K4Me2表达增加时,可引起组蛋白高度乙酰化,从而使组蛋白H3乙酰化增加。
本研究提示干扰LSD1基因后肿瘤细胞发生表观遗传学改变,进而促使细胞凋亡,肿瘤细胞受到抑制,有望成为肿瘤治疗的靶点。
(致谢:本文实验在闽南师范大学生物科学院中心实验室完成,感谢实验室的老师对本实验的支持。)
| [1] | Shi Y, Lan F, Matson C, et al. Histone demethylation mediated by the nuclear amine oxidase homolog LSD1[J]. Cell, 2004, 119(7): 941-53. |
| [2] | Naqasawa S,Sedukhina A S, Nakaqawa Y,et al. Relationship between LSD1 expression and E-cadherin expression in prostate cancer[J]. J Int Urol Nephrol, 2015, 47(3):485-90. |
| [3] | Naqasawa S, Sedukdina A S, Nakaqawa I, et al.LSD1 overexpression is associated with poor prognosis in basal-like breast cancer, and sensitivity to PARP inhibition[J].PLos One,2015, 10(2):e0118002. |
| [4] | Chen C, Ge J, Lu Q, et al.Expression of Lysine-specific demethylase 1 in human epithelial ovarian cancer[J].J Ovarian Res, 2015,8(1):28. |
| [5] | Lei Z J, Wang J, Xiao H L, et al. Lysine-specific dem ethylase 1 promotes the stemness and chemoresistance of Lgr5+ liver cancer initiating cells by suppressing negative regulators of β-catenin signaling[J]. J Oncogene, 2015,34:3188-98. |
| [6] | Kontaki H,Talianidis I. Lysine methylation regulates E2F1-induced cell death[J]. J Molell, 2010, 39(1):152-60. |
| [7] | Wang J, Hevi S, Kurash J K, et al. The lysine demethylase LSD1 (KDM1) is required for maintenance of global DNA methylation[J].J Nat Genet,2009,41(1):125-9. |
| [8] | Nicholson T B,Chen T.LSD1 demethylates histone and non-histone proteins[J].J Epigenetics, 2009,4(3):129-32. |
| [9] | Lan F, Nottke A C, Shi Y. Mechanisms involved in the regulation of histone lysine demethylases[J].J Curr Opin Cell Biol, 2008,20(3):316-25. |
| [10] | Miao F, Natarajan R. Mapping global histone methylation patterns in the coding regions of human genes[J]. J Mol Cell Biol, 2005,25(11):4650-61. |

