


2. 暨南大学生命科学技术学院, 广东 广州 510632
2. College of Life Science and Technology, Jinan University, Guangzhou 510632, China
肝癌是一种常见的消化系统恶性肿瘤,恶性程度极高,初期临床症状并不明显,80%的病例发现时已属中晚期,且由于多数合并肝硬化,伴有肝功能异常,无法接受根治性手术,化疗是其主要的治疗手段[1, 2]。铂类药物是临床上应用最广的抗癌药物之一,但其在治疗过程中会产生明显的毒副作用及耐药性。近年来,在非铂类金属药物中,金属钌配合物受到广泛的关注,其高效、低毒、易被肿瘤组织吸收的特点,被认为是国际上最有前途的抗癌药物之一[3, 4]。因此,将钌配合物开发成为一种潜在的新型抗癌药物具有重要意义。
目前,大量的研究集中于钌多吡啶配合物,该类配合物大多数具有强烈的电子吸收光谱和荧光发射光谱,有灵敏可调性,可用于分子开关。本团队在前期工作中合成了一系列苯并咪唑吡啶类金属钌配合物(Fig1),发现该类配合物,在肿瘤细胞与正常细胞之间具有良好的选择性,具有良好的抗肿瘤活性,通过激活线粒体凋亡信号通路和活性氧(ROS)介导的p53信号通路而高效地诱导乳腺癌细胞凋亡,但是,其体内抗肿瘤活性也有待进一步评价[5, 6]。而这些凋亡信号通路和肝癌细胞凋亡密切相关,细胞凋亡对肝癌的发生起负调控作用,肝癌细胞可以通过药物诱导的细胞凋亡而被清除。抑癌基因p53是肿瘤治疗的靶点,它在诱导肝癌细胞凋亡的过程中扮演着重要的角色。目前关于该类配合物对肝癌的作用及分子机制尚未有报道,这也是值得深入探讨的科学问题。因此,本文选择多种肝癌肿瘤细胞株和L02人正常肝脏细胞株,采用MTT法对配合物的体外抗肿瘤活性进行筛选。结果表明,该类配合物能不同程度的抑制不同肝癌细胞的增殖,而对L02人肝脏细胞无明显毒性。通过流式细胞术分析、Western blot、荷瘤裸鼠模型等对其抗肿瘤活性进行综合评价,初步探讨该配合物的抗肿瘤作用机制,为高效、低毒的新型抗肝癌药物开发提供依据。
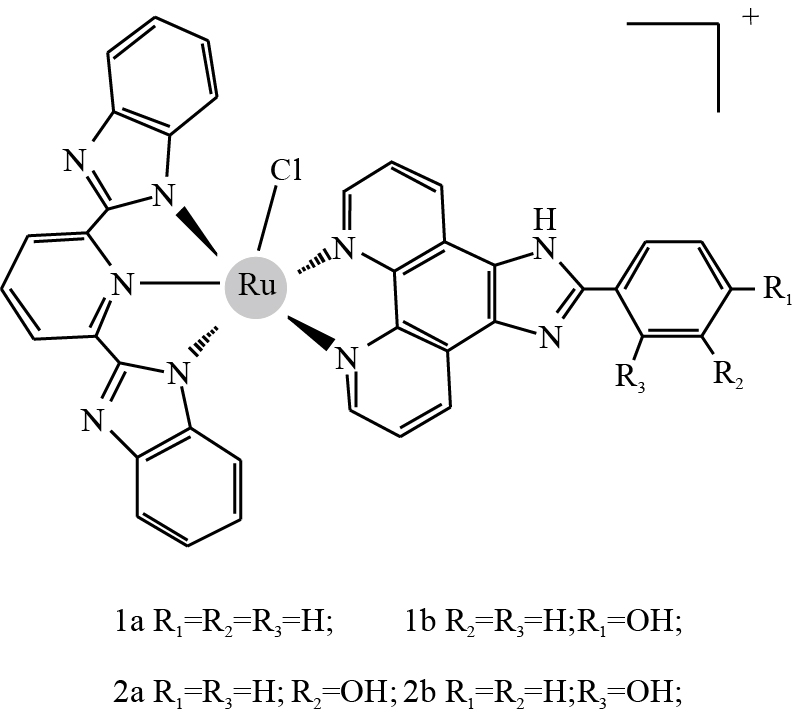
|
| Fig 1 Chemical structure of Ru complexes used in this study |
四氮唑蓝(MTT)、DAPI、TUNEL、 DMSO、DMEM和RPMI 1640培养基等均购自Sigma-Aldrich公司。抗体均为Cell Signaling Technology产品。BCA蛋白定量试剂盒,酶活性检测试剂盒为碧云天公司。细胞培养耗材为捷倍斯公司。ELX800型酶标仪 (美国Bio-Tek公司);流式细胞仪(Beckman Coulter,美国);净化工作台(苏州安泰),二氧化碳培养箱(Thermo,美国),荧光显微镜及成像系统(Nikon,Eclipse E600,日本),Western blot电泳仪(Bio-Rad,美国)。
1.2 细胞本实验选择的几种人肝癌细胞Hep 3B、Huh 7、HepG2、SMMC7721及肝脏正常细胞L02均购自ATCC公司。
1.3 实验动物本实验正常体质量为16~18 g BALB/C裸小鼠,为4~6周龄。由暨南大学实验动物中心提供。在无特殊病原条件下饲养。
2 方法 2.1 化合物的制备本研究所使用的钌配合物参考前期方法合成[5],并用质谱及核磁共振(NMR)进行验证。
2.2 细胞培养将受试样品用含有胎牛血清的RPMI1640和DMEM配成一定浓度的原液,再依次稀释到需要的浓度。培养基(DMEM和RPMI等)添加小牛血清(10%),青霉素(1×105 U·L-1)和链霉素(5×104 U·L-1)。培养条件:37℃,5% CO2。根据细胞生长状况每2~3 d换培养液1次,当细胞生长状态稳定,呈对数生长期时,用于实验。
2.3 体内实验以裸鼠荷瘤模型来评价药物体内的抗肿瘤效果。106个Hep 3B人肝癌细胞细胞(重悬于PBS)注射于裸鼠腋下,待1周成瘤后,开始给药。剂量设置为:高剂量组:5 mg·kg-1 2b;低剂量组:2.5 mg·kg-1 2b;正常对照组:PBS。每组10只小鼠,给药方式为尾静脉给药,连续给药16 d。停药后,记录裸鼠体重的变化,测量肿瘤体积的变化,处死裸鼠后,称取肿瘤质量。肿瘤体积=L×W2/2。L为肿瘤最长轴,W为肿瘤宽度。
2.4 MTT法测定细胞存活率实验取对数生长期的细胞,接种于96孔培养板,每孔100 μL,细胞浓度为2×107·L-1,培养24 h后,再分别加入不同浓度2b 100 μL,置37℃,5% CO2培养特定72 h。加入MTT (5 g·L-1),20 μL/孔,5 h后离心弃上清液,加入二甲基亚枫 (DMSO) 100 μL/孔,振荡15 min左右,待细胞内紫色结晶溶解后,置于酶标仪测定OD值,波长为570 nm。计算细胞存活率,同时作图并求得半数抑制浓度(IC50)。
2.5 流式细胞分析Hep 3B细胞用不同浓度的2b处理72 h后,参考文献[7]的方法操作,离心收集细胞,用 PBS 清洗两次,加入70%乙醇,-20℃放置固定过夜,之后进行细胞碘化丙啶(PI)染色。利用Beckman流式细胞分析仪测定DNA含量。细胞周期分布利用软件MultiCycle (Phoenix Flow Systems,San Diego,CA)。用DNA柱状图表示细胞在G0/G1、S和G2/M各相的分布比例。通过测得的sub-G1峰表示凋亡细胞亚二倍体DNA含量。每个样品分析10 000颗细胞。
2.6 TUNEL-DAPI 双染检测在载玻片上培养的细胞经药物处理后,3.7%的甲醛固定10 min,再加入含有0.1%的Triton X-100的PBS。然后加入10 μmol·L-1 的TUNEL染液,避光37℃孵育1 h,加入10 μmol·L-1的DAPI 染色15 min,PBS 洗涤,荧光显微镜拍照。
2.7 Caspase 活性检测将适量的细胞裂解液加入细胞,在冰上裂解1 h,离心后收集上清液,用BCA法测定蛋白含量。将细胞裂解液加入96孔板中,再加入caspase底物、半胱氨酸蛋白酶-3(caspase-3)、半胱氨酸蛋白酶-8(caspase-8)和半胱氨酸蛋白酶-9(caspase-9),然后在37℃下孵育1 h。利用荧光酶标仪测定caspase活性,激发波长和发射波长分别为380 nm和440 nm。
2.8 Western blot 检测蛋白表达细胞经药物处理后,加入适量的细胞裂解液,在冰上裂解1 h,提取细胞总蛋白,用BCA法测定蛋白含量,取100 μg总蛋白,以12% SDS-PAGE凝胶电泳分离后,转到PVDF膜上,封闭奶粉在室温下封闭 1 h,TBST洗膜3次,加入单克隆抗体在4℃下孵育过夜。TBST洗膜3次,以HRP连接的二抗室温孵育1 h,利用ECL显示反应蛋白产物,曝光,显影,定影。β-actin作为蛋白加样内参照。
3 结果 3.1 抗肿瘤活性的研究首先,使用MTT法检测所合成的苯并咪唑吡啶钌配合物对Hep 3B、Huh 7、及SMMC7721等3种人肝癌细胞的增殖抑制活性,同时研究其对L02人正常肝脏细胞的细胞毒性。如Tab1所示,苯并咪唑吡啶钌配合物均能不同程度的抑制不同人肝癌细胞的增殖,特别是配合物2b,对Hep 3B表现出良好的特异性,其IC50值12.1 μmol·L-1明显的低于其他肿瘤细胞。同时,该配合物对L02正常细胞无明显的毒性,IC50值大于200 μmol·L-1,提示该类配合物在肿瘤细胞与正常细胞之间具有良好的选择性。
| Compounds | IC50/μmol·L-1 | |||
| Hep 3B | Huh 7 | SMMC7721 | L02 | |
| 1a | 45.3 | 50.1 | 105.9 | >200 |
| 1b | 23.7 | 32.9 | 40.2 | >200 |
| 2a | 20.8 | 27.6 | 78.0 | >200 |
| 2b | 12.1 | 21.5 | 47.6 | >200 |
在MTT 筛选中发现Hep 3B细胞对2b最为敏感,于是选用该细胞作为模型研究所合成钌配合物的抗肝癌作用机制。首先,使用流式细胞仪对2b作用后细胞周期的改变进行分析,检测凋亡特有的凋亡峰(Sub-G1 phase),并计算凋亡百分数 (AP: %)。结果如Fig2所示,2b能明显地诱导Hep 3B细胞凋亡,表现为Sub-G1峰的升高,且呈剂量依赖关系。当2b的浓度增加到20 μmol·L-1时,细胞凋亡率从1.6%(对照组)提高到62.4%。同时,我们观察到2b的处理对G0/G1、S及G2/M其细胞百分比没有明显的改变。这些结果说明2b通过诱导细胞凋亡而抑制肝癌细胞生长的。
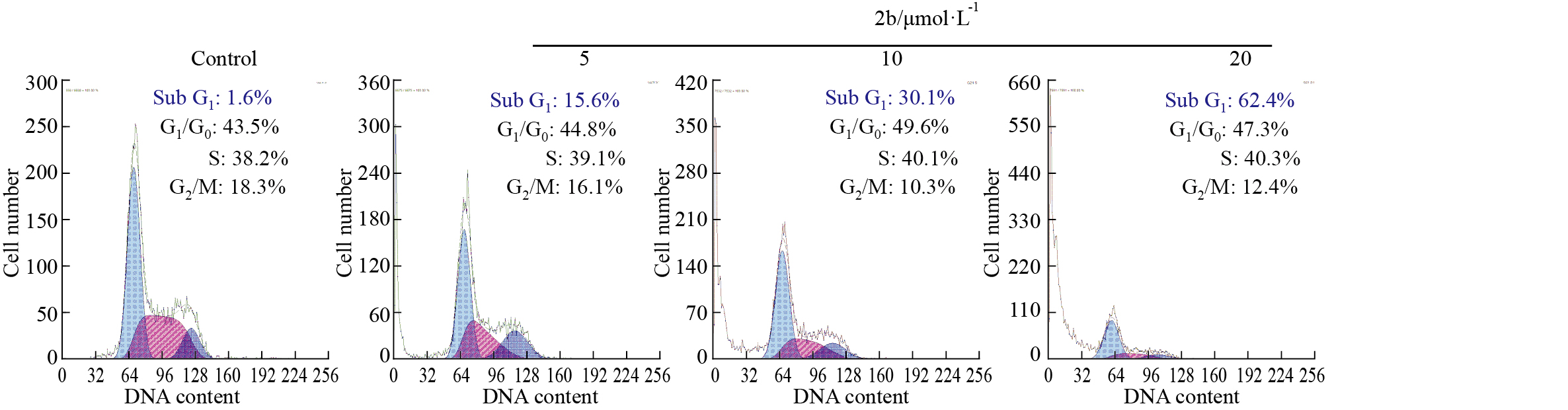
|
| Fig 2 Cell apoptosis induced by 2b Hep 3B cells after treatment with different concentrations of 2b for 72 h were stained with PI solution. Cell apoptosis and cell cycle distribution were analyzed by flow cytometry. |
Hep 3B细胞经不同浓度2b处理后进行固定及TUNEL-DAPI 双染。结果如Fig3所示,2b处理导致细胞呈现核浓缩(蓝色),染色加深,同时观察到DNA的断裂(绿色),且随着2b浓度增加而加剧。本结果进一步证明细胞凋亡是2b抑制肿瘤细胞生长的主要机制。

|
| Fig 3 Representative photomicrographs of DNA fragmentation and nuclear condensation induced by 2b Hep 3B cells after treatment with different concentrations of 2b for 72 h were examined by TUNEL-DAPI co-staining assay (200 magnification). The images shown here are representatives of three independent experiments with similar results. |
为了阐明2b诱导凋亡的机制,我们检测了细胞凋亡过程中的关键酶caspase-3、caspase-8和caspase-9 的活性,结果如Fig4 所示。我们可以看出2b 作用后的Hep 3B细胞中,caspase-3和caspase-9 的活性均有剂量依赖性的提高,而caspase-8不被激活。当2b浓度为20 μmol·L-1时,caspase-9活性上升为原来的1.8倍,这表明2b是通过激活外源性的信号通路而诱导Hep 3B细胞凋亡的。
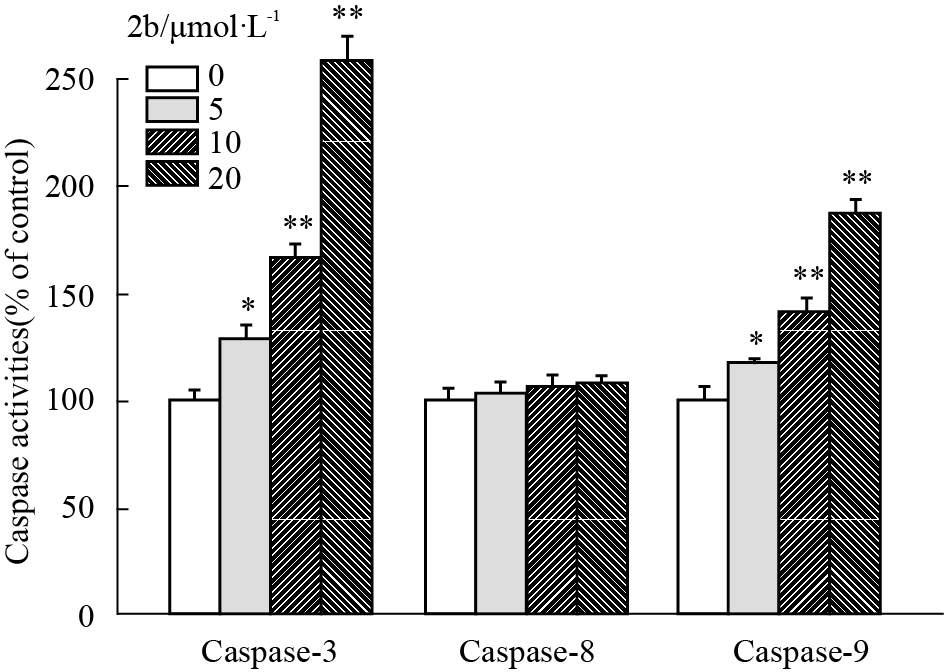
|
| Fig 4 Caspase activities of Hep 3B cells induced by 2b Hep 3B cells after treatment with indicated concentrations of 2b for 72 h were collected. Caspase activity was measured with whole cell extracts by a fluorometric method. *P < 0.05,**P < 0.01 vs control |
为了进一步探讨2b诱导肿瘤细胞凋亡的信号通路,我们检测了细胞中p53和p21蛋白质的表达水平。Western blot 检测结果显示(Fig5),用2b作用Hep 3B细胞24 h 后,细胞中p53蛋白磷酸化,总的p53蛋白和p21蛋白质的表达水平明显升高。
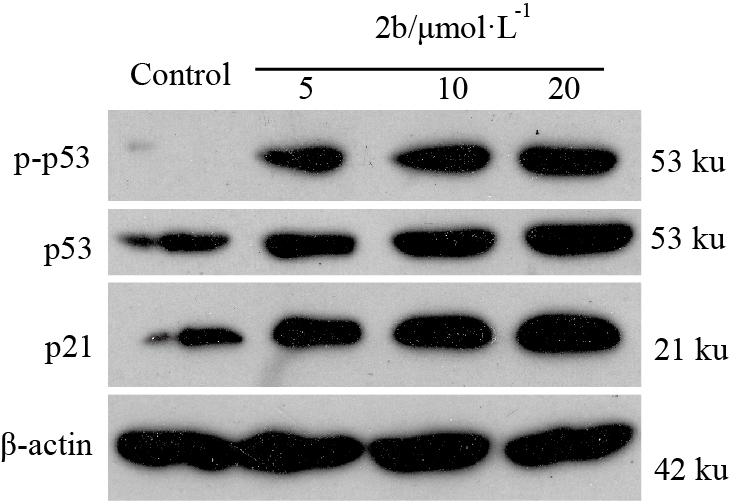
|
| Fig 5 Western blot analysis for the expression levels of p-p53,p53 and p21 in Hep 3B cells induced by 2b Hep 3B cells after treatment with indicated concentrations of 2b for 72 h were collected. Equal loading was confirmed by analysis of β-actin in the protein extracts. |
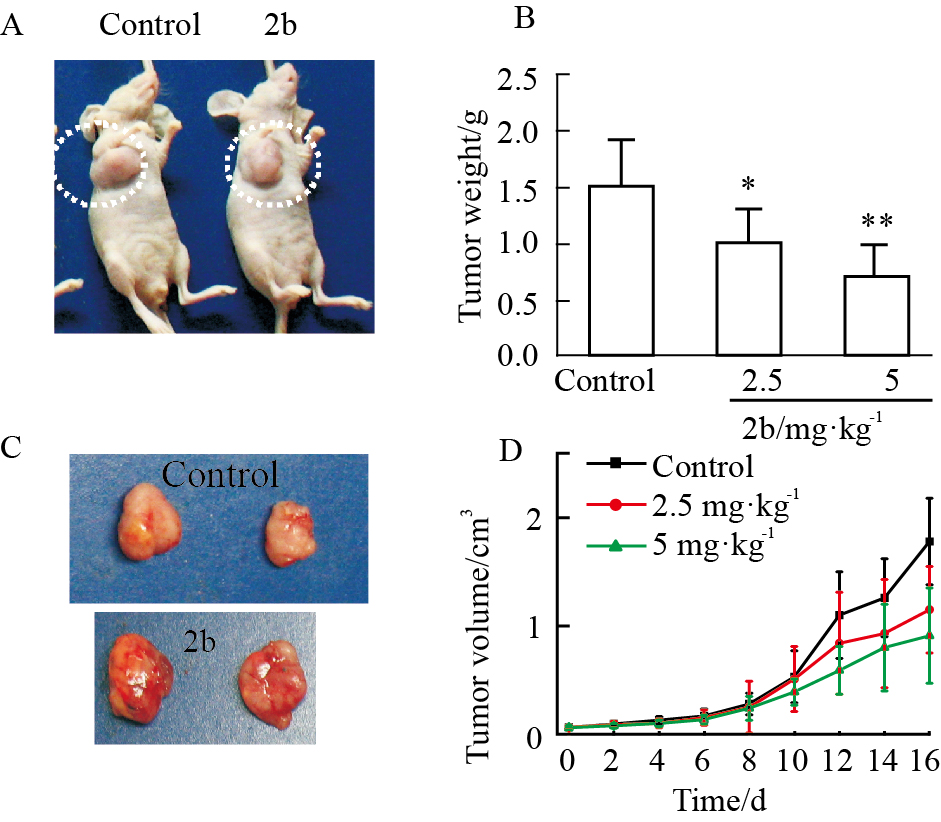
对于为进一步评价2b在体内的抑制肿瘤生长效果,我们进行荷瘤裸鼠实验。2b经过20 d的隔天给药,裸鼠肿瘤的生长明显受到抑制,2b能够降低肿瘤的重量(Fig6A,B),减少肿瘤的体积(Fig6C,D)。这些结果表明,2b可在体内有效地抑制裸鼠的肿瘤生长。
|
| Fig 6 2b inhibits tumor weight (A/B) and volume tumor (C/D) of Hep 3B cells in nude mice *P < 0.05,**P < 0.01 vs control |
细胞凋亡是维持机体细胞群增殖与死亡的重要方式,这种方式一旦失调就会导致机体疾病,甚至肿瘤的发生、肿瘤细胞凋亡是一个关键的调节机制[8]。细胞凋亡会出现许多形态学方面的变化,如质膜的改变、胞质和细胞核的固缩、核内DNA裂解。本研究通过MTT比色法观察,苯并咪唑吡啶钌配合物均能抑制不同人肝癌细胞的增殖,特别是配合物2b对Hep 3B的特异性最好,其IC50值为12.1 μmol·L-1。通过TUNEL-DAPI 双染实验,在荧光显微镜下观察到,2b诱导Hep 3B 细胞出现了细胞核浓缩,DNA断裂等凋亡特征。凋亡的主要生化改变是DNA在凋亡内切酶的作用下,切断成片段状,部分DNA流失,细胞内的DNA总量减少。凋亡细胞的DNA总含量减少,它在流式细胞仪检测中出现特殊的Sub-G1凋亡峰。流式细胞仪检测结果表明,2b诱导Hep 3B 细胞出现了Sub-G1峰,且Sub-G1峰的累积呈浓度依赖性。
Caspase家族在介导细胞凋亡的过程中起着非常重要的作用,其中,caspase-3 是细胞凋亡信号传导中的关键性效应酶,它正常以酶原(32 ku)的形式存在于胞质中,在凋亡的早期阶段,它被激活,活化的caspase-3裂解为12 ku和17 ku的亚单位,最终导致细胞凋亡[9]。细胞凋亡包括内源性线粒体途径和外源性死亡受体途径,caspase-8是外源性凋亡途径的执行分子,caspase-9是内源性凋亡途径的执行者[10]。本研究发现,caspase-3和caspase-9的活性被2b激活,而caspase-8的活性不被激活,提示2b诱导Hep 3B 细胞凋亡是通过激活内源性凋亡途径实现的。
抑癌蛋白p53的表达减少与多种肿瘤的发生相关,包括肝癌。p53能通过内源性和外源性凋亡通路直接或间接地诱导细胞凋亡,从而抑制肿瘤[11]。一般认为,p53的促凋亡功能与线粒体释放凋亡因子有关。p53介导的凋亡是由DNA断裂激活的,其活性可通过特定氨基酸残基的磷酸化、乙酰化等来调节[12]。p53蛋白可通过调节p21与Bax在细胞周期阻滞及诱导细胞凋亡中发挥重要作用[13]。本实验中,我们发现2b诱导Hep 3B 细胞中p53磷酸化,且提高p53总蛋白表达量,同时,p21的蛋白表达量也明显地增加了。
钌配合物2b的体内抗肝癌活性,在荷瘤裸鼠实验中得到进一步的证明,2b能够减少肿瘤的体积和降低肿瘤的质量。综上所述,本实验室设计合成的苯并咪唑吡啶钌配合物具有良好的抗肝癌活性,它通过诱导肿瘤细胞凋亡而抑制其增殖,因此,具有潜在的应用开发前景,可作为候选化学药物进行深入的临床前抗肿瘤研究。然而该配合物的作用靶标和深入的药理作用机制,有待于进一步研究。
(致谢:本实验在暨南大学靶向药物研究室完成,感谢实验室的老师对本实验的帮助与指导。)
| [1] | 陈绍俊,黄海欣,李桂生. 原发性肝癌的内科治疗现状[J].中国肿瘤,2013,22(2):115-9.Chen S J,Huang H X,Li G S. Present status of medical treatment for hepatocellular carcinoma[J].Bull Chin Cancer, 2013,22 (2):115-9. |
| [2] | Yang X, Chen L, Liu Y, et al. Ruthenium methylimidazole complexes induces apoptosis in lung cancer A549 cells through intrinsic mitochon-drial pathway[J]. Biochimie,2012,94(2):345-53. |
| [3] | Bergamo A, Sava G. Ruthenium complexes can target determinants of tumour malignancy[J].Dalton Trans, 2007,7 (13): 1267-72. |
| [4] | Sava G, Bergamo A, Zorzet S, et al. Influence of chemical stability on the activity of the antimetastasis ruthenium compound NAMI-A[J]. Eur J Cancer, 2002,38 (3): 427-35. |
| [5] | Zhao Z, Luo Z, Wu Q, et al.Mixed-ligand ruthenium polypyridyl complexes as apoptosis inducers in cancer cells, the cellular translocation and the important role of ROS-mediated signaling[J].Dalton Trans, 2014,43(45):17017-28. |
| [6] | Li L,Cao W, Zheng W,et al. Ruthenium complexes containing 2,6-bis(benzimidazolyl)pyridine derivatives induce cancer cell apoptosis by triggering DNA damage-mediated p53 phosphorylation[J]. Dalton Trans, 2012,41(41), 12766-72. |
| [7] | 张秀娟,侯喆,白雪莹,季宇彬.杨梅素作用于人肝癌HepG-2细胞凋亡信号转导途径的研究[J].中国药理学通报,2014,30(1):71-6.Zhang X J, Hou J, Bai X Y, Ji Y B. Studies on myricetin inducing human hepatoma HepG-2 cells apoptosis through signal transduction pathway[J].Chin Pharmacol Bull, 2014,30(1):71-6. |
| [8] | Scheit K, Bauer G. Direct and indirect inactivation of tumor cell protective catalase by salicylic acid and anthocyanidins reactivates intercellular ROS signaling and allows for synergistic effects[J]. Carcinogenesis, 2015,36(3):400-11. |
| [9] | Juraver-Geslin H A, Durand B C. Early development of the neural plate: New roles for apoptosis and for one of its main effector Caspase-3[J]. Genesis, 2015,53(2):203-24. |
| [10] | Orrenius S, Gogvadze V, Zhivotovsky B. Mitochondrial oxidative stress: implications for cell death[J]. Annu Rev Pharmacol Toxicol, 2007,47:143-83. |
| [11] | Turner N, Moretti E, Siclari O, et al.Targeting triple negative breast cancer: is p53 the answer[J].Cancer Treat Rev, 2013,39(5):541-50. |
| [12] | Chen T, Wong Y S. Selenocystine induces apoptosis of human melanoma A-375 cells by activating ROS-mediated mitochondrial pathway and p53 phosphorylation[J]. Cell Mol Life Sci, 2008,65(17):2763-75. |
| [13] | Vernet-Tomás M, Baáos N, Sabadell D, et al.p53 expression in breast cancer predicts tumors with low probability of non-sentinel nodes infiltration[J]. J Obstet Gynaecol Res,2015 Feb 6. doi: 10.1111/jog.12670. |

