


大黄是蓼科植物掌叶大黄Rheum palmatum L.、唐古特大黄Rheum tanguticum’ Maxim. ex Balf.或药用大黄Rheum officinale Baill.的干燥根和根茎,2010版中国药典介绍大黄具有泻下攻积、清热泻火、凉血解毒、逐瘀通经、利湿退黄的功效。大黄素(emodin)是大黄的主要有效成分之一,有研究发现大黄素具有抗炎、降糖、降脂等作用,并能改善胰岛素抵抗,具有治疗2型糖尿病(type 2 diabetes mellitus,T2DM)的潜在价值[1, 2, 3]。
葡萄糖转运体4(glucose transporter type 4,GLUT4)是脂肪细胞和肌细胞摄取葡萄糖的重要转运体[4],并受AMP依赖的蛋白激酶[adenosine 5’-monophosphate (AMP)-activated protein kinase,AMPK]和过氧化物酶体增殖物激活受体(peroxisome proliferator-activated receptor γ,PPARγ)的调控。激活AMPK或PPARγ均可促进细胞编码GLUT4基因和GLUT4蛋白向细胞膜转位,是治疗T2DM的重要靶点[5, 6, 7]。课题组前期发现,大黄素对链脲佐菌素(STZ)诱导T2DM大鼠的胰岛素有增敏作用,并明显上调T2DM大鼠皮下脂肪组织细胞膜上GLUT4蛋白的表达[8],但对其药理作用的分子机制尚不明确。本研究进一步从AMPK和PPARγ途径探讨大黄素对脂肪细胞葡萄糖摄取的作用机制。
1 材料 1.1 实验动物与细胞株♂ Wistar大鼠[上海斯莱克实验动物有限责任公司,许可证号:SCXK(沪)2012-0002],由福建中医药大学实验动物中心饲养;小鼠3T3-L1成纤维细胞(中国科学院上海生命科学研究院)。
1.2 药品与试剂大黄素(纯度 ≥ 98%,陕西森弗生物技术有限公司,货号:20111120006);Revertaid First Strand cDNA Synthesis Kit(美国Fermentas公司);RNeasy® Mini Kit(德国Qiagen公司,货号:74104);6-NBDG(Sigma-Aldrich,货号:72987);SDS-PAGE凝胶配制试剂盒(上海碧云天生物技术研究所);GW9662(Sigma-Aldrich公司,货号:M6191);Compound C(Sigma-Aldrich公司,货号:P5499);抗体AMPKα1/2(Santa Cruz公司,货号:sc-25792)、p-AMPKα1/2(Santa Cruz公司,货号:sc-33524)、PPARγ(Santa Cruz公司,货号:sc-7273)、GLUT4(Santa Cruz公司,货号:sc-7938)、IRS-1(Santa Cruz公司,货号:sc-559)和p-IRS-1(Santa Cruz公司,货号:sc-33956);小鼠18S rRNA探针引物(货号:4319413E,Applied Biosystems)。
1.3 仪器凝胶成像分析系统(Bio-Rad,型号:ChemiDoc XRS+),PCR仪(Bio-Rad,型号:C1000),荧光定量PCR仪(Applied Biosystems,型号:7900HT),高速台式冷冻离心机(Thermo Fisher,型号:Primo R)。
2 方法 2.1 细胞诱导及处理方法3T3-L1前脂肪细胞接种到24孔板中,培养于37 ℃、5% CO2培养箱中。用第1诱导液(10%胎牛血清和1%双抗的高糖DMEM,0.5 mmol·L-1异丁基甲基黄嘌呤,1.0 mg·L-1胰岛素和1.0 μmol·L-1地塞米松)培养细胞48 h,更换为第2诱导液(10%胎牛血清和1%双抗的高糖DMEM,1 mg·L-1胰岛素)培养16 d,采用油红O染色法染色观察细胞内有油滴聚集,即表示3T3-L1细胞已诱导分化为成熟的脂肪细胞。经10 μg·L-1 LPS干预24 h后,实验分为Control组、Emodin给药组(1、10、50 μmol·L-1),收集细胞检测各项指标。同时,3T3-L1脂肪细胞经10 μg·L-1 LPS干预24 h,分为Control组、Emodin组、GW9662(5 μmol·L-1)+Emodin组、Compound C(10 μmol·L-1)+Emodin组。各组加入20 μmol·L-1葡萄糖类似物6-NBDG培养30 min。吸去培养液,用PBS洗涤细胞3遍,加入含1%曲通X-100的0.1 mol·L-1 pH 10磷酸钾缓冲液70 μL,避光裂解细胞10 min后,加入30 μL DMSO,轻轻摇动,使其与裂解液充分混匀后,用激发波长466 nm和发射波长540 nm荧光检测每孔荧光强度。
2.2 动物造模及处理方法STZ诱导T2DM模型的方法参照Lai等[9]的报道。♂ Wistar大鼠(200±20) g经适应性喂养后,改换高脂饲料饲养6周。经腹腔注射25 mg·kg-1 STZ,4周后检查大鼠空腹血糖(FBG)水平,FBG>7.8 mmol·L-1的大鼠视为T2DM模型。实验大鼠随机分为Control组和大黄素给药组,给药组每天灌胃大黄素100 mg·kg-1,Control组灌胃等体积的0.5% Na-CMC,连续灌胃21 d,并观察大鼠每天的体重变化和进食情况。d 21 取内脏脂肪组织进行后续实验。
2.3 Real-time PCR检测mRNA的表达按照QIAGEN RNeasy® Mini Kit试剂盒的操作步骤提取动物组织或细胞总RNA,用Revertaid First Strand cDNA Synthesis Kit试剂盒进行逆转录为cDNA。PCR反应以cDNA为模板,反应条件为50 ℃ 2 min,95 ℃预变性15 s,退火60℃ 30 s,40个循环。每个实验重复处理3批样品,每批样品分别以同一批样品的内参计算ΔΔCt,以2-ΔΔCt计算各组mRNA的表达量。ΔΔCt = 各组(Ct目的基因-Ct内参)-对照组(Ct目的基因-Ct内参)。PCR引物由上海捷瑞生物工程有限公司参照GenBank合成。引物序列详见Tab1。
| Gene | Species | Primer sequences |
| GLUT4 | Mouse | 5′-CTTCTTTGAGATTGGCCCTGG-3′ 5′-AGGTGAAGATGAAGAAGCCAAGC-3′ |
| Adiponectin | Mouse | 5′-AAAGGAGAGCCTGGAGAAGC-3′5′-AAAGGAGAGCCTGGAGAAGC-3′ |
| chREBP-α | Mouse | 5′-CGACACTCACCCACCTCTTC-3′5′-TTGTTCAGCCGGATCTTGTC-3′ |
| chREBP-β | Mouse | 5′-TCTGCAGATCGCGTGGAG-3′5′-CTTGTCCCGGCATAGCAAC-3′ |
| Adiponectin | Rat | 5′-AATCCTGCCCAGTCATGAAG-3′5′-GGAACATTGGGGACAGTGC-3′ |
| GAPDH | Rat | 5′-TGAAGGTCGGTGTCAACGGATTTGGC-3′5′-CATGTAGGCCATGAGGTCCACCAC-3′ |
用含1% PMSF的RIPA裂解液裂解动物组织或细胞,离心取上清液,用BCA法检测蛋白浓度,加1×上样缓冲液,100 ℃变性10 min。用SDS-PAGE凝胶进行电泳、转膜、封闭、4 ℃孵育一抗过夜,TBST洗膜3遍后,孵育二抗2 h,用Bio-Rad凝胶成像系统进行ECL显影。
2.5 统计学处理实验数据用SPSS 20.0软件进行统计分析,所有结果以  ± s表示,组间比较采用Student-t检验或one-way ANOVA进行统计。
± s表示,组间比较采用Student-t检验或one-way ANOVA进行统计。
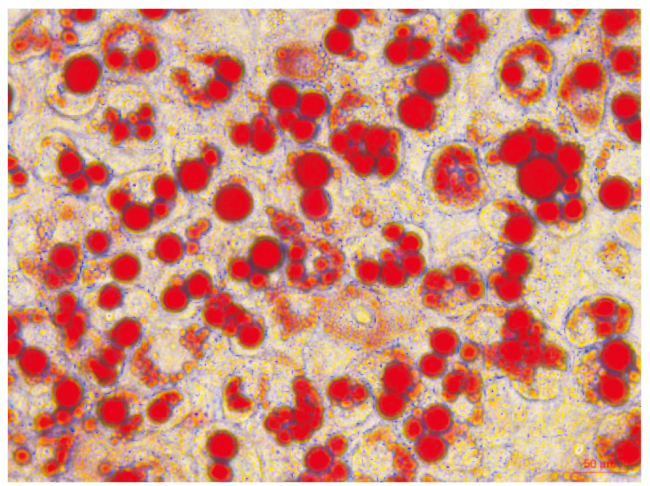
诱导分化后的3T3-L1细胞,体积变大,多呈圆形,胞质内容丰富,用油红O染色可见红色脂滴富集细胞核周(Fig1)。表明3T3-L1脂肪细胞已经诱导分化成熟。
|
| Fig 1 Differentiated 3T3-L1 adipocytes strained by oil red O (scale bar=50 μm) |
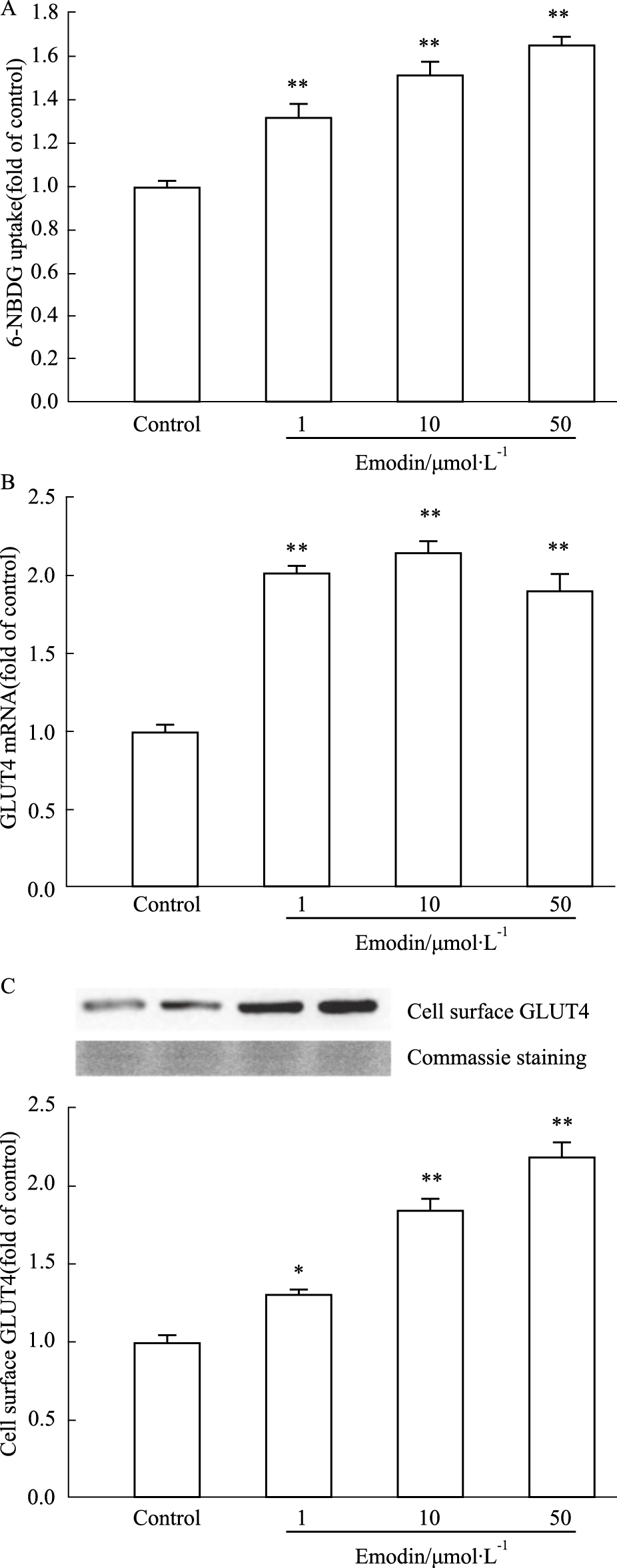
与Control组相比,大黄素给药组明显提高3T3-L1脂肪细胞对6-NBDG的摄取,并提高细胞膜上GLUT4的mRNA及蛋白表达水平,且差异有显著性(P < 0.05)(Fig2)。
|
| Fig 2 Emodin enhanced 6-NBDG uptake (A) and mRNA (B) and protein (C) expression of cell surface GLUT4 in 3T3-L1 adipocytes (n=3) *P < 0.05, **P < 0.01 vs control |
与Control组相比,大黄素给药组可提高3T3-L1脂肪细胞Adiponectin、chREBP-α和chREBP-β的mRNA表达(P < 0.05)。同时,大黄素给药组也提高了3T3-L1细胞IRS-1蛋白磷酸化水平,且差异有显著性(P < 0.05),见Fig3。

|
| Fig 3 Emodin enhanced mRNA expression of Adiponectin (A), chREBP-α (C), chREBP-β (D) and protein expression of p-IRS-1/total IRS-1 (B) in 3T3-L1 adipocytes (n=3) *P < 0.05, **P < 0.01 vs control |
与Control组相比,大黄素给药组可提高3T3-L1脂肪细胞AMPKα1/2蛋白磷酸化水平,且差异有显著性(P < 0.05)。同时,与Control组相比,大黄素给药组可提高3T3-L1脂肪细胞对6-NBDG的摄取。与Emodin组相比,Compound C组降低细胞对6-NBDG的摄取,而Compound C+Emodin组3T3-L1脂肪细胞对6-NBDG的摄取也降低(P < 0.05),见Fig4。

|
| Fig 4 Emodin enhanced protein expression of p-AMPK/total AMPK (A) and enhanced 6-NBDG uptake and uptake was inhibited by compound C (B) in 3T3-L1 adipocytes (n=3) *P < 0.05 vs control; #P < 0.05 vs emodin |
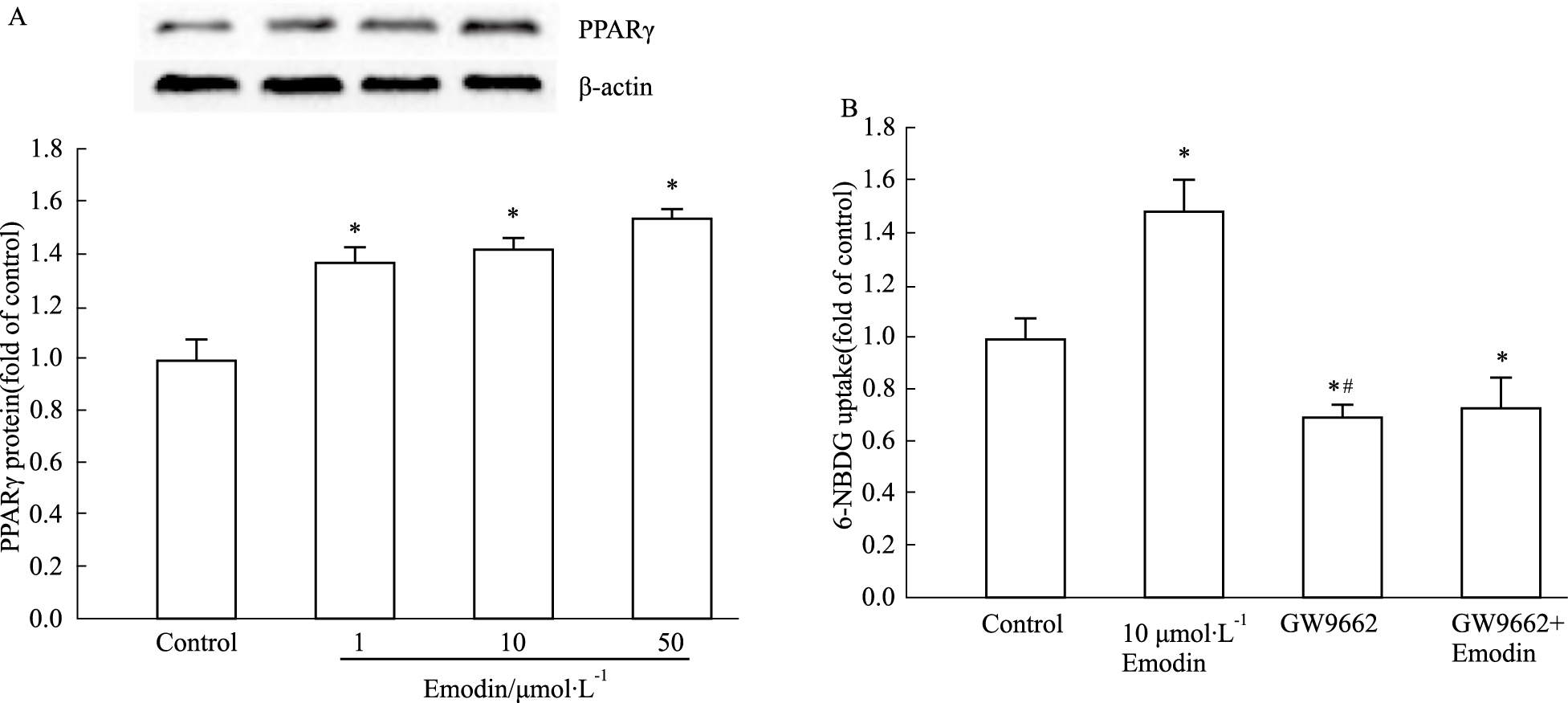
与Control组相比,大黄素给药组可提高3T3-L1脂肪细胞PPARγ蛋白表达水平,且差异有显著性(P < 0.05)。同时,与Control组相比,大黄素给药组可提高3T3-L1脂肪细胞对6-NBDG的摄取。与Emodin组相比,GW9662组降低细胞对6-NBDG的摄取,而GW9662+Emodin组3T3-L1脂肪细胞对6-NBDG的摄取也降低(P < 0.05),见Fig5。
|
| Fig 5 Emodin enhanced protein expression of PPARγ (A) and enhanced 6-NBDG uptake and uptake was inhibited by GW9662 (B) in 3T3-L1 adipocytes (n=3) *P < 0.05 vs control; #P < 0.05 vs emodin |
与Control组相比,Emodin组可提高T2DM大鼠脂肪组织细胞膜上GLUT4的蛋白表达和Adiponectin的mRNA表达,且差异有显著性(P < 0.01),见Fig6。

|
| Fig 6 Emodin enhanced protein expression of cell surface GLUT4 (A) and mRNA expression of Adiponectin (B) in adipose tissue of T2DM rats (n=4) **P < 0.01 vs control |
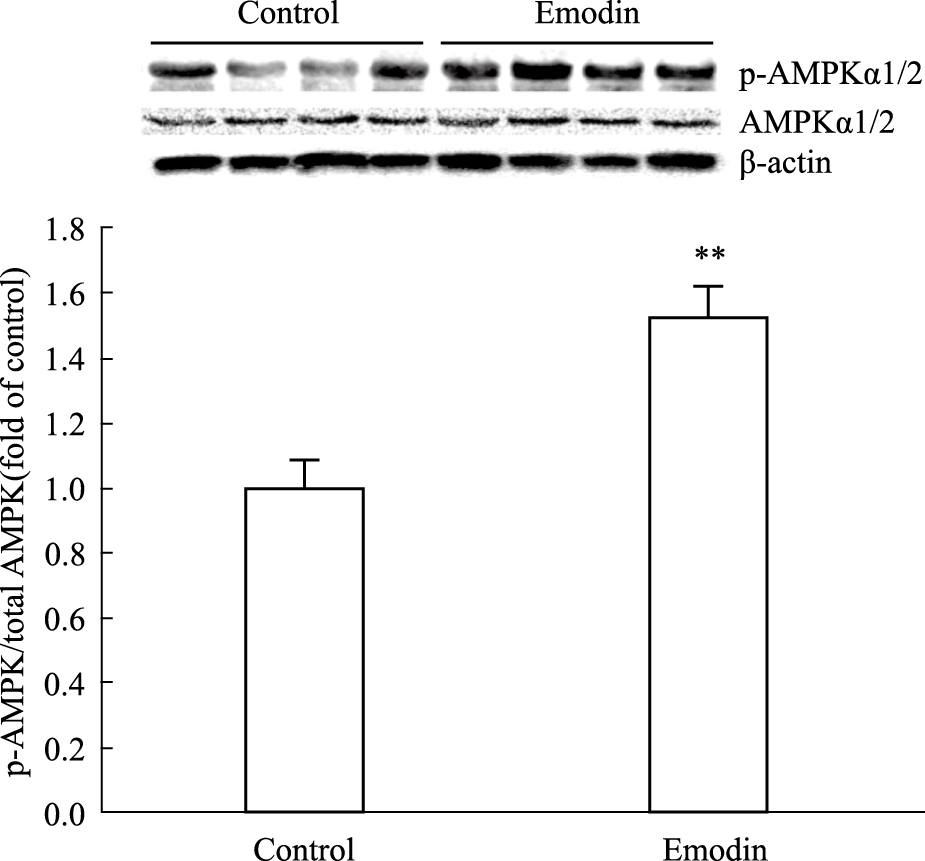
与Control组相比,Emodin组可提高T2DM大鼠的AMPKα1/2的蛋白磷酸化水平,且差异有显著性(P < 0.01),见Fig7。
|
| Fig 7 Emodin enhanced protein expression of p-AMPK/total AMPK in adipose tissue of T2DM rats (n=4) **P < 0.01 vs control |
脂肪细胞是全身能量与代谢的关键调节者[10]。当血糖浓度升高时,胰岛素诱导脂肪细胞摄取葡萄糖转化为脂质。T2DM患者由于肝脏、脂肪和肌肉等组织的胰岛素抵抗,导致血糖持续升高[11]。因此,增加脂肪细胞的胰岛素敏感度和葡萄糖摄取是治疗T2DM的手段之一。
Adiponectin是内源性胰岛素增敏激素[12],IRS-1是胰岛素受体的底物之一[13],大黄素能够促进二者的表达,提示大黄素可通过激活Adiponectin和IRS-1,提高3T3-L1脂肪细胞对胰岛素的敏感度。chREBP-α和chREBP-β是体内脂肪生成和糖分解的转录调控因子[10],chREBP的激活可促进葡萄糖向脂质转化。本实验研究结果显示,大黄素的降糖作用可能通过激活脂肪细胞chREBP的转录和促进脂肪细胞表面葡萄糖转运体GLUT4的葡萄糖转运实现的。同时,大黄素可激活3T3-L1脂肪细胞AMPKα1/2和PPARγ的表达,并且经AMPK和PPARγ抑制后,大黄素对3T3-L1脂肪细胞的葡萄糖摄取作用的影响明显减弱,表明大黄素促进3T3-L1脂肪细胞对葡萄糖的摄取与AMPK和PPARγ的信号通路有关。
综上所述,大黄素可增加3T3-L1脂肪细胞的胰岛素敏感度,促进3T3-L1脂肪细胞的葡萄糖摄取功能,发挥降血糖作用,其作用机制与激活Adiponectin及IRS-1,进而激活AMPK和PPARγ的信号通路有关。
(致谢:本实验在福建省中药学重点实验室完成,感谢实验室的老师对本实验的帮助与指导。)
| [1] | 刘 晗, 高 云. 大黄素药理作用的分子机制研究进展[J]. 中国药理学通报, 2009, 25(12):1552-5.Liu H, Gao Y. Research progress in molecular mechanism of the pharmacological actions of emodin[J]. Chin Pharmacol Bull,2009, 25(12): 1552-5. |
| [2] | 张 蓉, 朱榕峰, 徐 俊, 等. 大黄素改善脂多糖引起的胰岛素抵抗机制研究[J]. 上海中医药杂志, 2010,44(8):71-3.Zhang R, Zhu R F, Xu J, et al. Molecular mechanisms of emodin in inhibiting insulin resistance induced by lipopolysacchide[J]. Shanghai J Tradit Chin Med, 2010,44(8):71-3. |
| [3] | 张喜平, 李宗芳. 大黄素的药理作用研究概况[J]. 中国药理学通报, 2003,19(8):851-4.Zhang X P, Li Z F. General situation in pharmacological studies on emodin[J]. Chin Pharmacol Bull, 2003,19(8):851-4. |
| [4] | Govers R. Cellular regulation of glucose uptake by glucose transporter GLUT4[J]. Adv Clin Chem, 2014,66:173-240. |
| [5] | 葛 斌, 谢梅林, 顾振纶, 等. AMPK作为治疗2型糖尿病新靶点的研究进展[J]. 中国药理学通报, 2008,24(5):580-3.Ge B, Xie M L, Gu Z L, et al. AMPK acts as a new target for the treatment of type 2 diabetes[J]. Chin Pharmacol Bull, 2008,24(5):580-3. |
| [6] | Wu Z, Xie Y, Morrison R F, et al. PPARgamma induces the insulin-dependent glucose transporter GLUT4 in the absence of C/EBPalpha during the conversion of 3T3 fibroblasts into adipocytes[J]. J Clin Invest, 1998,101(1):22-32. |
| [7] | Zhang B B, Zhou G, Li C. AMPK: an emerging drug target for diabetes and the metabolic syndrome[J]. Cell Metab, 2009,9(5):407-16. |
| [8] | 向 青, 赖文芳, 许 文, 张小琴. 大黄素对2型糖尿病大鼠脂肪组织葡萄糖转运蛋白4表达的影响[J]. 福建中医药大学学报, 2014,24(5):22-4. Xiang Q, Lai W F, Xu W, Zhang X Q. The influences of emodin on glucose transporter type 4 indispose tissue of T2DM rats[J]. J Fujian Univ TCM, 2014,24(5):22-4. |
| [9] | Lai W, Tian X, Xiang Q, et al. 11β-HSD1 modulates LPS-induced innate immune responses in adipocytes by altering expression of PTEN[J]. Mol Endocrinol, 2015,29(4):558-70. |
| [10] | Herman M A, Peroni O D, Villoria J, et al. A novel ChREBP isoform in adipose tissue regulates systemic glucose metabolism[J]. Nature, 2012,484(7394):333-8. |
| [11] | Marzagalli R, Scuderi S, Drago F, et al. Emerging role of PACAP as a new potential therapeutic target in major diabetes complications[J]. Int J Endocrinol, 2015,2015:1-11. |
| [12] | Anusree S S, Priyanka A, Nisha V M, et al. An in vitro study reveals the nutraceutical potential of punicic acid relevant to diabetes via enhanced GLUT4 expression and adiponectin secretion[J]. Food Funct, 2014,5(10):2590-601. |
| [13] | Zheng J, Wang K, Jin P, et al. The association of adipose-derived dimethylarginine dimethylaminohydrolase-2 with insulin sensitivity in experimental type 2 diabetes mellitus[J]. Acta Biochim Biophys Sin, 2013,45(8):641-8. |

