


2. 军事医学科学院放射与辐射医学研究所, 北京 100850
高月(1963-),女,博士,研究员,研究方向:中药药理学,通讯作者,Tel:010-66931312,E-mail:gaoyue@bmi.ac.cn;
 , ZHOU Tao2, MA Zeng-chun2, LIANG Qian-de2, TANG Xiang-lin2, XIAO Cheng-rong2, TAN Hong-ling2, XIAO Yong2, WANG Yu-guang2
, ZHOU Tao2, MA Zeng-chun2, LIANG Qian-de2, TANG Xiang-lin2, XIAO Cheng-rong2, TAN Hong-ling2, XIAO Yong2, WANG Yu-guang2
 , GAO Yue2
, GAO Yue2

2. Institute of Radiation Medicine, Academy of Military Medical Sciences, Beijing 100850, China
人参(Panax ginseng C. A.)是常见的补益中药,具有大补元气、复脉固脱、生津养血、安神益智之功效,是目前常用的一味临床中药。其中人参皂苷是其主要的药理活性成分,约占人参组成的4%。现代药理学研究证明,人参皂苷具有调节机体免疫力[1]、延缓衰老[2]、改善心脑血管[3]、增强记忆力[4]、抑制肿瘤细胞生长[5]等作用,临床用药时常与其他西药联合使用。多种药物同时服用时,常会由于彼此之间的相互影响而产生不可预期的药物不良反应。药物之间的相互作用与多种因素有关,其中以药物代谢酶即细胞色素P450 (cytochrome P450)与药物相互作用的关系最为密切[6]。CYP3A作为P450家族中最重要的I相药物代谢酶系统,参与超过50%的临床药物的代谢[7]。研究已证明孕烷 X 受体 (PXR) 是调控CYP3A4 基因表达的关键转录因子,许多药物对PXR活性都有潜在的激动效应,从而诱导CYP3A的表达,导致其与CYP3A底物类药物联合使用时影响其代谢而致药物不良反应的发生[8, 9]。
目前,针对人参皂苷对于药物代谢酶影响的研究还较少。本实验室前期工作建立了基于分泌型Gaussia荧光素酶报告基因pGLuc-Basic系统,将报告基因载体和人PXR表达载体共转染HepG2细胞[10],并利用该模型筛选了人参中主要皂苷类成分对PXR活性的激动效应,初步研究发现人参皂苷F1有明显激活PXR活性的作用。于是本研究进一步探索了人参皂苷F1对LS174T细胞中CYP3A4 mRNA表达及酶活性的影响,以确证其是否通过激活PXR,从而诱导了CYP3A4的基因表达及酶活性,将有助于提示人参皂苷F1与其他药物联合应用时会产生的药物相互作用,为人参皂苷F1的临床应用提供实验依据。
1 材料与方法 1.1 材料 1.1.1 药品与试剂人参皂苷F1 (ginsenoside F1),批号111763-201209,购自中国食品药品检定研究院;利福平(rifampicin,RIF),批号:B74218,购自美国Merck公司;胎牛血清(批号:NXA0544)、MEM培养基(批号:NWE0403)、非必需氨基酸(NEAA,批号:AWG16123)、EDTA胰酶(批号:SLBC7668)均购自美国Hyclone公司;Guisssia荧光检测试剂盒(批号:0451201)购自美国NEB公司;TRIzol购自美国Sigma公司;反转录聚合酶链反应试剂盒及qPCR试剂盒均购自北京全式金生物技术有限公司;P450-GloTM CYP3A4 Assay with Luciferin-IPA(批号:0000009296)购自美国Promega公司;其他试剂均为国产分析纯。
1.1.2 主要仪器MCO-20AIC型二氧化碳培养箱(日本SANYO公司);超净工作台(北京长城空气净化设备公司);J-301型超高速离心机(Avanti公司);VictorX5型酶标仪(美国PerkinElmer公司);SteponeTM 272006169型Real-Time PCR仪(美国Applied Biosystem公司);DU-600型紫外分光光度计(Beckman公司)。
1.2 方法 1.2.1 细胞系和细胞培养LS174T(人结肠癌细胞)购自北京协和细胞库,由本实验室传代保存,初次复苏的细胞代数为第13代;PXR-CYP3A4稳定转染HepG2工程细胞株由本实验室构建并保存。二者均用含10%灭活胎牛血清的MEM培养基,放入37℃、5% CO2孵箱,按常规方法培养,并取对数生长期细胞用于实验。
1.2.2 荧光素酶报告基因检测取本实验室构建的工程细胞株,并参照前期实验工作方法[11],以细胞数1×105/孔接种于96孔板中,待细胞密度达80%后去掉培养液,换无血清MEM培养基,按不同浓度分别加入20、50、100、200 μmol·L-1的人参皂苷F1,同时设置10 μmol·L-1的利福平(RIF)为阳性对照组,每组药物设置6个复孔。分别在给药24、48 h后,吸取细胞培养液上清,进行荧光检测。荧光素酶活性的检测用 NEB BioLux Gaussia Luciferase Assay Kit检测试剂盒,在BioLuxGluc Assay Buffer 1mL中加BioLuxGluc Substrate 10 μL,混匀后,吸取20 μL细胞培养基上清至检测板孔中,然后每孔加入50 μL荧光检测试剂并混匀。然后用酶标仪进行化学发光检测,并记录检测结果。药物对PXR的激活效应用诱导倍数(fold induction)来反映,即每组的诱导倍数=药物处理组的荧光素酶活性值/溶剂对照组的荧光素酶活性值,并以此预测其对CYP3A4的诱导效应。
1.2.3 MTS检测LS174T细胞活性取对数生长期的LS174T细胞,制备成5×107·L-1的细胞悬液,按每孔100 μL接种于96孔板,放入37 ℃、5% CO2孵箱培养;24、48 h后更换无血清培养基,并加入不同浓度人参皂苷F1(10、20、50、100、200、300、400、500 μmol·L-1),同时设置对照组和空白组,每组6个复孔;分别在24、48 h后,每孔加入MTS试剂10 μL,继续孵育3~4 h;用酶标仪测定每孔450 nm处的吸光度值(OD值),按以下公式计算细胞存活率:细胞存活率(IC)/%=(实验组OD值-空白组OD值)/(对照组OD值-空白组OD值)×100%。
1.2.4 Q-PCR检测CYP3A4 mRNA水平变化不同浓度人参皂苷F1(20、50、100、200 μmol·L-1)分别处理LS174T 细胞24、48 h后,弃去培养基,用TRIzol法提取细胞总RNA;紫外分光光度计检测总RNA浓度和纯度(ODA260/A280比值在1.8~2.0之间可用)。RT-PCR试剂盒将总RNA反转录成cDNA后进行荧光实时定量PCR检测(本实验重复3次),具体操作参照说明书进行。用于扩增的特异性引物序列见Tab1。
| Gene | Forward primer(5′→3′) | Reverse primer(5′→3′) |
| CYP3A4 | CAATAAGGCACCACCCACCTAT | TTCTTGCTGAATCTTTCAGGGAG |
| GAPDH | TGTTGCCATCAATGACCCCTT | AGCATCGCCCCACTTGATTTTG |
参照Yang等[12]的方法,取LS174T细胞,制备成5×107·L-1的细胞悬液,按每孔100 μL接种于96孔板,放入37 ℃、5% CO2孵箱培养;24 h后更换无血清培养基,并加入不同浓度人参皂苷F1(20、50、100、200 μmol·L-1),同时设置空白对照组,每组6个复孔;分别在处理24、48 h后,每孔加入稀释好的5 μmol·L-1的底物Luciferin-IPA 50 μL,37℃环境下孵育30~60 min,再每孔加入等体积的Luciferin Detection Reagent,混匀;取50 μL混合液至不透光的白板,继续孵育15~20 min,然后用酶标仪进行化学发光检测,并记录检测结果。其诱导效应由药物处理组细胞活性值与空白对照组活性值的比值来反映。
1.2.6 统计学分析所有数据均重复3次,采用SAS 9.2软件进行统计学处理,结果用 ± s表示,两组之间比较用t检验。
± s表示,两组之间比较用t检验。
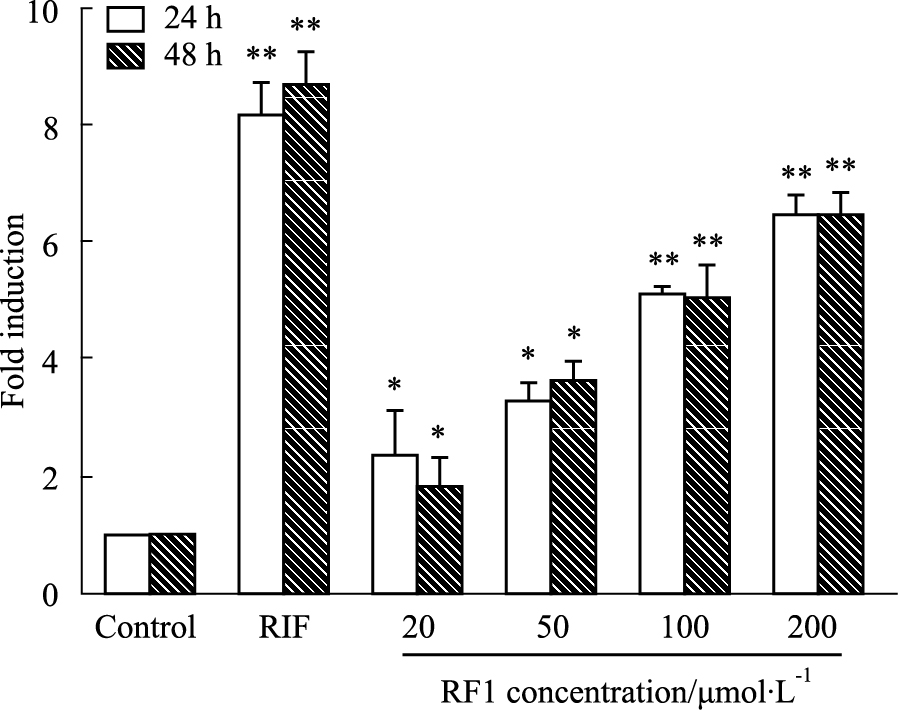
荧光素酶报告基因检测结果显示,人参皂苷F1能够明显增强PXR的转录活性。如Fig1所示,随着人参皂苷F1浓度的增加(20、50、100、200 μmol·L-1),PXR的转录活性逐渐增强(P < 0.01),并呈现一定的浓度依赖性;阳性对照药利福平(RIF)组亦明显增强了PXR的转录活性(P < 0.01)。
|
Fig.1
Effect of ginsenoside F1 on transactivation
of PXR( ± s,n=6)
*P<0.05, **P<0.01 vs control group ± s,n=6)
*P<0.05, **P<0.01 vs control group
|
MTS结果显示,随着人参皂苷F1浓度的升高,细胞存活率逐渐下降。如Fig2所示,低浓度的人参皂苷F1对细胞的存活率没有影响(如10、20 μmol·L-1);当人参皂苷F1浓度高于300 μmol·L-1时,对LS174T的细胞活性抑制率可达40%。因此,本实验选取200 μmol·L-1以下的浓度作为人参皂苷F1的实验浓度。

|
Fig.2
Effect of ginsenoside F1 on
cell viability of LS174T( ± s,n=6) ± s,n=6)
|
荧光实时定量PCR结果显示,与对照组相比,不同浓度人参皂苷F1(20、50、100、200 μmol·L-1)分别处理LS174T 24、48 h后,能明显诱导CYP3A4 mRNA的表达,如Fig3所示,当人参皂苷浓度为200 μmol·L-1时,诱导作用最为明显(P < 0.01)。其中,阳性对照药利福平(RIF)组对CYP3A4 mRNA表达的诱导作用可达5倍以上(P < 0.01)。

|
Fig.3
Effect of ginsenoside F1 on expression of
CYP3A4 mRNA in LS174T cells( ± s,n=3)
*P<0.05,**P<0.01 vs control group. ± s,n=3)
*P<0.05,**P<0.01 vs control group.
|
在对CYP3A4 mRNA水平检测的基础上,进一步对CYP3A4酶活性进行了检测,结果显示人参皂苷F1可以浓度依赖性地增强CYP3A4的酶活性。如Fig4所示,阳性对照药利福平(RIF)组,可明显增强CYP3A4的酶活性达3.43倍(P < 0.05);低浓度的人参皂苷F1(20 μmol·L-1)对CYP3A4的酶活性没有明显影响,50、100、200 μmol·L-1的人参皂苷F1可明显增强CYP3A4的酶活性,并呈现浓度依赖性。

|
Fig.4
Effect of ginsenoside F1 on enzyme activity
of CYP3A4 in LS174T cells( ± s,n=6)
*P<0.05 vs control group. ± s,n=6)
*P<0.05 vs control group.
|
本实验室前期研究工作建立了基于分泌型Gaussia荧光素酶报告基因pGLuc-Basic系统,将报告基因载体和人PXR表达载体共转染HepG2细胞,通过G418抗性筛选获得稳定转染细胞株,该细胞株具有使用分泌型荧光素酶载体、检测方便、具备高通量潜力的优势,并采用双远端增强子模式,实现可能的高诱导、高灵敏度,提高了筛选的效率[13]。
本研究基于以上筛选技术,发现人参皂苷F1能够明显激活孕烷X受体(PXR)的转录活性,并呈现明显的浓度依赖性。为进一步确证人参皂苷F1对CYP3A4的影响,本实验又选取了PXR表达较高的LS174T细胞,从CYP3A4的基因表达和酶活性两个方面进行了研究。结果显示,人参皂苷F1通过激活PXR以后,对CYP3A4的活性及表达有明显的增强作用。前期本实验室的筛选结果显示10 μmol·L-1的人参皂苷F1对PXR没有转录激活作用[13],与本次实验的结果不一致,这可能与两次实验所采用的人参皂苷F1浓度不一致有关,因此进一步说明在特定浓度下高通量筛选又是可能会漏掉有阳性作用的筛选对象,改变筛选浓度可能会发现新的有阳性作用的化合物。PXR是CYP3A4的关键转录调控因子,药物通过激活PXR介导的信号通路调节CYP3A4的表达是影响药物在体内代谢的重要途径[8, 9]。某种药物通过诱导或抑制P450酶特定的亚型或许就会改变另一种药物的代谢清除特性,从而导致不利于机体的药物相互作用。CYP3A4的底物范围非常广泛,包括胆汁酸、内源性甾体激素以及50%的临床常用药物[14]。人参作为目前临床上常用的一味中药,其相关制品引起的临床上药物相互作用已有报道[15],如丹参注射液与华法林合用时,丹参会增加华法林的血药浓度而导致出血[16]。本实验中人参皂苷F1对PXR-CYP3A4通路的激活效应,提示当其与CYP3A4底物类药物联合使用时,可能会影响其代谢而导致不良的药物相互作用,临床联合用药时应引起重视。
中草药中含有的诸多天然活性成分,具有广泛的生理功能,在临床上的应用日益普遍,尤其以中西药联合给药的方式。也有越来越多的研究报道有些中药或其有效成分会作用于药物代谢酶而产生药物相互作用,影响到其他药物的代谢,甚至产生毒理效应,如五味子和甘草处理大鼠后,会激活PXR并诱导大鼠肝微粒体中CYP3A4的表达,加速华法林和丙咪嗪等药物的代谢清除[17]。因此,有必要加强中草药及其有效成分对PXR-CYP3A4通路的影响及其作用机制的研究,对中药更广泛的临床应用及中西药的联合使用都具有重大意义。
(致谢:本实验在军事医学科学院放射与辐射医学研究所二所二室完成,衷心感谢指导老师高月研究员、王宇光副研究员提供的实验室、实验器材及资金支持。)
| [1] | 于学涛, 王淑萍. 人参皂苷Rg3联合化疗治疗对胃癌术后患者的临床观察[J].中华肿瘤防治杂志, 2010,17(10): 779-81.Yu X T, Wang S P. Clinical observation on treatment for postoperative gastric cancer by ginsenoside Rg3 combined with chemotherapy[J]. Chin J Cancer Prev Treat, 2010,17(10): 779-81. |
| [2] | Cho W C, Chung W S, Lee S K, et al. Ginsenoside Re of Panaxginseng possesses significant antioxidant and anti-hyperlipidemic effects in streptozotocin induced diabetic rats[J]. Eur J Pharmacol, 2006,550(1-3): 173-9. |
| [3] | Liu X, Wang L, Wen A, et al. Ginsenoside Rd improves outcome of acute ischaemicstroke:a randomized, double-blind, placebo-controlled, multicenter trial[J]. Europ J Neurol, 2012,19: 855-63. |
| [4] | Zhang G, Liu A, Zhou Y, et al. Panax Ginsenoside Rg2 protects memory impairment via anti-apoptosis in a rat model with vascular dementia[J]. J Ethno Pharmacol, 2008,115(3): 441-8. |
| [5] | Ye R D, Han J L, Kong X W, et al. Protective effects of Ginsenoside Rd on PC12 cells against hydrogen peroxide[J]. Biol Pharm Bull, 2008,31(10): 1923-7. |
| [6] | Spatzenegger M, Jaeger W. Clinical importance of hepatic cytochrome P450 in drug metabolism[J]. Drug Metab Rev, 1995,27(3):397-417. |
| [7] | Guengerich F P. Cytochrome P4503A4: regulation and role in drug metabolism[J]. Annu Rev Pharmacol Toxicol, 1999,39:117. |
| [8] | Wang Y M, Su Sien Ong, Sergio C, et al. Role of CAR and PXR in xenobiotic sensing and metabolism[J]. Expert Opin Drug Metab Toxicol, 2012,8 (7): 803-17. |
| [9] | Tolson A H, Hongbing W. Reguaton of drug-metabolizing enzymes by xenobiotic receptors: PXR and CAR[J]. Adv Drug Deliv Rev, 2010,62(13): 1238-49. |
| [10] | Wang Y G, Ye X, Ma Z C, et al. Induction of cytochrome P4501A1 expression by Ginsenoside Rg1 and Rb1 in HepG2 cells[J]. Eur J Pharmacol, 2008,601(1-3): 73-8. |
| [11] | 周涛,王宇光,马增春,等. 银杏内酯B通过激活孕烷X受体诱导CYP3A4的表达[J].中国药理学通报,2014,30(7):926-31.Zhou T, Wang Y G, Ma Z C, et al. Ginkgolide B induces CYP3A4 expression through activation of human pregnane X receptor[J]. Chin Pharmacol Bull, 2014,30 (7): 926-31. |
| [12] | Yang J, Yan B. Photochemotherapeutic agent 8-methoxypsoralen induces cytochrome P4503A4 and carboxylesterase HCE2: evidence on an involvement of the pregnane X receptor[J]. Toxicol Sci, 2007,95(1): 13-22. |
| [13] | 王宇光,刘浩生,肖勇,等.人参中皂苷成分的孕烷X受体激动特性筛选[J].药学学报,2013,48(1): 144-8.Wang Y G, Liu H S, Xiao Y, et al. Screening of pregnane X receptor activation from ginsenosides[J]. Acta Pharmaceu Sin, 2013,48(1): 144-8. |
| [14] | Rendic S, Di Carlo F J. Human cytochrome P450 enzymes: a status report summarizing their reaction, substrates, inducers and inhibitors[J]. Drug Metab Rev, 1997,29(1-2): 413-580. |
| [15] | Gurley B J, Gardner S F, Hubbard M A, et al. Clinical assessment of effects of botanical supplementation on cytochrome P450 phenotypes in the elderly: Stjohns'wort, garlic oil,Panax ginseng and Ginkgo biloba[J]. Drugs Aging, 2005,22(6): 525-39. |
| [16] | Freeman B D, Zehnbauer B A, Megrath S, et al. Cytochrome P450 polymorphisms are associated with reduced warfarin dose[J]. Surgery, 2000,128(2): 281-5. |
| [17] | Mu Y, Zhang J, Zhang S, et al. Traditional Chinese medicines Wu Wei Zi (Schisandra chinensis Baill) and Gan Cao(Glycyrrhiza uralensis Fisch) activate pregnane X receptor and increase warfarin clearance in rats[J]. J Pharmacol Exp Ther, 2006,316(3): 1369-77. |