


2. 安徽医科大学研究生学院, 安徽 合肥 230032
 , LIANG Miao1, ZHAO Jia-wei1, 2, WANG Yu-guang1, TAN Hong-ling1, LIANG Qian-de1, TANG Xiang-lin1, XIAO Cheng-rong1, GAO Yue1
, LIANG Miao1, ZHAO Jia-wei1, 2, WANG Yu-guang1, TAN Hong-ling1, LIANG Qian-de1, TANG Xiang-lin1, XIAO Cheng-rong1, GAO Yue1

2. Graduate School of Anhui Medical University, Hefei 230032, China
中药化学成分多种多样,当作为口服药物应用时,有些中药成分可直接吸收,而有些成分在代谢过程中活性降低或转变为无活性的物质,导致药理学上的失活,还有些成分可代谢转化为有药理活性的物质或活性增强而起作用,即活化过程。药物在胃肠道的代谢过程包括Ⅰ相反应和Ⅱ相反应,催化Ⅰ相反应的关键酶是细胞色素P450 酶(CYP450)酶家族,作为机体对药物或外源物代谢的最主要功能蛋白,主要包括6种重要亚型:CYP1A2、CYP2B6、CYP2C9、CYP2C19、CYP2D6、CYP3A4[1, 2]。中药强调合并用药,方剂以复方为主,因此中药配伍存在与P450酶有关的中药间相互作用,药物代谢酶是决定药物体内过程的关健因素,它们的抑制或诱导作用是药物联合应用时产生药动学相互作用的主要机制[3]。
四物汤(SiWu decoction,SWD)是补血名方,本室前期采用活性指导下的化学成分分析,发现了四物汤中促进造血功能的主要物质基础为多糖、阿魏酸、川芎嗪、芍药苷等,重构了基于四物汤有效成分的新组方,并且首次揭示了芍药苷具有促进造血的活性[4, 5, 6, 7, 8],四物汤及其配伍对大鼠肝脏P450酶的研究结果表明,四物汤复方对大鼠肝脏CYP1A2具有诱导作用,对CYP2B6具有抑制作用[6]。本文根据4种有效成分在四物汤中的百分含量确定药物的给药剂量,探索四物汤中4种有效单体成分对CYP450酶活性影响,进一步在基因和蛋白水平进行确证,从药物代谢酶角度为四物汤配伍规律提供实验依据。
1 材料 1.1 药品与试剂四物汤由熟地、当归、白芍、川芎组成,全部购自同仁堂中药厂。果糖、阿魏酸、磷酸川芎嗪、芍药苷、咪达唑仑、甲苯磺丁脲、非那西丁、右美沙芬、扑热息痛、普萘洛尔均购于中国食品药品检定研究院。S-美芬妥因、1’-羟基咪达唑仑、4-羟基甲苯磺丁脲、4-羟基美芬妥因、右啡烷、安非他酮、4-羟基安非他酮均购自美国BD公司。还原型辅酶Ⅱ购自Roche公司。RNA提取试剂盒(Biomed公司),逆转录酶及Q-PCR扩增试剂(TransGen公司)。CYP1A2、CYP2C11、CYP2B1、CYP3A1及内参β-actin引物由英潍捷基合成。脱脂奶粉、硝酸纤维膜购自北京普利莱基因技术有限公司。CYP2B1抗体购自Santa Cruz公司(美国),发光剂购自Millipore Coporation,过硫酸胺购于 Amersham Biosciences 公司,TEMED购自生工生物工程(上海)有限公司,抗GADPH鼠单克隆抗体、山羊抗小鼠IgG、蛋白分子量marker、组织蛋白抽提试剂盒、高效显影液试剂、30%丙烯酰胺-甲叉双丙烯酰胺、2×Sample Buffer、吐温-20均购自北京康为试剂公司。甲醇和乙腈为色谱纯,购自Fisher(美国),实验用水为超纯水,其他试剂均为分析纯。
1.2 动物和分组Wistar大鼠,在动物中心饲养3 d后,进行称重,随机分组。分为空白对照组、四物汤组、果糖组、阿魏酸组、川芎嗪组、芍药苷组,每组8只动物。
1.3 仪器Agilent 1290型超高效液相色谱仪(UHPLC,美国Agilent公司);Agilent 6410B型三重四极杆串联质谱仪(美国Agilent公司);Agilent ZORBAX EclipsePlus-C18色谱柱(100 mm×2.1 mm,3.5 μm,美国Agilent 公司);RE52CS型旋转蒸发器(上海亚荣生化仪器厂);电热恒温水浴锅(北京长安科学仪器厂);SHB-ⅢA循环水式多用真空泵(郑州长城科工贸有限公司);Western blot转膜仪(Bio-Rad公司),电泳仪(Amersham公司),转移脱色摇床(海门市其林贝尔仪器制造有限公司);BS 223S型电子天平(塞多利斯科学仪器有限公司);ABI Step One Plus荧光定量PCR仪(ABI公司)。
2 方法 2.1 供试样品的制备四物汤水煎液按《太平惠民和剂局方》规定的剂量称取组成,熟地15 g,当归10 g,白芍10 g,川芎6 g,共计41 g·d-1。四物汤复方组给药剂量根据实验室前期研究选取高剂量10 g·kg-1·d-1,其他各组给药剂量按其在复方中百分含量进行换算(果糖3.34%,阿魏酸0.02%,川芎嗪0.11%,芍药苷0.22%),即果糖0.334 g·kg-1·d-1,阿魏酸0.002 g·kg-1·d-1,川芎嗪0.011 g·kg-1·d-1,芍药苷0.022 g·kg-1·d-1。连续灌胃给药7 d,禁食,制备肝微粒体。空白对照组给予等量的生理盐水。
2.2 肝微粒体的制备参考本室建立的方法提取肝微粒体[9],大鼠脱臼处死,用生理盐水灌洗肝脏呈土黄色。将肝脏剪碎,按1 ∶ 4(W/V)加入TMS缓冲液,冰浴中匀浆后12 000×g,离心20 min,取上清液105 000×g离心60 min,弃上清,沉淀部分即微粒体。
2.3 逆转录及实时定量聚合酶链式反应(Q-PCR)参考本室建立的方法进行Q-PCR检测[9],大鼠处死后迅速取出肝脏,置于液氮中保存。按RNA提取试剂盒说明书提取肝脏总RNA。取总RNA 1μg进行反转录,条件为42℃ 30 min,85℃ 5 min。逆转录产物2 μL,加入2×TransStart Green qPCR SuperMix 10 μL,Forward Primer 0.4 μL,Reverse Primer 0.4 μL,Passive Reference Dye 0.4 μL,加ddH2O 补足反应体系至20 μL,荧光实时定量PCR的条件为94℃30 s,94℃ 5 s,60℃ 30 s,循环数为40。以β-actin作为内参基因,进行PCR扩增的实时定量分析,实验重复测定3次。特异性引物序列见Tab1。
| Gene | Forward primer(5′→3′) | Reverse primer(5′→3′) |
| CYP1A2 | GTCACCTCAGGGAATGCTGTG | GTTGACAATCTTCTCCTGAGG |
| CYP2B1 | ACCGGCTACCAACCCTTGAT | TGTGTGGTACTCCAATAGGGACAA |
| CYP2C11 | CTGCTGCTGCTGAAACACGTG | GGATGACAGCGTACTATCAC |
| CYP3A1 | GGAAATTCGATGTGGAGTGC | AGGTTTGCCTTTCTCTTGCC |
| β-actin | TTCAACGGCACAGTCAAG | CACACCCATAACAAACAT |
参考本室建立的方法进行[9],以流动相A(含0.1%甲酸和5 mmol·L-1甲酸铵的纯水)和B(含0.1%甲酸的乙腈)梯度洗脱:30%B(0 min),95%B(1.5-3.5 min),30%B(3.6 min);柱温25℃,流速为0.45 ml·min-1,运行时间4.5 min;进样体积10 μL。内标为普奈洛尔(100 μg·L-1)。以ESI源正离子MRM方式检测,毛细管温度320℃,毛细管电压+4000V,雾化电压25psi,干燥气流速10 L·min-1,其它质谱分析参数见Tab2。
| Compounds analyte | Ion pairs (m/z) | Fragmentor /V | Collection energy CE/V | Retention time/min |
| Acetaminophen | 152.1/110.1 | 110 | 10 | 2.70 |
| 4-Hydroxytolbutamide | 287/171.1 | 105 | 14 | 3.55 |
| 4-Hydroxy Mephenytoin | 235.2/150.1 | 100 | 14 | 3.36 |
| Dextrorphan | 258.2/157.1 | 145 | 40 | 2.91 |
| Hydroxybupropione | 256.7/239.1 | 90 | 10 | 3.22 |
| 1′-Hydroxymidazolam | 342.1/324.1 | 145 | 18 | 3.49 |
| Proranolol | 260/116.2 | 120 | 16 | 3.28 |
参考本室建立的方法进行[10],孵育体系包括肝微粒体(0.5 g·L-1),NADPH(1 mmol·L-1),CYP探针底物非那西丁(50 μmol·L-1)、甲苯磺丁脲(120 μmol·L-1)、美芬妥因(40 μmol·L-1)、右美沙芬(5 μmol·L-1)和咪达唑仑(5 μmol·L-1),K2HPO4/KH2PO4缓冲液(0.05 mol·L-1,pH=7.4)补足体系至200 μL。37℃水浴预孵育5 min后加入同样预孵育5 min的NADPH启动反应,37℃水浴孵育30 min,加入200 μL的甲醇 ∶ 乙腈(1 ∶ 1)含有内标盐酸普奈洛尔100 mg·L-1的溶液终止反应,13 000×g、4℃离心10 min,取上清液进样,定量分析各底物的代谢产物生成率,测得酶活性。
2.6 大鼠肝脏CYP2B1蛋白表达的测定称取0.1 g肝脏组织,加入1 mL组织蛋白抽提试剂,研磨后冰上孵育20 min,于10 000×g 离心15 min提取蛋白,用BCA法测定蛋白含量。每组蛋白上样量为20 μg,120V恒压电泳。采用电转印仪转印3 h,用封闭液室温下封闭1 h,加入稀释后的CYP2B1一抗(1 ∶ 200)及GADPH抗体(1 ∶ 500)在室温下孵育2 h,用TBST在室温下脱色摇床洗3次。洗膜后加入适量稀释的二抗,于室温孵育1 h,用TBST室温脱色摇床洗3次,进行化学发光反应。
2.7 数据分析实验数据以x±s表示,运用SAS统计学软件,两组间比较采用t检验,多组间比较采用F检验。
3 结果 3.1 四物汤及其成分对大鼠肝脏CYP450酶活性的影响利用Cocktail 探针法对给药前后大鼠肝微粒体的酶活性变化进行检测,四物汤组及芍药苷组与对照组相比对CYP1A2酶活性具有上调作用(P<0.05),果糖和川芎组与对照组相比对CYP1A2酶活性具有下调作用(P<0.05)。四物汤、果糖、阿魏酸、芍药苷以及川芎嗪组与对照组相比,对CYP2B6酶活性均具有抑制作用。果糖、阿魏酸、川芎嗪3组与对照组相比对CYP2C9酶活性具有下调作用,且果糖组下调作用较强。果糖组和芍药苷组与对照组相比对CYP2D6酶活性具有下调作用。见Tab3。
| (μmol·min-1·g Pro) | ||||||
| Group | CYP1A2 activity | CYP2B6 activity | CYP2C9 activity | CYP2C1 activity | CYP2D6 activity | CYP3A4 activity |
| *P<0.05, **P<0.01 vs control | ||||||
| Control | 0.047±0.0089 | 0.021±0.0041 | 0.024±0.0062 | 0.0025±0.0006 | 0.24±0.02 | 0.0572±0.0051 |
| SiWu decoction | 0.049±0.0088* | 0.018±0.0026** | 0.023±0.0033 | 0.0023±0.0004 | 0.24±0.02 | 0.0574±0.0045 |
| Fructose | 0.033±0.0076* | 0.012±0.0022** | 0.016±0.0026** | 0.0017±0.0003* | 0.22±0.03* | 0.0572±0.0044 |
| Ferulic acid | 0.042±0.0089 | 0.014±0.0022** | 0.020±0.0021* | 0.0020±0.0004* | 0.24±0.02 | 0.0572±0.0026 |
| Peoniflorin | 0.049±0.0077* | 0.011±0.0047** | 0.023±0.0021 | 0.0022±0.0005 | 0.21±0.02** | 0.0579±0.0074 |
| Ligustrazine | 0.034±0.0049* | 0.014±0.0027** | 0.019±0.0041* | 0.0021±0.0004* | 0.25±0.02 | 0.0551±0.0075 |
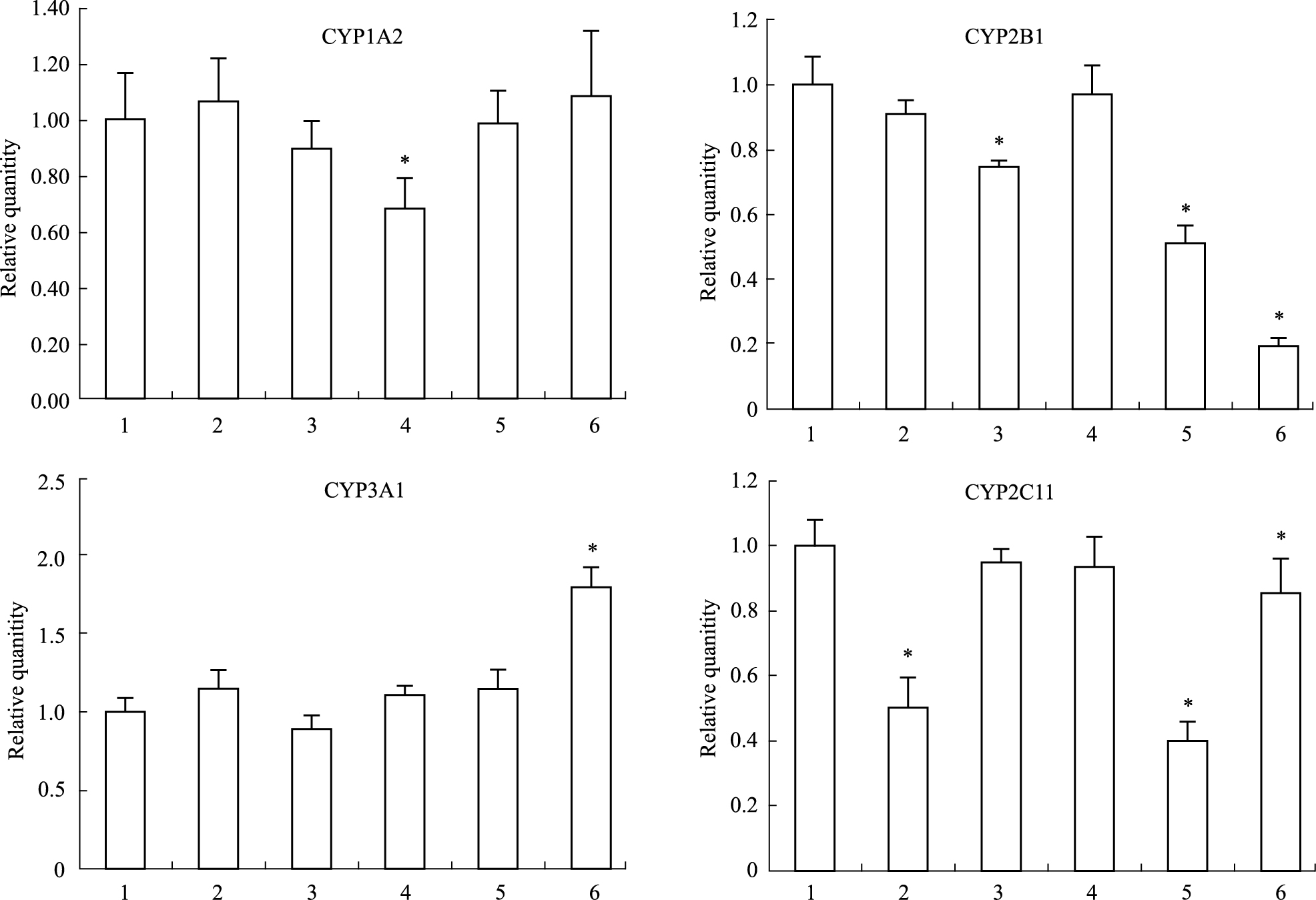
选择CYP1A2、CYP2B1、CYP2C11、CYP3A1 4种CYP450酶亚型进行在mRNA检测,川芎嗪组与对照组相比对CYP1A2的mRNA具有下调趋势,四物汤组与对照组相比对CYP1A2的mRNA是上调趋势,作用趋势与酶活性水平一致。阿魏酸、果糖及芍药苷3组与对照组相比对CYP2B1的mRNA具有明显抑制作用(P<0.05),果糖组与对照组相CYP2C11的mRNA具有明显抑制作用。见Fig1。
|
| Fig 1 Effect of SiWu decoction and its active components on cytochrome P450 mRNA in rats detected by Q-PCR 1:Control; 2:SiWu decoction; 3:Ferulic acid; 4:Ligustrazine; 5:Fructose; 6:Peoniflorin.*P<0.05 vs control group. |
利用Western blot检测了大鼠肝脏CYP2B1的蛋白表达,研究结果显示,与对照组相比,四物汤组、果糖、阿魏酸、芍药苷、川芎嗪4组对CYP2B1的蛋白表达均降低。见Fig2。

|
| Fig 2 Effect of SiWu decoction and its active components on CYP2B1 in rats liver detected by Western blot 1:Control; 2:SiWu decoction; 3:Ferulic acid; 4:Ligustrazine; 5:Fructose; 6:Peoniflorin. |
细胞色素P450酶(cytochrome P450,CYP450),属于血红素蛋白基因超家族,编码一系列的代谢酶系统,主要存在于肝微粒中,参与生物体内源性和外源性物质的生物转化,90%临床使用的药物要经过这些亚酶进行I相代谢。细胞色素P450酶作为人体重要的I 相药物代谢酶系统,对药物代谢和药物之间的相互作用有着重要影响[11]。中药方剂以复方为主,含有多种中药,因此中药配伍存在与P450酶有关的中药间相互作用的机会可能更多,药物对P450酶产生影响,进一步受到影响的P450酶再作用于复方中其他成分,这就是基于P450酶的中药配伍研究的分子基础[12]。本文分析四物汤及其有效成分对P450酶活性、mRNA及蛋白表达水平的影响,发现基于药物代谢酶的中药相互作用模式,为临床用药提供理论依据。
检测四物汤中药效学物质果糖、阿魏酸、川芎嗪、芍药苷对CYP450酶活性、mRNA基因转录水平及蛋白表达水平的影响,结果发现果糖对CYP1A2、CYP2B6、CYP2C9、CYP2D6酶活性具有抑制作用,并且对CYP2C9、CYP2C19的调节作用要强于其他成分。阿魏酸对CYP2C9、CYP2B6酶活性具有抑制作用,对其他亚酶活性无影响。川芎嗪对CYP1A2、CYP2C9、CYP2B6的酶活性具有抑制作用。芍药苷对CYP1A2酶活性具有诱导作用,对CYP2D6、CYP2B6酶活性具有抑制作用。4种单体成分对CYP3A4酶活性和mRNA转录水平的影响并不是很明显。阿魏酸、果糖、芍药苷组对CYP2B1mRNA的表达具有抑制作用,与酶活性水平一致。进一步考察4种单体成分对CYP2B1在蛋白水平表达的影响,结果也具有抑制作用,提示单体成分对CYP2B1的调控有可能是作用于蛋白翻译环节,值得深入研究。
口服药物的吸收可能会受到肝细胞对其代谢的影响,细胞色素P450酶介导了许多药物之间的相互作用。从而改变了药物的药理-毒理效应,导致药效加强或副作用减轻,也可使某药效降低,或使某效应丧失,或出现毒性加重,或出现不应有的毒副作用。本文研究结果说明复方对CYP1A2具有诱导作用,对CYP2B6具有抑制作用,四物汤、四味单药以及两两配伍对CYP2B1的酶活性和mRNA表达有抑制作用[9],4种单体成分对CYP2B1的酶活性和mRNA表达水平也有抑制作用,CYP2B1在四物汤配伍以及临床合理用药中的地位和作用值得进一步研究。
(致谢:本实验在军事医学科学院放射与辐射医学研究所药理毒理研究室完成。)
| [1] | Zhou X, Chan K, Yeung J H. Herb-drug interactions with Danshen (Salvia miltiorrhiza): a review on the role of cytochrome P450 enzymes[J]. Drug Metab Drug Int, 2012, 27(1):9-18. |
| [2] | Lee S Y, Lee J Y, Kang W, et al. In vitro and in vivo assessment of cytochrome P450-mediated herb-drug interaction of Ssang-hwa-tang[J]. Food Chem, 2013, 136(2):450-7. |
| [3] | 谭 妍, 沈国林, 庄笑梅, 等. 四物汤效应成分基于 CYP 酶的相互作用研究[J]. 中国药理学通报, 2014, 30(10):1456-61. Tan Y, Shen G L, Zhuang X M, et al. In vitro investigation on CYP enzyme based interaction of active components from SIWU decoction[J]. Chin Pharmacol Bull, 2014, 30(10):1456-61. |
| [4] | Lee S Y, Lee J Y, Kang W, et al. Cytochrome P450-mediated herb-drug interaction potential of Galgeun-tang[J]. Food Chem Toxicol, 2013, 51:343-9. |
| [5] | 马增春, 高 月, 谭洪玲, 等.用分子中药组学技术研究四物汤补血的作用机理[J].世界科学技术中医药现代化, 2005, 7(3):24-8. Ma Z C, Gao Y, Tan H L, et al. Study of blood-tonifying mechanisms of siwutang of Traditional Chinese Medicine by technology of TCM moleculomics[J]. World Sci Techol/Mod Tradit Chin Med Mat Med, 2005, 7(3):24-8. |
| [6] | 梁乾德, 路晓钦, 马增春, 等.四物汤促进造血功能成分的初步研究[J].中国中药杂志, 2004, 29(6):546-9. Liang Q D, Lu X Q, Ma Z C, et al. Preliminary study on hematopoietic constituents of SI-WU-TANG[J]. Chin J Chin Mat Med, 2004, 29(6):546-9. |
| [7] | 高 月, 马增春, 梁乾德, 等. 四物汤的方证结合研究[J]. 世界科学技术中医药现代化, 2010, 12(2):211-6. Gao Y, Ma Z C, Liang Q D, et al. Si-Wu-Tang and blood deficiency[J]. World Sci Techol/Mod Tradit Chin Med Mat Med, 2010, 12(2):211-6. |
| [8] | 王东根, 马增春, 邵 帅, 等. 新型四物方补血活性部位的初步筛选[J]. 解放军药学学报, 2011, 27(2):95-8. Wang D G, Ma Z C, Shao S, et al. Screening of hematopoietic constituents of New Siwu prescriptions[J]. Pharm J Chin PLA, 2011, 27(2):95-8. |
| [9] | 高 月, 马增春, 刘永学, 等.四物汤及其提取物对辐射致血虚证小鼠造血作用的研究[J].天津中医药, 2003, 20(6):47-51. Gao Y, Ma Z C, Liu Y X, et al. Effects of Si_Wu_Tang and its extracts on medullary hematopoiesis in mice of blood deficiency induced by 60Coγirradiation[J]. Tianjin J Tradit Chin Med, 2003, 20(6):47-51. |
| [10] | 梁 淼, 马增春, 高 月, 等.四物汤及其配伍对大鼠肝脏P450酶活性及mRNA表达的影响[J].中国中药杂志, 2013, 38(21):3720-5. Liang M, Ma Z C, Gao Y, et al. Effect of Siwu decoction and its combined administration on hepatic P450 enzymatic activity and mRNA expression in rats[J]. Chin J Chin Mat Med, 2013, 38(21):3720-5. |
| [11] | 李 晗, 王宇光, 马增春, 等.基于临床用量的参附注射液对大鼠肝脏主要药物代谢酶的影响[J]. 药学学报, 2013, 48(5):728-33. Li H, Wang Y G, Ma Z C, et al. Effect of Shenfu injection on CYP450s of rat liver[J]. Acta Pharm Sin, 2013, 48 (5): 728-33. |
| [12] | Zheng L, Lu Y, Cao X, et al. Evaluation of the impact of polygonum capitatum, a traditional Chinese herbal medicine, on rat hepatic cytochrome P450 enzymes by using a cocktail of probe drugs[J]. J Ethnopharmacol, 2014, 158:276-82. |
| [13] | Dinger J, Meyer M R, Maurer H H. Development and validation of a liquid-chromatography high-resolution tandem mass spectrometry approach for quantification of nine cytochrome P450 (CYP) model substrate metabolites in an in vitro CYP inhibition cocktail[J]. Anal Bioanal Chem, 2014, 406(18):4453-64. |