


2. 中国科学院天津工业生物技术研究所, 天津 300308
窦德泉(1962-),男,博士,副教授,研究方向:天然产物、植物资源开发,通讯作者,Tel:010-80799163,E-mail:doudequan@126.com
2. Tianjin Institute of Industrial Biotechnology, Chinese Academy of Sciences, Tianjin 300308, China
肺癌作为高发病率、高死亡率的恶性肿瘤,对人们生命健康构成巨大威胁。天然植物是药物开发的重要来源,植物代谢产物具有天然的抗癌、抑癌效果,从植物代谢产物中筛选和发掘新的化合物是开发低毒高效抗癌药物的重要途径。
罗汉果(Siraitia grosvenorii)为卫生部首批公布的“药食两用”中药材,《中国药典》记载罗汉果具有清热润肺功效。罗汉果为葫芦科植物,主要种植于我国广西地区[1]。文献报道,甜苷是罗汉果中的主要活性成分之一,研究发现罗汉果甜苷具有止咳、抗氧化、降糖、祛痰等作用[2, 3, 4, 5] ,说明罗汉果对肺部疾病具有明确的药用效果。
我们对罗汉果中单体成分进行分离和活性筛选,发现罗汉果醇具有诱导肺癌细胞A549凋亡的作用。目前,针对罗汉果醇活性的研究较少,其抑制癌症机制不详。实验首次探讨了罗汉果醇对肺癌细胞的作用效果和机制,为罗汉果的“润肺”功效提供了新线索,同时为罗汉果的药物开发提供了参考和依据。
1 材料与方法 1.1 试剂罗汉果干果购自北京同仁堂药店。常规化学试剂购自中国国药公司。Annexin V-FITC/PI双染试剂盒(BD公司);p21、Bcl-2、β-actin蛋白抗体购自Sigma公司。XAD-16树脂购自Rohm & Haas公司;Diaion PA树脂购自三菱公司。人肺癌细胞株A549购于上海生命科学研究院细胞资源中心,细胞接种于含10%小牛血清的RPMI 1640(Gibco公司)完全培养基中,在37 ℃、5% CO2饱和湿度培养箱中培养。
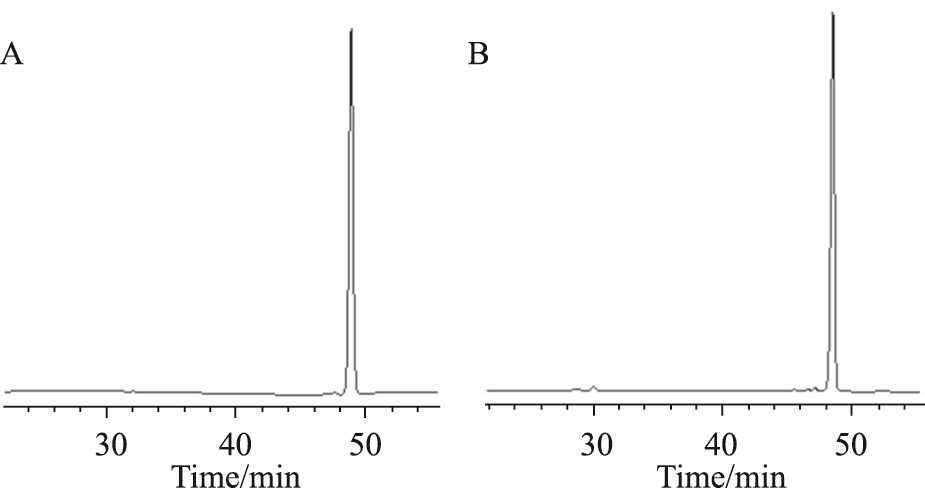
1.2 罗汉果醇的制备罗汉果醇的制备方法如下:① 将罗汉果粉碎,按罗汉果与水质量比为1 ∶ 6~8的比例加入水,在80~95℃条件下提取2次,每次2 h,合并提取液;② 向提取液中加入絮凝剂,除去提取液中的鞣质和可溶性蛋白,得到澄清的水溶液;③ 将所述水溶液采用XAD-16树脂进行吸附,用30%~50%乙醇进行洗脱,得到富集罗汉果甜苷的水-乙醇混合溶液;④ 将所述混合溶液减压浓缩,并回收乙醇,浓缩至浸膏状,向浸膏中加入4~5倍质量的去离子水,稀释浸膏,得到粗品甜苷的水溶液;⑤ 将粗品甜苷的水溶液采用Diaion PA树脂进行脱色处理,收集下柱液,得到富集液;⑥ 向所述富集液中加入盐酸至终浓度0.5 mol·L-1,在80~90℃,反应时间为6~8 h;⑦ 利用半制备液相色谱分离制得罗汉果醇。其HPLC图如Fig1所示(色谱条件:反相C18柱;紫外检测波长为214 nm;流动相为乙腈/水,0~20 min,25% 乙腈;20~40 min,25%~50% 乙腈;40~60 min,50%乙腈等度洗脱。流速为1.0 mL·min-1;柱温25℃),得到纯度>98%的罗汉果醇。
|
| Fig 1 HPLC of mogrol A: Reference substance; B: Sample |
胰蛋白酶消化对数生长期的肺癌细胞A549,调整细胞浓度至1×106·L-1,以每孔100 μL接种于96孔培养板中培养24 h。加入100 μL含不同浓度药物的培养液,使药物终浓度分别为0.1、1、10、100、200、250 μmol·L-1,培养24 h后,进行MTT比色分析: 向板孔中加入浓度为5 g·L-1 MTT液15 μL,37 ℃避光继续培养4 h,终止培养,小心吸去孔内培养基,每孔加DMSO 150 μL,摇床震荡10 min,置于酶标仪490 nm检测吸光度(A),按以下公式计算抑制率:细胞生长抑制率/%=(对照组A490-试验组A490)/对照组A490×100%。
1.4 细胞形态观察将经严格消毒的盖玻片置于6孔板中,选取对数生长期的肺癌细胞A549,将细胞调至浓度1×107·L-1,转移至6孔板培养,培养24 h后加入药物,使药物的终浓度分别为0、10、100 和250 μmol·L-1,培养24 h后,吸出废液,每孔加入0.5 mL固定液,固定25 min,PBS 洗2次,每次洗3 min,加入Hoechst 33258染液,室温避光染色20 min。使用荧光显微镜观察细胞形态变化。
1.5 细胞凋亡检测选取对数生长期的肺癌细胞A549,用药物培养24 h后,收集细胞,用 200 μL 冷PBS 洗涤细胞2次,收集细胞;加入50 μL的结合液(binding buffer)重悬细胞,加入2 μL的Annexin V-FITC 混匀,加入5 μL PI混匀,避光、室温作用10 min,进行流式细胞仪检测。
1.6 细胞周期检测选取对数生长期的肺癌细胞A549,分别用不同浓度罗汉果醇培养24 h后,用0.25%胰酶消化,收集用药组和对照组细胞,用 PBS洗涤细胞2次,70%冷乙醇(-20℃)固定,4℃过夜,离心去乙醇,用1 mL的PBS洗细胞1次,加入含 RNase A的PBS 500 μL,再加入碘化丙啶(PI)染色混匀(RNase A终浓度为50 mg·L-1,PI终浓度为25 mg·L-1),37℃避光孵育 30 min,用流式细胞仪检测。
1.7 p21、Bcl-2蛋白表达的分析肺癌细胞A549药物培养24 h。终止细胞培养后,吸除培养液,PBS(0.01 mol·L-1,pH 7.4)洗涤,加入含PMSF裂解液50 μL每孔,置冰浴裂解30 min,14 000 r·min-1离心10 min,获得总蛋白。BCA比色法测蛋白浓度,取50 μg总蛋白,经12%SDS聚丙烯酰胺凝胶电泳分离后,电转移至PVDF膜,5%脱脂牛奶(含0.1% Tween 20) 封闭1 h,加抗体p21、Bcl-2以及β-actin,一抗4℃孵育过夜(β-actin作为上样量对照);TBS-T洗膜3次,每次5 min;加辣根过氧化物酶(HRP)标记的二抗,室温孵育1 h,用漂洗液(TBS-T)洗膜3次,每次10 min,加入ECL避光孵育5 min,荧光影像分析仪显影、扫描、分析。
1.8 统计学分析SPSS 11.0统计软件进行统计分析,数据用x±s表示。采用t检验。
2 结果 2.1 罗汉果醇对肺癌细胞增殖的抑制作用MTT实验结果如Fig2所示,罗汉果醇具有抑制肺癌细胞A549增殖的作用,随着药物浓度的增加,其抑制率也随之增加(P<0.05),显示罗汉果醇对A549细胞具有抑制作用。

|
| Fig 2 Inhibitory effects of mogrol on proliferation of A549 cells with different doses |
荧光染色结果如Fig3所示,对照组细胞核完整,着色均匀,荧光成弥散状,未出现细胞凋亡现象;药物组中,随药物浓度的升高,细胞染色质呈颗粒荧光状,细胞出现皱缩,细胞核发生裂解,出现细胞凋亡的典型特征,说明罗汉果醇具有诱导肺癌细胞凋亡的作用。

|
| Fig 3 Fluorescence photomicrograph of A549 cells stained with Hoechst 33258 (×400) A:Control;B:Mogrol 10 μmol·L-1;C:Mogrol 100 μmol·L-1;D:Mogrol 250 μmol·L-1 |
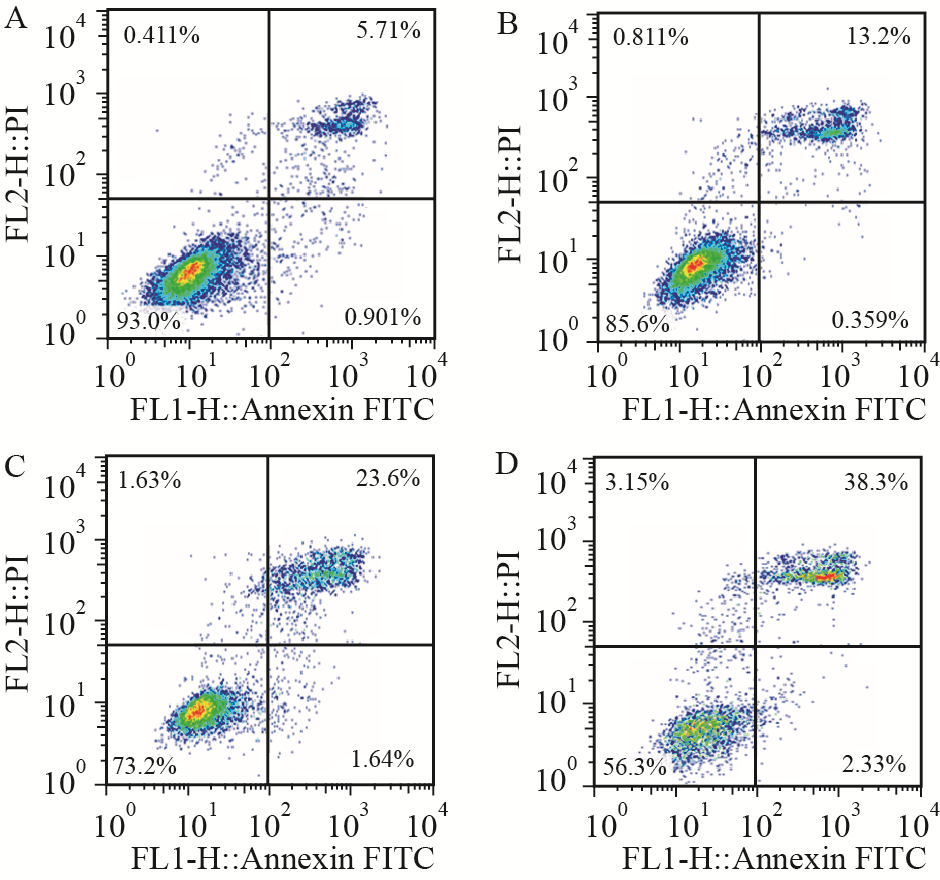
流式细胞术检测细胞凋亡结果表明,罗汉果醇可诱发肺癌细胞A549凋亡,随着罗汉果醇浓度的升高,凋亡细胞比例逐步增加(Fig4),与“2.2”结果一致,进一步说明罗汉果具有诱导肺癌细胞凋亡的作用。
|
| Fig 4 Effect of mogrol on apoptosis of A549 cells A:Control;B:Mogrol 10 μmol·L-1;C:Mogrol 100 μmol·L-1;D:Mogrol 250 μmol·L-1 |
诱发细胞周期阻滞是药物抑制癌细胞增殖的重要途径。如Fig5所示,经罗汉果醇处理后,A549细胞细胞周期分布发生明显变化,随着罗汉果醇浓度的增加,处于G0/G1期细胞的比例逐渐升高,S期、G2期细胞数量则与药物浓度呈负相关,说明罗汉果醇能阻断A549细胞周期进程,诱导A549细胞G0/G1期阻滞。

|
| Fig 5 Effect of mogrol on cell-cycle distribution in A549 cells A:Control;B:Mogrol 10 μmol·L-1;C:Mogrol 100 μmol·L-1;D:Mogrol 250 μmol·L-1 |
Bcl-2为抗凋亡蛋白,能够抑制细胞的程序性凋亡。如Fig6B所示,经过罗汉果醇处理的A549细胞,其Bcl-2蛋白的表达明显下降,Bcl-2蛋白的表达量与罗汉果醇剂量呈现负相关,这也是罗汉果醇促进癌细胞凋亡的重要原因。p21作为重要的细胞周期调控蛋白,对细胞周期的进程发挥重要作用,过量的p21表达能干预细胞周期由G1期向S期发展进程。蛋白免疫实验表明,药物能上调p21蛋白的表达(Fig6A),而p21的过表达可诱发细胞阻滞于G0/G1期,与细胞周期检测的结果一致。

|
| Fig 6 Effects of mogrol on expression of p21 and Bcl-2 in A549 cells A: Effect of mogrol on p21 expression; B: Effect of mogrol on Bcl-2 expression.**P<0.01 vs control |
罗汉果收录于我国卫生部发布的“药食同源”药物名单之中。此外,罗汉果提取物通过了美国FDA认证,从自身的药用价值和安全性而言,罗汉果提取物具有被开发成为低副作用药物的潜力。
本研究从罗汉果中分离得到罗汉果醇单体,MTT法检测显示,罗汉果醇对A549细胞具有抑制作用。Hoechst 33258染色观察、Annexin V-FITC/PI流式分析证实了罗汉果醇具有促进肺癌细胞A549凋亡的作用。流式细胞检测同时发现,罗汉果醇具有诱发细胞周期阻滞的效果,经药物处理,A549细胞周期分布发生改变,G1期细胞比例升高,S期和G2期细胞比例降低,药物诱导细胞发生G0/G1期阻滞。从以上结果分析,罗汉果醇可能通过促进细胞凋亡、诱导细胞周期阻滞实现对肿瘤细胞生长的抑制作用。
针对罗汉果醇诱导细胞凋亡、细胞周期阻滞的现象,本研究对A549中周期蛋白、抗凋亡蛋白的表达情况进行了检测。文献报道,周期蛋白p21在细胞由G1期向S期转化中发挥关键作用[6, 7],p21的上调可阻断细胞周期进程[7, 8]。Western blot结果显示,药物上调了A549细胞中p21蛋白的表达,药物可能通过上调p21从而导致细胞发生G1期阻滞。Bcl-2蛋白具有抑制细胞凋亡的作用[9, 10, 11],罗汉果醇能明显下调A549细胞中Bcl-2蛋白的表达(P<0.01),通过下调细胞中抗凋亡蛋白Bcl-2的表达,从而促进了A549的凋亡。本研究表明,罗汉果提取物具有抑制肺癌细胞增殖的作用,其分子机制还有待进一步研究分析。
| [1] | 李 俊, 黄锡山, 张艳军, 等. 罗汉果化学成分的研究[J]. 中国中药杂志, 2007, 32(6): 548-9. Li J, Huang X S, Zhang Y J, et al. Chemical constituents of Siraitia grosvenorii (Swingle) C. Jeffrey[J]. Chin J Chin Mater Med, 2007, 32(6): 548-9. |
| [2] | 王 霆, 黄志江. 罗汉果甜苷的生物活性研究[J]. 中草药, 1999, 30(12): 914-6. Wang T, Huang Z J. Studies on the pharmacological profile of mogrosides[J]. Chin Tradit Herbal Drugs, 1999, 30(12): 914-6. |
| [3] | 戚向阳, 陈维军, 张俐勤, 等. 罗汉果皂甙清除自由基及抗脂质过氧化作用的研究[J]. 中国农业科学, 2006, 39(2): 382-8. Qi X Y, Chen W J, Zhang L Q, et al. Study on the inhibitory effects of natural sweetner mogrosides on radical and lipid peroxidation[J]. Sci Agric Sin, 2006, 39(2): 382-8. |
| [4] | 张俐勤, 戚向阳, 陈维军, 等. 罗汉果皂苷提取物对糖尿病小鼠血糖, 血脂及抗氧化作用的影响[J]. 中国药理学通报, 2006, 22(2): 237-40. Zhang L Q, Qi X Y, Chen W J, et al. Effect of mogroside extracts on blood glucose, blood lipid and antioxidation of hyperglycemic mice induced by alloxan[J]. Chin Pharmacol Bull, 2006, 22(2): 237-40. |
| [5] | 王 勤. 罗汉果化学成分及药理作用研究进展[J]. 中药材, 2001, 24(3): 215-6. Wang Q. Chemical constituents and pharmacological research of Siraitia grosvenorii[J]. Chin Med Mat, 2001, 24(3): 215-6. |
| [6] | Brugarolas J, Chandrasekaran C, Gordon J I, et al. Radiation-induced cell cycle arrest compromised by p21 deficiency[J]. Nature, 1995, 377(6549): 552-7. |
| [7] | Lepley D M, Pelling J C. Induction of p21/WAF1 and G1 cell-cycle arrest by the chemopreventive agent apigenin[J]. Mol Carcinogen, 1997, 19(2): 74-82. |
| [8] | Schreiber M, Muller W J, Singh G, et al. Comparison of the effectiveness of adenovirus vectors expressing cyclin kinase inhibitors p16INK4A, p18INK4C, p19INK4D, p21 (WAF1/CIP1) and p27KIP1 in inducing cell cycle arrest, apoptosis and inhibition of tumorigenicity[J]. Oncogene, 1999, 18(9): 1663-76. |
| [9] | Boise L H, González-García M, Postema C E, et al. Bcl-x, a bcl-2-related gene that functions as a dominant regulator of apoptotic cell death[J]. Cell, 1993, 74(4): 597-608. |
| [10] | Kroemer G. The proto-oncogene Bcl-2 and its role in regulating apoptosis[J]. Nat Med, 1997, 3(6): 614-20. |
| [11] | 史婷婷, 白建平, 梁月琴, 等. 芹菜素对大鼠缺血/再灌注心肌细胞凋亡及相关蛋白 Bcl-2, Bax, Caspase-3 表达的影响[J]. 中国药理学通报, 2011, 27(5): 666-71. Shi T T, Bai J P, Liang Y Q, et al. Effect of apigenin on the cardiomyocyte apoptosis in rats with ischemia and reperfusion and the expression of Bcl-2, Bax, Caspase-3[J]. Chin Pharmacol Bull, 2011, 27(5): 666-71. |

