


右心室重构及右心衰竭是肺动脉高压患者死亡的主要原因之一[1],逆转右心室重构,寻找有效的治疗药物具有重要意义。目前认为,导致右心室重构的原因主要有心肌细胞肥大、凋亡、炎性因子浸润及过氧化物酶体增殖物激活受体(peroxisome proliferator activated receptor,PPAR)被抑制等[2]。其中,PPARs表达的降低可导致心肌脂质和能量代谢紊乱,炎性因子生成增多,促进心室重构的发生[3]。野百合碱(monocrotaline,MCT)所致肺动脉高压继发的右心室重构模型是目前常用的右心室重构模型[4]。
蛇床子素(osthole,Ost)又名甲氧基欧芩酚、欧芹酚甲醚,是从伞形科蛇床的干燥成熟果实中提取的一种香豆素类化合物,具有抗炎、抗心律失常、抗肿瘤、抗骨质疏松症等作用[5]。已有研究表明,Ost在异丙肾上腺素所致的心肌纤维化病变中能上调PPARγ的表达[6]。因此,本研究采用MCT诱导的右心室重构模型,观察Ost对MCT诱导的右心室重构的作用,并探讨其可能的机制,为Ost的开发利用提供基础药理学依据。
1 材料与方法 1.1 药品、试剂及主要仪器Ost(纯度≥98%,南京泽朗医药科技有限公司);MCT(Sigma公司);PPARα、PPARγ兔抗大鼠抗体(美国Abcam公司);辣根过氧化物酶(HRP)标记的GAPDH抗体(上海康成生物工程有限公司);HRP标记的山羊抗兔IgG(英国CST公司);BCA蛋白浓度测定试剂盒、ECL+发光剂(江苏碧云天生物技术研究所);Leica光学显微镜及照相系统(德国Leica Microsystems Ltd);Mini-PROTEAN3电泳仪、Mini Trans-Blot转移系统、CCD成像系统(美国BIO-RAD公司)。
1.2 实验动物(200~220) g,♂,SD大鼠,清洁级,由第三军医大学大坪医院实验动物中心提供,许可证号:SCXK(渝)2012-0005。
1.3 主要溶液的配制 1.3.1 低剂量Ost的配制称取0.1 g Ost,滴0.25 mL吐温80助溶,加ddH2O溶至50 mL,混匀。
1.3.2 高剂量Ost的配制称取0.2 g Ost,滴0.25 mL吐温80助溶,加ddH2O溶至50 mL,混匀。
1.3.3 MCT的配制称取0.5 g MCT溶于10 mL 0.5 mol·L-1的HCl中,用0.5 mol·L-1的NaOH调pH至7.4,加生理盐水定容至50 mL。
1.4 分组、造模及给药所有大鼠适应性饲养1周后,随机选取10只,经颈背部一次性皮下注射生理盐水5 mL·kg-1作为正常对照组(Control),其余大鼠均经颈背部一次性皮下注射MCT(5 mL·kg-1)建立右心室重构模型,造模后将大鼠随机分为3组。分组情况如下:模型组(Model,n=15),Ost低、高剂量组(Ost-L、Ost-H,10、20 mg·kg-1,n=10)。其中,Ost-L、Ost-H剂量组于造模后d 1开始给药(5 mL·kg-1,ig,qd),Model组和Control组给予加有等量吐温80的ddH2O(5 mL·kg-1,ig,qd),至28 d。
1.5 右心室肥大指数的测定给药28 d后,称大鼠体重,予质量浓度为70 g·L-1的水合氯醛腹腔注射麻醉成功后打开胸腔,取出心脏,置于预冷的生理盐水中洗净,分离右心室游离壁,滤纸吸干表面水分,分别称取右心室重量(right ventricle,RV)和左心室加室间隔重量(left ventricle plus septum,LV+SEP),计算右心室肥大指数[RV hypertrophy index,RVHI=RV/(LV+SEP)]。
1.6 右心室形态学观察取约3 mm心肌组织,置于体积分数为0.04的甲醛溶液中,固定48 h后脱水、包埋、行HE染色,光镜下观察右心室形态学变化。
1.7 右心室PPARα和PPARγ蛋白的检测取各组大鼠右心组织约100 mg,剪碎后置于1 mL含有蛋白酶抑制剂的蛋白裂解液中,冰上匀浆提取总蛋白,BCA法对蛋白定量。SDS-PAGE凝胶电泳分离后,采用恒流220 mA分别湿转110、120和72 min,将PPARα、PPARγ、GAPDH蛋白转至PVDF膜上,用质量浓度为50 g·L-1的脱脂奶粉室温封闭2 h,分别放入相应的一抗稀释液中,PPARα(1 ∶ 1 000),PPARγ(1 ∶ 800),GAPDH(1 ∶ 5 000),4℃过夜,PPARα和PPARγ室温孵育二抗(1 ∶ 2 000)1 h,暗室曝光,采用Quantity One定量分析软件进行灰度分析。
1.8 统计学分析实验数据按完全随机对照要求收集整理,以 ± s 表示,采用SPSS 16.0软件进行ONE-WAY ANOVA处理,方差齐用LSD法,方差不齐用Dunnett,T2法。
± s 表示,采用SPSS 16.0软件进行ONE-WAY ANOVA处理,方差齐用LSD法,方差不齐用Dunnett,T2法。
与正常对照组相比,模型组大鼠RVHI明显升高(P<0.05)。与模型组相比,Ost-L、Ost-H剂量组大鼠RVHI降低(P<0.05)。见Tab1。
 ± s ,n=6~8)
± s ,n=6~8)
| Group | Dose/mg·kg -1 | RV/g | LV+SEP/g | RVHI |
| #P < 0.05 vs control;*P < 0.05 vs model | ||||
| Control | - | 0.138±0.025 | 0.547±0.103 | 0.254±0.022 |
| Model | - | 0.289±0.053 | 0.596±0.072 | 0.484±0.111 # |
| Ost-L | 10 | 0.204±0.032 | 0.518±0.036 | 0.390±0.057 * |
| Ost-H | 20 | 0.183±0.025 | 0.520±0.027 | 0.352±0.061 * |
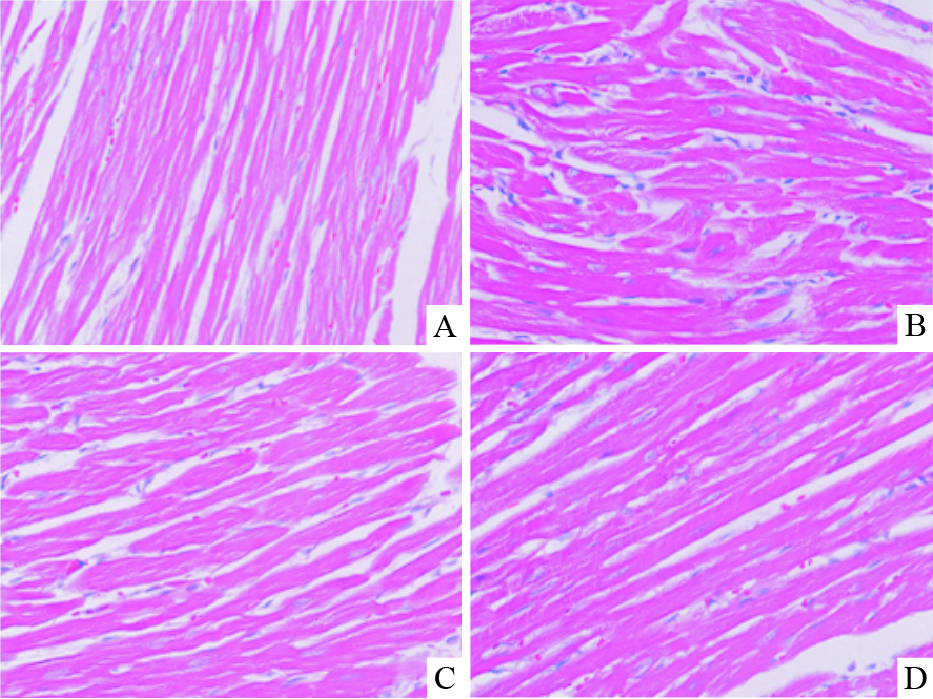
与正常对照组相比,模型组大鼠右心室心肌细胞排列紊乱,心肌细胞肥大畸形,胞质明显肿胀。与模型组相比,Ost-L、Ost-H剂量组大鼠心肌细胞排列较为整齐,胞质无明显肿胀。见Fig1。
|
| Fig 1 Effect of Ost on right ventricular morphology induced by MCT in rats (×400) A:Control;B:Model;C:Ost-L;D:Ost-H |
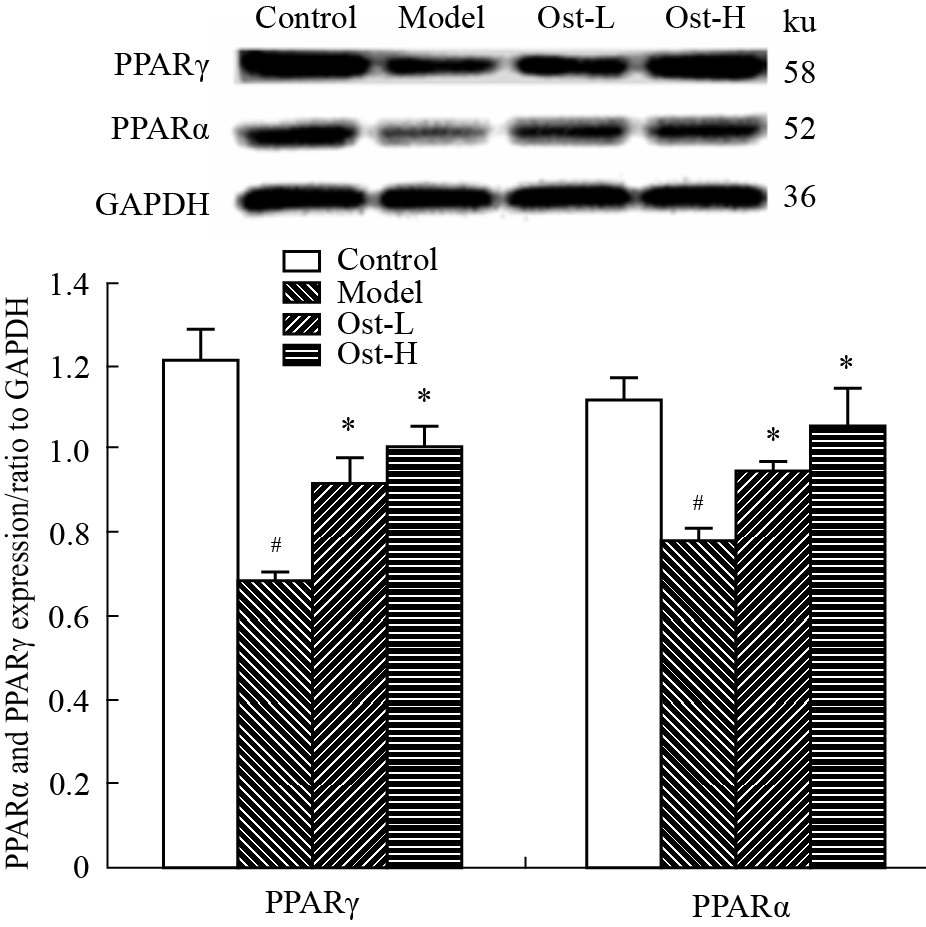
与正常对照组相比,模型组大鼠右心室PPARα、PPARγ蛋白的表达明显下调(P<0.05)。与模型组相比,Ost-L、Ost-H剂量组右心室PPARα、PPARγ蛋白的表达均上调(P<0.05)。见Fig2。
|
| Fig 2 Effect of Ost on expression of PPARα and PPARγ protein in right ventricle of rats induced by MCT (n=3) #P < 0.05 vs control;*P < 0.05 vs model |
MCT诱导的右心室重构模型是目前公认的制备右心室重构的模型之一[4]。MCT经肝代谢后生成野百合碱吡咯,可诱发右心室重构。该模型具有操作简单、模型稳定等优点。本研究结果显示,与正常对照组相比,模型组大鼠右心室肥大指数(RVHI)明显升高;右心室心肌细胞排列紊乱,心肌细胞肥大畸形,胞质明显肿胀,提示造模成功。与模型组相比,Ost-L、Ost-H剂量组大鼠RVHI降低;右心室心肌细胞排列较为整齐,胞质无明显肿胀,提示Ost具有改善MCT所致大鼠右心室重构的作用。
过氧化物酶体增殖物激活受体(PPARs)是一类由配体激活的核转录因子超家族成员,有PPARα、 PPARβ和PPARγ 3种亚型[7]。其中,PPARα主要调节心肌脂肪和能量代谢,通过调控基因编码线粒体脂肪酸β-氧化途径,为心脏提供ATP,起到保护心肌的作用[8]。PPARγ是一种重要的细胞分化转录因子,被其配体激活后,可与维甲酸x受体结合形成异源二聚体,转移到细胞核,与特定的应答元件结合,启动目标基因表达,主要控制糖脂代谢,参与细胞凋亡、炎症等病理过程,发挥抗炎作用[9, 10]。因 此,通过上调PPARα和PPARγ的表达可能对心室重构具有保护作用。本研究结果显示,与正常对照组相比,模型组大鼠右心室PPARα和PPARγ蛋白的表达明显下调,说明在MCT诱导的右心室重构中PPARα和PPARγ被抑制。与模型组相比,Ost-L、Ost-H剂量组大鼠右心室PPARα和PPARγ蛋白的表达明显上调,提示Ost可能通过上调PPARα和PPARγ的表达减轻MCT所致大鼠右心室重构的发生。
综上所述,Ost具有改善MCT所致大鼠右心室重构的作用,其机制可能与其上调PPARα和PPARγ的表达有关。为进一步确证该机制,笔者后期将通过采用体外心肌细胞肥大模型,配合使用PPARα和PPARγ的特异性激动剂、阻滞剂等工具药干预,继续探讨其机制。
(致谢:本文所有实验均在遵义医学院基础药理省部共建教育部重点实验室完成。)
| [1] | 杨丹莉,李晓辉,张海港,等. G蛋白抑制肽抑制野百合碱所诱导的右室重构[J].中国药理学通报, 2008, 24(12):1646-9.Yang D L, Li X H, Zhang H G, et al.GCIP-27 inhibits the right ventricle remodeling in monocrotaline-treated rats[J]. Chin Pharmacol Bull, 2008, 24(12):1646-9. |
| [2] | 魏大闯,肖学钧.肺动脉高压与右心室重构的关系[J].心血管病学进展, 2013, 34(5):648-51. Wei D C, Xiao X J. The relationship between pulmonary arterial hypertension and right ventricular remodeling[J]. Adv Cardiovasc Dis, 2013, 34(5):648-51. |
| [3] | Usuda D, Kanda T. Peroxisome proliferator-activated receptors for hypertension[J]. World J Cardiol, 2014, 6(8):744-54. |
| [4] | Campian M E,Hardziyenka M, Michel M C,Tan H L. How valid are animal models to evaluate treatments for pulmonary hypertension[J]? Naunyn Schmiedebergs Arch Pharmacol, 2006, 373(6):391-400. |
| [5] | 刘建新,连其深. 蛇床子素的药理学研究进展[J].时珍国医国药, 2005, 16(12):1235-7.Liu J X, Lian Q S. Research advances in pharmacological function of osthole[J]. Lishizhen Med Mat Med Res, 2005, 16(12):1235-7. |
| [6] | Chen R, Xue J, Xie M L. Reduction of isoprenaline-induced myocardial TGF-β1 expression and fibrosis in osthole-treated mice[J]. Toxicol Appl Pharmacol, 2011, 256(2):168-73. |
| [7] | 马晶晶,章 涛. PPARγ功能与疾病关系研究进展[J].中国药理学通报, 2012, 28(5):601-4.Ma J J, Zhang T. Function of PPARγ and its relationship with diseases:a present review[J]. Chin Pharmacol Bull, 2012, 28(5):601-4. |
| [8] | Kim T, Yang Q L. Peroxisome-proliferator-activated receptors regulate redox signaling in the cardiovascular system[J]. World J Cardiol, 2013, 5(6):164-74. |
| [9] | Son N H, Park T S, Yamashita H, et al. Cardiomyocyte expression of PPAR gamma leads to cardiac dysfunction in mice[J]. J Clin Invest, 2007, 117(10):2791-801. |
| [10] | Hong K M, Belperio J A, Keane M P, et al. Differentiation of human circulating fibrocytes as mediated by transforming growth factor-beta and peroxisome proliferator-activated receptor gamma[J].J Biol Chem, 2007, 282 (31):22910-20. |

