


杨雷(1977-),男,博士,副教授,研究方向:中西医结合抗心血管疾病发病机制,Tel:0377-62071309,E-mail:yanglei200609@126.com
毛秉豫(1958-),男,博士,教授,研究方向:心血管疾病的气血并治方药,Tel:0377-62071305,E-mail:maobingyu2005@126.com
蛋白激酶D(protein kinase D,PKD)属于进化上高度保守的钙/钙调蛋白依赖性的丝氨酸/苏氨酸激酶家族,其重要家族成员之一PKD1参与很多基础的生物进程调节,包括信号转导、细胞的增殖和分化、跨膜转运、分泌、免疫调节、心肌细胞的收缩、血管新生、肿瘤等[1]。特别是PKD1在肿瘤形成的进程中倍受关注,PKD1信号级联反应和胰腺癌、肝癌、胃癌、肠癌、乳腺癌、前列腺癌等的发生发展密切相关[2],其原因在于PKD1既可以直接促进癌细胞的增殖和分化,又促进癌细胞生长区域血管的新生。鉴于此,抗PKD1抑制肿瘤的方法在胰腺癌、乳腺癌等治疗中已经被提出,如特异的PKD1抑制剂CRT0066101可以明显抑制小鼠胰腺癌肿瘤细胞的增生[2]。
近年来,在缺血性心血管系统疾病的治疗中,内皮祖细胞(endothelial progenitor cells,EPCs)疗法是潜在的最有希望的治疗策略之一,其可以被诱导分化为心肌细胞和血管平滑肌细胞[3],实现缺血损伤心肌组织真正意义上的血管新生。PKD1既然可以促进肿瘤细胞的增殖和肿瘤组织中血管的新生,那么是否也可能有促进EPCs黏附、迁移、增殖,诱导EPCs分化为血管的作用?本研究拟对此进行探讨并分析其可能作用机制,为以“PKD1”这一潜在可能靶点治疗缺血性心血管疾病提供新的思路。
1 材料与方法 1.1 实验动物SD大鼠购自河南省实验动物中心,♂,清洁级,8周龄,重约200~240 g,动物生产许可证号:SCXK(豫)2010-0002,动物质量合格证号:1000142。
1.2 药物与试剂PKD1购自美国Pierce公司(生产批号为OSP00005W),PKD1特异阻断剂CID755673购自美国MedChemExpress公司(生产批号为2011756),DNA酶 I、Dulbecco′s PBS、FBS、胶原酶I、BrdU、BrdU鼠单克隆抗体购自上海宝曼生物科技有限公司(生产批号分别为LS002004、28374、SH30077、LS004194、83224、MMS-139S-250);EBM-2培养基购自北京达科为生物技术有限公司(生产批号为CC-3156);CD133、CD34、eNOS、VEGFR-2抗体购自天津恒业生物科技有限公司(生产批号为EL910835、EL162014、EL163112和EL171852);羊抗兔IgG、DAB显色液购自武汉博士德生物工程有限公司(生产批号为TC1378、DD1660);FN、FITC和DAPI购自北京碧橙蓝生物科技有限责任公司(生产批号为PA127507、PA185438和62247);其它试剂为国产分析纯。
1.3 主要仪器A2-1389型生物安全柜(美国Thermo Scientific公司);164-5052型PowerPac HC 电泳仪及FACSCanto II型流式细胞仪(美国BIO-RAD公司);Bullet Blender Storm组织细胞破碎仪(美国Next Advance公司);Nikon Tis型荧光显微镜及Nikon NIS-Elements Software BR分析系统(日本尼康公司)。
2 方法 2.1 EPCs的体外分离、培养和鉴定取体重为200~240 g的健康♂SD大鼠,颈椎脱臼处死后,75%乙醇浸泡10 min,无菌操作环境下取出胫腓骨,用含肝素及DNA酶 I的Dulbecco′s PBS反复冲洗骨髓,收集骨髓液,小心置入等量的淋巴细胞分离液之中,1 700 r·min-1离心30 min,无菌毛细吸管吸取分离液中间白膜层,5×PBS重悬细胞,离心后再用含2% FBS的EBM-2培养基重悬,按每平方厘米105个标准接种于培养板中,24 h后将未贴壁的细胞悬液转入预先用50 mg·L-1 FN包被的6孔细胞培养板中培养,3 d后换第1次液,之后每隔3 d换液1次,倒置显微镜下进行细胞形态学观察,7-10 d后,待细胞融合80%后,采用胶原酶Ⅰ消化后传代培养。对培养的内皮细胞观察其生长状态,分别在4、7、10、14 d照相并记录。对新分离的骨髓单核细胞进行滴片,于d 4、7、10、14取生长良好的原代细胞,重悬于PBS中,分别与EPCs细胞表面标记物CD133、CD34、VEGFR-2结合,再用FITC染色,DAPI 复染,检测上述标记物阳性表达的细胞。
2.2 PKD1对EPCs黏附的影响提前用50 mg·L-1 FN包被细胞培养板,每孔再接种5×104个EPCs,培养过夜,形成单皮层后转入无血清培养基培养5 h,用钙黄绿素标记EPCs后的制备单细胞悬液,37℃下孵育30 min。实验分5个组:A组,空白对照组;B组,25 μg·L-1 PKD1干预组;C组,50 μg·L-1 PKD1干预组;D组,100 μg·L-1 PKD1干预组;E组,PKD1(100 μg·L-1)+ CID755673 (100 μg·L-1) 干预组,以下简称CID755673干预组。每组设置6个复孔,实验重复3次。各组干预后,在37℃下、5% CO2孵箱中孵育30 min,用PBS轻轻冲洗细胞,去除未黏附细胞,倒置显微镜40×下,随机取6个视野拍照,计数黏附细胞个数,取平均值。
2.3 PKD1对EPCs迁移的影响用8 μm孔径的24孔transwell进行迁移实验,先分别在细胞小室的上、下室加入50 mg·L-1 FN,再注入含2% FBS的EBM-2培养基。然后在上室按照每孔2×104个的密度接种EPCs,在下层加入A组:空白对照EBM-2;B-D组:PKD1(25、50、100 μg·L-1);E组:PKD1(100 μg·L-1)+CID755673 (100 μg·L-1),每组设置6个复孔,实验重复3次。培养24 h后,用棉签擦去上室内的细胞,2%多聚甲醛固定,Giemsa染色,40×下随机取6个视野,倒置显微镜下计数迁移过膜的细胞数量,取平均值。
2.4 PKD1对EPCs增殖的影响将EPCs用含2% FBS的EBM-2的基础培养基重悬,每孔104个加入96孔培养板中,待细胞贴壁后,更换无血清培养基培养,每孔加入终浓度为10 μmol·L-1的BrdU孵育。实验分组同“2.2”。分别在培养的24、48和72 h后,每孔加入100 μL的BrdU鼠单克隆抗体(1 ∶ 100)室温孵育1 h后,wash buffer冲洗2次,加入辣根过氧化物酶标记的羊抗小鼠IgG(1 ∶ 2 000稀释)孵育1 h后,wash buffer再次冲洗2次,加入100 μL TMB过氧化物酶底物室温避光孵育30 min,加入100μL终止液,酶联免疫检测仪450 nm波长处读取各孔吸光度值(A450),取其平均值。
2.5 PKD1对EPCs血管形成能力的影响将EPCs用含2%FBS的EBM-2的基础培养基重悬,每孔5×104个加入Matrigel-Matrix预处理的48孔培养板中,待细胞贴壁后,更换无血清培养基培养。实验分组同“2.2”。在培养的72 h后,40×倒置显微镜下观察管状结构数量,随机选择6个视野照相,取其平均值。
2.6 PKD1对EPCs中eNOS mRNA转录表达的影响将EPCs用含2%FBS的EBM-2的基础培养基重悬,每孔105个加入6孔培养板中,待细胞贴壁后,更换无血清培养基培养。实验分组同“2.2”。在培养24 h后,TRIzol法提取EPCs总RNA,根据GenBank序列,分别设计eNOS的上下游引物为5′-CTGCTGCCCCAGATATCTTC-3′ 和5′-CAGGTACTGCAGTCCCTCCT-3′,产物长度为230bp。每组细胞取2μg总RNA,根据试剂盒的说明书逆转录合成cDNA,再取2 μg逆转录产物进行普通PCR,94℃,1 min,95℃,30 s,54℃,1 min,72℃,1 min,30个循环,延伸2 min。取反应产物10 μg进行1.5%琼脂糖凝胶电泳,EB染色后AlphaView SA软件摄图,并分析eNOS与β-actin基因的灰度比值。
2.7 PKD1对EPCs中eNOS蛋白表达的影响细胞培养实验设计同“2.6”。应用Next Advance Bullet Blender Storm组织细胞破碎仪将EPCs打碎,匀浆,4℃下12 000×g离心2min,提取组织总蛋白后Bradford法测定蛋白浓度,取其中20 μg蛋白进行12%的SDS-聚丙烯酰胺凝胶电泳,转移至硝酸纤维素膜上,5%的脱脂奶粉封闭2 h后洗膜,标记1 ∶ 250稀释的eNOS一抗,4℃过夜,洗膜,与辣根过氧化物酶标记的羊抗小鼠IgG(1 ∶ 2 000稀释)孵育1 h后TBST洗膜,冲洗后暗室曝光显影。同时以β-actin蛋白表达水平作为内参对照。胶片经成像分析系统扫描,并应用AlphaView SA软件分析各样本与β-actin蛋白灰度的比值,记录蛋白相对含量。
2.8 统计学处理采用SPSS 16.0统计软件系统,计量资料以 ± s 表示,多组间均数比较比较用单因素方差分析,组间多重比较用SNK-q检验。
± s 表示,多组间均数比较比较用单因素方差分析,组间多重比较用SNK-q检验。
EPCs结合FITC后呈现绿色,DAPI复染后胞核呈蓝色。EPCs呈卵圆形、纺锤形或者不规则状,CD133、CD34或VEGFR-2表达阳性,见Fig1。

|
| Fig 1 Immunofluorescence detection of CD34 (A/D), VEGFR-2 (B/E) and CD133 (C/F) for EPCs (×200) Cells were counterstained with DAPI for nucleus (blue, D-F). |
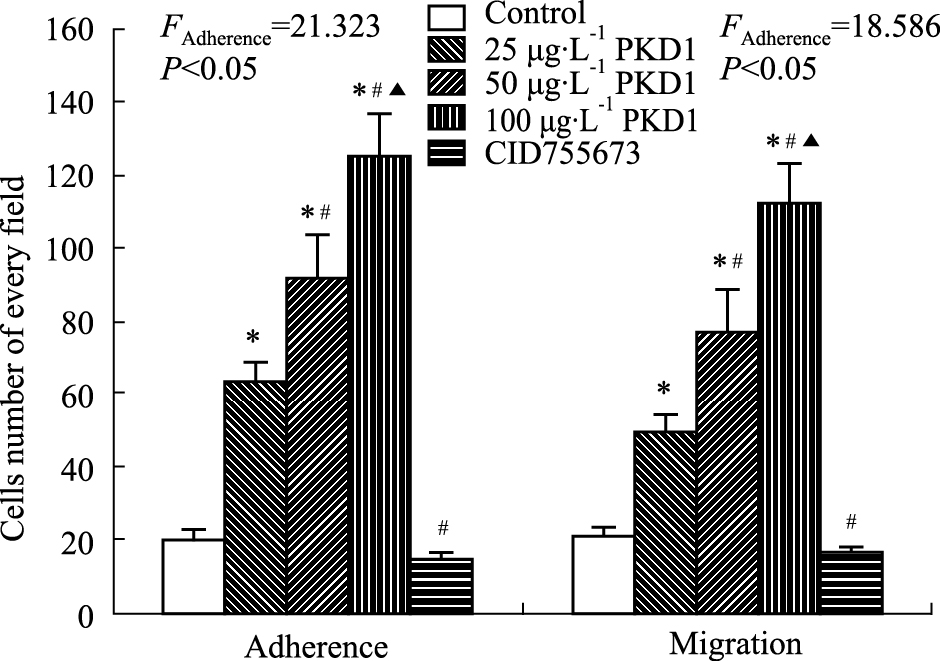
和对照组相比,PKD1各干预组促EPCs黏附、迁移的能力明显增强(P<0.05),且呈剂量依赖性(F黏附=21.323,F迁移=18.586,均P<0.05)。加入CID755673干预之后,EPCs的黏附、迁移的能力明显下降 (P<0.05)。见Fig2。
|
| Fig 2 Effect of PKD1 on migration and adherence in EPCs *P<0.05 vs control group; #P<0.05 vs 25 μg·L-1 PKD1 group; ▲P<0.05 vs 50 μg·L-1 PKD1 group. |
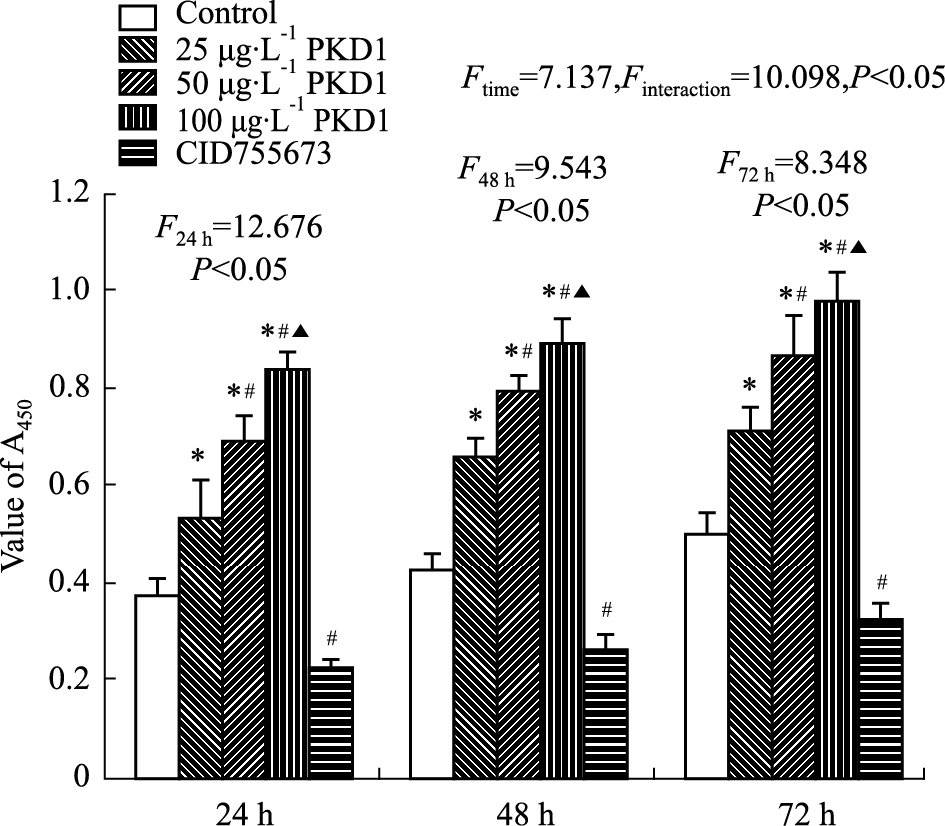
和对照组相比,24、48、72 h PKD1各剂量组促EPCs的增殖能力均明显升高(P<0.05),且随剂量增加促增殖能力呈上升趋势;加入CID755673干预之后,EPCs的增殖能力明显下降 (P<0.05)。24、48、72 h时间组组间相比,随时间推移,PKD1各剂量组促EPCs增殖能力均明显升高(F时间=7.137,P<0.05);且时间和剂量均明显影响EPCs增殖(F交互=10.098,P<0.05)。见Fig3。
|
| Fig 3 Effect of PKD1 on proliferation in EPCs *P<0.05 vs control group; #P<0.05 vs 25 μg·L-1 PKD1 group; ▲P<0.05 vs 50 μg·L-1 PKD1 group. |
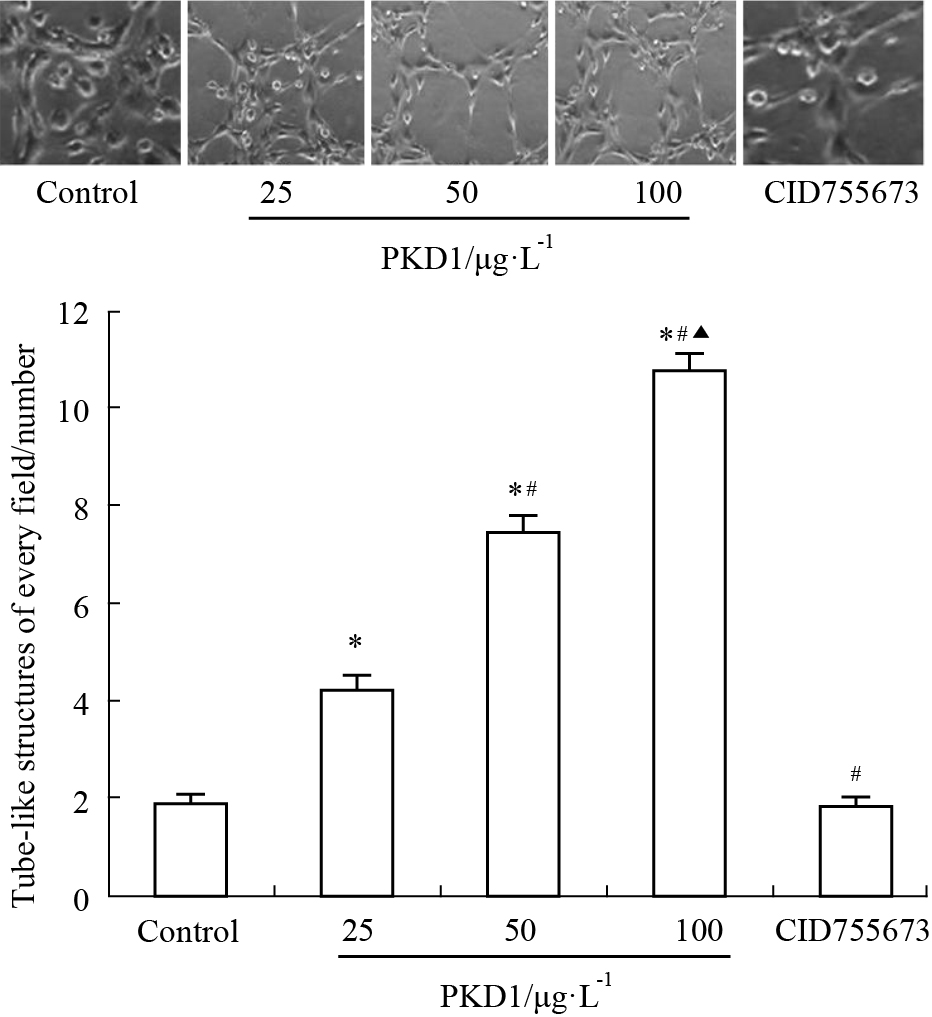
与对照组相比,PKD1各干预组EPCs管腔样结构的数目明显增加(P<0.05),且呈剂量依赖性增加趋势。加入CID755673干预之后,EPCs管腔样结构的数目明显减少(P<0.05),且管状结构结点模糊。见Fig4。
|
| Fig 4 Effect of PKD1 on numbers of tube-like structures in EPCs F=78.965, *P<0.05 vs control group; #P<0.05 vs 25 μg·L-1 PKD1 group; ▲P<0.05 vs 50 μg·L-1 PKD1 group. |
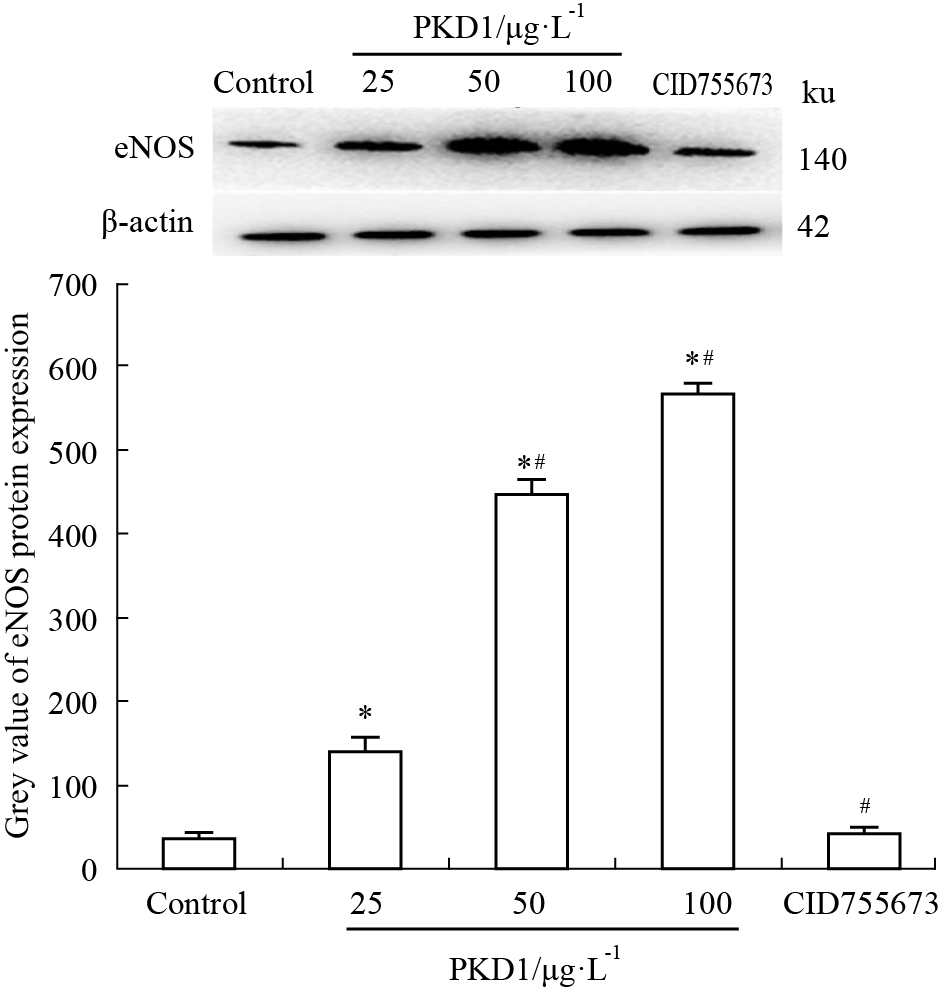
和对照组相比,PKD1各干预组EPCs中eNOS mRNA和蛋白表达水平均明显升高(P<0.05),和25 μg·L-1 PKD1干预组相比,50及100 μg·L-1 PKD1干预组EPCs中eNOS mRNA和蛋白表达水平均明显升高(P<0.05),但后两组组间比较无差异;加入CID755673干预之后,EPCs中eNOS mRNA和蛋白表达水平均明显降低(P<0.05)。见Fig5-6。

|
| Fig.5 Effect of PKD1 on mRNA expression of eNOS in EPCs *P < 0.05 vs control group; #P < 0.05 vs 25 μg·L-1 PKD1 group. |
|
| Fig.6 Effect of PKD1 on protein expression of eNOS in EPCs *P<0.05 vs control group; #P<0.05 vs 25 μg·L-1 PKD1 group. |
本研究结果从PKD1激活和阻断两方面均证实PKD1明显促进EPCs的黏附和迁移,且呈剂量依赖性。这可能与PKD1对细胞间黏附分子l(intercellular adhesion molecule 1,ICAM-1)和血管细胞黏附分子l(vascular cell adhesion molecule l,VCAM-1)的活化作用密切相关。ICAM-1和VCAM-1介导EPCs之间的黏附、趋化因子诱导的EPCs跨内皮的迁移,而黏附和迁移是归巢过程中的重要环节[3]。本研究结果同时证实,在24、48、72 h不同时间段,PKD1各剂量干预组均明显增加EPCs的增殖,且呈时间依赖性,时间和剂量方差交互分析证实两者均明显影 响EPCs的增殖。这表明,PKD1可以明显促进EPCs的增殖。进一步的研究结果表明,PKD1呈剂量依赖性提升EPCs的管腔样结构数量。之前的研 究证实EPCs向缺血组织归巢,分化为成熟的内皮细胞,并通过旁分泌的方式调控现存的内皮细胞,以一种和胚胎时期血管形成相似的方式分化成为血管内皮细胞,进而形成血管[4]。同时,PKD1还可以诱导生成多种生长因子,联合发挥作用,参与血管新生和组织再生的整个修复进程[5]。这和我们的研究结果高度吻合。这表明,PKD1可以通过调控EPCs的黏附、迁移、增殖以及血管形成能力,促进受损组织区域内微血管的新生,而在缺血性心肌组织损伤修复的进程中发挥着重要的作用。
本研究还分别从PKD1激活和阻断两个截然相反的角度证实PKD1可以明显上调EPCs中eNOS的mRNA和蛋白表达水平。eNOS和其产物NO在血管系统的稳态维持中扮演着重要的角色,不仅调控着血压水平、血管的紧张度,而且发挥着重要的抗炎、抗氧化、抗血栓形成效应[6]。eNOS的激活是通过1179的丝氨酸激活位点,Akt、CaMKII、AMPK、PKD1均可以通过这一位点而激活eNOS[7, 8]。之前的文献报道,在VEGF介导的eNOS激活的进程中,PKD1是必不可少的[9]。也有学者认为,eNOS属于新发现的PKD的底物,因为eNOS被各种氨基酸识别结合激活的位点恰恰均存在于现有报道的PKD底物之内,采用PKD1阻断剂或者基因沉默PKD1均可以以一种依赖eNOS的方式阻断动脉内皮细胞的迁移,减缓受损伤口的愈合[10]。和上述结果相似,我们的研究也表明,PKD1可能以一种依赖eNOS的方式促进EPCs的黏附、迁移、增殖和血管形成。
当前在缺血性心脏病的临床治疗进程中,由于心肌细胞分化和增殖能力极差,心肌组织缺血受损后通常以纤维组织进行疤痕修补,这对修复后的心脏功能产生较大的损害作用[11]。本研究结果对于后续的骨髓源性EPCs移植至心肌梗死大鼠动物模型或者心肌梗死患者受损的心肌组织中,促缺血区域局部血管的新生,以及干预PKD1诱导EPCs分化为内皮细胞,促内皮细胞迁移,减轻或者逆转损伤心肌组织纤维化修复进程,促损伤心肌组织心功能状态的恢复有积极的参考意义。
(致谢:本文的实验在南阳理工学院医学实验中心完成,实验由杨雷博士和毛秉豫教授共同设计,并进行经费资助。刘暖为实验的主要完成人,徐国昌主要负责统计学工作,叶松山、张培华、张瓅芳协助进行分子生物学实验。对以上同志的工作特别表示感谢!)
| [1] | 杨 雷,毛秉豫,徐国昌,等. 黄芪提取物对大鼠心肌梗死后心肌组织PKD1蛋白表达的影响[J].中国药理学通报,2013, 29(4): 512-9.Yang L, Mao B Y, Xu G C, et al. Effect of astragalus extract on the levels of PKD1 protein in rats with myocardial infarction[J]. Chin Pharmacol Bull, 2013, 29(4): 512-9. |
| [2] | Wille C,Seufferlein T,Eiseler T. Protein kinase D family kinases: roads start to segregate[J]. Bioarchitecture, 2014, 4(3): 111-5. |
| [3] | Palmefors H, DuttaRoy S, Rundqvist B, et al. The effect of physical activity or exercise on key biomarkers in atherosclerosis-a systematic review[J]. Atherosclerosis, 2014, 235(1): 150-61. |
| [4] | Liu Z J, Velazquez O C. Hyperoxia, endothelial progenitor cell mobilization, and diabetic wound healing[J]. Antioxid Redox Signal, 2008, 10(11): 1869-82. |
| [5] | Balaji S, King A, Crombleholme T M, et al. The role of endothelial progenitor cells in postnatal vasculogenesis: implications for therapeutic neovascularization and wound healing[J]. Adv Wound Care (New Rochelle), 2013, 2(6): 283-95. |
| [6] | Forstermann U, Sessa W C. Nitric oxide synthases: regulation and function[J]. Eur Heart J, 2012, 33(7): 829-37. |
| [7] | Hess C N, Kou R, Johnson R P, et al. ADP signaling in vascular endothelial cells: ADP-dependent activation of the endothelial isoform of nitric-oxide synthase requires the expression but not the kinase activity of AMP-activated protein kinase[J]. J Biol Chem, 2009, 284(47): 32209-24. |
| [8] | Ching L C,Kou Y R,Shyue S K,et al. Molecular mechanisms of activation of endothelial nitric oxide synthase mediated by transient receptor potentialvanilloid type 1[J]. Cardiovasc Res, 2011, 91(3): 492-501. |
| [9] | Hao Q, Wang L, Zhao Z J, et al. Identification of protein kinase D2 as a pivotal regulator of endothelial cell proliferation, migration, and angiogenesis[J]. J Biol Chem, 2009, 284(2): 799-806. |
| [10] | Aicart R C, Sánchez R L, Gómez P M, et al. Protein kinase D activity controls endothelial nitric oxide synthesis[J]. J Cell Sci, 2014, 127(Pt 15): 3360-72. |
| [11] | Kentaro J J, Masaaki L, Douglas W L. Endothelial progenitor cells in neovascularization of infracted myocardium[J]. J Mol Cell Cardiol, 2008, 45(4): 530-44. |
