


2. 湖南医药学院生理学教研室, 湖南 怀化 418000;
3. 暨南大学医学院药理学系, 广东 广州 510632;
4. 暨南大学国际学院, 广东 广州 510632;
5. 暨南大学医学院生理学系, 广东 广州 510632
罗海(1980-),男,博士,讲师,研究方向:细胞生理学,并列第一作者,Tel:0745-2382880,E-mail:h_luo@163.com
陈丽新(1955-),女,博士,教授,博士生导师,研究方向:分子药理学,通讯作者,Tel:020-85228865,E-mail:chenlixinw@sohu.com
 , LUO Hai2, 5
, LUO Hai2, 5 , LIN Jia-wei4, WEI Yan5, LI Yuan3, LIU Shan-wen3, MENG Long3, ZOU Li-li5, ZHU Lin-yan3, WANG Li-wei4, 5
, LIN Jia-wei4, WEI Yan5, LI Yuan3, LIU Shan-wen3, MENG Long3, ZOU Li-li5, ZHU Lin-yan3, WANG Li-wei4, 5
 , CHEN Li-xin3
, CHEN Li-xin3

2. Dept of Physiology, Hunan University of Medicine, Huaihua Hunan 418000, China;
3. Dept of Pharmacology of Medical College, Jinan University, Guangzhou 510632, China;
4. International School, Jinan University, Guangzhou 510632, China;
5. Dept of Physiology of Medical College, Jinan University, Guangzhou 510632, China
阿霉素(adriamycin,ADM)为蒽环类抗生素,抗瘤谱较广,疗效高,是临床常用的抗肿瘤药物。除白血病外,其对膀胱癌、胃癌、肺癌、卵巢癌、甲状腺癌、多发性骨髓瘤、乳腺癌、软组织肉瘤以及侵蚀性淋巴瘤等都有疗效[1]。阿霉素抗肿瘤作用机制包括诱导肿瘤细胞凋亡、抑制细胞周期以及使肿瘤细胞发生自噬等[2]。文献报道,阿霉素可能通过影响Bcl-2/Bax[3]、JNK凋亡通路[3]、p53凋亡通路[4]以及激活腺苷酸活化蛋白激酶(AMPK)[5]等诱导细胞凋亡,但其确切机制仍未十分明了。细胞凋亡早期出现的细胞容积减小称为凋亡性细胞皱缩(apoptotic volume decrease,AVD),是具有普遍性意义的细胞凋亡早期的标志性事件。我们实验室前期研究表明,氯通道参与过氧化氢诱导的肾上腺嗜铬细胞瘤PC12细胞凋亡[6]、紫杉醇[7]和丹参酮[8]诱导的低分化鼻咽癌CNE-2Z细胞的凋亡。这些结果提示多种抗肿瘤药物都可能通过激活氯通道引起AVD,继而诱导细胞发生凋亡,从而发挥其抗癌作用。
本研究旨在探讨阿霉素是否通过激活细胞氯通道而诱导凋亡性细胞皱缩,从离子通道的角度来探讨阿霉素诱导CNE-2Z细胞凋亡的作用机制。
1 材料与方法 1.1 细胞培养用含10%小牛血清、双抗(1×105 U·L-1青霉素与100 mg·L-1链霉素)的RPMI1640生长液,在37°C恒温培养箱(5% CO2、饱和湿度)内常规培养低分化鼻咽癌细胞(CNE-2Z),每两天传代1次。实验前取对数生长期的CNE-2Z细胞,用0.25% 胰酶进行消化传代,收集、重悬细胞,将细胞悬液接种于直径22 mm的圆形玻片上,置入培养箱使细胞贴壁,待细胞贴壁1 h后进行实验。
1.2 主要试剂与药品盐酸阿霉素固体粉末购于上海生工生物有限公司,用二甲基亚砜(DMSO)溶解,配制成浓度为2.5 mmol·L-1的储存液,储存在4℃冰箱中,使用前稀释至终浓度。氯通道阻断剂5-nitro-2-(3-phenylpropylamino)-benzoate (NPPB)购自Sigma公司,溶于dimethyl sulfoxide(DMSO)中,配成100 mmol·L-1的储存液,工作浓度为100 μmol·L-1。等渗灌流液组成(mmol·L-1):10 HEPES,0.5 MgCl2,70 NaCl,140 D-mannitol,2 CaCl2,用冰点渗透压计(Osmomat030,Gono2tec)调节溶液渗透压至300 mOsmol·L-1,用Tris-base调节pH至7.4。
1.3 细胞容积测量将贴有细胞的玻片置于灌流槽内,在倒置相差显微镜(IX71,Olympus,日本)下选择固定视野,用图像分析软件(Image-Pro Plus 6.3,Media Cybernetics,USA)控制数字式摄像机(RETIGA 4000R,QImaging,Canada),进行连续拍摄,每2 min拍摄一幅,直至2 h。拍摄的图片用 Scion Image 图像分析软件(Scion Corporation)处理,测量细胞直径与面积,用以下公式计算细胞容积( V ): V =4/3×(直径/2)3,并标准化细胞容积( V st): V st=( V t/ V o)×100%( V t:细胞的实际容积,V o:药物刺激前即等渗条件下(对照)的细胞平均容积)。实验分为空白对照组(Iso)、阿霉素组(ADM,2.5 μmol·L-1)、氯通道阻断剂NPPB组(100 μmol·L-1)、阿霉素(2.5 μmol·L-1) + NPPB(100 μmol·L-1)组。实验环境温度为室温(20℃~24℃)。
1.4 流式细胞术检测细胞凋亡细胞种植于6孔板中,培养箱中培养12 h,按上述实验分组进行处理。36 h后,收集细胞,用PBS冲洗,并用预冷的70%乙醇于-20℃固定30 min。PBS清洗并离心,加入 propidium iodide(PI,50 mg·L-1),室温避光染色15 min。用流式细胞仪(Coulter EPTCSXL-31240,Coulter,USA)进行分析。
1.5 膜片钳全细胞记录技术EPC-7 膜片钳放大器(List Electronic,Germany)用于记录全细胞电流,CED1401 (Cambridge,UK)用于数字化(采样频率3 kHz)电流和电压信号。拉制的电极是硼硅酸盐毛细玻璃管,其内径为0.86 mm,外直径为1.5 mm,内含细长丝,于垂直微电极拉制器(PB-7)上,分两步拉制。将电极内液充灌至电极容积的1/3至2/3间,此时阻抗约为(5-10)MΩ。全细胞记录模式构建完成后,开始记录实验数据。将细胞钳制在氯离子的平衡电位(0 mV)。按指令电压的顺序(±40,0 和±80 mV)循环记录氯电流变化。每一电位持续时间约200 ms,两电位之间间隔4 s。形成全细胞记录后,补偿电容。灌流等渗液3 min后,加入阿霉素,连续观察氯电流变化,待阿霉素激活氯电流达峰值,并平衡5 min后,灌流含氯通道阻断剂与阿霉素的等渗液,观察氯电流变化,直至电流抑制到最小值,并平稳3 min以上。实验数据用EPC (CED,Cambridge,UK)软件分析。实验环境温度为室温(20℃~24℃)。
全细胞膜片钳记录所需电极内液组成(mmol·L-1):1 EGTA[乙二醇-双-(2-氨基乙醚)四乙酸],1.2 MgCl2,70 N-methyl-D-glucamine chloride (NMDG-Cl),10 HEPES,140 D-mannitol和2 ATP,并用Tris-base调节pH至7.25。
1.6 统计学处理采用SPSS 12.0软件对实验数据进行统计与分析,数据用 x±s表示,采用方差分析(ANOVA)检验差异的显著性。
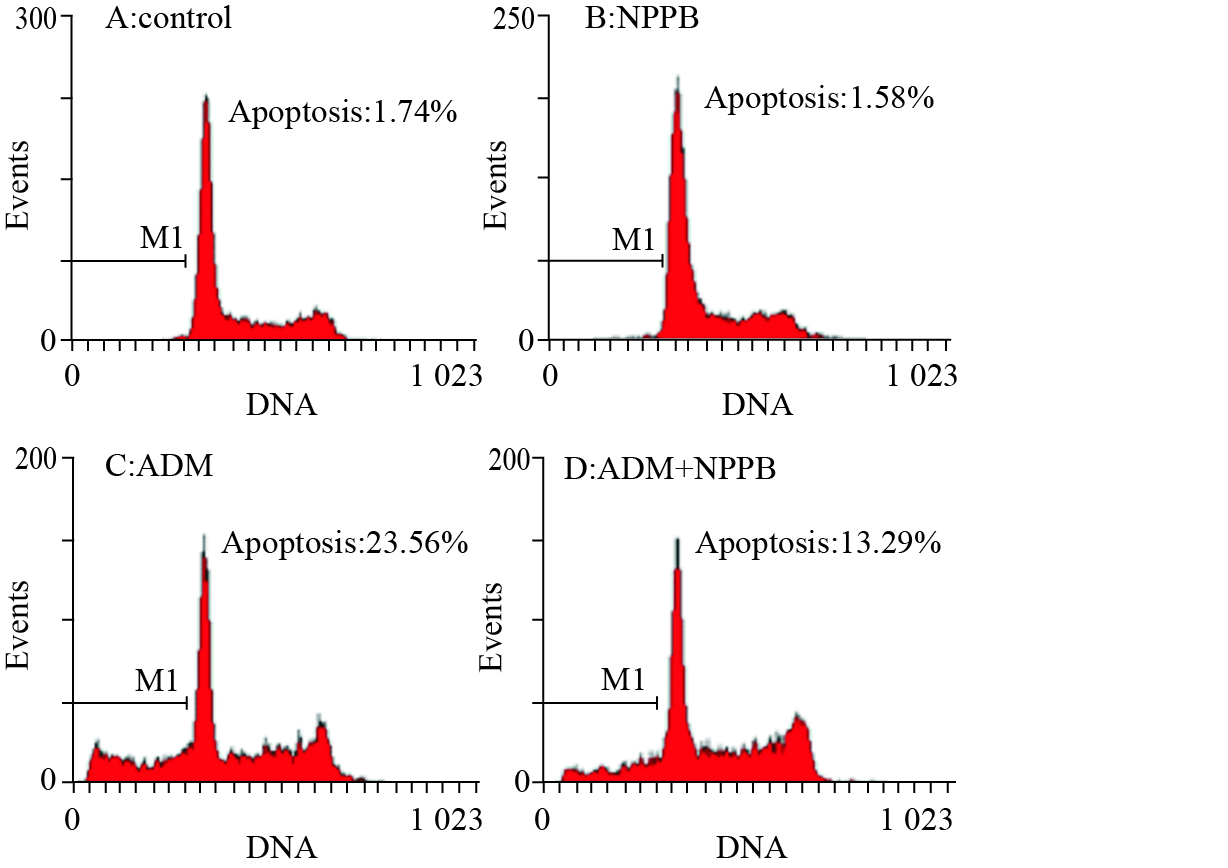
2 结果 2.1 氯通道阻断剂抑制阿霉素诱导的鼻咽癌细胞凋亡用流式细胞仪检测阿霉素诱导的鼻咽癌细胞凋亡率。实验结果显示,不加任何药物处理的空白对照组细胞,其凋亡率为(1.74±2.34)%( n =3)(Fig 1A),而用2.5 μmol·L-1的阿霉素处理36 h的细胞,凋亡率增加至(23.56±3.45)%( n =3,P < 0.01,vs control)(Fig 1C)。
|
| Fig 1 Inhibition of adriamycin-induced apoptosis by chloride channel blocker NPPB in nasopharyngeal carcinoma CNE-2Z cells Cells were incubated in the control medium (A) or in the medium contained 100 μmol·L-1 NPPB (B), 2.5 μmol·L-1 adriamycin (C) or 2.5 μmol·L-1 adriamycin plus 100 μmol·L-1 NPPB (D). |
为了探讨氯通道在阿霉素诱导的鼻咽癌细胞凋亡中的作用,我们观察了氯通道阻断剂NPPB对阿霉素诱导的凋亡的影响。结果显示,单纯用NPPB (100 μmol·L-1)处理的细胞,凋亡率为(1.58±1.35)%,与空白对照组相比,差异没有显著性( n =3,P >0.05,vs control)(Fig 1B)。NPPB(100 μmol·L-1)与阿霉素(2.5 μmol·L-1)共同处理细胞,CNE-2Z细胞凋亡率为(13.29±2.78)%,与阿霉素组凋亡率(23.56±3.45)%相比,差异有显著性( n =3,P < 0.01)(Fig 1D)。
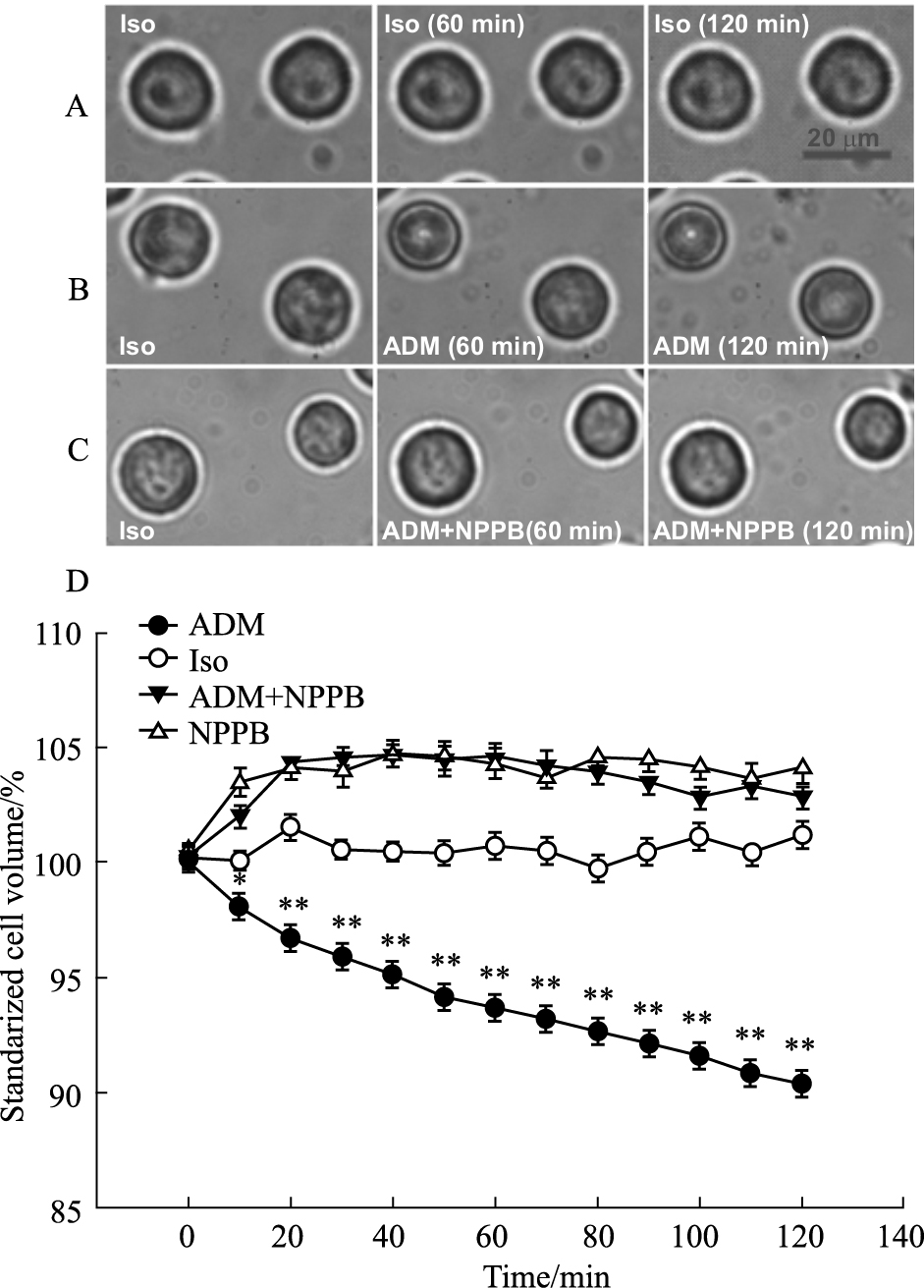
2.2 氯通道阻断剂抑制阿霉素诱导的鼻咽癌细胞凋亡性容积减小细胞图像分析结果显示,等渗液灌流细胞2 h,细胞容积及形态基本保持不变(Fig 2A)。而用含2.5 μmol·L-1阿霉素的等渗液灌流细胞10 min内,便可观察到CNE-2Z细胞的凋亡性容积减小的发生,在连续观察120 min的过程中,发现细胞体积逐渐减小,皱缩(Fig 2B)。而阿霉素和NPPB联合作用120 min时的细胞体积并没有减小(Fig 2C)。Fig 2D显示了药物作用前后120 min细胞容积变化百分率,阿霉素灌流120 min时细胞体积减小至(90.36±0.42)%( n=21,P < 0.01),阿霉素和NPPB联合作用组细胞体积为(102.83±0.44)%( n =27),与阿霉素组相比,差异有显著性( P < 0.01)。单纯用NPPB灌流细胞,细胞体积有所增大,120 min时为(104.05±0.65)%( n =14)。实验结果表明,氯通道阻断剂NPPB可以明显抑制阿霉素诱导的鼻咽癌细胞容积减小,提示阿霉素可能通过激活氯通道而诱导鼻咽癌细胞凋亡,早期发生的凋亡性容积减小。
|
| Fig 2 Inhibition of adriamycin-induced apoptotic volume decrease by chloride channel blocker NPPB A, B and C show typical cell images. D shows cell volume changes ( n =14~27; *P < 0.05,**P < 0.01 vs Iso). Iso: isotonic solution; ADM: isotonic solution containing 2.5 μmol·L-1 adriamycin; ADM+NPPB: isotonic solution containing 2.5 μmol·L-1 adriamycin and 100 μmol·L-1 NPPB; NPPB: isotonic solution with 100 μmol·L-1 NPPB. |
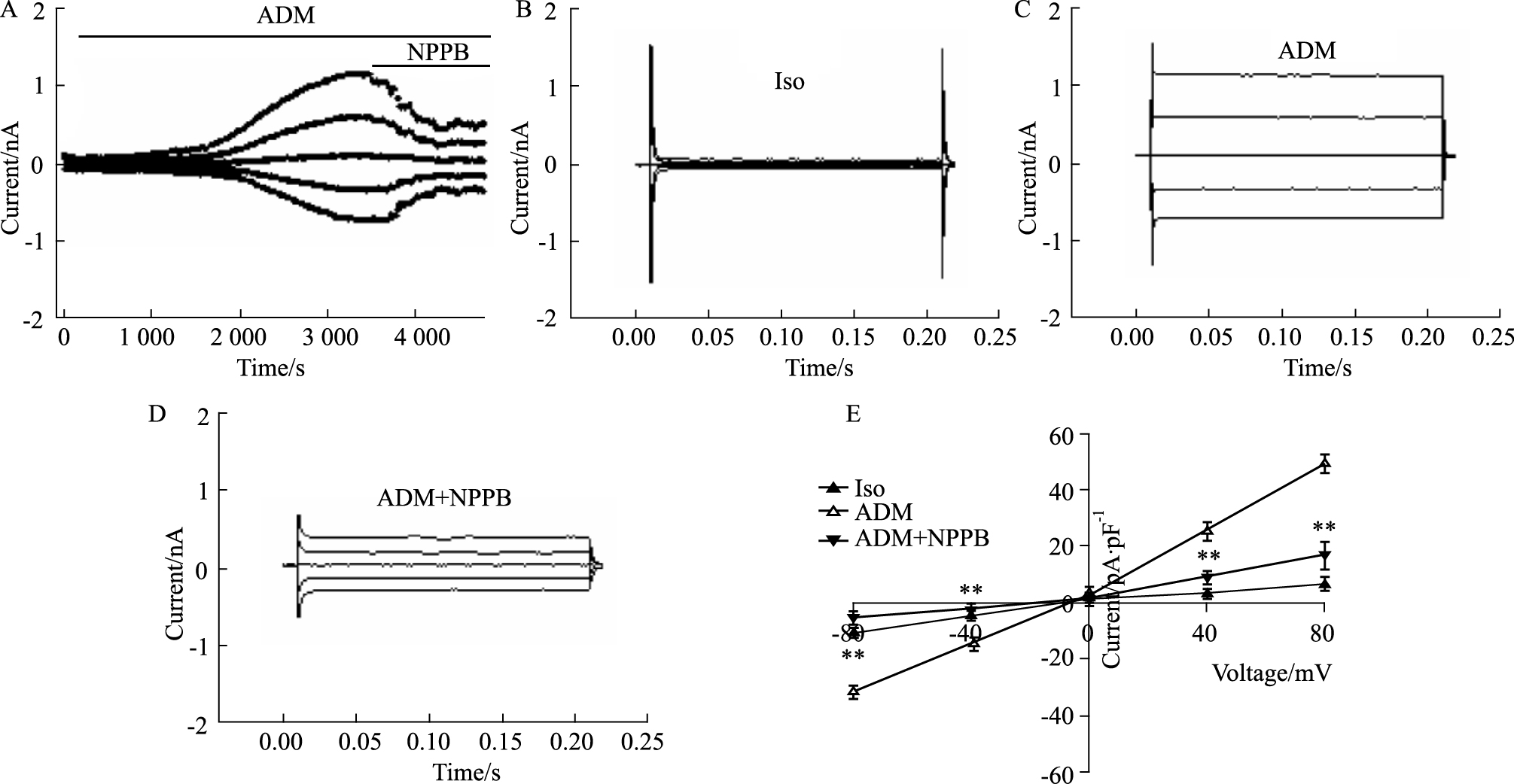
为了进一步验证阿霉素是否通过激活细胞氯通道而诱导细胞凋亡性容积减小,我们用全细胞膜片钳技术记录了阿霉素激活的CNE-2Z细胞氯电流。Fig 3A所示为阿霉素诱导的鼻咽癌细胞氯电流全程图。在等渗条件下,可记录到一个微弱且稳定的背景氯电流(Fig 3A、B)。胞外灌流阿霉素,可以明显激活氯电流,该电流具有外向优势,外向电流明显大于内向电流,且未见明显时间依赖性失活(Fig 3A、C)。该电流的翻转电位为(-3.00±0.84) mV ( n =8),接近氯离子平衡电位。当钳制电压为±80 mV时,该电流的平均峰值高达(-31.67±2.38) pA/pF(-80 mV)、(49.41±3.23) pA/pF(+80 mV)( n =6,P < 0.01,vs Iso)(Fig 3E)。在阿霉素激活氯电流且达平稳的基础上,加入氯通道阻断剂NPPB(100 μmol·L-1),氯电流迅速降低(Fig 3A、D)。其对外向电流的抑制率为(79.96±6.57)%(+80 mV),对内向电流抑制率为(76.64±4.66)%(-80 mV)( n =5,P < 0.01,vs ADM)(Fig 3E),对内外向电流间的抑制作用差异无统计学意义。以上实验结果提示,氯通道在阿霉素诱导CNE-2Z细胞凋亡早期的过程中起重要作用。
|
| Fig 3 Inhibition of adriamycin-activated chloride currents by chloride channel blocker NPPB A shows a typical time course of the adriamycin-activated chloride current. B,C and D present typical current traces of the background currents in the isotonic solution, the adriamycin-activated currents and inhibition of the currents by NPPB. E shows the current-voltage relationships under different conditions ( n =5~8,**P < 0.01 vs ADM). |
在所有实验中,用来配制NPPB的DMSO在灌流液中的终浓度低于1%( V/V ),其对阿霉素诱导的细胞容积减小及激活的氯电流没有影响,且24 h内无细胞毒性。
3 讨论细胞凋亡异常在肿瘤以及许多疾病的发生发展中起着重要的作用。细胞凋亡发生于生理以及病理状态下对不同刺激的应答过程中,具有一系列生化和形态学特征,其伴随着细胞进行性的体积缩小,以及线粒体细胞色素C释放、caspase激活、核固缩、DNA片段化和凋亡小体的形成[9]等。其中早期细胞皱缩或凋亡性容积减小(AVD)是在等渗状态下发生的细胞体积缩小,具有普遍的意义。研究表明[10],AVD发生于细胞色素C释放、caspase活化以及DNA断裂之前,是细胞凋亡早期的标志性事件。鉴于AVD在细胞凋亡早期触发机制中的关键性作用,深入探讨AVD的发生、发展过程及其机制,对于揭示凋亡规律有重要意义。
AVD的发生被认为与细胞内K+与Cl-浓度减小有关[11]。在凋亡早期,凋亡诱导剂激活钾通道与氯通道,促使K+与Cl-外流,并驱动水的外流,致使细胞体积减小发生AVD,进而诱发凋亡 [6, 12]。氯通 道参与细胞的多种生理功能,如细胞增殖[13]、迁移[14]、凋亡[6]、细胞溶血[15],还可参与冰片引起的细胞体积减小过程[16]。我们前文报道,中药丹参酮发挥抗肿瘤作用的机制可能是通过激活氯通道引起氯离子和水外流,诱导AVD发生,进而引起细胞凋亡[8]。阿霉素作为一种常用的抗肿瘤药物,它是否也可能通过激活氯通道诱导AVD和细胞凋亡?目前国内外没有相关报道。本实验采用活细胞影像系统实时拍摄细胞图像,分析细胞凋亡早期的细胞容积变化。实验结果表明,在阿霉素作用的10 min内,便可观察到CNE-2Z细胞凋亡性容积减小的发生;而在阿霉素继续作用的2 h内,细胞容积持续减小。流式细胞术检测到阿霉素诱导CNE-2Z细胞凋亡,氯通道阻断剂NPPB可以完全阻抑CNE-2Z细胞凋亡性容积减小、明显阻抑细胞凋亡,提示阿霉素可以激活CNE-2Z细胞氯通道,进而诱导细胞发生AVD和细胞凋亡。
为了进一步验证这个观点,我们用膜片钳法记录CNE-2Z细胞阿霉素激活的全细胞电流,直接观察阿霉素对氯通道的激活作用。结果显示,细胞外灌流阿霉素可激活一个外向电流,该电流与氯离子跨细胞流动所产生的电流一致,其翻转电位接近氯离子的平衡电位-0.9 mV(根据本实验所用细胞外灌流液及电极内液配方计算而得),该电流可被氯通道阻断剂NPPB抑制,由此推知该电流为氯通道所介导的氯电流。本实验结果为阿霉素激活氯通道提供了直接的实验证据。由于实验用细胞内外液主要离子为Na+、Cl-、Ca2+,而在本实验条件下计算出的Na+、Ca2+平衡电位均高于200 mV,因此该电流与上述两种阳离子电流无关。
本实验观察了阿霉素对氯通道的作用,以及阻断氯通道对阿霉素诱导凋亡和凋亡性容积减小作用的影响。结果表明,阿霉素可激活鼻咽癌细胞氯通道,氯通道阻断剂NPPB可以明显抑制阿霉素诱导的氯电流、拮抗阿霉素引起的细胞凋亡性容积减小和细胞凋亡,提示阿霉素可能通过激活氯通道诱导细胞凋亡,氯通道在阿霉素抗肿瘤机制中发挥重要作用。本实验的完成,加深了我们对阿霉素抗癌机制的认识。
(致谢:本研究主要在暨南大学医学院分子细胞学实验室完成,感谢陈丽新教授、王立伟教授、朱林燕副教授提供优良的学习环境及实验平台。)
| [1] | Carvalho C, Santos R X, Cardoso S, et al. Doxorubicin: the good, the bad and the ugly effect[J]. Curr Med Chem, 2009, 16(25): 3267-85. |
| [2] | Tacar O, Sriamornsak P, Dass C R. Doxorubicin: an update on anticancer molecular action, toxicity and novel drug delivery systems[J]. J Pharm Pharmacol, 2013, 65(2): 157-70. |
| [3] | Chen Y, Wan Y, Wang Y, et al. Anticancer efficacy enhancement and attenuation of side effects of doxorubicin with titanium dioxide nanoparticles[J]. Int J Nanomedicine, 2011, 6: 2321-6. |
| [4] | Zhou Y, Li G, Ji Y, et al. Cytoplasmic p21 induced by p65 prevents doxorubicin-induced cell death in pancreatic carcinoma cell line[J]. J Biomed Sci, 2012, 19: 15. |
| [5] | Chen M B, Shen W X, Yang Y, et al. Activation of AMP-activated protein kinase is involved in vincristine-induced cell apoptosis in B16 melanoma cell[J]. J Cell Physiol, 2011, 226(7): 1915-25. |
| [6] | Zuo W, Zhu L, Bai Z, et al. Chloride channels involve in hydrogen peroxide-induced apoptosis of PC12 cells[J]. Biochem Biophys Res Commun, 2009, 387(4): 666-70. |
| [7] | Zhang H, Li H, Yang L, et al. The ClC-3 chloride channel associated with microtubules is a target of paclitaxel in its induced-apoptosis[J]. Sci Rep, 2013, 3: 2615. |
| [8] | 李 媛, 刘善文, 李华荣, 等. 丹参酮ⅡA对低分化鼻咽癌细胞氯通道的激活作用[J]. 中国药理学通报, 2011, 27(9): 1205-9. Li Y, Liu S W, Li H R, et al. Activation of chloride channels by tanshinone ⅡA in nasopharyngeal carcinoma cells[J]. Chin Pharmacol Bull, 2011, 27(9): 1205-9. |
| [9] | Rich T, Allen R L, Wyllie A H. Defying death after DNA damage[J]. Nature, 2000, 407(6805): 777-83. |
| [10] | Maeno E, Ishizaki Y, Kanaseki T, et al. Normotonic cell shrinkage because of disordered volume regulation is an early prerequisite to apoptosis[J]. Proc Natl Acad Sci USA, 2000, 97(17): 9487-92. |
| [11] | Okada Y, Maeno E. Apoptosis, cell volume regulation and volume-regulatory chloride channels[J]. Comp Biochem Physiol A Mol Integr Physiol, 2001, 130(3): 377-83. |
| [12] | Okada Y, Shimizu T, Maeno E, et al. Volume-sensitive chloride channels involved in apoptotic volume decrease and cell death[J]. J Membr Biol, 2006, 209(1): 21-9. |
| [13] | Zhu L, Yang H, Zuo W, et al. Differential expression and roles of volume-activated chloride channels in control of growth of normal and cancerous nasopharyngeal epithelial cells[J]. Biochem Pharmacol, 2012, 83(3): 324-34. |
| [14] | Mao J, Li X, Chen W, et al. Cell cycle-dependent subcellular distribution of ClC-3 in HeLa cells[J]. Histochem Cell Biol, 2012, 137(6): 763-76. |
| [15] | 滕双凤, 刘振锋, 厉冰雪, 等. 氯通道阻断剂和白头翁皂苷的协同溶血作用[J]. 中国药理学通报, 2012, 28(10): 1379-83. Teng S F, Liu Z F, Li B X, et al. Synergistic effects of chloride channel blockers on the hemolysis induced by Pulsatilla saponin[J]. Chin Pharmacol Bull, 2012, 28(10): 1379-82. |
| [16] | 孟 龙, 王海波, 邓志钦, 等. 冰片对鼻咽癌细胞容积敏感性氯通道的激活作用[J]. 中国药理学通报, 2014, 30(12): 1671-6. Meng L, Wang H B, Deng Z Q, et al. Borneol activated volume-sensitive chloride channels in poorly differentiated nasopharyngeal carcinoma cells[J]. Chin Pharmacol Bull, 2014, 30(12): 1671-6. |