


2. 中国医科大学药学院临床药理教研室, 辽宁 沈阳 110001;
3. 中国医科大学呼吸疾病研究所, 辽宁 沈阳 110001;
4. 中国医科大学心血管疾病研究所, 辽宁 沈阳 110001;
5. 锦州九泰药业有限责任公司质量管理处, 辽宁 锦州 121011
2. Dept of Clinical Pharmacology, China Medical University, Shenyang 110001, China;
3. Institute of Respiratory Diseases, China Medical University, Shenyang 110001, China;
4. Institute of Cardiovascular Diseases, China Medical University, Shenyang 110001, China;
5. Dept of Quality Assurance, Jinzhou Jiutai Pharmaceutical Co., Ltd, Jinzhou Liaoning 121011, China
肺动脉高压(pulmonary arterial hypertension,PAH)的主要病理特征包括肺动脉压力升高、右心室肥厚、肺动脉重构、肺组织炎症反应等[1, 2, 3]。本课题组已经发现氟西汀通过缓解肺动脉重构、改善肺组织炎症反应,抑制野百合碱诱导的大鼠PAH[1]。影响PAH的因素很多,如核因子κB(nuclear factor-κB,NF-κB),它参与PAH大鼠肺动脉重构与肺组织炎症反应[4]。研究发现泛素蛋白酶体系统成员泛素羧基末端水解酶L1(ubiquitin carboxy terminal hydrolase L1,UCH-L1)具有去泛素化作用,可逆转NF-κB的活化,对抗炎症反应和血管重构[5]。但是UCH-L1是否参与野百合碱诱导的PAH大鼠肺动脉重构、肺组织炎症,是否参与氟西汀抑制野百合碱诱导的大鼠PAH,均不清楚。因此,本研究建立野百合碱诱导的大鼠PAH,应用氟西汀进行干预,通过对UCH-L1的蛋白表达及NF-κB活性的检测来探讨UCH-L1在氟西汀抑制野百合碱诱导的大鼠PAH的作用。
1 材料与方法 1.1 药品与试剂野百合碱(C2401)购于Sigma公司;氟西汀为印度Cadila Pharmaceuticals公司产品;兔抗大鼠UCH-L1多克隆抗体(BS1293)购于Bioworld Technology公司;兔抗大鼠NF-κB p65多克隆抗体(sc-372),小鼠抗大鼠β-actin单克隆抗体(sc-47778)购于Santa Cruz公司; RIPA裂解液(P0013B),细胞核蛋白与细胞浆蛋白抽提取试剂盒(P0027)购于碧云天生物科技有限公司。
1.2 试验分组取6周左右150~180 g的♂Wistar大鼠(由中国医科大学实验动物部提供,动物合格证号:No.辽实动字034号)进行分组。分组一(每组3只大鼠):对照组,野百合碱组;给予野百合碱组大鼠一次性腹腔注射野百合碱60 mg·kg-1,给予对照组大鼠一次性腹腔注射同等体积的无水乙醇和生理盐水(体积比1 ∶ 4)混和液;常规饲养21 d[1]。分组二(每组8只大鼠):对照组,野百合碱组,氟西汀低剂量组,氟西汀高剂量组;给予野百合碱组、氟西汀低剂量组、氟西汀高剂量组大鼠一次性腹腔注射野百合碱60 mg·kg-1,给予对照组大鼠一次性腹腔注射同等体积的无水乙醇和生理盐水(体积比1 ∶ 4)混和液,之后分别灌胃给予氟西汀低剂量组和氟西汀高剂量组大鼠2 mg·kg-1·d-1和10 mg·kg-1·d-1氟西汀,灌胃给予野百合碱组和对照组大鼠同等体积的蒸馏水;常规饲养21 d[1]。
1.3 血流动力学参数测定对大鼠腹腔注射40 mg·kg-1戊巴比妥钠,使其麻醉。麻醉后将大鼠颈部皮肤切开,分离出颈动脉和颈外静脉。把充满肝素的PE-50管插入颈动脉中,并通过TP200P压力换能器、AP-611G载波放大器连接到R6000多导生理记录仪(均为日本Nihon Kondon公司产品),记录体循环压。把充满肝素的PV-1管(尖端弯曲)经颈外静脉、右心房、右心室插入肺动脉中,并通过P23ID压力换能器(日本Nihon Kondon公司)连接到多导生理记录仪,记录肺动脉压。
1.4 苏木精-伊红染色取大鼠右肺下叶固定于40 g·L-1多聚甲醛中,经脱水、透明、浸蜡、包埋后,将肺组织制成5 μm厚的石蜡切片。切片常规脱蜡至水后,依次放入苏木精染液5 min、体积分数为0.01的盐酸乙醇溶液数秒(分化)、自来水30 min(返蓝)、伊红染液4 min、自来水数秒,然后梯度乙醇脱水、二甲苯透明,树胶封片。光学显微镜下观察大鼠肺小动脉和肺组织形态。
1.5 免疫组织化学石蜡切片常规脱蜡至水后,微波抗原修复,再用体积分数为0.003的H2O2孵育灭活内源性过氧化物酶活性;室温下血清封闭后,依次加一抗(抗UCH-L1抗体1 ∶ 50)、二抗以及链霉亲和素-过氧化物酶;最后加DAB显色剂显色,并用苏木精复染;除封闭后不冲洗外,其他各步用磷酸盐缓冲液各冲洗3次。光学显微镜下观察大鼠肺小动脉、肺小支气管和肺组织UCH-L1分布情况。
1.6 Western blot取大鼠右肺下叶和肺动脉,将每一下叶分为两份。其中一份肺组织与肺动脉采用RIPA裂解液,按照说明书进行匀浆裂解,提取全蛋白;另一份肺组织采用细胞核蛋白与细胞质蛋白抽提取试剂盒,按照说明书提取细胞核蛋白和浆蛋白。将提取的蛋白制成上样液,经SDS-PAGE凝胶电泳、湿转转膜、封闭后,分别用1 ∶ 600的抗UCH-L1抗体、1 ∶ 500的抗NF-κB p65抗体或1 ∶ 2 000的β-actin抗体进行杂交;并在二抗孵育后,使用ECL发光液曝光。采用Quanlity One图像分析系统进行条带光密度值分析,分别以胞核NF-κB与胞质NF-κB的光密度值比作为NF-κB活化程度的指标,以UCH-L1与β-actin的光密度值比作为UCH-L1蛋白表达水平的指标。
1.7 统计学处理采用SPSS 13.0软件对实验数据进行统计学分析。所有数据以 x ±s 表示,组间样本采用单因素方差分析,两组间样本分析采用LSD检验。
2 结果 2.1 肺组织中泛素羧基末端水解酶L1的蛋白表达UCH-L1在大鼠大脑、腹主动脉、肺主动脉、肺组织、心均有表达;其中,脑中UCH-L1表达相对较多,肺组织相对较少(Fig 1A)。在正常大鼠肺组织中,UCH-L1蛋白表达于肺动脉平滑肌细胞、内皮细胞以及支气管与肺泡上皮细胞的胞质与胞核中(Fig 1C)。

|
| Fig 1 Changes of ubiquitin carboxyl terminal hydrolase L1 protein expression of pulmonary arteries and lungs in rats treated with monocrotaline CTL (control),MCT (monocrotaline 60 mg·kg-1,ip).AA,ab-dominalaorta;PA,pulmonary artery.Bar (C)=60 μm,Bar (D)=150 μm. |
Western blot与免疫组化结果显示:野百合碱组PAH大鼠肺动脉UCH-L1蛋白表达变化不明显(Fig 1B,Fig 1C)。野百合碱组PAH大鼠肺组织中UCH-L1蛋白表达明显减少(Fig 1B),主要是血管、气道周围等炎性细胞浸润区域基本无UCH-L1蛋白表达(Fig 1C,Fig 1D)。
2.3 氟西汀对野百合碱诱导的肺动脉高压大鼠血流动力学参数的影响Tab 1显示:野百合碱组、氟 西汀低剂量组与氟西汀高剂量组大鼠体质量明显低 于对照组;野百合碱组大鼠平均肺动脉压明显高于 对照组(P<0.01);氟西汀低剂量组与野百合碱组 相比,大鼠平均肺动脉压差异没有显著性,而氟西汀 高剂量组明显低于野百合碱组(P<0.01);各组间 平均体循环压力及心率则差异没有显著性。
| (x±s, n =8) | ||||
| Index | CTL | MCT | F2 | F10 |
| CTL (control), MCT (monocrotaline 60 mg·kg-1, ip), F2 (monocrotaline 60 mg·kg-1, ip+fluoxetine 2 mg·kg-1·d-1, po), F10 (monocrotaline 60 mg·kg-1, ip + fluoxetine 10 mg·kg-1·d-1, po). BW, body weight; HR, heart rate; mSAP, mean systemic arterial pressure; mPAP, mean pulmonary arterial pressure; * P < 0.05, ** P < 0.01 vs CTL group; ## P < 0.01 vs MCT group. | ||||
| BW/g | 332±18 | 234±36* | 220±52* | 240±46* |
| HR/bpm | 352±51 | 361±44 | 366±30 | 355±36 |
| mSAP/kPa | 17.5±2.7 | 15.7±3.1 | 16.4±2.4 | 16.9±3.3 |
| mPAP/kPa | 2.07±0.12 | 4.09±0.65** | 3.88±0.84** | 3.09±0.59*## |
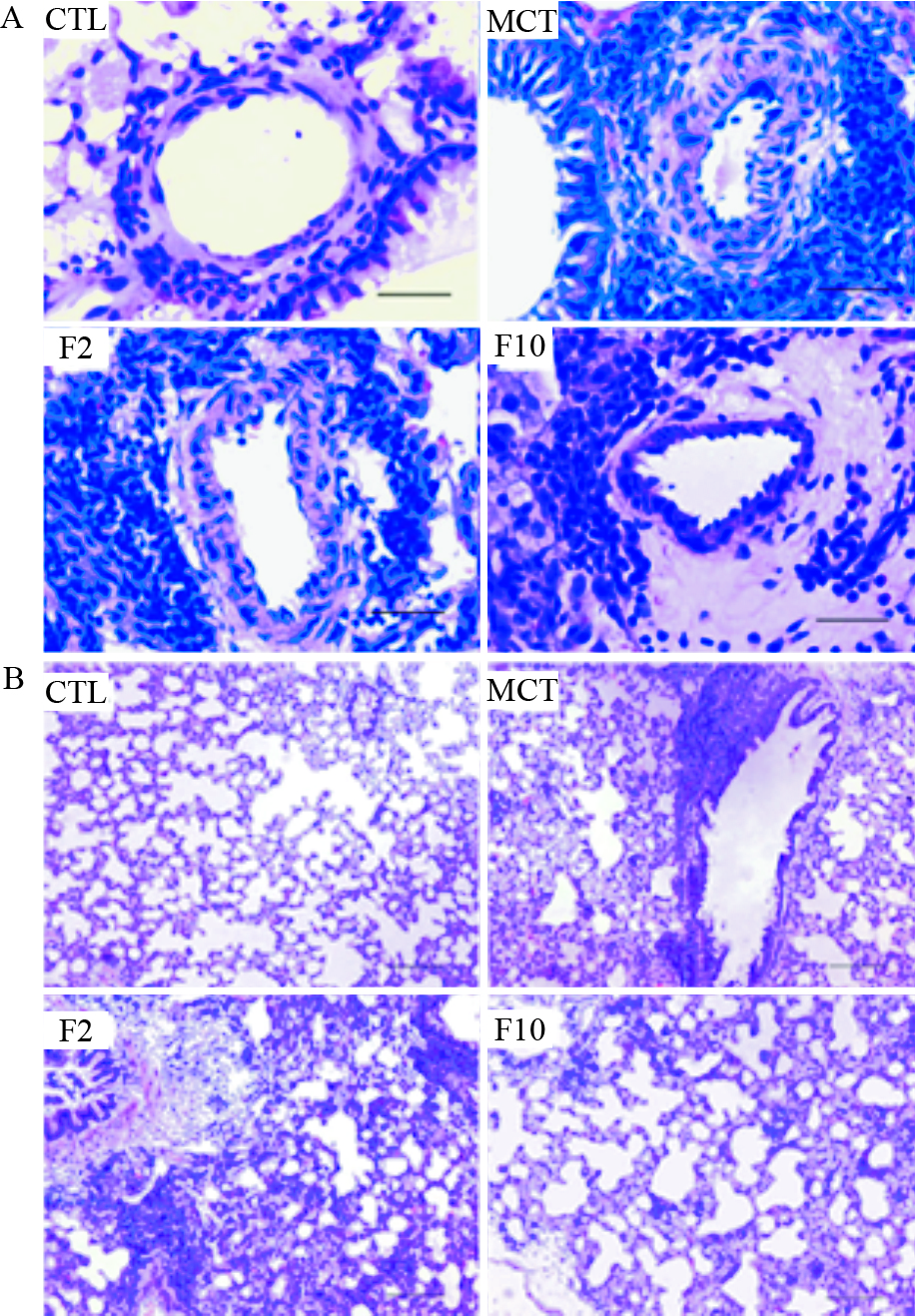
大鼠肺组织苏木精-伊红染色显示:对照组肺组织气道结构正常,无明显炎症细胞浸润,肺小动脉结构正常;野百合碱组肺血管肌层增厚,管腔狭窄,肺血管壁与气道管壁周围炎症细胞浸润;氟西汀低剂量组肺血管壁与气道管壁周围炎症细胞浸润,肺动脉壁肌层略厚;氟西汀高剂量组肺组织气道、肺小动脉恢复正常,有少量炎症细胞浸润(Fig 2)。
|
| Fig 2 Representative photomicrographs of pulmonary arterioles and lungs in different groups CTL (control),MCT (monocrotaline 60 mg· kg-1,ip),F2 (monocrotaline 60 mg· kg-1,ip+fluoxetine 2 mg· kg-1· d-1, po),F10(monocrotaline 60 mg·kg-1,ip+fluoxetine 10 mg·kg-1 ·d-1,po).Bar (A)=40 μm,Bar (B)=250 μm. |
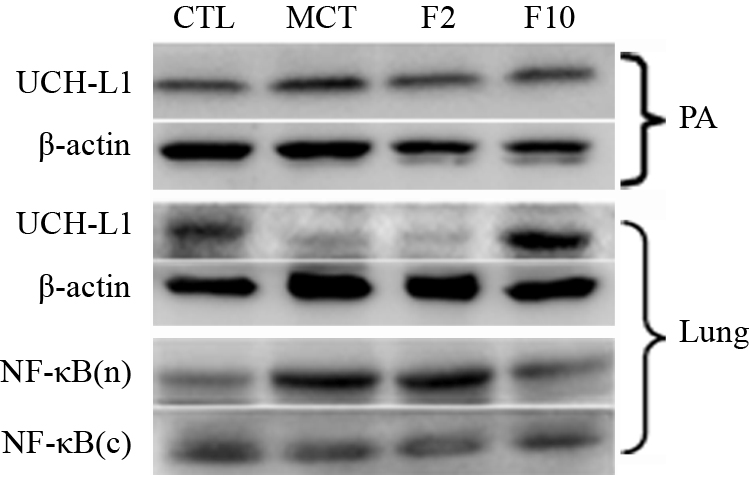
Westernblot结果显示:野百合碱诱导的肺动脉高压大鼠肺组织UCH-L1蛋白表达明显减少;氟西汀剂量依赖地上调肺组织UCH-L1蛋白表达,并且氟西汀高剂量组肺组织UCH-L1蛋白表达高于正常组(P<0.01);而各组之间大鼠肺动脉UCH-L1蛋白表达差异无显著性;氟西汀高剂量组肺动脉UCH-L1蛋白表达水平略有升高,但差异无统计学意义(Fig 3,Tab 2)。
|
| Fig 3 Western blot result of ubiquitin carboxyl terminal hydrolase L1 protein expression and nuclear factor-κB activity in different groups CTL (control),MCT (monocrotaline 60 mg· kg-1,ip),F2(monocrotaline 60 mg· kg-1,ip+fluoxetine 2 mg· kg-1· d-1,po),F10(monocrotaline 60 mg·kg-1,ip+fluoxetine 10 mg·kg-1 ·d-1,po).PA,pulmonaryartery;NF-κB (n),NF-κB (p65) innu-clear;NF-κB (c),NF-κB (p65) incytoplasm. |
| (x±s, n =3~5) | |||||
| Tissue | Index | CLT | MCT | F2 | F10 |
| CTL (control), MCT (monocrotaline 60 mg·kg-1, ip), F2 (monocrotaline 60 mg·kg-1, ip+fluoxetine 2 mg·kg-1·d-1, po), F10 (monocrotaline 60 mg·kg-1, ip + fluoxetine 10 mg·kg-1·d-1, po). BW, body weight; HR, heart rate; mSAP, mean systemic arterial pressure; mPAP, mean pulmonary arterial pressure; * P < 0.05, ** P < 0.01 vs CTL group; ## P < 0.01 vs MCT group. | |||||
| PA | UCH-L1/β-actin | 0.98±0.10 | 0.94±0.09 | 0.92±0.11 | 1.13±0.11 |
| Lung | UCH-L1/β-actin | 1.42±0.29 | 0.17±0.09** | 0.45±0.15** | 1.87±0.25**## |
| Lung | NF-κB(n)/NF-κB(c) | 0.43±0.35 | 1.42±0.35* | 1.83±0.69** | 0.62±0.14# |
Westernblot结果显示:野百合碱诱导的肺动脉高压大鼠肺组织中NF-κBp65核转位明显增加;氟西汀剂量依赖地抑制这一改变(Fig 3,Tab 2)。
3 讨论UCH-L1最早被命名为蛋白基因产物9.5,是一个具有223个氨基酸、9个外显子编码的25ku蛋白[6]。它占脑蛋白的1%~2%,也分布于心、血管、肾、大肠、胰岛、肾上腺髓质、甲状腺等组织器官[5, 6, 7, 8]。早期的研究未在肺组织中发现UCH-L1的表达[8]。然而,本研究不仅在大鼠脑、心、腹主动脉中检测到UCH-L1蛋白表达,而且在肺主动脉和肺组织中也发现UCH-L1蛋白的存在,其表达于肺动脉平滑肌细胞、内皮细胞以及气道上皮细胞的胞质与胞核中。近年一些研究也发现,UCH-L1在血管平滑肌细胞、血管内皮细胞以及气道上皮细胞中均有表达[5, 9]。这些结果与早期结果不一致,可能是因为肺组织蛋白表达太少或者早期检测手段不灵敏所致。
UCH-L1在血管重构与炎症反应过程中具有重要作用[5]。研究发现球囊损伤颈动脉的平滑肌细胞中UCH-L1mRNA增加;肿瘤坏死因子-α诱导血管平滑肌细胞增殖伴随UCH-L1蛋白上调;过表达的UCH-L1反而又抑制肿瘤坏死因子-α诱导的血管平滑肌细胞增殖和炎症响应[5, 10]。但是本研究并未检测出PAH大鼠的肥厚肺动脉中UCH-L1蛋白表达异于正常大鼠,反而发现炎性肺组织,尤其是血管、气道周围的炎性细胞胞质、胞核中UCH-L1蛋白表达明显减少。本研究还发现野百合诱导的PAH大鼠肺组织中NF-κBp65的核转位明显增加。可能是因为UCH-L1作为泛素蛋白酶体系统中的重要成员,去泛素化(即水解连接在蛋白上的单个泛素分子羧基末端,产生泛素单体),调控一些蛋白的降解,如减少蛋白I-κB-α的泛素化与降解,从而降低NF-κB的活性[5]。UCH-L1的下调可能将无法有效的对抗NF-κB的活化。这提示野百合碱可能通过减少UCH-L1蛋白表达,使NF-κB的活性增加,从而导致肺组织炎症反应。
本研究重现了选择性5-HT再摄取抑制剂氟西汀抑制PAH大鼠肺动脉重构与肺组织炎症反应,并发现氟西汀抑制肺组织NF-κBp65的核转位增多。有研究表明NF-κB是PAH大鼠的靶点之一,NF-κB抑制剂抑制野百合碱诱导的大鼠PAH[4]。氟西汀不仅在肺组织中具有抗炎作用,在神经、肠等模型中同样可抑制NF-κB信号通路,表现出抗炎作用[11, 12]。本研究还发现氟西汀上调PAH大鼠肺动脉(差异无统计学意义)、肺组织中UCH-L1蛋白表达。这与报道的氟西汀增加UCH-L1mRNA相一致[13]。又由于UCH-L1可减少NF-κB的核转位[5],提示氟西汀可能通过上调UCH-L1、抑制NF-κB的活性,而达到对抗肺组织炎症的作用。
因此,UCH-L1在野百合碱诱导的大鼠PAH中具有重要作用;氟西汀抑制野百合碱诱导的肺组织炎症,与UCH-L1上调而降低NF-κB的活性有关。
(致谢:本实验分别在中国医科大学临床药理教研室与辽宁医学院药理学教研室完成,感谢各教研室老师和同学的支持和帮助。)
| [1] | Wang H M, Wang Y, Liu M, et al. Fluoxetine inhibits monocrotaline-induced pulmonary arterial remodeling involved in inhibition of RhoA-Rho kinase and Akt signalling pathways in rats[J]. Can J Physiol Pharmacol, 2012, 90(11): 1506-15. |
| [2] | 刘晓艳, 孟刘坤, 李 君, 魏英杰. 分泌型簇蛋白在肺动脉高压大鼠中的表达变化[J]. 中国药理学通报, 2014, 30(6): 764-8. Liu X Y, Meng L K, Li J, Wei Y J. Expression pattern of secretory clusterin in pulmonary arterial hypertension rats[J]. Chin Pharmacol Bull, 2014, 30(6): 764-8. |
| [3] | 李明星, 王 勇, 蒋德旗, 王 艳. 参与肺动脉平滑肌细胞增殖信号转导机制及信号转导抑制剂的研究进展[J]. 中国药理学通报, 2015, 31(5): 605-10. Li M X, Wang Y, Jiang D Q, Wang Y. Advances in research on signal transduction mechanisms and their inhibitors for the proliferation of pulmonary artery smooth muscle cells[J]. Chin Pharmacol Bull, 2015, 31(5): 605-10. |
| [4] | Farkas D, Alhussaini A A, Kraskauskas D, et al. Nuclear factor κB inhibition reduces lung vascular lumen obliteration in severe pulmonary hypertension in rats[J]. Am J Respir Cell Mol Biol, 2014, 51(3): 413-25. |
| [5] | Takami Y, Nakagami H, Morishita R, et al. Ubiquitin carboxyl-terminal hydrolase L1, a novel deubiquitinating enzyme in the vasculature, attenuates NF-κB activation[J]. Arterioscler Thromb Vasc Biol, 2007, 27(10): 2184-90. |
| [6] | Wang R, Zhang M, Zhou W, et al. NF-kappaB signaling inhibits ubiquitin carboxyl-terminal hydrolase L1 gene expression[J]. J Neurochem, 2011, 116(6): 1160-70. |
| [7] | Suong D N, Thao D T, Masamitsu Y, Thuoc T L. Ubiquitin carboxyl hydrolase L1 significance for human diseases[J]. Protein Pept Lett, 2014, 21(7): 624-30. |
| [8] | Wilkinson K D, Deshpande S, Larsen C N. Comparisons of neuronal (PGP 9.5) and non-neuronal ubiquitin C-terminal hydrolases[J]. Biochem Soc Trans, 1992, 20(3): 631-7. |
| [9] | Carolan B J, Heguy A, Harvey B G, et al. Up-regulation of expression of the ubiquitin carboxyl-terminal hydrolase L1 gene in human airway epithelium of cigarette smokers[J]. Cancer Res, 2006, 66(22): 10729-40. |
| [10] | Ichikawa T, Li J, Dong X, et al. Ubiquitin carboxyl terminal hydrolase L1 negatively regulates TNFalpha-mediated vascular smooth muscle cell proliferation via suppressing ERK activation[J]. Biochem Biophys Res Commun, 2010, 391(1): 852-6. |
| [11] | Koh S J, Kim J W, Kim B G, et al. Fluoxetine inhibits hyperresponsive lamina propria mononuclear cells and bone marrow-derived dendritic cells, and ameliorates chronic colitis in IL-10-deficient mice[J]. Dig Dis Sci, 2015, 60(1): 101-8. |
| [12] | Blatteau J E, Barre S, Pascual A, et al. Protective effects of fluoxetine on decompression sickness in mice[J]. PloS One, 2012, 7(11): e49069. |
| [13] | Lauterbach E C. Psychotropic drug effects on gene transcriptomics relevant to Parkinson's disease[J]. Prog Neuropsychopharmacol Biol Psychiatry, 2012, 38(2): 107-15. |

