


AP25是我们课题组自主设计合成的由25个氨基酸组成的抗肿瘤多肽,其中含有两对二硫键,其序列获得国家发明专利授权(专利号:ZL2005100 40378.5),具有开发为一类抗肿瘤新药的前景。体外对15种肿瘤细胞株的MTT试验显示,它可以有效抑制MGC-803、HeLa、HCT116、U87和MDA-MB-231等肿瘤细胞的增殖,还可以有效抑制内皮细胞的迁移,其IC50为7.3 μmol·L-1;体内对2种人的肿瘤细胞药效学实验发现,它可以有效抑制人的乳腺癌、结肠癌生长,抑制效果相当于化学药物多西他赛;我们还对AP25的大鼠及食蟹猴的药代动力学进行了研究,获得了其体内代谢特征数据,包括血浆半衰期、组织分布及排泄的数据;急性毒性试验发现,SD大鼠经静脉单次给予多肽AP25的最低致死剂量(MLD)为200 mg·kg-1;机制研究显示,AP25与血管内皮细胞表面的整合素αvβ3及其协同受体硫酸肝素糖蛋白(glypican-1)相互作用,并被募集至细胞表面的脂筏区域,通过一系列信号转导作用下调Src激酶的活性,引起RhoGTP转化为RhoGDP,降低RhoA和Rac1蛋白的活性,从而引起actin张力纤维和黏着斑复合物的解聚,最终抑制肿瘤血管内皮细胞的迁移,达到抑制肿瘤血管生成的作用[1, 2]。
多西他赛为紫杉醇类抗肿瘤药物,通过干扰细胞有丝分裂和分裂间期细胞功能所必须的微管网络而起到抗肿瘤作用。多西他赛可与游离的微管蛋白结合,促进微管蛋白装配成稳定的微管,同时抑制其解聚,从而抑制细胞的有丝分裂,最终导致肿瘤细胞的死亡,具有较高的抗肿瘤活性。多西他赛对乳腺癌、非小细胞肺癌、前列腺癌、宫颈癌、卵巢癌、胃癌等都有良好的临床疗效。但多西他赛也能引起严重的毒副反应,如骨髓抑制、过敏反应、体液潴留、脱发、乏力、黏膜炎、关节痛或肌肉痛、低血压、胃肠道反应与恶心、呕吐或腹泻等。
化疗是目前临床上治疗肿瘤原发病灶或转移灶的主要手段,但是化疗单一用药容易产生耐药性,不良反应大,而且疗效不够理想[3],因此,肿瘤的治疗已从最初的单一用药向联合用药方向转变,从机制的互补、作用的协同、不良反应的减轻等方面发挥作用[4]。其中,靶向药物与化疗药物联用可降低化疗药物的剂量,从而降低其毒副作用,因此在肿瘤的治疗上有广泛的应用前景。然而当两种不同作用机制的药物联合应用时,其给药剂量及给药顺序的不同对药效的发挥均有极大的影响,有些血管生成抑制剂与化疗或放疗联合应用时具有协同作用[5, 6],但也有些联合应用时却具有拮抗作用[7]。因此,如何合理地联合血管生成抑制剂和化疗药物,确立最佳联合给药方案和用药时机,从而最大限度地发挥药物的治疗作用是目前探索改善肿瘤治疗手段切实可行的研究方向[8]。本文对多肽AP25与多西他赛联合给药治疗乳腺癌进行研究,结合金氏公式,评价多肽AP25与化药联用的效果及其抑制作用与给药剂量的相关性,为开发AP25为抗肿瘤药物提供依据。
1 材料与仪器 1.1 实验动物和细胞株BALB/c裸鼠,SPF级,上海西普尔-必凯实验动物有限公司。实验动物质量合格证许可证号:SCXK(沪)2013-0016,合格证号:0132238。日龄:35~40 d,体质量:18~22 g,♀,每 组动物数:阴性对照组12只,其他每组6只。小鼠乳腺癌MDA-MB-231细胞株购自中科院上海细胞所。
1.2 主要药物与试剂McCoy’s 5A培养基(美国Gibco公司);胰蛋白酶(美国Gibco公司);胎牛血清(FBS);青霉素、链霉素(美国Sciencell公司);AP25(本课题组,批号121128);多西他赛(江苏恒瑞制药有限公司,批号H20020543);生理盐水(山东鲁抗辰欣药业有限公司,批号1207117102)。
1.3 主要仪器CO2培养箱,恒温培养箱,倒置显微镜,Canon照相机。
2 方法 2.1 MDA-MB-231乳腺癌细胞的培养从液氮罐中取出一支MDA-MB-231乳腺癌细胞冻存管,于37 ℃水浴中快速融化,无菌条件下滴入15 mL的离心管离心,在培养瓶中加入10 mL 含10% 的FBS的McCoy’s 5A培养基,将离心后的细胞用1 mL 培养基重悬滴入细胞培养瓶中,置37 ℃,5 % CO2培养箱中培养。
2.2 MDA-MB-231乳腺癌细胞裸鼠皮下移植瘤模型的建立将乳腺癌MDA-MB-231细胞株进行传代培养,当获得大量培养细胞后,收集并接种于裸鼠右侧腋下,接种量为每鼠1×106个细胞/0.1 mL,待肿瘤体积达75~100 mm3时进行分组、给药。给药期间,观察并记录裸鼠状态,测量裸鼠体重,并用游标卡尺测量瘤体大小,体重和瘤体积每2 d测量1次。将动物随机分为8组,阴性组12只,其他组每组6只。给药21 d,以尾静脉注射方式给药,阴性组给生理盐水,多西他赛组分别注10、5 mg·kg-1剂量的多西他赛,AP25组分别注射20、10 mg·kg-1剂量的AP25,联合给药组先注射多西他赛,然后再注射AP25。给药体积为每只0.2 mL,给药方案见Tab1。d 22时颈椎脱臼处死裸鼠,剥离瘤块,称重并计算抑瘤率。
| Group | Drug | Dose/mg·kg-1 | Days/mouse, i.v. |
| G1 | Normal saline | 21 days, 0.2 mL·d-1 | |
| G2 | Docetaxel | 10 | d 1, 2, 3, 3 times |
| G3 | Docetaxel | 5 | d 1, 2, 3, 3 times |
| G4 | AP25 | 20 | 21 days, 0.2 mL·d-1 |
| G5 | AP25 | 10 | 21 days, 0.2 mL·d-1 |
| G6 | Docetaxel | 10 | d 1, 2, 3,3 times |
| AP25 | 20 | 21 days, 0.2 mL·d-1 | |
| G7 | Docetaxel | 5 | d 1, 2, 3, 3 times |
| AP25 | 10 | 21 days, 0.2 mL·d-1 | |
| G8 | Docetaxel | 5 | d 1, 2, 3, 3 times |
| AP25 | 20 | 21 days, 0.2 mL·d-1 |
剂量设置:多西他赛剂量10 mg·kg-1由临床上药物有效剂量通过人与小鼠剂量换算公式计算得来;多西他赛剂量 5 mg·kg-1由10 mg·kg-1减半得来;通过本课题组前期体内外实验摸索,确定多西他赛(10 mg·kg-1)及多西他赛(5 mg·kg-1)为阳性对照。AP25剂量20、10 mg·kg-1由本课题组前期体内外实验摸索得来,作为本次实验的给药组。
2.3 肿瘤测量及抗肿瘤活性评价方法 2.3.1 肿瘤体积及抑制率肿瘤体积(tumor volume,TV)的计算公式为:TV= 1/2×a×b2,其中 a、b 分别表示长宽。根据测量的结果计算出相对肿瘤体积(relative tumor volume,RTV),计算公式为:RTV=Vt/V0。其中 V0为分笼给药时(即d0)测量所得肿瘤体积,Vt为每次测量时的肿瘤体积。
肿瘤体积抑制率/%=(阴性对照组平均体积-给药组平均体积)/ 阴性对照组平均体积×100%。每2 d测一次瘤体积,根据体积抑制率可动态观察各给药组的抑瘤效果。
2.3.2 肿瘤瘤重及抑瘤率抑瘤率/%=(阴性对照组平均瘤重-给药组平均瘤重) / 阴性对照组平均瘤重×100%。给药21 d后,完成治疗。对裸鼠剖瘤,并对剖出的肿瘤进行称重。然后计算出瘤重抑瘤率。
2.3.3 裸鼠体重和存活情况每2 d测1次裸鼠体重,观察裸鼠体重变化情况和生长状态,旨在检测药物的毒副作用。
2.4 联合作用评价采用金氏公式评价两种药物的联合作用。金氏公式表达式:
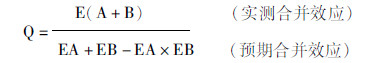
EA、EB分别表示A和B两种药物单独用药的效应;E(A+ B)表示药物A和药物B联合用药的效应。通过判读Q值来评价二药物在联合使用后的治疗效果是否优于单独给药。如果Q在0.85-1.15之间为单纯相加,Q > 1.15为协同作用,Q < 0.85为拮抗作用。
2.5 免疫组化检测治疗完成后,脱椎处死裸鼠,剖瘤。每组取2-3个样本进行免疫组化。瘤组织置于4%甲醛中固定,经脱水、透明、渗蜡、石蜡包埋,用CD31抗体进行染色,观察肿瘤组织中微血管密度(MVD)。微血管密度的计数:肿瘤组织中的微血管定位在血管内皮细胞的细胞膜和细胞质,呈棕黄色,阳性定位在血管内皮细胞的细胞膜和细胞质。根据Weidner法[9]进行MVD计数,首先在低倍镜(×100)下观察整张切片,找到肿瘤组织中微血管较密集的区域,再在高倍镜(×200)下选择5个视野计数血管数,取其平均值作为此样本的MVD值。任何1个被染为棕黄色的内皮细胞或内皮细胞簇,只要与相邻的微血管、肿瘤细胞或其他结缔组织界限分明,都被认为是1个微血管,进行计数[10],管腔大于8个细胞或带有较厚肌层的血管不计数。
2.6 统计学处理 采用SPSS 19.0软件中配对样品t检验分析(Paired-samples t test),结果以 ± s 表示。
± s 表示。
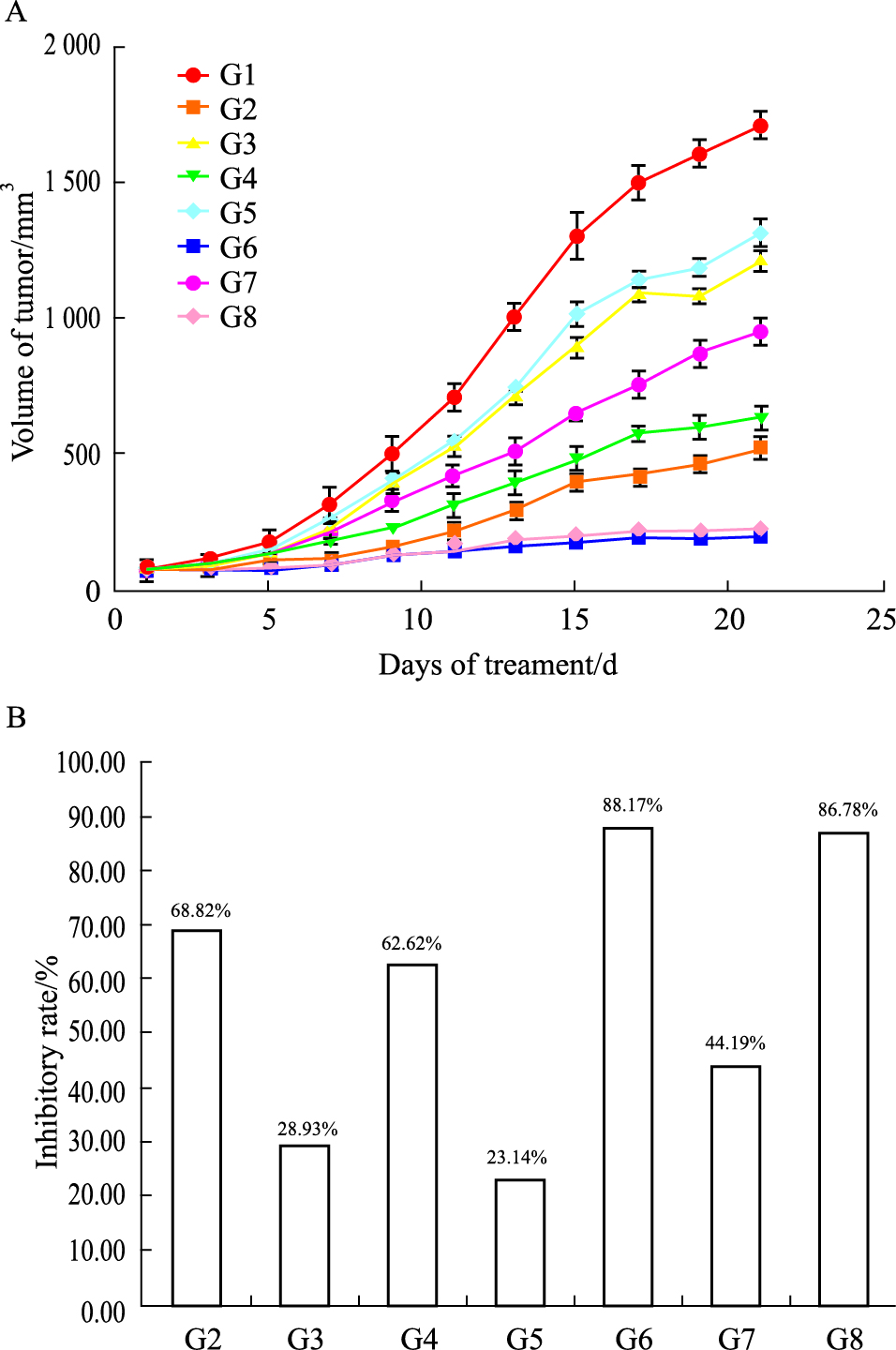
肿瘤体积变化及体积抑制率见Fig1-A、1-B,22 d剖瘤时所测的体积中,阴性组肿瘤体积为(1 722.42±46.89) mm3;单独给药治疗组G2(多西他赛10 mg·kg-1)、G3(多西他赛5 mg·kg-1)、G4(AP25 20 mg·kg-1)、G5(AP25 10 mg·kg-1)的肿瘤体积分别为(537.04±19.69) mm3、(1 224.05±27.94) mm3、(643.77±23.74) mm3、(1 323.75±39.77) mm3;联合给药组G6(多西他赛10 mg·kg-1+AP25 20 mg·kg-1)、G7(多西他赛5 mg·kg-1 + AP25 10 mg·kg-1)、G8(多西他赛5 mg·kg-1 + AP25 20 mg·kg-1)的肿瘤体积分别为(203.73±6.67) mm3、(961.18±20.34) mm3、(227.71±5.21) mm3。与阴性组相比,G2、G4、G6、G8治疗组肿瘤体积差异有显著性(P < 0.01);根据Fig1-B中的肿瘤体积动态抑制率变化看,G2、G4、G6、G8治疗组在7~21 d期间的抑瘤率比较明显,在给药后期尤其明显。
|
| Fig 1 Tumor volume and inhibition rate A: Tumor volume;B: Inhibition rate on d21 according to tumor volume. G1: normal saline; G2: Docetaxel (10 mg·kg-1); G3: Docetaxel (5 mg·kg-1); G4: AP25: (20 mg·kg-1); G5: AP25 (10 mg·kg-1); G6: Docetaxel (10 mg·kg-1) +AP25 (20 mg·kg-1); G7: Docetaxel (5 mg·kg-1) +AP25 (10 mg·kg-1); G8: Docetaxel (5 mg·kg-1) +AP25 (20 mg·kg-1). |
阴性组瘤重为(1.50±0.11) g,联合给药组瘤重均明显小于阴性组(P < 0.01),分别为G6组(0.17±0.05) g、G7组(0.76±0.12) g、G8组( 0.19±0.06) g。与阴性组相比,联合给药组肿瘤较小,且中心有较大面积坏死部分,表明瘤体新生血管生成受到抑制,供血不足,见Fig2。

|
| Fig 2 Photos of tumors at the end of the study indicate the therapeutic effects of docetaxel and AP25 on mice G1: Normal saline; G2: Docetaxel (10 mg·kg-1); G3: Docetaxel (5 mg·kg-1); G4: AP25 (mg·kg-1); G5: AP25 (10 mg·kg-1); G6: Docetaxel (10 mg·kg-1) + AP25 (20 mg·kg-1); G7: Docetaxel (mg·kg-1) +AP25 (10 mg·kg-1); G8: Docetaxel (5 mg·kg-1) +AP25 (20 mg·kg-1). |
据瘤重计算出的抑瘤率见Tab2,其中单独给药组多西他赛(10 mg·kg-1)和多西他赛(5 mg·kg-1)的抑瘤率分别是71.36%和32.83%,AP25(20 mg·kg-1)和AP25(10 mg·kg-1)的抑瘤率分别是62.05%和25.26%;联合给药组G6、G7、G8抑瘤率分别是88.58%、49.43%和87.69%。
| Group | Drug | Dose/mg·kg-1 | Tumor weight/g | Inhibition rate/% | MVD(CD31) |
| *P < 0.05,**P < 0.01 vs control group. | |||||
| G1 | Control | 1.50±0.11 | 25.53±6.63 | ||
| G2 | Docetaxel | 10 | 0.43±0.07** | 71.36 | 15.06±3.16** |
| G3 | Docetaxel | 5 | 1.01±0.16** | 32.83 | 18.62±4.04* |
| G4 | AP25 | 20 | 0.57±0.08** | 62.05 | 17.56±3.68** |
| G5 | AP25 | 10 | 1.12±0.27** | 25.26 | 19.79±3.33* |
| G6 | Docetaxel | 10 | 0.17±0.05** | 88.58 | 10.04±1.37** |
| AP25 | 20 | ||||
| G7 | Docetaxel | 5 | 0.76±0.12** | 49.43 | 17.74±2.85* |
| AP25 | 10 | ||||
| G8 | Docetaxel | 5 | 0.19±0.06** | 87.69 | 11.78±3.50** |
| AP25 | 20 | ||||
体重情况见Fig3,含多西他赛的治疗组G2、G3、G6、G7、G8小鼠体重明显下降且偏低,表明多西他赛在有效剂量下有很大的毒副作用;阴性组小鼠体重明显增加;AP25组小鼠体重略微减轻,表明多肽AP25无明显毒副作用。从动物存活情况看,所有组动物全部存活。

|
| Fig 3 Mice weight G1: Normal saline; G2: Docetaxel (10 mg·kg-1); G3: Docetaxel (5 mg·kg-1); G4: AP25 (20 mg·kg-1); G5: AP25 (10 mg·kg-1); G6: Docetaxel (10 mg·kg-1) + AP25 (20 mg·kg-1); G7: Docetaxel (5 mg·kg-1) +AP25 (10 mg·kg-1); G8: Docetaxel (5 mg·kg-1) +AP25 (20 mg·kg-1). |
金氏公式计算得到:多西他赛(10 mg·kg-1)与AP25(20 mg·kg-1)联合使用,0.85 < Q=0.99 < 1.15,联合作用为相加;多西他赛(5 mg·kg-1)与AP25(20 mg·kg-1)联合使用,Q=1.18 > 1.15,联合作用为协同。
3.5 免疫组化分析如(Tab2,Fig4)所示:阴性组MVD为25.53±6.63,AP25(20 mg·kg-1)、AP25(10 mg·kg-1)MVD分别为17.56±3.68、19.79±3.33,与阴性组对比,差异具有显著性,表明AP25在有效剂量下对肿瘤新生血管有明显抑制作用。在联合用药组中,多西他赛(mg·kg-1)联合AP25(20 mg·kg-1)组MVD为10.04±1.37,多西他赛(5 mg·kg-1)联合AP25(20 mg·kg-1)组MVD为11.78±3.50,抑制肿瘤血管效果好于多西他赛单独给药组和AP25单独给药组,进一步提示传统化药与血管生成抑制剂联用具有多靶点、多途径联合抗肿瘤的效果。

|
| Fig 4 Microvasculature of each histological grade using CD31 immunostaining(×200) G1: Normal saline; G2: Docetaxel (10 mg·kg-1); G3: Docetaxel (5 mg·kg-1); G4: AP25 (20 mg·kg-1); G5: AP25 (10 mg·kg-1); G6: Docetaxel (10 mg·kg-1) + AP25 (20 mg·kg-1); G7: Docetaxel (5 mg·kg-1) +AP25 (10 mg·kg-1); G8: Docetaxel (5 mg·kg-1) +AP25 (20 mg·kg-1). |
1972年,Folkman提出了著名的肿瘤新生血管学说,认为新生血管为肿瘤提供营养和氧气,并为肿瘤的转移提供通道,是肿瘤生长、浸润和转移的重要基础[11]。在癌症临床治疗上,血管生成抑制剂类药物与化疗药物联合应用非常普遍,很多文献报道,两者联合应用具有协同作用[12, 13, 14, 15, 16]。
实验结果表明,多肽AP25(20 mg·kg-1)与多西他赛(5 mg·kg-1)联合使用具有协同作用,二者联用可以明显提高抑制肿瘤生长的效果,而且可以降低多西他赛的用药剂量。这个结果可以为乳腺癌的临床合理用药提供一些建议,降低化疗药物用量,从而减少毒副反应,降低耐药性,减轻肿瘤患者的痛苦。
综合分析实验结果,多肽AP25与多西他赛联合使用达到协同作用的原因可能首先是两种药物的抗肿瘤作用机制不同,多西他赛(docetaxel)是以微管为靶点的抗肿瘤药物,属于细胞周期特异性药物,作用于M期,能促进微管异常聚合并保持其稳定,从而抑制细胞有丝分裂时纺锤体形成以及微管的其他功能,抑瘤效果明显;多肽AP25为整合素阻断剂类抗肿瘤多肽,作用靶点为血管内皮细胞表面的整合素αvβ3,整合素作为细胞与细胞、细胞与ECM黏附的重要受体,通过结合配体中的RGD序列介导细胞与ECM之间的相互作用,抑制内皮细胞迁移及肿瘤细胞的浸润、转移,进而影响肿瘤新生性血管系统。多肽AP25与多西他赛是两种具有完全不同作用机制的药物,两者联合使用,可以增强抑制肿瘤生长的效果,达到协同作用。其次,二种药物联用还能减少化药用量,降低化药毒性。多西他赛虽然具有明显的抗肿瘤效果,但作为细胞毒类的化疗药物,它也能引起严重的毒副反应,如骨髓抑制、过敏反应、体液潴留、脱发、乏力、黏膜炎、关节痛和肌肉痛、低血压、胃肠道反应与恶心、呕吐或腹泻等。而多肽AP25作为以整合素为靶点的抗肿瘤多肽,与多西他赛相比,细胞毒性明显降低(从实验中裸鼠的体重增长趋势即可看出)。因此两者联合使用,降低了多西他赛的用量,大幅度降低了化疗的毒副作用,提高了机体抵御肿瘤细胞的能力,最终提高了抗肿瘤疗效,达到协同作用。
其他还有很多因素可以影响化疗联合用药的抗肿瘤疗效,比如多肽AP25与多西他赛之间是否存在相互作用,从而提高各自的抗肿瘤疗效,或者二者合用是否与机体产生反应,从而提高联合用药的抗肿瘤药效,我们还需要做进一步的药代动力学研究和机制研究,从而为开发AP25为抗肿瘤药物奠定基础。
(致谢:本实验在中国药科大学多肽药物创制工程研究中心完成。感谢导师徐寒梅教授为本实验提供充足的资金支持和整体的思路指导;感谢胡加亮老师的精心指导;感谢何俊劲、郝静超、程昊冉、吴晓东同学的尽心协助。)
| [1] | 张晓娟, 王文静, 王晶晶, 等. 多肽AP25抗肿瘤活性研究 [J]. 中国药理学通报, 2013, 29 (9): 1225-9.Zhang X J, Wang W J, Wang J J, et al. Study on the activity of anti-tumor peptide AP25 [J]. Chin Pharmacol Bull, 2013, 29 (9):1225-9. |
| [2] | 张 弛, 杨永晶, 潘 丽, 等. 抗肿瘤多肽AP25体外活性研究 [J]. 中国药理学通报, 2012, 28 (10): 1375-8.Zhang C, Yang Y J, Pan L, et al. Study on the in vitro activity of anti-tumor peptide AP25 [J]. Chin Pharmacol Bull, 2012, 28 (10): 1375-8. |
| [3] | 彭 军. 抗肿瘤药物联合化疗新进展 [J]. 中国医院药学杂志, 2003, 23 (12): 754-6.Peng J. The new development of combination of anti-tumor drug and chemotherapy [J]. Chin J Hospit Pharm, 2003, 23 (12): 754-6. |
| [4] | 岑 娟, 李运曼. 多药耐药肿瘤的联合用药 [J]. 国外医药抗生素分册, 2009, 30 (5): 224-8.Cen J, Li Y M. Combination therapy on mulidrug-resistance tumor [J]. World Notes Antib, 2209, 30 (5): 224-8. |
| [5] | Sucharita J M, Alexander B, George F A. Synergistic antiangiogenic effects of stathmin inhibition and taxol exposure [J]. Mol Cancer Res, 2007, 5 (8): 773-82. |
| [6] | Teresa T, Natalie J S, Daniel L G. Investigation of two dosing schedules of vandetanib (ZD6474), an inhibitor of vascular endothelial growth factor receptor and epidermal growth factor receptor signaling, in combination with Irinotecan in a human colon cancer xenograft model [J]. Clin Cancer Res, 2007, 13 (21): 6450-8. |
| [7] | An C, Pieter W, Judith J. Antiangiogenic compounds interfere with chemotherapy of brain tumors due to vessel normalization [J]. Mol Cancer Ther, 2008, 7 (1): 71-8. |
| [8] | 徐端正. 药物联合作用评价 [J]. 生理科学进展, 1992, 23 (3): 248-53.Xu D Z. The evaluation of combination of drugs [J]. Prog Physiol Sci, 1992, 23 (3): 248-53. |
| [9] | Weidner N, Semple J P, Welch W R, et al. Tumor angiogenesis and metastas is correlation in invasive breast carcinoma [J]. N Engl J Med, 1991, 324 (1): 1-8. |
| [10] | 白丽淼, 黄晓峰, 徐寒梅. 人结肠癌HT-29移植瘤不同生长阶段微血管密度及相关因子的表达研究[J]. 中国药理学通报, 2014, 30 (6):796-800. Bai L M, Huang X F, Xu H M. Investigation of microvessel density and related factors expression for xenografts tumor of HT29 cells in nude mice at different growth stage [J]. Chin Pharmacol Bull, 2014, 30 (6): 796-800. |
| [11] | Folkman J. Anti-angiogenesis: new concept for therapy of solid tumors [J]. Ann Surg, 1972, 175: 409-16. |
| [12] | Zhuang H Q, Yuan Z Y. Process in the mechanisms of endostain combined with radiotherapy [J]. Cancer Lett, 2209, 282: 9-13. |
| [13] | Matsui H, Suzuka K. Combination chemotherapy with Methotrexate, etoposide and actinomycin D for high-risk gestational trophoblasic tumors [J]. Gynecol Oncol, 2000, 78: 28-31. |
| [14] | De G, Giovanni R, Michele A. Phase Ⅱstudy of Oxaliplatin and Gemcitabine salvage chemotherapy in patients with Cisplatin refractory nonseminomatous germ sell tumor [J]. Ugo Europ Urol, 2006, 50: 1032-9. |
| [15] | Wang S, An R F, Han X B, Combination chemotherapy with 5-fluo-rouracil, Methotrexate and etoposide for patients with high-risk gestational trophoblasic tumors: A report based on our 11-year clinical experiences [J]. Gynecol Oncol, 2006, 103: 1105-8. |
| [16] | Grundy R G. Primary postoperative chemotherapy without radiotherapy for treatment of brain tumors other than ependymoma in children under 3 years: Results of the first UKCCSG/SIOP CNS 9204 trial [J]. Eur J Cancer, 2010, 46 (1): 120-33. |
