


2. 中南大学临床药理研究所 湖南省遗传药理学重点实验室, 湖南 长沙 410078;
3. 湖南省分子靶标新药研究协同创新中心, 湖南 衡阳 421001
2. Institute of Clinical Pharmacology, Hunan Key Laboratory of Pharmacogenetics, Central South University, Changsha 410078, China;
3. Hunan Province Cooperation Innovation Center for Molecular Target New Drug Study, Hengyang Hunan 421001, China
糖尿病是一种非常常见的代谢型疾病,具有多种并发症,其中糖尿病脑病是糖尿病发生过程中一种主要的中枢神经系统并发症,包含认知障碍和大脑的神经生理及结构的改变[1, 2],严重危害人民的身心健康。其发病机制尚不十分明确,近年来发现脑源性神经营养因子(brain-derived neurotrophic factor,BDNF)、诱导型一氧化氮合酶(inducible nitric oxide synthase,iNOS)和氧化应激可能与糖尿病脑病的发生密切相关[3, 4, 5]。此外,胆碱能神经元中乙酰胆碱含量的降低能够促使糖尿病脑病的发生[6]。
大黄酚(chrysophanol,CHR)是蓼科植物掌叶大黄中的主要有效成分。以往的研究发现,它对Aβ25-35诱导的阿尔茨海默病模型大鼠学习记忆具有明显的神经保护作用[7]。同时,大黄酚对大鼠全脑缺血/再灌注损伤引起的学习记忆障碍也具有保护作用[8]。然而,大黄酚对糖尿病脑病是否具有神经保护作用以及其具体的分子机制,目前尚未见报道。因此,本研究通过探讨大黄酚对糖尿病脑病的神经保护作用及机制,为临床上治疗糖尿病脑病提供理论指导。
1 材料与方法 1.1 动物、主要试剂和仪器成年3月龄♂ Wistar大鼠(n=48,300~350 g),由中南大学实验动物部提供。STZ(美国Sigma公司)。大黄酚(南京清泽医药科技开发有限公司,实验前用N,N-二甲基甲酰胺,吐温-80和生理盐水按照1∶1∶1的比例溶解)。盐酸多奈哌齐片(中国卫材药业)。糖过氧化物酶诊断试剂盒(印度Span Diagnostic)。胆碱酯酶(AChE)和胆碱乙酰基转移酶(ChAT)活性检测试剂盒(南京建成生物技术研究所)。iNOS活性检测试剂盒(江苏碧云天生物技术研究所)。BDNF活性检测试剂盒(美国Promega)。Centrifuge 5810R低温高速离心机(德国Eppendorf),酶标仪(南京德铁)。
1.2 糖尿病大鼠模型制作及药物干预随机选取48只Wistar大鼠,单次腹腔注射链脲霉素(STZ,剂量65 mg·kg-1,溶剂0.1 mol·L-1柠檬酸钠缓冲液),其余8只大鼠给予等剂量柠檬酸钠缓冲液腹腔注射作为对照组。给予STZ 72 h之后,使用糖过氧化物酶诊断试剂盒检测血糖,快速血糖浓度大于2 500 mg·L-1认为糖尿病模型制作成功,可以进行下一步实验。本实验分为如下6组,每组8只:(1) 对照组(Con);(2)模型组(DM);(3)低剂量治疗组(CHR 0.014);(4)中剂量治疗组(CHR 0.07);(5)高剂量治疗组(CHR 0.35);(6)阳性对照组(Don)。其中模型组中给予等量的生理盐水作为对照,大黄酚以腹腔注射方式分别按照0.014、0.07和0.35 mg·kg-1给药,多奈哌齐也是腹腔注射给药(1 mg·kg-1),1d 1次,连续给药21 d。各组实验动物每周测体重和血糖。给药结束后,进行后续的水迷宫实验。
各实验组给药21 d后,采用Morris水迷宫实验考察各组实验动物的空间学习记忆能力,参照以前实验方法,并作修改[8]。实验d 1将大鼠放入水中自由游泳2 min,水迷宫里未放平台。d 2~4为定位航行实验,记录各组实验动物的逃逸潜伏期(找到平台所需的时间)。d 5为空间探索实验,记录各组实验动物在60s内穿梭平台的次数和位于平台所在象限内(目标象限)探索时间。
1.4 AChE、ChAT、iNOS、CAT、SOD和GSH-PX活性及BDNF浓度测定各实验组动物在麻醉状态下断头迅速剥离海马,按照试剂盒说明书测定海马组织中AChE、ChAT、iNOS、CAT、SOD和GSH-PX活性及BDNF浓度。
1.5 统计学分析实验结果均以 ± s表示,使用单因素方差分析(One-Way ANOVA)进行统计学分析。
± s表示,使用单因素方差分析(One-Way ANOVA)进行统计学分析。
给予大黄酚治疗21 d后,我们首先探索大黄酚对糖尿病大鼠模型体重和血糖的影响。Tab1的研究结果表明,与正常对照组比较,STZ诱导的糖尿病大鼠模型的体重明显减少(P<0.01)。而大黄酚治疗21 d后,糖尿病大鼠模型中体重减少的现象得到明显地逆转(P<0.01),且呈现剂量依赖性。与此同时,相比于正常对照组,糖尿病大鼠模型的血糖明显升高(P<0.01)。而不同剂量的大黄酚明显降低了糖尿病大鼠的血糖浓度(P<0.01)。大黄酚改善糖尿病大鼠模型的体重和血糖的作用与阳性对照药多奈哌齐的作用非常相似(P>0.05)。
( ± s , n=8) ± s , n=8) |
|||
| Treatment | Dose/mg·kg-1 | Body weight/g | Plasma glucose/10 mg·L-1 |
| Con | 331.25±3.66 | 119.25±2.25 | |
| DM | 116.25±2.98** | 589.15±2.19** | |
| CHR | 0.014 | 236.36±3.66## | 299.12±2.55## |
| CHR | 0.07 | 259.43±4.66## | 265.60±4.12## |
| CHR | 0.35 | 269.36±4.88## | 231.25±2.78## |
| **P<0.01 vs Con group; ##P<0.01 vs DM group. Con, control group; DM, diabetes group; CHR (0.014), chrysophanol (0.014 mg·kg-1)-treated group; CHR (0.07), chrysophanol (0.07 mg·kg-1)-treated group; CHR (0.35), CHR (0.35 mg·kg-1)-treated group. | |||
为了阐明大黄酚对糖尿病大鼠模型学习记忆功能的影响,我们使用了Morris水迷宫实验进行考察。 Fig1结果表明,糖尿病大鼠模型在d 1~4的实验中,逃逸潜伏期均比正常对照组明显增加(P<0.01)。同时,在d 5的空间探索实验时,模型组中穿梭平台的次数和在目标象限中探索的时间均比正常对照组明显缩短(P<0.01)。而大黄酚干预后,明显减少了逃逸潜伏期,增加了穿梭次数和在目标象限中探索的时间(P<0.01),且呈现剂量依赖性。其中0.35 mg·kg-1大黄酚改善糖尿病大鼠模型的学习记忆作用与阳性对照药多奈哌齐的作用非常相似(P>0.05)。

|
Fig 1
Effects of chrysophanol on escape latency (A), number of crossing platform (B) and percentage of time spent in target quadrant (C) on diabetic rats ( ± s , n=8)
**P<0.01 vs Con group; ##P<0.01 vs DM group. Con, control group; DM, diabetes group; CHR (0.014), chrysophanol (0.014 mg·kg-1)-treated group; CHR (0.07), chrysophanol (0.07 mg·kg-1)-treated group; CHR (0.35), CHR (0.35 mg·kg-1)-treated group; Don, donepezil (1 mg·kg-1)-treated group. ± s , n=8)
**P<0.01 vs Con group; ##P<0.01 vs DM group. Con, control group; DM, diabetes group; CHR (0.014), chrysophanol (0.014 mg·kg-1)-treated group; CHR (0.07), chrysophanol (0.07 mg·kg-1)-treated group; CHR (0.35), CHR (0.35 mg·kg-1)-treated group; Don, donepezil (1 mg·kg-1)-treated group.
|
AChE和ChAT是学习记忆功能调节中的两种关键酶,因此我们检测了不同实验组海马中AChE和ChAT的活性。Fig2的结果表明,糖尿病大鼠模型海马中AChE的活性明显高于正常对照组(P<0.01),而ChAT的活性却明显低于正常组(P<0.01)。不同剂量(0.014、0.07和0.35 mg·kg-1)大黄酚治疗后,海马中AChE的活性明显降低(P<0.01),同时ChAT的活性明显增高(P<0.01)。且0.35 mg·kg-1大黄酚改变糖尿病大鼠模型海马中AChE和ChAT活性的作用与阳性对照药多奈哌齐的作用非常相似(P>0.05)。

|
Fig 2
Effects of chrysophanol on AChE (A) and ChAT (B) in the hippocampus of diabetic rats ( ± s , n=8)
**P<0.01 vs Con group; ##P<0.01 vs DM group. Note see Fig 1. ± s , n=8)
**P<0.01 vs Con group; ##P<0.01 vs DM group. Note see Fig 1.
|
为了探索大黄酚对糖尿病大鼠模型海马中BDNF浓度的影响,我们使用ELISA法检测了不同实验组海马中BDNF的浓度。从Fig3可以看出,不同剂量(0.014、0.07和0.35 mg·kg-1)大黄酚干预后,海马中BDNF的浓度明显提高(P<0.01)。且0.35 mg·kg-1大黄酚改变糖尿病大鼠模型海马中BDNF浓度的作用与阳性对照药多奈哌齐的作用非常相似(P>0.05)。

|
Fig 3
Effects of chrysophanol on BDNF content in the hippocampus of diabetic rats ( ± s , n=8)
**P<0.01 vs Con group; ##P<0.01 vs DM group. Note see Fig 1 ± s , n=8)
**P<0.01 vs Con group; ##P<0.01 vs DM group. Note see Fig 1
|
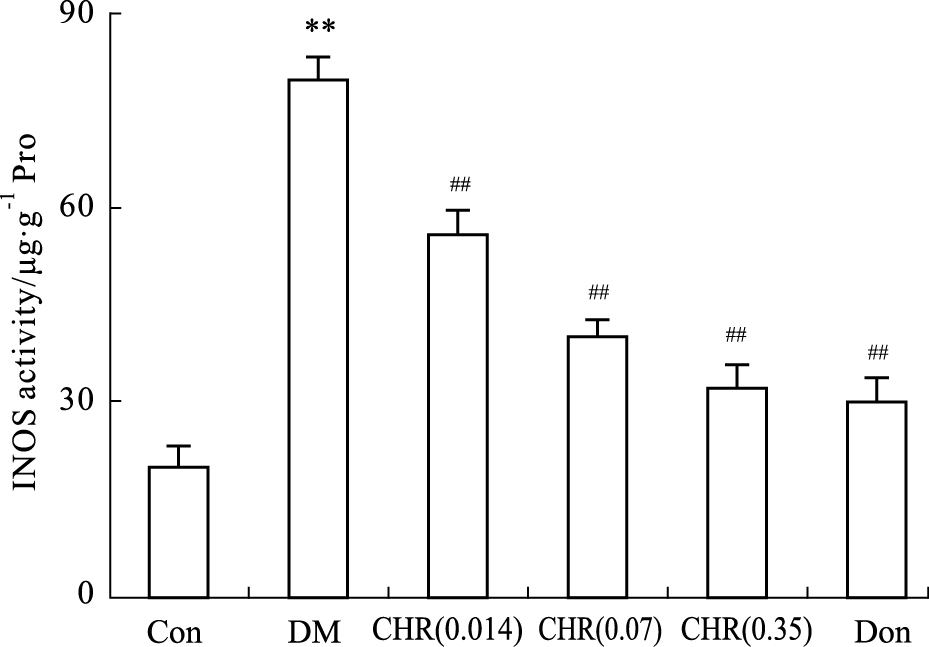
我们还探索了大黄酚对糖尿病大鼠模型海马中iNOS活性的影响。Fig4的结果表明,糖尿病 大鼠模型海马中iNOS的活性明显高于正常对照组(P<0.01)。而使用不同剂量(0.014、0.07和0.35 mg·kg-1)的大黄酚能够明显抑制模型组海马中iNOS的活性(P<0.01)。且这种抑制作用与阳性对照药多奈哌齐的作用非常相似(P>0.05)。
|
Fig 4
Effects of chrysophanol on iNOS activity in the hippocampus of diabetic rats ( ± s , n=8)
**P<0.01 vs Con group; ##P<0.01 vs DM group. Note see Fig 1. ± s , n=8)
**P<0.01 vs Con group; ##P<0.01 vs DM group. Note see Fig 1.
|
Fig5的结果表明,糖尿病脑病大鼠模型海马中抗氧化指标(包括CAT,SOD和GSH)活性均明显低于正常对照组(P<0.01)。而不同剂量(0.014、0.07和0.35 mg·kg-1)的大黄酚明显提高了CAT,SOD和GSH的活性(P<0.01)。且0.35 mg·kg-1大黄酚的抗氧化作用与阳性对照药多奈哌齐的作用非常相似(P>0.05)。

|
Fig 5
Effects of chrysophanol on the activities of CAT (A), SOD (B) and GSH-PX (C) in the hippocampus of diabetic rats ( ± s , n=8)
**P<0.01 vs Con group; ##P<0.01 vs DM group. Note see Fig 1. ± s , n=8)
**P<0.01 vs Con group; ##P<0.01 vs DM group. Note see Fig 1.
|
BDNF是神经营养因子中的重要成员。以往许多研究表明,BDNF不仅对胚胎神经元的发生、发育和存活具有重要的调节作用,而且对发育成熟的神经元功能的维持以及神经退行性疾病中细胞损伤具有重要的保护作用[3]。糖尿病脑病是一种以认知功能障碍为主要特点的神经退行性疾病,BDNF的减少与糖尿病脑病的发生发展密切相关。事实上,Nitta等[9]研究证实,4周龄使用STZ诱导的糖尿病大鼠皮层和海马中BDNF的表达均明显减少。这可能证实BDNF与糖尿病诱发的神经细胞凋亡密切相关。与以往的研究结果一致,我们当前的研究结果表明,糖尿病大鼠模型海马中BDNF的浓度明显低于正常对照组。而且不同剂量的大黄酚明显提高了糖尿病大鼠海马中BDNF的浓度,提示大黄酚对糖尿病脑病的神经保护作用可能与上调BDNF有关。
氧化应激在糖尿病脑病的发生发展过程中发挥着重要的作用。而活性氮在氧化应激的参与中扮演着重要角色。据报道,一氧化氮(NO)中过氧亚硝酸盐阴离子(OONO-)对细胞产生严重的氧化损害作用[10]。OONO-主要是NO与超氧阴离子(O-2)反应生成的。而合成NO的一种重要的酶是iNOS。Celik等[11]研究发现,糖尿病大鼠大脑iNOS活性增加,使NO增加,同时抗氧化酶SOD和CAT的活性明显降低,最终导致氧化应激引起的细胞损害明显加重。以往的研究也表明,通过下调iNOS表达和抑制氧化应激能够对糖尿病脑病产生明显的神经保护作用[11]。与以往的研究报道一致,我们当前的研究结果表明,糖尿病大鼠海马中iNOS的活性明显增加,同时抗氧化物酶(CAT、SOD和GSH-PX)的活 性均明显低于正常大鼠。而大黄酚干预后,明显抑制了糖尿病大鼠海马内iNOS的活性,同时增强了抗氧化物酶(CAT、SOD和GSH-PX)的活性。
综上,我们的研究结果表明,大黄酚对糖尿病脑病大鼠模型具有神经保护作用,并且这种保护作用可能是通过增强胆碱能神经元功能,上调BDNF,抑制iNOS的活性及抑制氧化应激来实现的。我们的研究结果将提示大黄酚可能作为治疗糖尿病脑病患者的新型药物。
| [1] | Somfai G M, Knippel B, Ruzicska E, et al. Soluble semicarbazide-sensitive amine oxidase (SSAO) activity is related to oxidative stress and subchronic inflammation in streptozotocin-induced diabetic rats[J]. Neurochem Int,2006, 48(8): 746-52. |
| [2] | Sehirli O, Tozan A, Omurtag G Z, et al. Protective effect of resveratrol against naphthalene-induced oxidative stress in mice[J]. Ecotoxicol Environ Saf, 2008, 71(1): 301-8. |
| [3] | 尹国平,陈 丽. 神经营养因子与糖尿病脑病[J].国际内分泌代谢杂志,2006, 26(2):119-44. Yin G P, Chen L. Neurotrophic factors and diabetic neuropathies in brain[J]. Intern J Endocrinol Metab,2006, 26(2): 119-44. |
| [4] | 陈艳瑜,魏倩萍,胡义平.姜黄素对糖尿病脑病大鼠氧化应激及海马iNOS表达的影响[J].第二军医大学学报,2010, 31(12):1300-4 Chen Y Y, Wei Q P, Hu Y P. Effect of curcumin on oxidative stress and hippocampus iNOS expression in diabetic encephalopathy rats[J]. Acad J Sec Mil Med Univ, 2010, 31(12):1300-4. |
| [5] | 马冬影,刘继平,吉薇薇,等.小檗碱对糖尿病脑病大鼠海马组织氧化应激及BDNF表达的影响[J]. 中药药理与临床,2012, 28(5):39-41. Ma D Y, Liu J P, Ji W W, et al. Effect of berberine on hippocampal tissue oxidative stress levels and BDNF expression in diabetic encephalopathy rats[J]. Pharmacol Clin Chin Mater Med, 2012, 28(5):39-41. |
| [6] | Wang C Y, Zheng W, Wang T, et al. Huperzine A activates Wnt/β-catenin signaling and enhances the nonamyloidogenic pathway in an Alzheimer transgenic mouse model[J]. Neuropsychopharmacology, 2011, 36(5): 1073-89. |
| [7] | 董晓华,张丹参.大黄酚对Aβ25-35所致AD大鼠学习记忆及LTP的影响[J]. 中国药理学通报,2009, 25(5):682-5 Dong X H, Zhang D S. Effects of chrysophanol on memory impairment and LTP in AD rats induced by Aβ25-35[J]. Chin Pharmacol Bull, 2009, 25(5):682-5. |
| [8] | 李 超,张丹参,赵晓倩,等. 三种大黄酚制剂改善脑缺血/再灌注小鼠记忆功能的实验筛选研究[J]. 中国药理学通报,2010, 26(12):1607-12. Li C, Zhang D S, Zhao X Q, et al. Experimental screening study of three chrysophanol formulations on learning and memory function of mice with cerebral ischemia reperfusion[J]. Chin Pharmacol Bull, 2010, 26(12):1607-12. |
| [9] | Nitta A, Murai R, Suzuki N, et al. Diabetic neuropathies in brain are induced by deficiency of BDNF[J]. Neurotoxicol Teratol, 2002, 24(5):695-701. |
| [10] | Hink U, Li H, Mollnau H, et al. Mechanisms underlying endothelial dysfunction in diabetes mellitus[J]. Cir Res, 2001, 88(2):E14-22. |
| [11] | Celik S, Erdogan S. Caffeic acid phenethyl ester (CAPE) protects brain against oxidative stress and inflammation induced by diabetes in rats[J]. Mol Cell Biochem, 2008, 312(1-2):39-46. |

