


2. 河北医科大学药理学教研室, 河北 石家庄 050017
2. Dept of Pharmacology, Hebei Medical University, Shijiazhuang 050017, China
肺动脉高压因其基础疾病不同,发病机制也不尽相同,但却有相似的组织病理学变化,如内膜纤维化、管壁增厚及局部血栓形成,最终导致肺循环血流动力学紊乱,肺动脉压力增高。目前认为,肺动脉高压发病的细胞与分子机制中肺血管内皮细胞特别是肺微血管内皮细胞(pulmonary microvascular endothelial cells,PMVECs)受损起着关键性作用[1]。PMVECs是肺组织的重要实质细胞,在肺损伤过程中,既是首位受损伤的靶细胞,又是活跃的炎症细胞和效应细胞,有着复杂的代谢功能,对肺循环相关疾病的发生、发展起着不可忽视的重要作用[2]。
研究资料表明,多种生物活性物质,特别是生物活性小分子的分泌或活性异常参与了急性肺损伤、肺动脉高压的病理进程[3]。Apelin作为一种新的血管活性多肽,在肺组织中和其受体APJ联合表达水平最高[4]。对肺动脉高压临床和动物模型的实验研究也表明Apelin/APJ系统参与了肺动脉高压发生发展[5]。Apelin除了具有多数舒血管活性物质所具有的功能外,还有调节免疫反应、抗细菌、抗病毒感染的功能,对内皮细胞功能的维护起着重要作用[6]。然而,Apelin在肺损伤中的作用和机制还远未明了,如Apelin/APJ系统在PMVECs炎性损伤中的动态变化如何,外源性给予Apelin能否保护PMVECs,是否可能改善各种肺动脉高压,从而作为新的治疗靶点,都值得进一步的探讨。因此,本课题首次从细胞水平出发,探讨了Apelin/APJ系统在脂多糖(LPS)诱导大鼠PMVECs损伤中的作用及可能机制,为进一步阐明Apelin与肺动脉高压的关系及其防治作用提供基础实验资料。
1 材料与方法 1.1 材料 1.1.1 动物Wistar ♂大鼠(100~150 g)用于原代培养PMVECs,由河北医科大学实验动物中心提供。
1.1.2 药品与试剂Apelin购自美国Santa Cruz公司,用无血清DMEM培养液溶解配制成10-3 mol·L-1的母液,-80℃保存,临用时用培养液稀释成所需浓度;LPS(Escherichia coli 055: B5)购自美国Sigma-Aldrich公司;DMEM培养基和胎牛血清购自美国Gibco公司;MTT、胰蛋白酶购自北京索来宝科技有限公司;PCNA、Akt、p-Akt抗体购自Abcam公司;β-actin抗体购自北京中杉金桥公司;IRDye 800、IRDye 700标记的二抗购自美国Rockland公司;Apelin、APJ上下游引物购自生工生物工程(上海)股份有限公司;TRIzol、M-MLV第一链合成系统购自美国Invitrogen公司;PCR Master Mix(2×) 购自美国Thermo公司;其他试剂均为国产分析纯。
1.1.3 实验仪器二氧化碳培养箱、HEALFORCE超净工作台,上海力申仪器公司;5412R低温离心机,德国Eppendorf公司;倒置显微镜、光学显微镜,日本Olympus公司;Floustar多功能微板分析仪,德国BMG公司;ND-1000紫外/可见光分光光度计,美国NanoDrop公司;Odyssey双色红外激光成像系统,Gene Company Limited;DYY-11型多用电泳仪、DYC-Z22A型电泳槽,北京六一仪器厂;凝胶成像仪,美国Thermo Forma公司。
1.2 方法 1.2.1 PMVECs培养与鉴定采用组织块种植法原代培养[7, 8]:大鼠腹腔注射3 000 U肝素钠并麻醉后,无菌环境下从右心室注入D-Hanks液对心肺进行灌注,取出肺组织,剪去肺表面的脏层胸膜,剪下肺表面1~3 mm深的肺外缘组织,清洗后将其剪成约1 mm3大小的组织块,均匀接种到25 cm2一次性无菌塑料培养瓶内,加事先配制好的DMEM培养液(含20%胎牛血清、100 kU·L-1青霉素、100 kU·L-1链霉素、50 μg·L-1 VEGF、90 kU·L-1肝素钠)约1.5 mL于培养瓶内,以刚好浸没组织块为宜,避免组织块漂浮。于培养箱中静置培养,每天换液1次以去除血细胞。贴壁60 h时,轻轻去除组织块,更换培养液,继续培养。每3 d换液1次,直至瓶底细胞基本汇合后,传代培养。运用镜下观察、机械刮除及差速消化法进行纯化,去除成纤维细胞及平滑肌细胞等混杂细胞。VIII因子相关抗原免疫细胞化学染色进行鉴定。
1.2.2 细胞分组与处理取对数生长期的PMVECs消化分离,并制备合适密度的细胞悬液,接种于96孔板或培养瓶中,用含10%胎牛血清的DMEM培养液培养1~2 d至细胞融合达80%左右时,用含0.1%胎牛血清培养液培养24 h作同步化处理。然后随机分为LPS(10 mg·L-1)处理不同时间组、Apelin不同浓度组,用于不同指标的检测。其它实验中,另取上述同步化的细胞随机分为对照组、LPS(10 mg·L-1)组、Apelin(10-9、10-8 mol·L-1)组:对照组加入等体积的0.1%胎牛血清培养液处理,Apelin组先用不同浓度Apelin预处理,2 h后加入终浓度为10 mg·L-1的LPS刺激细胞24 h,检测PMVECs活力、PCNA蛋白表达以及Akt的磷酸化水平。
1.2.3 MTT法检测细胞活力细胞悬液以适当的密度接种于96孔板中,每孔200 μL,培养24 h使细胞完全贴壁。细胞生长同步化,按“1.2.2 ”方法分组并接受不同处理,每组设6个平行孔。① 在LPS、Apelin作用不同时间对PMVECs影响的实验中,将同步化的细胞随机分为LPS(10 mg·L-1)、Apelin(10-8 mol·L-1)处理0、3、6、12、24、48 h组,各处理组在时间点到达后每孔加入20 μL MTT溶液(5 g·L-1),置培养箱中继续培养4 h,然后吸弃各孔上清液终止培养,每孔加入200 μL二甲基亚砜(DMSO)溶液溶解紫色结晶,室温条件下轻轻震荡10 min,置Floustar多功能微板分析仪上,于490 nm波长条件下测定各孔光密度值(OD值);② 在观察Apelin不同浓度对细胞活力的影响实验中,各组在加入终浓度为10-10、10-9、10-8、10-7、10-6 mol·L-1 Apelin后继续培养24 h,然后按上述方法加入MTT进行测定;③ 在观察Apelin对LPS诱导的PMVECs损伤的影响实验中,同步化的细胞先加入不同浓度的Apelin预处理,2 h后加入终浓度为10 mg·L-1的LPS处理细胞24 h,然后按上述方法加入MTT进行测定。
1.2.4 RT-PCR实验将生长良好的PMVECs按“1.2.2 ”方法分组,同步化的细胞经LPS处理不同时间后,收集细胞,采用TRIzol一步法抽提细胞总RNA,采用ND-1000紫外/可见光分光光度计进行RNA定量。用M-MLV第一链合成系统试剂盒合成cDNA,产物用PCR Master Mix(2×)系统试剂盒进行PCR 扩增。Apelin、APJ以及β-actin的引物序列见Tab1。PCR 反应条件为:94 ℃ 2 s,94 ℃ 15 s,55 ℃ 30 s,72 ℃ 40 s,72 ℃ 5 min,共35个循环。取PCR产物4 μL,直接上样,进行10 g·L-1琼脂糖凝胶电泳,100 V恒压电泳,20~40 min,Gold view显色,凝胶成像系统观察扩增产物条带的大小及亮度,使用Biocapture系统成像,拍照,Bio1D软件进行图像分析,测定产物条带的灰度值,计算目标产物与β-actin的比值,作为各扩增产物mRNA的相对表达量。
| Gene | Forward primer sequence | Reverse primer sequence | Product size/bp |
| Apelin | 5′-TGCTCTGGCTCTC CTTGACT-3′ | 5′-ATGGGTCCCTTAT GGGAGAG-3′ | 190 |
| APJ | 5′-TTCCTTCTAGGCA CCACAGG-3′ | 5′-CTGTTTTCCGGGAT GTCAGT-3′ | 413 |
| β-actin | 5′-CCAAGGCCAACC GCGAGAAGATGAC-3′ | 5′-AGGGTACATGGTG GTGGCGCCAGAC-3′ | 587 |
将生长良好的PMVECs按“1.2.2 ”方法分组,各组经LPS处理后,收集细胞,加入RIPA细胞裂解液裂解细胞,提取蛋白,使用ND-1000紫外/可见光分光光度计进行蛋白定量。等量蛋白(40 μg)上样,SDS聚丙烯酰胺凝胶电泳分离,电转至PVDF膜上(4℃,2 h),室温下含50 g·L-1脱脂奶粉的TBST封闭1 h,加入一抗(β-actin、PCNA、Akt、p-Akt),4℃过夜,次日TBST液洗膜后,加入相应二抗(1 ∶5 000稀释),37℃,1 h。TBST液洗膜3次,Odyssey 9120双色红外激光成像系统扫描PVDF膜并成像保存。PCNA蛋白的相对含量用其灰度值与β-actin 的灰度值的比值表示,Akt的磷酸化水平用p-Akt/Akt来表示。
1.2.6 统计方法采用SPSS 15.0软件进行数据分析,Origin 7.5软件进行图像处理。实验数据以 ± s表示,采用单因素方差分析,Dunnet t检验进行组间比较。
± s表示,采用单因素方差分析,Dunnet t检验进行组间比较。
采用组织贴块法并加以改良成功培养出大鼠PMVECs,接种后24 h发现组织块周围有较多细胞呈放射状贴壁生长(Fig1A)。去除组织块后,剩下的细胞继续培养3~5 d,形成细胞单层,呈梭形或多角形,排列紧密,汇合成片,呈典型的铺路鹅卵石状(Fig1B)。另外,我们采用VIII因子相关抗原免疫细胞化学染色进行鉴定,结果表明,约95%的细胞表现为VIII因子相关抗原表达阳性,高倍镜下可见胞质呈棕黄色(Fig1C),结合我们的取材部位为肺外边缘组织,可以证实分离培养的细胞为PMVECs。

|
| Fig 1 Morphology and identification of rat PMVECs A: Morphology of primary rat PMVECs was observed after the explants had been cultured for 24 h; B: Primary rat PMVECs cultured for 3 days after removal of the explants; C: Identification of rat PMVECs was carried out by immunocytochemical stain of coagulation factor Ⅷ-related antigen. |
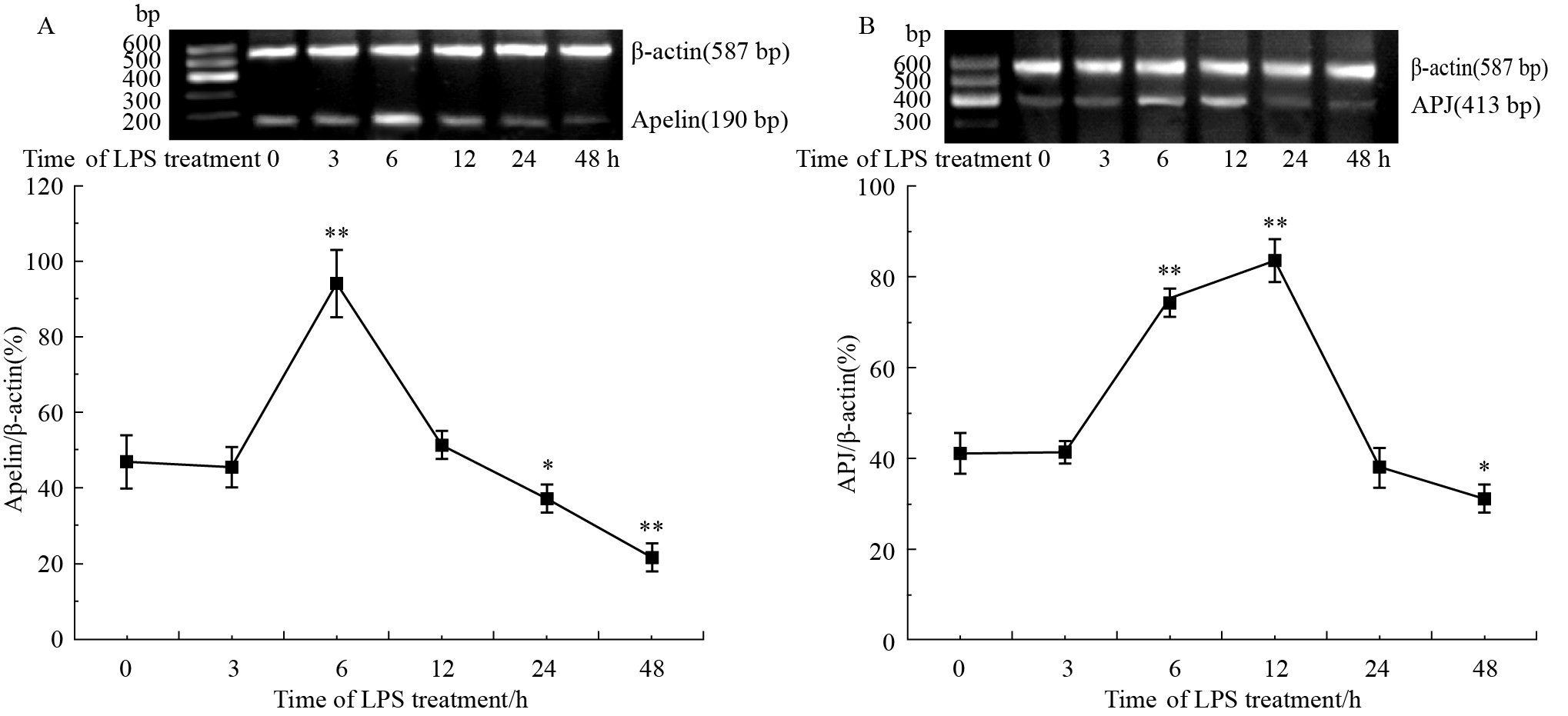
PCR产物经1.0%琼脂糖凝胶电泳后,可在相应位置见到清晰条带。分析结果表明,10 mg·L-1 LPS作用于PMVECs后,Apelin mRNA表达升高,在6 h达到高峰(P < 0.01);6 h后Apelin mRNA的表达呈不同程度地下降,在24 h和48 h Apelin mRNA的表达明显低于对照组(P < 0.05或P < 0.01,Fig2A)。另外,APJ mRNA的表达在LPS作用不同时间中也表现出先升高后降低的趋势。与对照组相比,APJ mRNA表达在6 h即明显升高(P < 0.01),在12 h达到高峰(P < 0.01),随后又明显下降,在48 h时,APJ mRNA的表达也明显低于对照组(P < 0.05,Fig2B)。提示Apelin/ APJ系统可能参与了LPS诱导的大鼠PMVECs损伤。
|
Fig 2
Changes of mRNA expression of Apelin and APJ in rat PMVECs after LPS (10 mg·L-1) treatment for indicated durations( ± s,n=3)
*P<0.05, **P<0.01 vs control group (LPS 0 h). ± s,n=3)
*P<0.05, **P<0.01 vs control group (LPS 0 h).
|
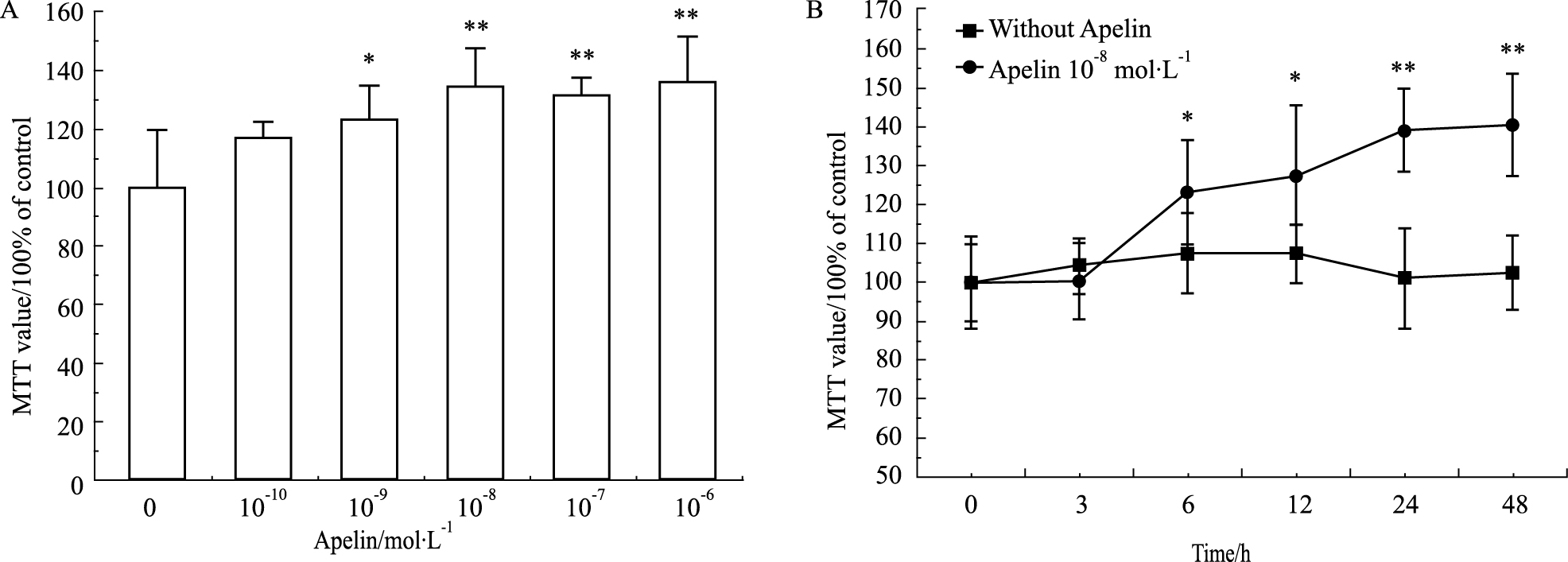
首先观察了不同浓度Apelin作用24 h对大鼠PMVECs增殖的影响,结果表明,与对照组相比,10-10 mol·L-1 Apelin对大鼠PMVECs增殖没有明显影响,随着浓度增加,10-9、10-8、10-7、10-6 mol·L-1 Apelin明显促进了大鼠PMVECs增殖(P < 0.05或P < 0.01,Fig3A)。但Apelin浓度超过10-8 mol·L-1并没有表现出更强的促增殖作用。随后,我们观察了10-8 mol·L-1 Apelin作用不同时间对大鼠PMVECs增殖的影响,结果表明,与对照组(Apelin 0 h)相比,Apelin作用6~48 h明显诱导细胞增殖(P < 0.05或P < 0.01,Fig3B)。
|
Fig 3
Effect of Apelin on proliferation of rat PMVECs examined by MTT assay( ± s,n=3)
A: Effect of Apelin (10-10, 10-9, 10-8, 10-7, 10-6 mol·L-1) on the proliferation of rat PMVECs; B: The proliferation of rat PMVECs was detected after Apelin (10-8 mol·L-1) treatment for indicated durations. *P<0.05, **P<0.01 vs control group (without LPS treatment). ± s,n=3)
A: Effect of Apelin (10-10, 10-9, 10-8, 10-7, 10-6 mol·L-1) on the proliferation of rat PMVECs; B: The proliferation of rat PMVECs was detected after Apelin (10-8 mol·L-1) treatment for indicated durations. *P<0.05, **P<0.01 vs control group (without LPS treatment).
|
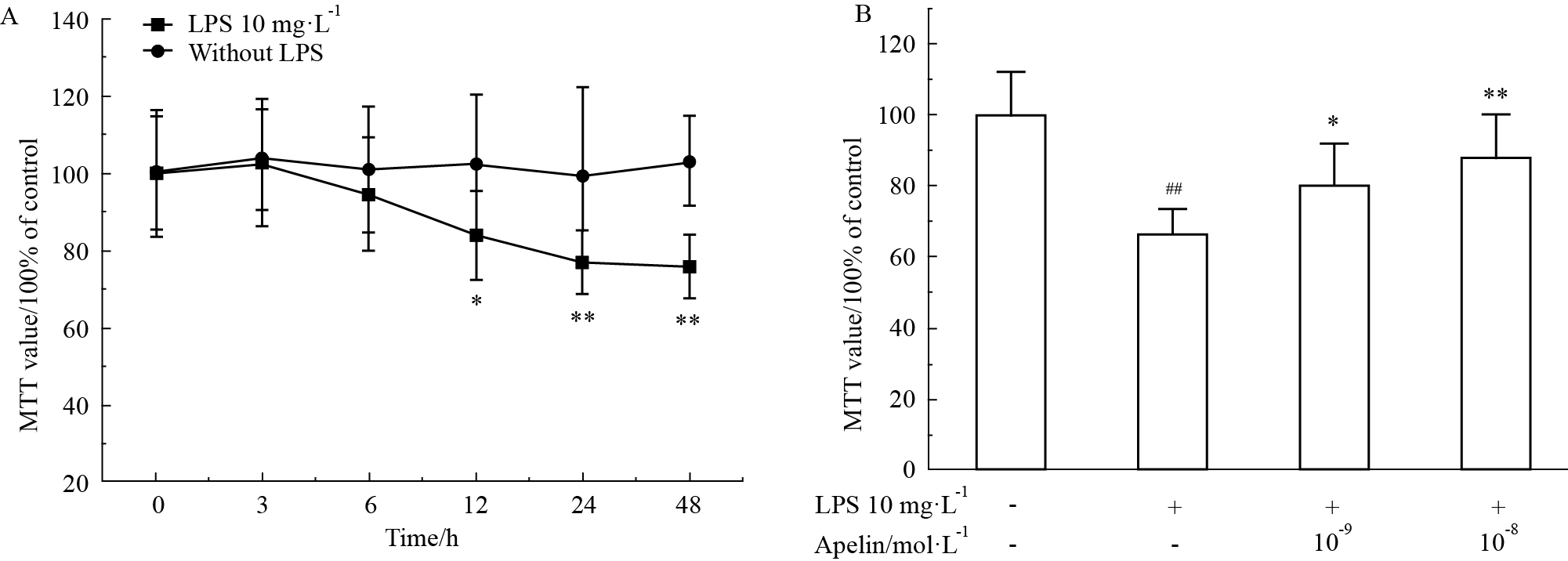
首先观察了10 mg·L-1 LPS作用不同时间对大鼠PMVECs生长的影响,结果表明,与对照组(LPS 0 h)相比,10 mg·L-1 LPS作用12 h即开始明显抑制细胞生长(P < 0.05),随着作用时间的延长(24、48 h),细胞生长进一步受到抑制(P < 0.01,Fig4A)。另外,我们还观察了Apelin (10-9、10-8 mol·L-1)对LPS作用24 h诱导的PMVECs损伤的影响,结果表明,10-9、10-8 mol·L-1 Apelin对LPS导致的细胞损伤有不同程度的改善(与LPS组相比,P < 0.05或P < 0.01,Fig4B)。
|
Fig 4
Injury of LPS on rat PMVECs and intervention effect of Apelin( ±s,n=3)
A: The injury of rat PMVECs was detected after LPS (10 mg·L-1) treatment for indicated durations. *P<0.05, **P<0.01 vs control group (LPS 0 h); B: Apelin relieved the LPS-induced cell injury. ##P<0.01 vs control group; *P<0.05, **P<0.01 vs LPS alone group. ±s,n=3)
A: The injury of rat PMVECs was detected after LPS (10 mg·L-1) treatment for indicated durations. *P<0.05, **P<0.01 vs control group (LPS 0 h); B: Apelin relieved the LPS-induced cell injury. ##P<0.01 vs control group; *P<0.05, **P<0.01 vs LPS alone group.
|
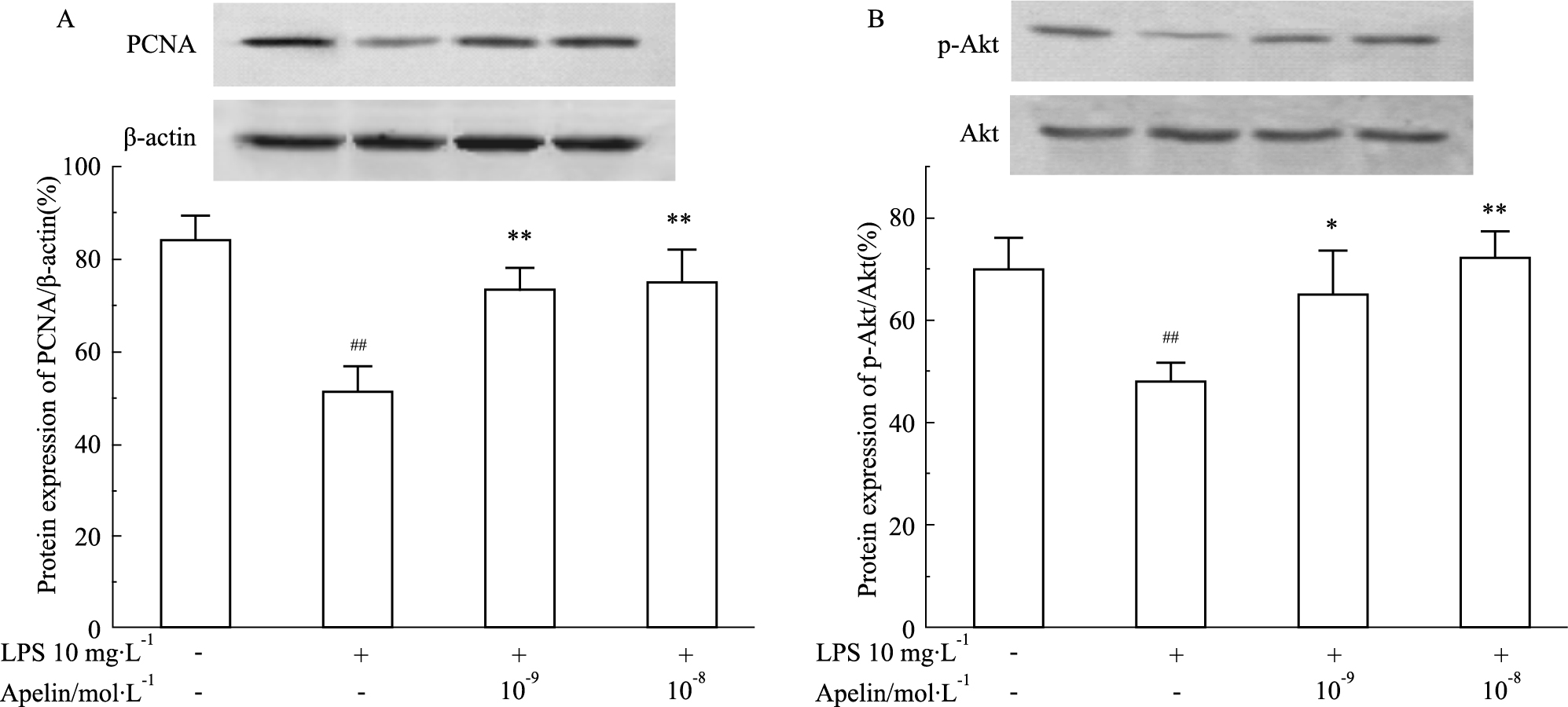
PCNA表达的高低反映了细胞的增殖能力。Western blot结果显示,与对照组相比,LPS作用24h明显降低了PMVECs中PCNA蛋白表达(P < 0.01),也明显抑制了Akt的磷酸化水平(P < 0.01)。而Apelin (10-9、10-8 mol·L-1) 预处理均明显干预了LPS诱导的PCNA蛋白表达及Akt磷酸化水平的降低(P < 0.05或P < 0.01,Fig5)。
|
Fig 5
Effect of LPS on the protein expression of PCNA and the phosphorylation of Akt and the intervention effect of Apelin( ±s,n=3)
A: The protein expression of PCNA in different groups. The bar chart shows the semiquantitative analysis of the PCNA protein expression normalized to β-action; B: The phosphorylation of Akt in different groups. The extent of Akt phosphorylation was quantified as the relative protein expression of p-Akt/Akt.##P<0.01 vs control group; *P<0.05, ** P<0.01 vs LPS alone group. ±s,n=3)
A: The protein expression of PCNA in different groups. The bar chart shows the semiquantitative analysis of the PCNA protein expression normalized to β-action; B: The phosphorylation of Akt in different groups. The extent of Akt phosphorylation was quantified as the relative protein expression of p-Akt/Akt.##P<0.01 vs control group; *P<0.05, ** P<0.01 vs LPS alone group.
|
肺微血管与急性肺损伤、肺动脉高压等疾病的发病机制密切相关。而构成肺微血管的重要细胞PMVECs以紧密连接的方式内覆于肺血管腔表面,不仅参与凝血、血管再生以及血管通透性等过程,也是各种细胞因子和炎性因子的作用靶点,在肺损伤相关疾病的进程中起着关键作用[9]。本实验中,我们严格控制实验细节,成功培养大鼠PMVECs,并采用机械刮除法和局部消化法去除杂细胞,获得了较为理想的细胞来源。
众所周知,肺脏易受细菌、病毒等感染因素的侵袭,且肺部存在的反复感染与肺部疾病本身、肺动脉高压的发展密切相关。Apelin作为一种新的血管活性多肽,在肺组织中和APJ联合表达水平最高。令人感兴趣的是,Apelin除了类似于多数舒血管活性物质所具有的功能外,还有调节免疫反应、抗炎、抗病毒感染的功能。众多肺动脉高压临床和动物模型实验研究也表明,Apelin/APJ系统可能参与了肺动脉高压的发生发展。Goetze等[10]也发现动脉高压患者血浆Apelin水平明显低于正常对照组。因此,具有内源性保护作用的Apelin生成减少或代谢异常可能是导致肺循环稳态失衡的重要因素之一。在本实验中,我们观察了Apelin对大鼠PMVECs增殖的影响,结果表明,随着浓度增加,Apelin明显促进了大鼠PMVECs增殖。但Apelin浓度超过10-8 mol·L-1并没有表现出更强的促增殖作用。随后,我们观察了10-8 mol·L-1 Apelin作用不同时间对大鼠PMVECs增殖的影响,发现Apelin作用6~48 h能明显诱导大鼠PMVECs增殖。这些结果表明Apelin对内皮细胞功能的维护起着重要作用。
LPS作为革兰阴性杆菌外膜上的一种糖蛋白,是强烈的炎症启动因子,可导致组织细胞发生功能障碍、结构破坏乃至凋亡坏死等一系列病理改变[11]。LPS可直接或间接损伤PMVECs,形成肺水肿、低氧血症或肺动脉高压[12, 13],但涉及的机制仍需进一步阐明。本实验中我们观察了LPS作用不同时间PMVECs中Apelin、APJ mRNA表达的变化,发现二者mRNA的表达在LPS作用不同时间中表现出先升高后降低的趋势,可能是由于LPS在短时间内能够使Apelin、APJ mRNA表达水平呈代偿性上升,但随着作用时间延长,基因表达受到明显抑制。提示Apelin/APJ系统可能参与了LPS诱导的大鼠PMVECs损伤。接下来的MTT实验结果也表明,Apelin还不同程度地改善了LPS诱导的PMVECs细胞损伤。进一步提示,Apelin/APJ系统对于维护内皮细胞功能起着重要作用。
为深入探讨Apelin保护PMVECs的作用机制,本实验还观察了PCNA蛋白表达以及Akt信号通路在LPS诱导PMVECs损伤中的变化,以及Apelin对此的干预作用。PCNA是分子质量为36 ku的核蛋白,在调节DNA合成和细胞增殖方面起重要作用[14]。结果表明,Apelin对LPS诱导的PCNA蛋白表达的降低有明显的抑制作用,提示Apelin的PMVECs保护作用与升高PCNA蛋白表达有关。另外,Apelin能明显逆转LPS诱导的Akt磷酸化水平的降低,促进Akt磷酸化。据报道,PI3K/Akt信号通路的激活通过降低促凋亡基因的活性、上调抗凋亡基因的表达而在维护细胞功能方面发挥着关键作用。Akt是PI3K下游的直接靶蛋白,其磷酸化参与细胞活动的多种调节[15]。因此,Akt磷酸化通路可能是Apelin发挥微血管内皮细胞保护作用的机制之一。
综上所述,Apelin/APJ系统参与了LPS诱导的大鼠PMVECs损伤,Apelin对于维护PMVECs功能,干预LPS诱导的PMVECs损伤起着重要作用,可能与其激活Akt磷酸化通路有关。
(致谢:该实验主要在河北医科大学药理学教研室完成,感谢该室在实验技术和仪器设备上提供的帮助。)
| [1] | Krotova K, Patel J M, Block E R, Zharikov S. Hypoxic upregulation of arginase II in human lung endothelial cells[J]. Am J Physiol Cell Physiol, 2010, 299(6): C1541-8. |
| [2] | Figueroa X F, Chen C C, Campbell K P, Damon D N. Are voltage dependent ion channels involved in the endothelial cell control of vasomotor tone[J]? Am J Physiol Heart Circ Physiol, 2007, 293(9): H1371-83. |
| [3] | Tsushima K, King L S, Aggarwal N R, et al. Acute lung injury review[J]. Intern Med, 2009, 48(9): 621-30. |
| [4] | Sorhede W M, Magnusson C, Ahren B. The APJ receptor is expressed in pancreatic islets and its ligand, apelin, inhibits insulin secretion in mice[J]. Regul Pept, 2005, 131(1-3): 12-7. |
| [5] | Kim J. Apelin-APJ signaling: a potential therapeutic target for pulmonary arterial hypertension[J]. Mol Cells, 2014, 37(3): 196-201. |
| [6] | Andersen C U, Markvardsen L H, Hilberg O, Simonsen U. Pulmonary apelin levels and effects in rats with hypoxic pulmonary hypertension[J]. Respir Med, 2009, 103(11): 1663-71. |
| [7] | 时全星,孙 新,李 娟,等. 肺微血管内皮细胞的原代培养[J].现代生物医学进展,2010,10(19):3609-12. Shi Q X, Sun X, Li J, et al. Primary culture of pulmonary microvascular endothelial cells in rats[J]. Prog Mod Biomed, 2010,10(19):3609-12. |
| [8] | 王 艳, 汪 宁, 林辰雨. 脑微血管内皮细胞的原代培养方法概述[J]. 中国药理学通报, 2013, 29(2): 294-6. Wang Y,Wang N,Lin C Y. Overview of the methods of brain microvascular endothelial cells in primary culture[J]. Chin Pharmacol Bull, 2013, 29(2):294-6. |
| [9] | Kuebler W M. Inflammatory pathways and microvascular responses in the lung[J]. Pharmacol Rep, 2005, 57(Supp 1): 196-205. |
| [10] | Goetze J P, Rehfeld J F, Carlsen J, et al. Apelin: a new plasma marker of cardiopulmonary disease[J]. Regul Pept, 2006, 133(1-3): 134-8. |
| [11] | Chen H, Bai C, Wang X. The value of the lipopolysaccharide-induced acute lung injury model in respiratory medicine[J]. Expert Rev Respir Med, 2010, 4(6): 773-83. |
| [12] | Zhao Y I, Gorshkova I A, Berdyshev E, et al. Protection of LPS-induced murine acute lung injury by sphingosine-1-phosphate lyase suppression[J]. Am J Respir Cell Mol Biol, 2011, 45(2): 426-35. |
| [13] | 徐秀娟,孙耕耘,尤青海,张 丹.cAMP反应元件结合蛋白在LPS致肺微血管内皮细胞损伤过程中的作用[J].中国药理学通报,2014,30(7):965-9. Xu X J,Sun G Y,You Q H,Zhang D. Role of CREB in LPS-induced injury of RPMVEC[J]. Chin Pharmacol Bull, 2014, 30(7): 965-9. |
| [14] | 徐 慧,戴元荣,李凤琴,等.罗红霉素对哮喘平滑肌细胞增殖以及微囊蛋白-1及PI3K/Akt的影响[J].中国药理学通报,2015,31(3):407-11. Xu H, Dai Y R, Li F Q, et al. Effect of roxithromycin on asthma smooth muscle cells proliferation, caveolin-1 and PI3K/Akt pathway[J]. Chin Pharmacol Bull, 2015, 31(3):407-11. |
| [15] | Penumatsa K, Abualkhair S, Wei L, et al. Tissue transglutaminase promotes serotonin-induced AKT signaling and mitogenesis in pulmonary vascular smooth muscle cells[J]. Cell Signal, 2014, 26(12): 2818-25. |

