


2. 河北省中医院妇科, 河北 石家庄 050011;
3. 河北省重点实验动物实验室, 河北 石家庄 050017;
4. 河北医科大学第一医院, 河北 石家庄 050030
 , LI Yan-qing2
, LI Yan-qing2 , TENG Xu1, 3, ZHOU Jing-jing1, GUO Zan1, WANG Xin1, ZHANG Zi-wei4, ZHANG Yi1
, TENG Xu1, 3, ZHOU Jing-jing1, GUO Zan1, WANG Xin1, ZHANG Zi-wei4, ZHANG Yi1

2. Dept of Gynecology, Hebei Traditional Chinese Medicine Hospital, Shijiazhuang 050011, China;
3. Hebei Key Lab of Laboratory Animal Science, Shijiazhuang 050017, China;
4. The First Hospital of Hebei Medical University, Shijiazhuang 050030, China
代谢综合征(metabolic syndrome,MS)包括肥胖、胰岛素抵抗、血脂异常、血压升高和葡萄糖耐受不良等在内的一系列危险因素。MS中的任何一个因素都可能引起心脏病变,而上述因素的联合作用还可能进一步增加风险[1]。MS 能够使冠心病的发病率增加2倍,死亡率增加3倍[2]。越来越多的证据表明,MS能够同时导致心脏结构和功能的恶化,最终发展成为心力衰竭。而包括心肌细胞凋亡在内的心肌结构病理性改变是导致心功能降低,并最终发展成为心力衰竭的重要病理机制[3]。因此,如何通过改善心肌细胞凋亡,进而治疗MS患者心功能异常已成为重要的研究靶点和策略。
慢性间歇性低压低氧(chronic intermittent hypobaric hypoxia,CIHH)是指间断性的模拟高海拔的低压低氧,在两次低压低氧之间恢复常压常氧[4]。我实验室前期研究证实CIHH具有明显的心血管保护作用,改善心肌缺血/再灌注损伤导致的心功能降低和心律失常的发生。我们前期通过Langendorff心脏离体灌流实验证实,果糖喂养诱导的MS大鼠缺血后在再灌注过程中心功能明显降低,而CIHH能够明显改善果糖喂养大鼠心功能的下降[5]。但是,CIHH对MS大鼠心肌细胞凋亡的影响及其机制目前仍不清楚。因此,本实验目的在于证实CIHH能够改善MS大鼠的心肌细胞凋亡,并探讨其机制。
1 .材料与方法 1.1 MS模型制备和CIHH处理♂,体质量250~300 g,Sprague-Dawley(SD)大鼠(河北医科大学动物中心)随机分为4组:对照组(control)、果糖(fructose,F)组、CIHH组、果糖+CIHH(CIHH-F)组。需要果糖喂养的大鼠饮用质量浓度为100 g·L-1的果糖,共喂养42d。CIHH组大鼠每天8 ∶ 00 am置于低压低氧舱内,给予模拟海拔5 000m(PO2=11.2 kPa)的处理,每天持续6 h,其余时间将大鼠置于饲养室内(常压常氧),共给予42 d的间歇性低压低氧处理。CIHH-F组大鼠同时进行果糖喂养和CIHH处理。所有大鼠自由饮食,每天计算饮水量,每周称量体重1次。
1.2 血压测量使用鼠尾动脉压测量装置(LE5001,pressure meter,Panlab),每周测量清醒大鼠鼠尾动脉收缩压(systolic arterial pressure,SAP)1次。每只大鼠每次测量重复3次,取平均值。实验满42 d后,饥饿大鼠12 h,经颈总动脉插管测量大鼠的动脉血压。测量结束后处死大鼠,分别取血和心脏进行相应指标监测。
1.3 血浆生化指标检测大鼠血液经抗凝离心(3 000 r·min-1,15 min)后取上层血浆,用以检测血浆葡萄糖(葡萄糖氧化法,北京科美东雅生物技术有限公司产品)、胆固醇(胆固醇酯酶法,山东3V生物工程有限公司产品)、甘油三酯(甘油三酯水解酶法,山东3V生物工程有限公司产品)和胰岛素(ELISA,北京北方生物技术研究所产品)含量。
1.4 心肌组织HE染色和TUNEL染色心肌组织经4%多聚甲醛固定,石蜡包埋切片(厚度6μm),HE染色后观察心肌组织结构变化。TUNEL染色观察心肌细胞凋亡情况,操作依据TUNEL试剂盒(Roche Applied Science,Indianapolis,IN)说明书进行。
1.5 心肌组织caspase-3活性测定取心肌组织约20mg匀浆,Bradford法测定蛋白浓度,酶标法检测caspase-3活性(106 U·g-1 protein)。详细操作按照caspase-3活性测定试剂盒(碧云天生物技术研究所)说明书进行。
1.6 心肌组织Western blot取心肌组织约50 mg匀浆,提取总蛋白,Western blot 检测Bcl-2、Bax以及β-actin的蛋白表达。简要过程为:将提取的心肌组织蛋白进行蛋白定量(Bradford法)后,十二烷基硫酸钠-聚丙稀酰胺凝胶电泳,硝酸纤维素膜转膜,脱脂奶粉封闭,一抗4℃ 孵育过夜(兔抗Bcl-2和兔抗Bax购自Santa Cruz公司;兔抗β-actin购自GeneTex公司),TBST清洗3次,二抗(购自GeneTex公司)室温孵育1 h,发光,扫描仪扫描胶片,保存图片。应用NIH image 软件对图片中条带进行灰度测量,Bcl-2和Bax的相对表达量为其条带灰度与β-actin条带灰度之比。
1.7 统计学分析计数资料采用 x±s ,两组以上比较采用单因素方差分析,进一步进行组间比较采用Turkey检验。
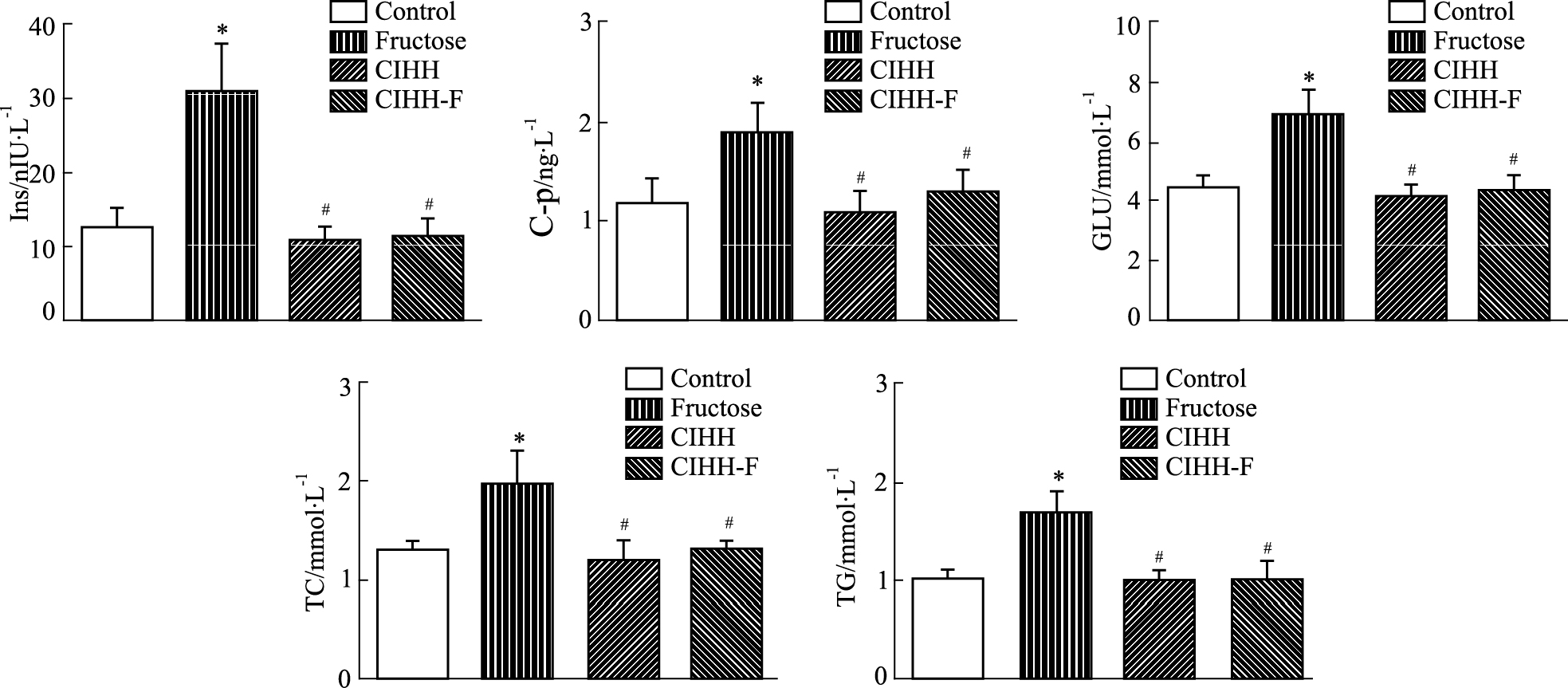
2 .结果 2.1 CIHH明显改善果糖喂养大鼠的MS一般特征和心脏改变与对照组大鼠相比,F组大鼠空腹血浆胰岛素、胰岛素C肽(C peptide,C-p)、葡萄糖、胆固醇和甘油三酯明显升高(Fig1,P < 0.05)。而CIHH-F组大鼠上述血浆生化指标的异常明显改善(Fig1,P < 0.05)。CIHH组血浆生化指标与对照组大鼠差异无显著性(Fig1,P > 0.05)。
|
| Fig.1 Effect of CIHH on blood biochemicals in fructose-fed rats (x±s ,n=6) CIHH: Chronic intermittent hypobaric hypoxia treated group; Fructose: Fructose treated group; CIHH-F: CIHH and fructose treated group; Ins: Insulin; C-p: Insulin C peptide; GLU: Glucose; TC: Total cholesterol; TG: Triglycerides. *P < 0.05 vs control group; #P < 0.05 vs fructose group. |
F组大鼠较对照组大鼠收缩压、体重指数、心 重/体重和左室重/心重明显升高。而CIHH-F组大鼠上述指标明显改善。与对照组大鼠相比,CIHH组大鼠上述指标差异无显著性(Tab1)。
| Groups | Body mass index/kg·m-2 | SAP/kPa | HW/BW/mg·g-1 | LVW/HW/g·g-1 | |||
| CIHH: Chronic intermittent hypobaric hypoxia treated group; Fructose: Fructose treated group; CIHH-F: CIHH and fructose treated group; HW/BW: Ratio of total heart weight to body weight; LVW/THW: Ratio of left ventricular weight plus inter-ventricular septum weight to total heart weight. *P < 0.05 vs control rats; #P < 0.05 vs fructose group. | |||||||
| Control | 6.3±0.02 | 15.5±0.64 | 4.32±0.15 | 0.78±0.01 | |||
| Fructose | 7.0±0.02* | 20.4±0.90* | 4.77±0.13* | 0.85±0.02* | |||
| CIHH | 6.1±0.03# | 15.0±0.93# | 4.26±0.17# | 0.77±0.02# | |||
| CIHH-F | 6.3±0.02# | 15.2±1.13# | 4.35±0.18# | 0.79±0.02# | |||
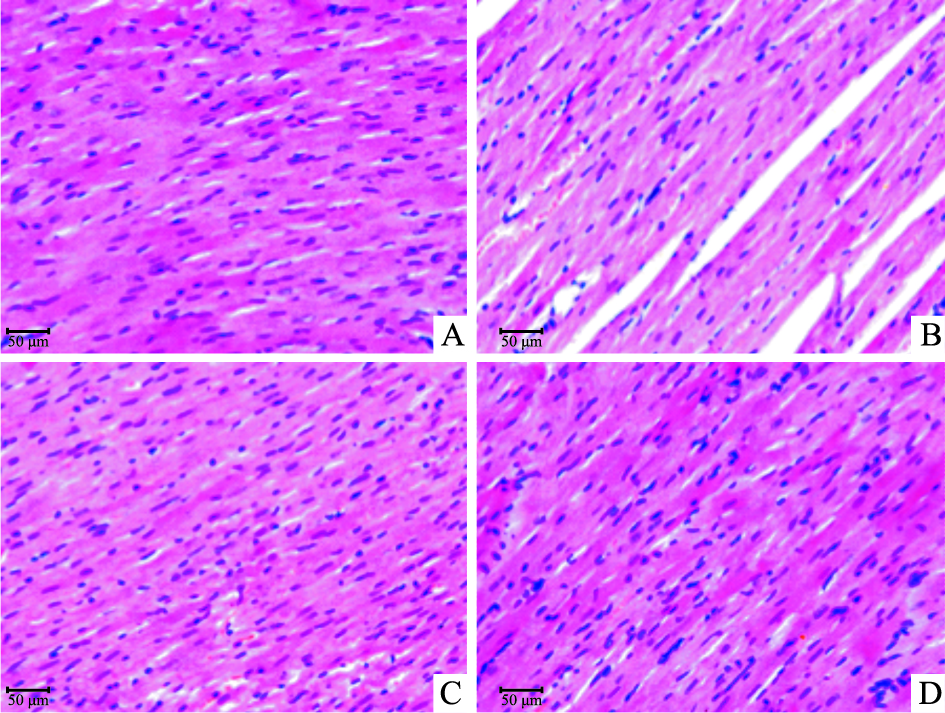
HE染色结果显示,对照组和CIHH组大鼠心肌细胞排列整齐,未见明显的变性、坏死和炎症细胞浸润等。F组大鼠心肌细胞水肿,排列紊乱,细胞之间间隙增宽,结缔组织增多。而CIHH-F组大鼠心肌结构损伤较F组大鼠明显改善(Fig2)。
|
| Fig.2 Histological analysis of hearts of control, CIHH, fructose-fed and CIHH-F groups(200×)(x±s ,n=6) A:Control; B:Fructose;C:CIHH;D:CIHH-F |
TUNEL染色显示,对照组和CIHH组大鼠仅见少量、散在的凋亡心肌细胞。F组大鼠凋亡心肌细胞数量明显增加,而CIHH-F组大鼠凋亡心肌细胞数量较F组大鼠明显降低(Fig3 A,B)。

|
| Fig.3 Effect of CIHH on apoptosis in fructose-fed rats A: Histological analysis of myocardium of control, CIHH, Fructose-fed and CIHH-F groups (400×); B: Quantitative analysis of apoptosis in four groups (n=6); C: Caspase3 activity analysis in four groups (n=6). *P < 0.05 vs control group; #P < 0.05 vs fructose group. |
caspase-3活性检测同样显示,与对照组相比,F组大鼠心肌caspase-3活性明显升高。CIHH能够明显抑制果糖诱导的caspase-3活性升高。而单纯CIHH组心肌caspase-3活性与对照组无差别(Fig3C)。
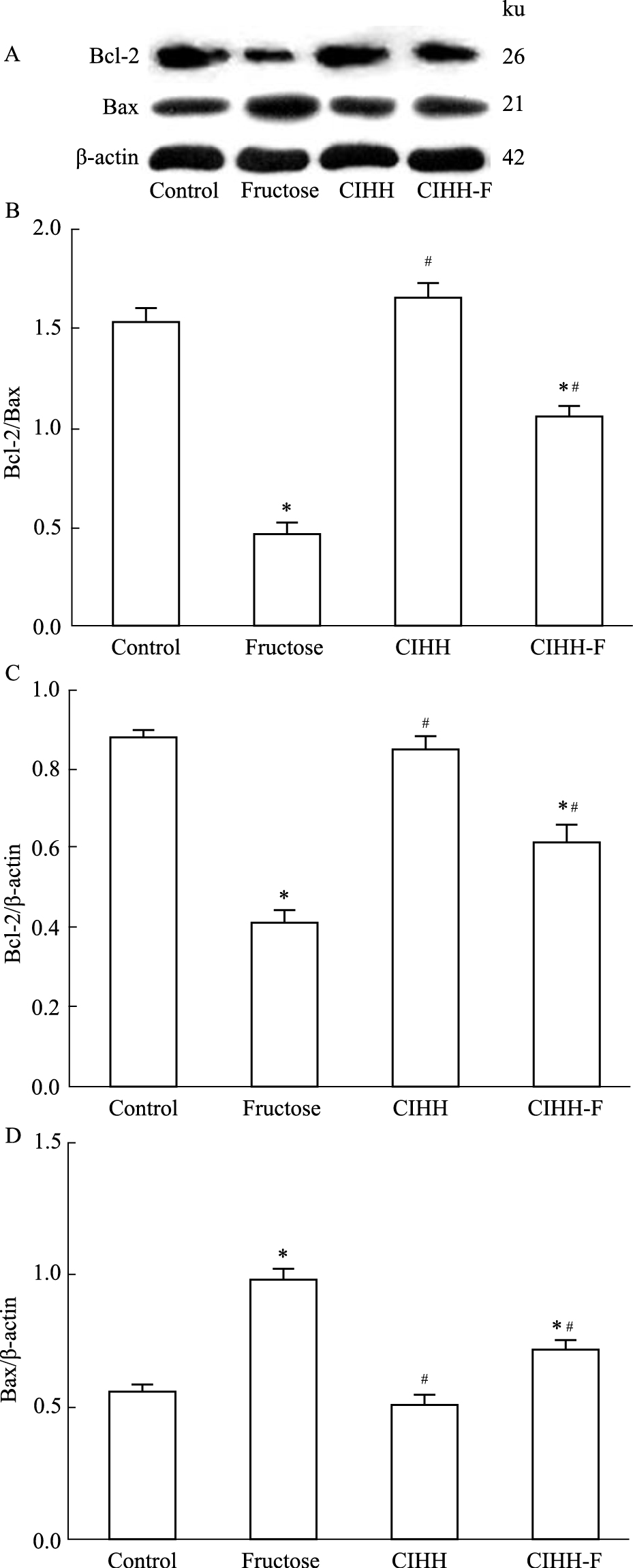
2.3 CIHH可能通过上调Bcl-2/Bax比值抑制心肌细胞凋亡Western blot结构显示,与对照组大鼠相比,F组大鼠心肌组织Bcl-2蛋白表达明显下调,Bax蛋白表达明显上调,Bcl-2/Bax比值明显降低。CIHH能够明显改善果糖喂养导致的上述蛋白的表达改变。而单纯CIHH和对照组相比,上述蛋白表达和比值无明显差异(Fig4)。
|
| Fig.4 Protein expression of Bcl-2 and Bax in myocardium detected by Western blot A: Represents protein expression of Bcl-2, Bax, and β-actin; B: Represents the ratio of protein expression of Bcl-2/Bax (n=6); C: Quantitative analysis of protein expression of Bcl-2 (n=6); D: Quantitative analysis of protein expression of Bax (n=6). *P < 0.05 vs control group; #P < 0.05 vs fructose group. |
我们利用果糖喂养诱导的大鼠MS模型证实,CIHH能够明显改善MS大鼠的相关症状,包括高血压、高血糖、血脂紊乱和胰岛素抵抗等。而且,CIHH能够明显改善MS大鼠的心肌细胞凋亡,其机制可能是通过抑制线粒体途径发挥改善心肌细胞凋亡的作用。上述结果可能为MS患者心肌损伤的预防和治疗提供新的靶点和思路。
由于富含果糖饮料的消费增加,人们日常摄入的果糖量相应增加。而越来越多的研究证实高果糖摄入量是促进MS发生发展的关键因素之一。果糖喂养的大鼠能够诱导出与人MS及其相似的病理生理改变,包括胰岛素抵抗、体重增加、高脂血症、高胰岛素血症、高甘油三脂血症、葡萄糖耐量降低、高血压、心功能异常和心力衰竭等[6]。本实验中,我们应用10%果糖水喂养大鼠42 d同样成功诱导出MS的相应表现,如高血压、高血糖、高甘油三脂血症、高胆固醇血症和高胰岛素血症等。上述结果提示,通过果糖喂养制备大鼠MS模型是可行的,能够成功诱导出MS的相关病理生理表现。
心肌损伤和心功能异常是MS的重要并发症之一,并最终导致患者的死亡率增加[1]。肥胖饮食诱导的MS大鼠心功能明显降低,电镜观察显示心肌纤维排列紊乱、线粒体水肿,天狼星红染色显示间质纤维化明显增加[7]。高脂饮食+25%果糖水喂养的MS大鼠同样表现出心功能的抑制,以及心肌炎症细胞浸润和胶原纤维沉积增加[8]。单纯应用高果糖饲料(50%果糖浓度)喂养的MS大鼠,心肌HE染色显示心肌结构紊乱、组织间隙明显增宽,TUNEL染色显示左室心肌凋亡细胞数明显增加[3]。我们的实验结果同样显示,10%果糖水喂养大鼠的心肌组织表现出明显的结构损伤,细胞水肿、排列紊乱、间隙增宽和结缔组织增多,凋亡的心肌细胞数量明显增加。而上述心肌组织的病理变化和细胞凋亡可能是导致心功能降低的重要原因。
越来越多的研究显示,CIHH具有明显的心血管调节和保护作用。CIHH能够明显改善缺血诱导的心肌细胞L 型钙电流峰值的降低[9],抑制右心室乳头肌β-肾上腺素能受体活性[10],从而发挥心血管保护作用。此外,CIHH能够明显改善正常和MS大鼠缺血/再灌注诱导的心功能降低和细胞凋亡[5, 11]。本实验中,我们进一步证实,CIHH能够明显改善果糖喂养导致的的大鼠心肌细胞凋亡。CIHH改善心肌细胞凋亡的作用可能是其发挥心血管保护作用的重要机制之一。
线粒体途径是诱导心肌细胞凋亡的重要途径之一。Bcl-2家族是调节细胞凋亡线粒体途径的关键因子。根据功能,Bcl-2家族成员可分为两类:一类是细胞凋亡的抑制因子,例如Bcl-2、Bcl-Xl等;另一类是细胞凋亡的促进因子,例如Bax、Bak和Bad等。其中,Bcl-2和Bax及其比值是应用最多的研究细胞凋亡的指标。已有的研究发现,CIHH能够改善缺血/再灌注导致的大鼠心肌Bcl-2的表达下调,同时抑制Bax的表达上调,通过抑制线粒体途径改善心肌细胞凋亡,进而减轻心肌缺血/再灌注损伤[11]。本研究中同样发现,果糖喂养的MS大鼠心肌组织Bcl-2表达下调,Bax表达上调,Bcl-2/Bax比值明显降低,而CIHH能够明显改善上述指标的变化。上述结果提示,CIHH可能通过抑制线粒体途径改善心肌细胞的凋亡。
此外,其它的研究和本文都发现CIHH在改善异常的心功能和细胞凋亡时,对正常的心功能和细胞凋亡水平并没有明显的影响[5, 11]。这些实验结果提示,CIHH的主要作用是维持体内结构和功能的稳态,而不是对某一生理功能或病理生理过程进行单向的调节,即单纯的增强或者减低某一功能或病理生理过程。而其具体的调节作用及详细机制仍需进行深入细致的研究。
| [1] | Ilkun O, Boudina S. Cardiac dysfunction and oxidative stress in the metabolic syndrome: an update on antioxidant therapies[J]. Curr Pharm Des, 2013, 19(27): 4806-17. |
| [2] | Nisoli E, Clementi E, Carruba M O, Moncada S. Defective mitochondrial biogenesis: a hallmark of the high cardiovascular risk in the metabolic syndrome[J]? Circ Res, 2007, 100 (6): 795-806. |
| [3] | Cheng S M, Cheng Y J, Wu L Y, et al. Activated apoptotic and anti-survival effects on rat hearts with fructose induced metabolic syndrome [J]. Cell Biochem Funct, 2014, 32 (2): 133-41. |
| [4] | Zhang Y, Zhou Z N. Beneficial effects of intermittent hypobaric hypoxia on the body [J]. Chin J Appl Physiol, 2012, 28 (6):504-9. |
| [5] | Zhou J J, Wei Y, Zhang L, et al. Chronic intermittent hypobaric hypoxia prevents cardiac dysfunction through enhancing antioxidation in fructose-fed rats [J]. Can J Physiol Pharmacol, 2013, 91 (5): 332-7. |
| [6] | Mottillo S, Filion K B, Genest J, et al. The metabolic syndrome and cardiovascular risk a systematic review and meta-analysis [J]. J Am Coll Cardiol, 2010, 56 (14): 1113-32. |
| [7] | Li C B, Li X X, Chen Y G, et al. Huang-lian-jie-du-tang protects rats from cardiac damages induced by metabolic disorder by improving inflammation-mediated insulin resistance [J]. PLoS One, 2013, 8 (6): e67530. |
| [8] | Alam M A, Kauter K, Brown L. Naringin improves diet-induced cardiovascular dysfunction and obesity in high carbohydrate, high fat diet-fed rats [J]. Nutrients, 2013, 5(3): 637-50. |
| [9] | Zhang Y, Zhong N, Zhou Z N. Effects of chronic intermittent hypobaric hypoxia on the L-type calcium current in rat ventricular myocytes [J]. High Alt Med Biol, 2010, 11 (1): 61-7. |
| [10] | Guan Y, Gao L, Ma H J, et al. Chronic intermittent hypobaric hypoxia decreases beta-adrenoceptor activity in right ventricular papillary muscle [J]. Am J Physiol Heart Circ Physiol, 2010, 298 (4): H1267-72. |
| [11] | Dong J W, Zhu H F, Zhu W Z, et al. Intermittent hypoxia attenuates ischemia/reperfusion induced apoptosis in cardiac myocytes via regulating Bcl-2/Bax expression [J]. Cell Res, 2003,13(5):385-91. |