


心室重构作为心脏事件的独立危险因素,与心律失常、心力衰竭和猝死等有密切的关系[1],表现为心肌肥厚、心腔扩大、心脏的收缩和舒张功能障碍,是心脏疾病走向终末期的一个必然阶段[2]。近年来研究表明,PPARα、PPARγ 的激活对心血管具有保护效应,且心室重构时PPARα、PPARγ 被抑制,导致心肌脂质和能量代谢紊乱,因此PPARα、PPARγ 在心室重构的过程中发挥着重要的作用[3]。
淫羊藿具有“补肾阳,祛风湿,益气力,强心力”等功效。淫羊藿苷(icariin,Ica)是淫羊藿的主要活性成分之一,具有降血压、抗肿瘤、增强免疫力、调节内分泌及抗骨质疏松等作用[4]。本研究拟进一步确证Ica是否具有抗自发性高血压大鼠心室重构的作用,及该作用是否与PPARα、PPARγ 的表达变化有关。
1 材料与方法 1.1 动物14周龄♂自发性高血压大鼠(SHR),14周龄同源正常的京都大鼠(WKY),SPF级,体质量260~300 g,购于北京维通利华实验动物技术有限公司,许可证号SCXK(京)2012-0001。
1.2 试剂与仪器淫羊藿苷(纯度 ≥ 98 %)购于南京泽朗医药有限公司;RNA 逆转录试剂盒购自宝生物工程(大连)有限公司;PPARα、PPARγ mRNA引物由宝生物工程(大连)有限公司合成;BCA蛋白浓度测定试剂盒购自江苏碧云天生物技术研究所;PPARα、PPARγ 兔抗大鼠抗体购自美国Abcam公司;辣根过氧化物酶(HRP)标记山羊抗兔IgG购自江苏碧云天生物技术研究所;real-time RT-PCR 扩增仪、 i-mark酶标仪、电泳仪、Trans-Blot转移系统及CCD成像系统均系美国BIO-RAD 公司产品; Leica光学显微镜为德国Leica Microsystems Ltd产品。
1.3 分组及给药21只14周龄♂ SHR大鼠随机分为模型组、Ica低剂量组(20 mg·kg-1)、Ica高剂量组(40 mg·kg-1),7只WKY大鼠为空白对照组。所有大鼠适应性喂养1周后,Ica低、高剂量组灌胃给药,每日2次,至26周龄,空白和模型组灌胃给予等体积双蒸水,实验结束后处死全部动物,取标本备用。
1.4 观察指标及检测 1.4.1 心肌中羟脯氨酸(Hyp)含量的检测采用ELISA方法检测大鼠心肌羟脯氨酸含量。称取50~60 mg心肌组织放入1 mL PBS缓冲液中冰浴匀浆,离心后取上清,稀释标准品、加样、温浴、洗涤、加酶、洗涤、显色、测定。计算大鼠心肌中Hyp含量。胶原相对浓度(mg·g-1)=Hyp相对浓度×7.46[5]。
1.4.2 形态学观察取各组大鼠心脏组织,置于10 %福尔马林固定48 h后,经脱水、包埋、切片和Masson染色,Leica光学显微镜下观察心肌形态结构,并拍照记录。
1.4.3 心肌组织中PPARα、PPARγ mRNA的表达每组各取心脏标本5例,采用real-time RT-PCR法检测。PPARα、PPARγ 的mRNA引物序列由宝生物工程(大连)有限公司合成,见Tab1。目的基因表达相对定量法:以PCR扩增过程中荧光信号强度达到阈值所需的循环数(cycle threshold,Ct值)为统计参数,依次计算平均Ct值=(Ct1 + Ct2)/2(重复管);dCt =平均Ct值-中间值;基因的表达=2-dCt;相对定量=目的基因的表达/内参基因的表达×100,将空白对照组的mRNA 表达量设定为100。
| Gene | Gene code | Up stream(5′-3′) | Down stream(3′-5′) |
| PPARα | NM_013196.1 | GGCAATGCACTGAACATCGAG | GCCGAATAGTTCGCCGAAAG |
| PPARγ | NM_001145366.1 | GGAGCCTAAGTTTGAGTTTGCTGTG | TGCAGCAGGTTGTCTTGGATG |
| β-actin | NM_031144.2 | GGAGATTACTGCCCTGGCTCCTA | GACTCATCGTACTCCTGCTTGCTG |
Western blot 法测定心肌组织中PPARα、PPARγ 蛋白含量,每组大鼠取心脏组织,每个样本加入总蛋白裂解液,在冰块中操作匀浆,BCA法进行蛋白定量,用酶标仪在波长为560 nm 的条件下测得OD 值,配成同体积同浓度后,加入上样缓冲液变性,加样进行分离胶和浓缩胶板中电泳,取胶放入转印槽中进行转印,取出转印膜,5% 脱脂奶粉封闭,TBST清洗,放入稀释好的一抗中,PPARα (1 ∶1 000)、 PPARγ (1 ∶800),4℃过夜。放入稀释后的二抗中(1 ∶3 000),加超敏ECL发光剂进行显色。采用Quantity One定量分析软件系统对图像进行灰度值测定。
1.5 统计学处理采用SPSS 16.0软件进行统计分析,实验数据 ± s表示,组间比较采用方差分析,组内比较采用t检验。
± s表示,组间比较采用方差分析,组内比较采用t检验。
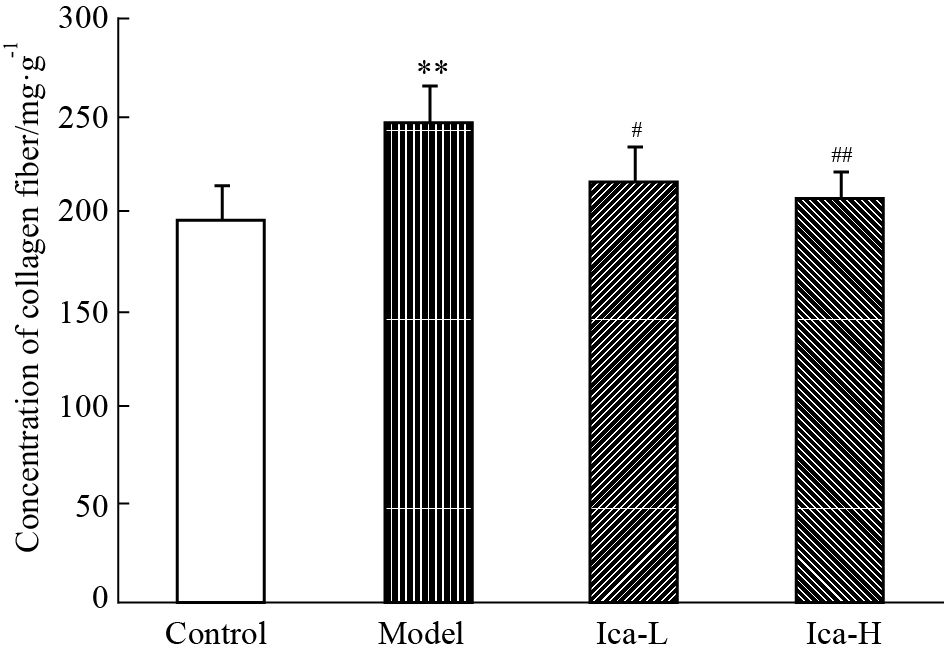
与空白组相比,模型组心肌中胶原含量明显上升(P < 0.01),与模型组相比,Ica低、高剂量组的胶原含量明显下降(P < 0.01或P < 0.05),见Fig1。
|
Fig.1
Effect of Ica on concentration of collagen fiber of left ventricle ( ± s,n=5)
**P<0.01 vs control;#P<0.05,##P<0.01 vs model ± s,n=5)
**P<0.01 vs control;#P<0.05,##P<0.01 vs model
|
Masson染色显示,与空白组相比,模型组心肌细胞肥大、延长,排列紊乱,胶原聚集,血管周围纤维化和心肌间质纤维化明显增加。与模型组相比,Ica低、高剂量组心肌细胞排列较整齐,血管周围纤维化及间质纤维化均减轻,且高剂量组减轻更为明显。见Fig2。

|
| Fig.2 Masson staining of myocardial cells (×400) A:Control,B:Model,C:Ica-L,D:Ica-H |
与空白组相比,模型组PPARα、PPARγ mRNA的表达下调(P < 0.01或P < 0.05)。与模型组相比,Ica低、高剂量组PPARα、PPARγ mRNA的表达明显上调(P < 0.05或P < 0.01),见Fig3。

|
Fig.3
Effect of Ica on the mRNA expression of PPARα,PPARγ in SHR ( ± s,n=5)
*P<0.05,**P<0.01 vs control;#P<0.05,##P<0.01 vs model ± s,n=5)
*P<0.05,**P<0.01 vs control;#P<0.05,##P<0.01 vs model
|
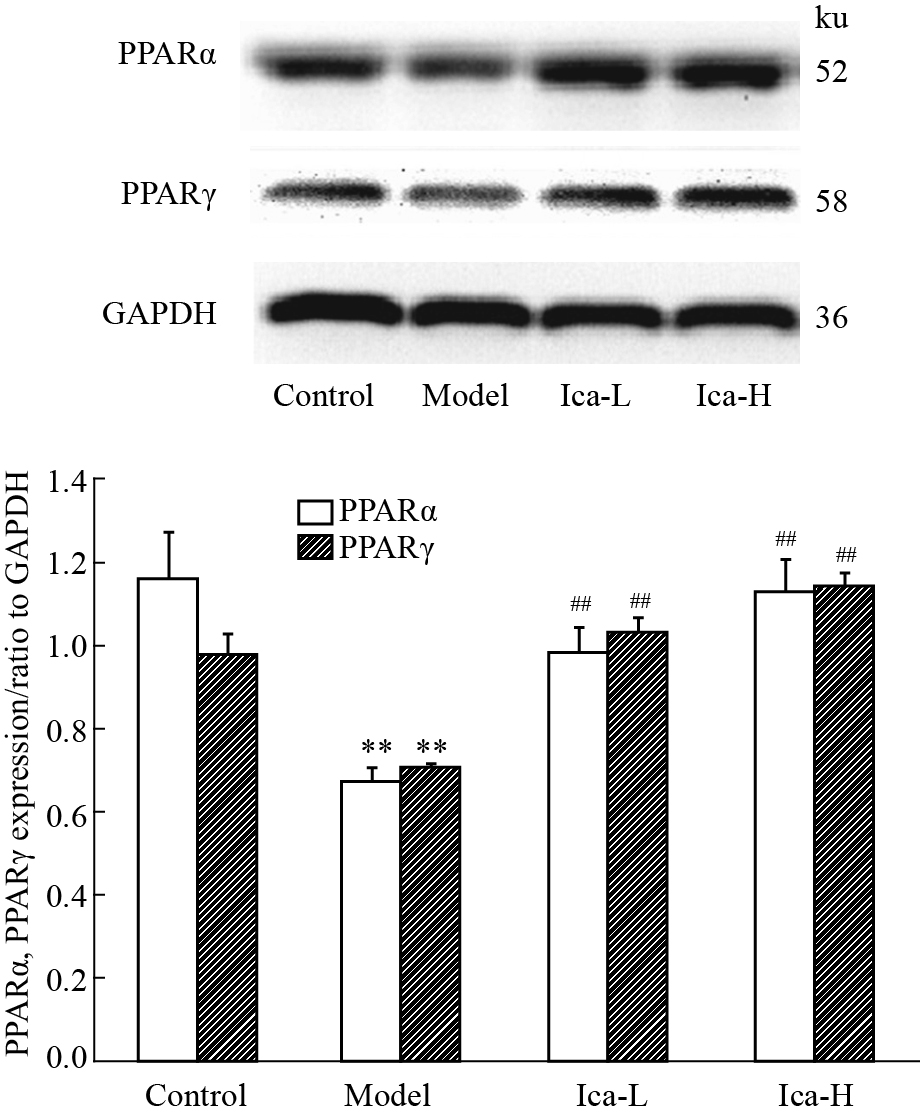
与空白组相比,模型组PPARα、PPARγ 蛋白含量明显减少(P < 0.01)。与模型组相比,Ica低、高剂量组PPARα、PPARγ 蛋白含量明显增高(P < 0.01),见Fig4。
|
Fig.4
Effect of Ica on the protein expression of PPARα andPPARγ in SHR ( ± s,n=3)
**P<0.01 vs control;##P<0.01 vs model ± s,n=3)
**P<0.01 vs control;##P<0.01 vs model
|
SHR大鼠与人类原发性高血压的发病过程和机制非常相似,还能继发一系列高血压性心血管病变。有研究表明,Ica可抑制压力超负荷所致的大鼠心肌纤维化[5],且SHR大鼠在24周龄时即可明显发生血管周围纤维化和间质纤维化[6]。本研究中,与空白对照组相比较,模型组SHR大鼠Hyp含量明显上升,心肌细胞排列紊乱,且细胞肥大、延长,血管周围纤维化和间质纤维化,可认为心室重构模型成功。而Ica低、高剂量组给药至26周龄时,心肌细胞排列较模型组整齐,大鼠心肌Hyp较模型组明显下降,血管周围纤维化程度及间质纤维化减少。故认为,Ica具有抗自发性高血压大鼠心室重构的作用。
心肌在泵血过程中,处于不间断的收缩和舒张的状态,消耗大量的葡萄糖和脂肪酸。葡萄糖和脂肪酸代谢失衡,脂肪酸氧化分解减少,葡萄糖代谢增加是心脏由代偿性肥厚转为充血性心衰的重要机制之一。过氧化物酶体增殖物激活受体(peroxisome proliferator activated receptors,PPARs )是一类由配体激活的核转录因子,共有3个亚型:PPARα、PPARβ/δ、PPARγ[7]。PPARs具有多种生物效应,可促进脂肪细胞的分化,调节机体的糖平衡,抑制炎性因子降低炎症形成,对心血管具有保护作用[8]。研究表明,PPARs通过调节心肌细胞的脂肪酸代谢,改变心肌细胞葡萄糖转运蛋白的含量,从而减轻心室重构[9, 11]。PPARα在心脏内的作用主要是调节脂肪和能量代谢为心脏提供ATP,起到保护效应[10]。已有研究表明,PPARα 激动剂可逆转AngⅡ诱导的心肌细胞肥大,并抑制心肌细胞的凋亡[11]。PPARγ 除了可调节脂肪细胞分化、能量代谢,还在炎症过程中发挥着重要的作用[12]。PPARγ 激动剂对心肌缺血/再灌注具有保护作用,还可抑制心肌肥厚并改善左心室功能[13]。本实验研究显示,与空白对照组相比较,模型组大鼠PPARα、PPARγ mRNA和蛋白的表达明显降低,而Ica组PPARα、PPARγ mRNA和蛋白的表达与模型组相比明显上调,提示PPARα、PPARγ参与Ica对自发性高血压大鼠心室重构的调节,从而减轻心室重构。
| [1] | Kolesnyk IuM, Kolesnyk MIu, Abramov AV. Pathological remodeling of myocardium in spontaneous hypertensive rats with experimental diabetes mellitus: the role of mitochondrial dysfunction [J].Fiziol Zh,2014,60(3):18-26. |
| [2] | Karaahmet T,Tigen K,Dundar C,et al. The effect of cardiac fibrosis on left ventricular remodeling,diastolic function,and N-terminal pro-B-type natriuretic peptide levels in patients with nonischemic dilated cardiomyopathy [J]. Echocardiography, 2010,27(8):854-960. |
| [3] | 杨永曜,李隆贵. PPARα,PPARγ及其配体对心室重构作用的研究进展[J]. 临床心血管病杂志,2006,22(1):61-3.Yang Y Y, Li L G. Progress in research on the effect of left ventricular remodeling by PPARα,PPARγ and and its ligand[J]. J Clin Cardiol (China), 2006,22(1):61-3. |
| [4] | 李叶丽,王颖婉,李意奇,等. 淫羊藿苷通过降低醛固酮水平抗自发性高血压大鼠肾间质纤维化[J]. 中国药理学通报,2014,30(4):519-22.Li Y L, Wang Y W, Li Y Q,et al. Anti-renal interstitial fibrosis effect of icariin in SHR by reducing aldosterone levels[J].Chin Pharmacol Bull, 2014,30(4):519-22. |
| [5] | 张丽梅,杨 竞,李意奇,等.淫羊藿苷抑制TGF-β1/Smad2 信号通路改善压力超负荷所致的大鼠心肌纤维化[J]. 中国药理学通报, 2013,29(10):1422-5.Zhang L M,Yang J,Li Y Q,et al. Anti-myocardial fibrosis activity of icariin in pressure overload rats through inhibition of TGF-β1/Smad2 signal pathway[J]. Chin Pharmacol Bull, 2013,29(10):1422-5. |
| [6] | Bradshaw A D, Baicu C F, Rentz T J, et al. Pressure overload-induced alterations in fibrillar collagen content and myocardial diastolic function: role of secreted protein acidic and rich in cysteine (SPARC) in post-synthetic procollagen processing[J]. Circulation, 2009, 119(2): 269-80. |
| [7] | 于学军,何作云,戚文航. 自发性高血压大鼠左室不同部位心肌纤维化的动态变化[J]. 临床心血管杂志,2001,17(10):466-8.Yu X J,He Z Y,Qi W H. Study of dynamic changes of myocardial fibrosis in different areas of SHRs' left ventricle[J]. J Clin Cardiol (China), 2001,17(10):466-8. |
| [8] | Usuda D, Kanda T. Peroxisome proliferator-activated receptors for hypertension [J]. World J Cardiol, 2014,26(8):744-54. |
| [9] | Hafstad A D, Khalid A M, Hagve M, et al. Cardiac peroxisome proliferator-activated receptor-alpha activation causes increased fatty acid oxidation, reducing efficiency and post-ischaemic functional loss[J]. Cardiovasc Res, 2009, 83(3):519-26. |
| [10] | Kim T, Yang Q. Peroxisome-proliferator-activated receptors regulate redox signaling in the cardiovascular system [J]. World J Cardiol, 2013,5(6):164-74. |
| [11] | 张瑞英,莫成利,富 路. PPARα对动脉粥样硬化、急性心肌梗死﹑糖尿病心肌病的作用及机制研究进展[J]. 心血管病学进展, 2008,29(4):613-6.Zhang R Y, Mo C L,Fu L. Progress of mechanism and effect of PPARα on atherosclerosis acute myocardial infarction and diabetic cardiomyopathy[J]. Adv Cardiovasc Dis, 2008,29(4):613-6. |
| [12] | Nanayakkara G, Viswaprakash N, Zhong J, et al. PPARγ activation improves the molecular and functional components of I(to) remodeling by angiotensin II[J]. Curr Pharm Des, 2013,19(27):4839-47. |
| [13] | 曾正英,廖高鸿,吕雅斐,陈国良. PPARs激动剂在心脑血管疾病中的研究进展[J]. 中国药物化学杂志, 2014,24(2):147-56.Zheng Z Y, Liao G H, Lü Y F, Chen G L. Research progress of PPARs agonists on cardiovascularand cerebrovascular diseases [J]. Chin J Med Chem, 2014,24(2):147-56. |

