


2. 中国人民解放军第九七医院急诊科, 江苏 徐州 221000
2. Dept of Emergency Medicine, the 97th Hospital of PLA, Xuzhou Jiangsu 221000, China
疼痛是身体和内脏受到损害的警报信号,是许多疾病的共同症状,不仅给病人带来痛苦,而且严重的疼痛可以产生疼痛性休克,威胁病人生命。因此,开发高效、低毒的镇痛药一直受到国内外医学界的关注。
杨梅黄酮(myricetin)是从常绿灌木杨梅的叶子中提取的黄酮类化合物,具有特殊的化学活性和生理作用,目前已有许多的文献报道了黄酮类化合物的镇静、抗氧化、抗肿瘤、抗炎等生物学作用[1, 2]。杨梅叶在自然界具有极易获取的优势,天然植物中黄酮类化合物的分析和性能研究已成为植物化学研究的前沿。研究显示,黄酮类化合物对细胞膜的兴奋性具有调节作用,能通过促进电压依赖性K+外流,降低细胞膜的兴奋性[3]。但从杨梅叶中提取分离出来的天然活性物质黄酮类单体化合物的镇痛作用及作用机制报道较少,我们拟应用行为学和电生理方法对杨梅黄酮的外周镇痛作用及机制进行初步的探讨,为杨梅黄酮能否开发成安全、高效的镇痛药物提供理论和实验依据。
1 材料与方法 1.1 材料本研究选用Sprague-Dawley大鼠24只,性别不限,体质量180~250 g,由徐州医学院实验动物中心提供。饲养在12 h/12 h 明暗光线交替的安静环境中,自由进食、水。所有实验均遵守《实验动物使用规范》。采用随机数字法分为两组(每组30只):生理盐水对照组(Saline 组)、完全弗氏佐剂致炎性痛组(CFA 组)。
1.2 炎性痛模型的建立大鼠在异氟烷(2%~4%)吸入麻醉下,应用100 μL 微量注射器将用生理盐水稀释后的100 μL 浓度为50%的完全弗氏佐剂(CFA)注入大鼠左侧后肢足底中心皮下,建立慢性炎性痛模型。对照组仅足底皮下注射生理盐水100 μL。
1.3 热缩足反射潜伏期(thermal withdrawal latency,TWL)测定大鼠在有机玻璃箱内适应30 min后,按照Hargreaves法,将大鼠放置于3 mm 厚的15 cm×15 cm×15 cm 的有机玻璃箱中,用热痛敏刺激仪照射大鼠左后肢足底后外侧。从照射开始至大鼠出现抬腿回避的时间为TWL。此过程中光源刺激强度恒定不变。自动切断时间为25 s,以防止组织损伤。每只动物连续测定5 次,测量间隔3 min,取后3 次比较平稳的数据平均值为大鼠TWL。
1.4 离体膜片钳记录大鼠经戊巴比妥钠(40 mg·kg-1)腹腔麻醉,暴露L4和L5 背根节,取出背根节放于正常人工脑脊液(artificial cerebral spinal fluid,ACSF)(mmol·L-1):NaCl 125、KCl 3.8、NaH2PO3 1.2、NaHCO3 26、glucose 10、MgCl2 1.0、CaCl2 2.0,剥除表面被膜,放置在2 mL消化液 (1 mg蛋白酶及1.6 mg胶原酶用ACSF稀释至2 mL备用)消化45 min,取出孵育1 h后移至记录槽,压片固定。在显微镜下选择直径<15 μmol·L-1的小神经元进行记录。用电阻为4~8 MΩ,充灌电极内液(mmol·L-1):KCl 140、NaCl 9、HEPES 10、EGTA 0.2、MgCl2 1、K2-ATP 3、Na-GTP 1 玻璃微电极进行巨阻封接,破膜后形成全细胞模式。
在检测钾电流时时将细胞外液更换为测钾外液(mmol·L-1):choline chloride 150、KCl 5、CaCl2 2、KCl 3、MgCl2 1、HEPES 10、CdCl2 1、D-glucose 10,并且在液槽中加入0.5 μmol·L-1 TTX孵育5 min,将细胞钳置于-90 mV 持续500 ms,然后给予-75~35 mV阶跃电压刺激,每次递增10 mV,持续时间300 ms,记录到外向钾电流。上述液体调整pH值为7.3左右,渗透压调整至280~300 mmol·L-1,以上药品均购自Sigma公司。
1.5 统计学分析所有计量资料均用 ± s表示,采用SPSS 16.0 软件进行统计处理,多组比较用单因素重复测量方差分析(one-way repeated-measures ANOVA),组间比较用t检验。
± s表示,采用SPSS 16.0 软件进行统计处理,多组比较用单因素重复测量方差分析(one-way repeated-measures ANOVA),组间比较用t检验。
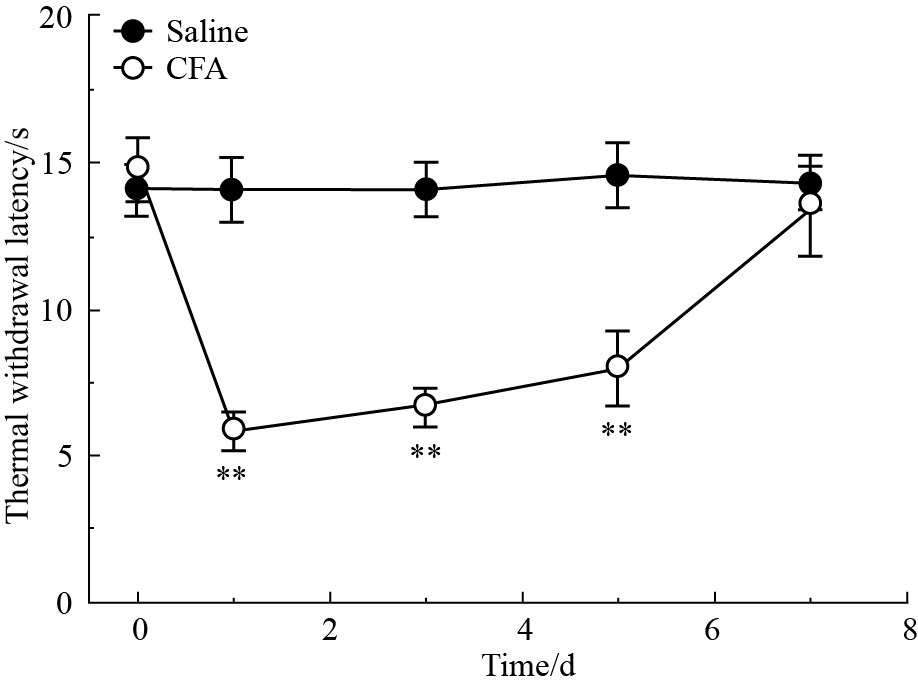
CFA 组(n=12)和Saline 组(n=12)比较,术前TWL 差异无统计学意义(P>0.05)。左侧足底皮下注射CFA 致炎后1、3、5 d TWL 明显降低,低于术前的基础值(14.03±0.88)s (P<0.05),与Saline 组比较,差异有统计学意义(P<0.01)。同时伴有患足典型外周炎症表现,包括红肿、缩爪等保护性行为,而且这一效果持续5 d左右后逐渐减轻。Saline 组大鼠术前和术后的TWL 未见明显变化,差异无统计学意义(P>0.05),见Fig1。
|
| Fig.1 Timecourse of development of thermal hypersensitivity in rats after intraplanta with CFA or saline Each data point represents the mean TWL value on the selected day.Thermal hypersensitivity appeared rapidly (~24 h) following CFA injection (open circles,n=12) and lasted for a long time compared to those in saline group (filled circles,n=12).**P<0.01 vs saline group. |
CFA组大鼠腹腔注射杨梅黄酮5 mg·kg-1对大鼠TWL无明显影响(P>0.05)。腹腔注射杨梅黄酮50 mg·kg-1后TWL明显升高(9.37 s±0.47 s,n=10),与给药前TWL(5.49 s±0.37 s)相比差异有统计学意义,与CFA 组相比也增高,差异有统计学意义(P<0.05);这一效应在给药后30 min 达到最大,3 h后衰减至接近给药前水平(6.35 s±0.69 s)。腹腔注射杨梅黄酮50、500与5 mg·kg-1相比结果差异有统计学意义(P<0.05),见Fig2。

|
| Fig.2 Intraperitoneal administration of myricetin attenuated thermal hyperalgesia induced by CFA (n=10) *P < 0.05,**P < 0.01 vs CFA group;#P < 0.05 vs myricetin 5 mg·kg-1. |
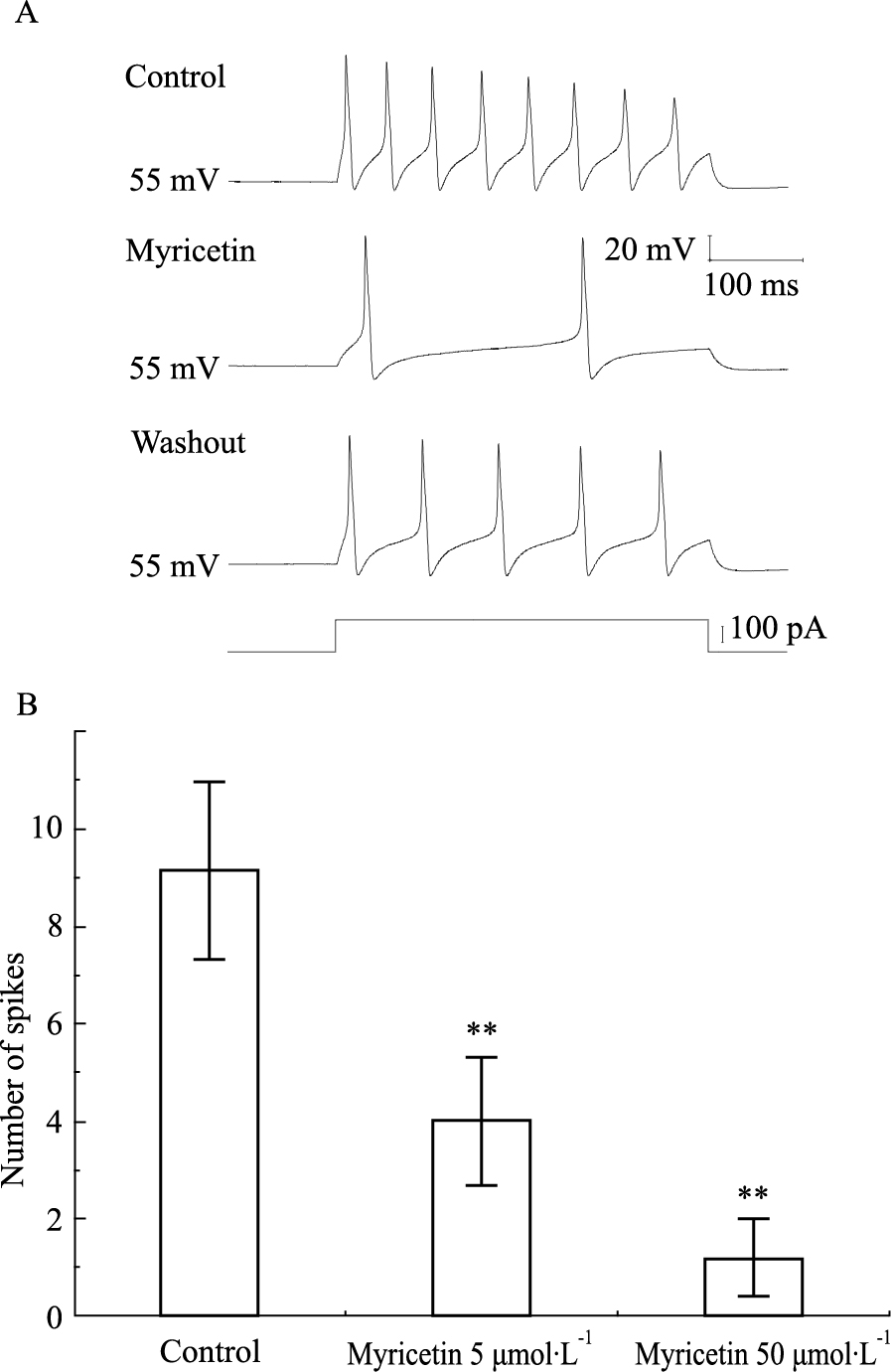
当全细胞记录模式形成后,在电流钳模式下记录DRG神经元的放电特性。当给予一个步阶为200 pA,持续时间为400 ms的阶跃电流时,结果如Fig3A所示,膜电位去极化时爆发多个动作电位。5、50 μmol·L-1的杨梅黄酮明显抑制神经元的放电频率 (P<0.01),其作用有剂量相关性(Fig3B)。
|
| Fig.3 The inhibitory effect of myricetin on action potential frequency of DRG neurons in rats A:Representative traces showing the spike firings in response to a depolarizing current step in DRG neurons;B:The summarized data showed that the action potential frequency was inhibited by myricetin 5 μmol·L-1(n=7) and 50 μmol·L-1(n=7) on dose related tendency.**P<0.01 vs control |
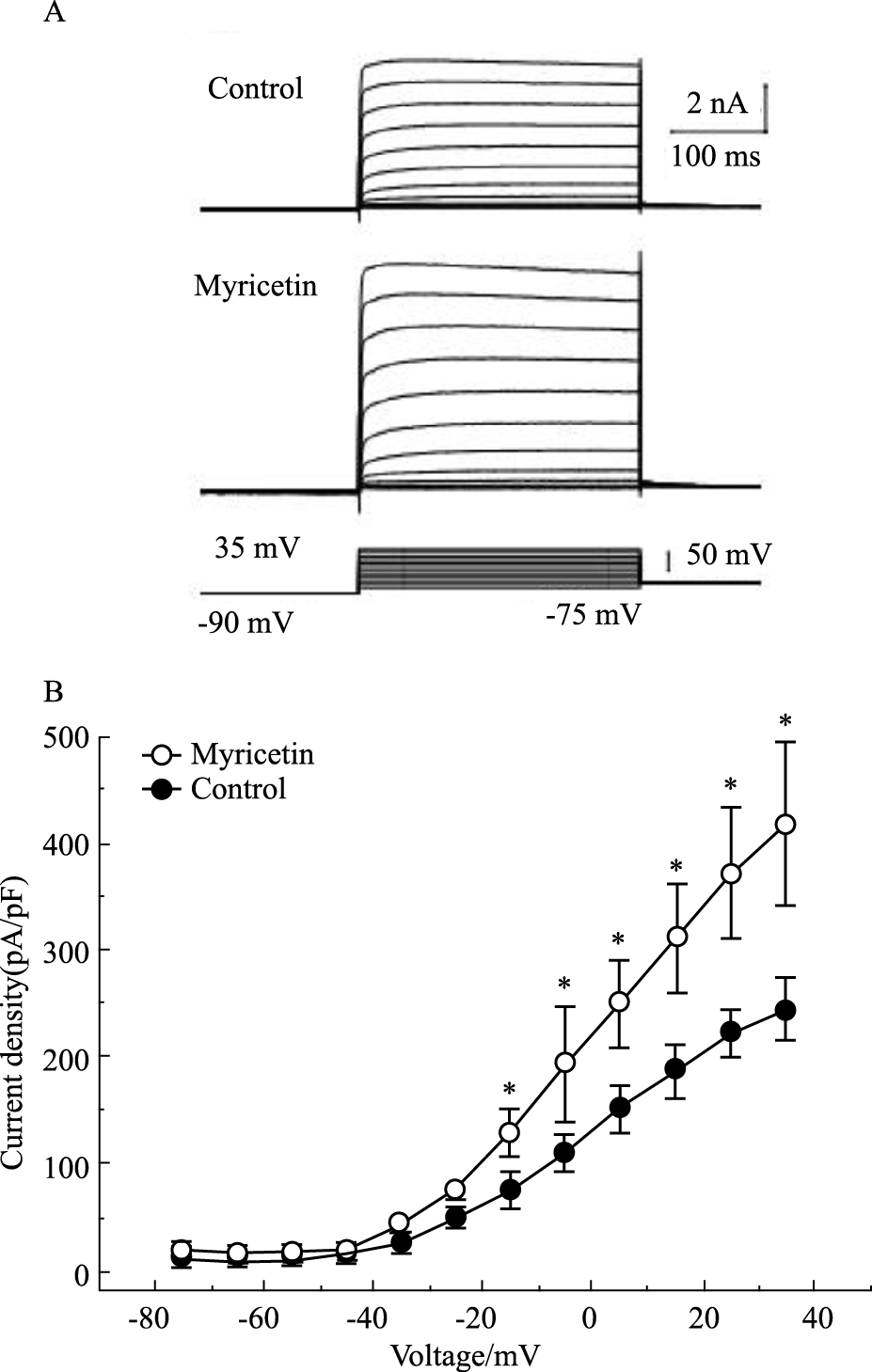
在电压钳模式下记录到外向钾电流(Fig4A),杨梅黄酮5 μmol·L-1增加电流幅度。电流-电压曲线表明,在-10 mV至+30 mV之间,杨梅黄酮明显增加了K+通道电流(P<0.05)(Fig4B)。为进一步研究钙离子在杨梅黄酮引起的K+通道电流增强中的作用,更换灌流液为不含Ca2+且含有200 μmol·L-1 CdCl2的细胞外液,当用此灌流液处理时,杨梅黄酮引起的K+通道电流增强的现象被完全阻断(Fig5)。
|
| Fig.4 Effects of myricetin on potassium channel currents in DRG neurons A:The currents evoked in response to a series of step pulse of 300 ms in an increment of 10 mV.First hyperpolarized to-75 mV from a holding potential of-90 mV then depolarized to 35 mV.These series of currents were enhanced after perfused with myricetin;B:The statistic current-voltage relationship curves showed that the currents were enhanced by myricetin when voltage varied in the rang of-75 mV to 35 mV (n=5).*P<0.05 vs control |

|
| Fig.5 Effects of myricetin on potassium channel currents in DRG neurons in calcium free perfusion solution A:Myricetin-induced enhancement of potassium current was abolished in the calcium free solution;B:The statistic current-voltage relationship curve showed that the current enhanced by myricetin was abolished in the calcium free solution when voltage varied in the rang of-75 mV to 35 mV (n=3) |
杨梅为杨梅科、杨梅属常绿灌木,原产中国的亚热带。明代的《本草纲目》和宋代的《食疗本草》对杨梅的药用功效均有记载。随着对杨梅叶所含成分的深入研究,人们已从杨梅叶中分离出黄酮类、三萜类等活性成分[4],目前认为杨梅黄酮,又称杨梅树皮素是发挥药理作用的主要化学成分之一。黄酮类化合物常有特殊的化学和生理活性,天然植物中黄酮类化合物的分析和性能研究已成为当前国内外植物化学研究的前沿。杨梅黄酮是黄酮类化合物家族中的一种,属于黄酮醇类,具有广泛的生物学活性。人们已发现黄酮类化合物有抗炎、抗病毒、抗氧化、抗衰老、免疫调节等作用。而DRG 作为痛觉传入的第一级神经元在痛觉的外周机制中起着极为重要的作用[5]。实验中,我们观察到杨梅黄酮能够抑制炎症痛大鼠的热痛敏行为,且杨梅黄酮能抑制背根节小神经元的放电频率,降低神经元的兴奋性,使其向中枢传入的冲动减少,表明杨梅黄酮的镇痛作用可能是通过直接抑制背根节神经元的兴奋性实现的。
电压依赖性钾通道在生物体内分布非常广泛,是目前已知种类最多的一种通道。其在调节膜电位、动作电位波形[6]、放电模式及频率[7]等方面均有重要作用。进一步的实验观察到杨梅黄酮可以增强背根节神经元电压依赖性K+通道的电流,而且此现象依赖于细胞外液中Ca2+的存在。因此,我们推测杨梅黄酮引起的胞内Ca2+浓度的增加会激活钙依赖性钾电流,引起电压依赖性 K+外流增加,从而加强了对DRG神经元兴奋性的抑制作用。此外,杨梅黄酮是否可以通过中枢神经系统等其他的途径产生镇痛作用还不清楚,其能否研发为新型、高效的镇痛药物还需要深入探讨。
| [1] | Ma Z G, Wang J, Jiang H, et al.Myricetin reduces 6-hydroxydopamine-induced dopamine neuron degeneration in rats[J].Neuroreport, 2007, 18(11): 1181-5. |
| [2] | Shimmyo Y, Kihara T, Akaike A, et al.Three distinct neuroprotective functions of myricetin against glutamate-induced neuronal cell death: involvement of direct inhibition of caspase-3[J].J Neurosci Res, 2008, 86(8): 1836-45. |
| [3] | Cermak R, Wolffram S, Kuhn G. Effect of the flavonol quercetin on membrane conductances in rat colonic crypt cells[J].Eur J Pharmacol, 2004, 503(1-3): 31-4. |
| [4] | 廖华卫,刘恩桂,王定勇.杨梅树皮的化学成分研究[J].中南药学, 2006, 4(3): 196-9.Liao H W, Liu E G, Wang D Y. Chemical constituents of the bark of Myrica ruba[J]. Cent S Pharm, 2006, 4(3): 196-9. |
| [5] | 吴海璇, 冯璐璐, 贺秋兰, 魏 明. 蛇床子素对髓核致坐骨神经痛大鼠DRG 中CGRPR1 表达的影响[J]. 中国药理学通报, 2013, 29(2):241-7Wu H X, Feng L L, He Q L, Wei M. Effect of osthole on expression of CGRPR1 in DRG of rats with nucleus pulposus-induced sciatica [J]. Chin Pharmacol Bull, 2013, 29(2):241-7. |
| [6] | Tsantoulas C, Zhu L, Shaifta Y, et al. Sensory neuron downregulation of the Kv9.1 potassium channel subunit mediates neuropathic pain following nerve injury[J]. J Neurosci, 2012,32(48):17502-13. |
| [7] | Hao J, Padilla F, Dandonneau M, et al. Kv1.1 channels act as mechanical brake in the senses of touch and pain[J]. Neuron, 2013,77(5):899-914. |

