


2. 广东省生物技术候选药物研究重点实验室, 广东 广州 510006
2. Guangdong Province Key Laboratory for Biotechnology Drug Candidates, Guangzhou 510006, China
电压门控性氯通道3(voltage-gated chloride channel 3,ClC-3)是ClC家族成员之一,广泛分布于脑、肾、肝、骨骼肌、心脏和胰腺等组织器官,主要定位在细胞膜和细胞质内的囊泡膜,生理功能目前尚未完全清楚,可能通过容积激活性氯电流参与细胞容积的调节,从而参与细胞增殖、分化、凋亡和迁移等过程[1]。ClC-3在某些疾病的发生发展中也有重要作用,可能通过调控心肌细胞容积及活性氯电流参与心肌肥大的形成[2],高表达可能参与了肺动脉高压和肺动脉炎症的机体适应性反应[3],其缺失可能是脑海马神经元退化的病因[4]。研究发现,在宫颈癌、肺癌、乳腺癌、膀胱移行细胞癌和人胶质瘤组织中ClC-3高表达[5, 6, 7],采用氯通道阻断剂可有效抑制乳腺癌细胞的增殖,应用ClC-3反义寡核苷酸可增强其抑制效果[8]。这些都提示ClC-3与肿瘤的关系非常密切,可能会在肿瘤的发生和发展过程中发挥重要作用。转移是大多数肿瘤患者死亡的原因,ClC-3是否参与肿瘤转移过程更加值得研究和探讨。本研究利用慢病毒介导的shRNA技术,转导人高转移肝癌细胞株MHCC97H,建立稳定干扰ClC-3基因的细胞株,并进一步观察其体外侵袭和迁移能力的改变,为进一步研究ClC-3在肿瘤发生发展中的作用,以及以ClC-3为靶点的肿瘤治疗的可行性奠定基础。
1 材料与方法 1.1 材料高转移人肝癌细胞MHCC97H、人胚肾细胞293FT、大肠杆菌stb13、慢病毒包装系统PLLU2G、pLV/helper-SL3、pLV/helper-SL4和pLV/helper-SL5由本实验室保存,胎牛血清和RPMI 1640培养基购自Gibco公司,XhoⅠ、HpaⅠ内切酶和T4 DNA连接酶购自NEB公司,质粒提取试剂盒和DNA凝胶回收试剂盒购自OMEGA公司,转染试剂Lipofectamine 2000和总RNA提取试剂TRIzol购自Invitrogen公司,反转录试剂盒ReverTra Ace qPCR RT Master Mix和荧光定量PCR试剂盒SYBR Green Realtime PCR Master Mix购自广州美津生物技术有限公司,小鼠抗人GAPDH单克隆抗体、HRP标记的山羊抗兔或山羊抗小鼠IgG均购自碧云天生物技术研究所,兔抗人ClC-3多克隆抗体购自Abcam公司,化学发光试剂购自Bio-Rad公司,Matrigel购自BD公司,Transwell小室购自Corning公司。
1.2 方法 1.2.1 干扰序列设计在GenBank检索出人ClC-3基因核苷酸序列(基因号NM_001829),设计针对人ClC-3的3个干扰RNA序列(Tab1)。正义与反义siRNA之间由6个碱基(CTCGAG)的loop环连接,上游链5′端加上一个T碱基,下游链5′端加上Xho I酶切粘端。同时设计1条无关序列作为阴性对照,作用序列为5′-GCTCTGGAGCAGTTCCGATAT-3′,通过BLAST验证该序列对任何基因无干扰效应。Oligo DNA由上海英骏生物技术有限公司合成。
| Oligo name | Oligo sequences (5′to 3′) |
| shClC-3-1-F | TCGACGCAAGTCCACGAAATTTCTCGAGAAATTTCGTGGACTTGCGTCG TTTTTC |
| shClC-3-1-R | TCGAGAAAAACGACGCAAGTCCACGAAATTTCTCGAGAAATTTCGTGGA CTTGCGTCGA |
| shClC-3-2-F | TGCTGCTTTAGTGGCTGCATTTCTCGAGAAATGCAGCCACTAAAGCAGC TTTTTC |
| shClC-3-2-R | TCGAGAAAAAGCTGCTTTAGTGGCTGCATTTCTCGAGAAATGCAGCCAC TAAAGCAGCA |
| shClC-3-3-F | TCCTACCTCTTTCCAAAGTATACTCGAGTATACTTTGGAAAGAGGTAGGT TTTTC |
| shClC-3-3-R | TCGAGAAAAACCTACCTCTTTCCAAAGTATACTCGAGTATACTTTGGAA AGAGGTAGGA |
空载体PLLU2G含有增强型绿色荧光蛋白(enhanced green fluorecence protein,EGFP)序列,用限制性内切酶XhoⅠ和HpaⅠ双酶切空载体,并回收酶切片段。上下游Oligo DNA经退火形成双链DNA,然后与线性化后的空载体PLLU2G在T4 DNA连接酶作用下16℃过夜连接,连接产物转化感受态细胞stb13。37℃培养16 h后挑阳性克隆进行菌落PCR鉴定,PCR引物为载体多克隆位点两端的引物,序列为pLLU2G-flank-F:5′-AGGCTTAATGTGCGATAAAAGAC-3′,pLLU2G-flank-R:5′-GAGCTTATCGATACCGTCGAC-3′,空载体质粒会扩增出239 bp的片段,插入shRNA序列的质粒会扩增出302 bp的片段。PCR鉴定阳性的菌落接种LB液体培养基中培养过夜,提取质粒送测序。经测序鉴定正确的重组质粒分别命名为PLLU2G-shClC-3-1、PLLU2G-shClC-3-2、PLLU2G-shClC-3-3、PLLU2G-shControl。
1.2.3 慢病毒包装收集对数生长期的293FT细胞,接种5×106个于10 cm的培养皿中,37℃、5%CO2的培养箱中培养过夜。按照说明书用脂质体进行共转染:将辅助质粒pLV/helper-SL3、pLV/helper-SL4、pLV/helper-SL5和目的质粒各4 μg与40 μL Lipofectamine 2000用3 mL的无血清Opti-MEM I培养液制备成DNA-脂质体复合物,滴加到293FT细胞中。分别收集转染后48 h和72 h的上清液,用0.45 μm滤器进行过滤,滤液经超速离心后浓缩,分装,保存于-80℃。PLLU2G-shClC-3-1、PLLU2G-shClC-3-2、PLLU2G-shClC-3-3和 PLLU2G-shControl经包装后获得的慢病毒分别命名为Lenti-shClC-3-1、Lenti-shClC-3-2、Lenti-shClC-3-3和Lenti-shControl。
1.2.4 病毒滴度测定滴度测定采用逐孔稀释法,测定前1 d将5×107·L-1的293FT细胞按每孔100 μL接种于96孔板中,常规培养24 h。准备10个无菌的EP管,每个管中加入90 μL培养基,取病毒原液10 μL加入到第1个管中,混匀后,取10μL加入到第2个管中,如此依次做10 ∶1倍比稀释。选取96孔板中所需的细胞孔,吸去90 μL培养基,加入稀释好的病毒溶液,37℃培养48 h后,加入新鲜培养基100 μL继续培养。96 h后在荧光显微镜下观察荧光表达情况,计数孔中荧光细胞数,结合稀释倍数计算病毒滴度:滴度(TU/ml)=荧光细胞数×有效稀释倍数。
1.2.5 稳定干扰细胞株的建立感染前1 d取对数生长期状态良好的MHCC97H细胞按每孔5×105个接种于6孔板。感染时,按照MOI=100稀释慢病毒,孔中分别加入含8 mg·L-1聚凝胺的4种稀释后病毒液1 mL,同时设定空白的靶细胞作为对照。培养16 h后,更换为新鲜RPMI 1640完全培养基2 mL继续培养,48 h后荧光显微镜下观察感染效率。将感染后的细胞用胰酶消化后制成单细胞悬液,按照每皿1 000个的密度接种于10 cm的培养皿,培养至形成单克隆细胞团,选择单克隆细胞再一次进行克隆,然后挑取足够数量单克隆细胞进行扩增培养,为下一步检测作准备。得到的3株稳定干扰细胞分别命名为MHCC97H/shClC-3-1、MHCC97H/shClC-3-2和MHCC97H/shClC-3-3,阴性对照细胞命名为MHCC97H/shControl。
1.2.6 定量PCR检测细胞ClC-3 mRNA干扰效率收集MHCC97H/shClC-3-1、MHCC97H/shClC-3-2、MHCC97H/shClC-3-3和MHCC97H/shControl细胞,按TRIzol试剂和反转录试剂盒说明书提供的方法提取细胞总RNA,并将其反转录为cDNA。以此cDNA为模板,应用荧光定量PCR试剂盒进行PCR扩增,ClC-3和GAPDH基因(内参照)引物由英潍捷基(上海)贸易有限公司合成。ClC-3:5′- GGTTCCATCAGGCTTGTTCATCC -3′(上游),5′- CCGACCTCACACCACTCCTTAAAG -3′(下游);GAPDH:5′- GTCTCCTCTGACTTCAACAGCG -3′(上游),5′- ACCACCCTGTTGCTGTAGCC -3′(下游)。PCR反应条件:95℃ 60s;95℃ 15s、60℃ 1 min,共40个循环。以2-ΔΔCt值表示ClC-3基因mRNA的相对表达水平。
1.2.7 Western blot检测细胞ClC-3蛋白干扰效率收集MHCC97H/shClC-3-1、MHCC97H/shClC-3-2、MHCC97H/shClC-3-3和MHCC97H/shControl细胞,加入细胞裂解液冰上裂解10 min,取蛋白上清用BCA蛋白浓度测定试剂盒测定浓度。取50~80 μg蛋白质进行10% SDS-PAGE电泳,分离后的蛋白质电转移至PVDF膜上,用含5%脱脂奶粉的封闭液室温封闭2 h;加入1 ∶1 000稀释的兔抗人ClC-3多克隆抗体和1 ∶2 000稀释的小鼠抗人GAPDH单克隆抗体,4℃反应过夜;TBS洗膜后,分别加入1 ∶2 000稀释的二抗(HRP标记的山羊抗兔或山羊抗小鼠IgG),室温反应2 h;TBS洗涤后,加入化学发光试剂,X线胶片曝光、显影和定影。扫描胶片,对各蛋白条带进行灰度值分析,以ClC-3蛋白条带灰度值与内参照GAPDH蛋白条带灰度值的比值表示ClC-3蛋白的相对表达水平。
1.2.8 Transwell小室实验检测细胞侵袭和迁移能力进行侵袭实验时,Transwell小室滤膜(孔径8 μm)外表面涂纤粘连蛋白5 μg,内表面涂Matrigel基质胶5 μg;24孔板内加入600 μL含10%胎牛血清的RPMI 1640培养基,将Transwell小室浸入24孔板中。用无血清RPMI 1640培养基重悬MHCC97H/shClC-3-2和MHCC97H/shControl细胞,将1×109·L-1的细胞悬液按每小室100 μL加到小室中,孵育6 h。取出Transwell小室,滤膜用甲醇固定1 min,HE染色,擦去滤膜内表面未穿过的细胞。于显微镜下(200×)计数穿过滤膜的细胞数。每膜计数上下左右中5个随机不同视野,每组设4个样本。细胞迁移实验与侵袭实验相似,只是滤膜内表面不涂Matrigel。
1.2.9 细胞划痕实验检测细胞迁移能力收集MHCC97H/shClC-3-2和MHCC97H/shControl细胞,按5×108·L-1接种2 mL于6孔板中,培养过夜至形成单细胞层。用10 μL吸头在单细胞层上划痕,然后用PBS清洗3次去除划下的细胞。细胞加入无血清,含0.05 mg·L-1表皮细胞生长因子的RPMI 1640培养基继续培养48 h,在不同时间点下拍照,测量划痕闭合宽度。
1.2.10 统计学方法应用SPSS 17.0软件进行统计学分析,计量资料以 表示,两组间数据的比较采用t检验,多组间数据的比较采用单因素方差分析,组间两两比较采用LSD检验。
表示,两组间数据的比较采用t检验,多组间数据的比较采用单因素方差分析,组间两两比较采用LSD检验。
PCR鉴定重组慢病毒质粒时,连接入shRNA片段的阳性克隆PCR片段大小为302 bp,而空载体克隆PCR片段大小为239 bp。将PCR产物进行电泳,第1对靶点序列结果显示2#、5#和6#克隆为阳性克隆,第2对靶点序列结果显示1#、2#、3#、4#、6#、7#和8#为阳性克隆,第3对靶点序列结果显示3#、5#、6#、7#和8#为阳性克隆(Fig1)。从每个靶点序列的阳性克隆中各选一个进行测序,结果显示序列均正确。

|
| Fig 1 Identification of recombinant lentiviral vectors with PCR A: PLLU2G-shClC-3-1; B: PLLU2G-shClC-3-2; C:PLLU2G-shClC-3-3. M: 100bp DNA marker; N: negative control (PLLU2G as template); P: positive control (PLLU2G-shRNA as template); 1~8: No. 1#~8# clones |
4质粒共转染48 h,荧光显微镜下观察到大量的绿色荧光产生,大部分细胞破裂释放病毒,证实慢病毒包装成功(Fig2A)。将病毒进行浓缩后,用逐孔稀释法测得Lenti-shClC-3-1、Lenti-shClC-3-2、Lenti-shClC-3-3和Lenti-shControl 4种病毒的滴度分别是7.0×1011 TU ·L-1、6.3×1011 TU ·L-1、7.2×1011 TU ·L-1和8.3×1011 TU·L-1。用4种慢病毒分别感染MHCC97H细胞后,都可观察到绿色荧光,感染率达到100%(Fig2B)。

|
| Fig 2 Packaging lentiviruses in 293FT cells and MHCC97H cells after infected with the recombinant lentiviruses under fluorescence microscope (200×) A: Packaging lentiviruses in 293FT cells; B: MHCC97H cells after infected with the recombinant lentiviruses. |
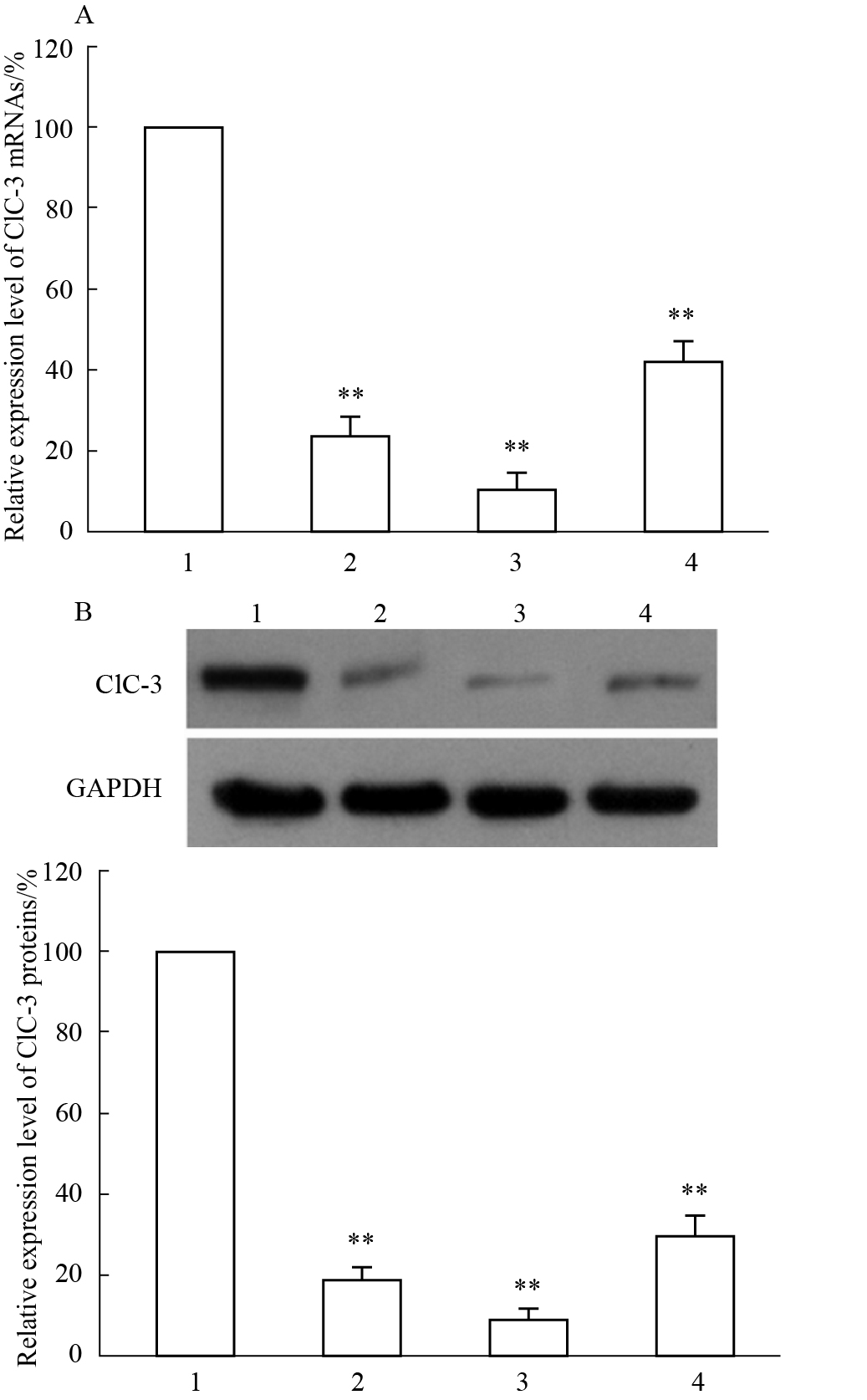
实时荧光定量PCR和Western blot检测结果显示,3株稳定干扰细胞ClC-3 mRNA和蛋白的相对表达水平都明显低于MHCC97H/shControl细胞。MHCC97H/shClC-3-1、MHCC97H/shClC-3-2和MHCC97H/shClC-3-3的ClC-3 mRNA干扰率分别是(76.70±4.28)%、(89.46±2.37)和(58.12± 5.29)%(Fig3A),ClC-3蛋白干扰率分别是(81.44±5.48)%、(92.14±5.92)%和(70.55±4.85)%(Fig3B),差异有统计学意义(P < 0.01)。MHCC97H/shClC-3-2细胞干扰效果最好,后续实验选用它作为细胞模型进行功能性研究。
|
Fig 3
Detection of ClC-3 interference efficiency ( , n=4)
1:MHCC97H/shControl; 2:MHCC97H/shCLCN3-1; 3:MHCC97H/shCLCN3-2; 4:MHCC97H/shCLCN3-3.The expression levels of ClC-3 mRNA and protein in stable interference cells were detected by real-time fluorescence quantitative-PCR (A) and Western blot (B). **P < 0.01 vs MHCC97H/shControl , n=4)
1:MHCC97H/shControl; 2:MHCC97H/shCLCN3-1; 3:MHCC97H/shCLCN3-2; 4:MHCC97H/shCLCN3-3.The expression levels of ClC-3 mRNA and protein in stable interference cells were detected by real-time fluorescence quantitative-PCR (A) and Western blot (B). **P < 0.01 vs MHCC97H/shControl
|
采用Transwell小室检测稳定干扰细胞株MHCC97H/shClC-3-2侵袭和迁移能力的变化(Fig4)。细胞侵袭实验中,MHCC97H/shControl和MHCC97H/shClC-3-2细胞中穿膜的细胞数分别为(181±13)和(105±11),MHCC97H/shClC-3-2细胞的穿膜数明显减少(P < 0.01);细胞迁移实验中,MHCC97H/shControl和MHCC97H/shClC-3-2细胞穿膜的细胞数分别为(372±19)和(189±14),MHCC97H/shClC-3-2细胞的数量也同样明显减少(P < 0.01)。结果表明干扰ClC-3可抑制MHCC97H细胞的侵袭和迁移。

|
Fig 4
Effect of ClC-3 interference on invasion and migration of MHCC97H cells detected by Transwell chamber assay ( , n=4) (200×)
**P<0.01 vs MHCC97H/shControl , n=4) (200×)
**P<0.01 vs MHCC97H/shControl
|
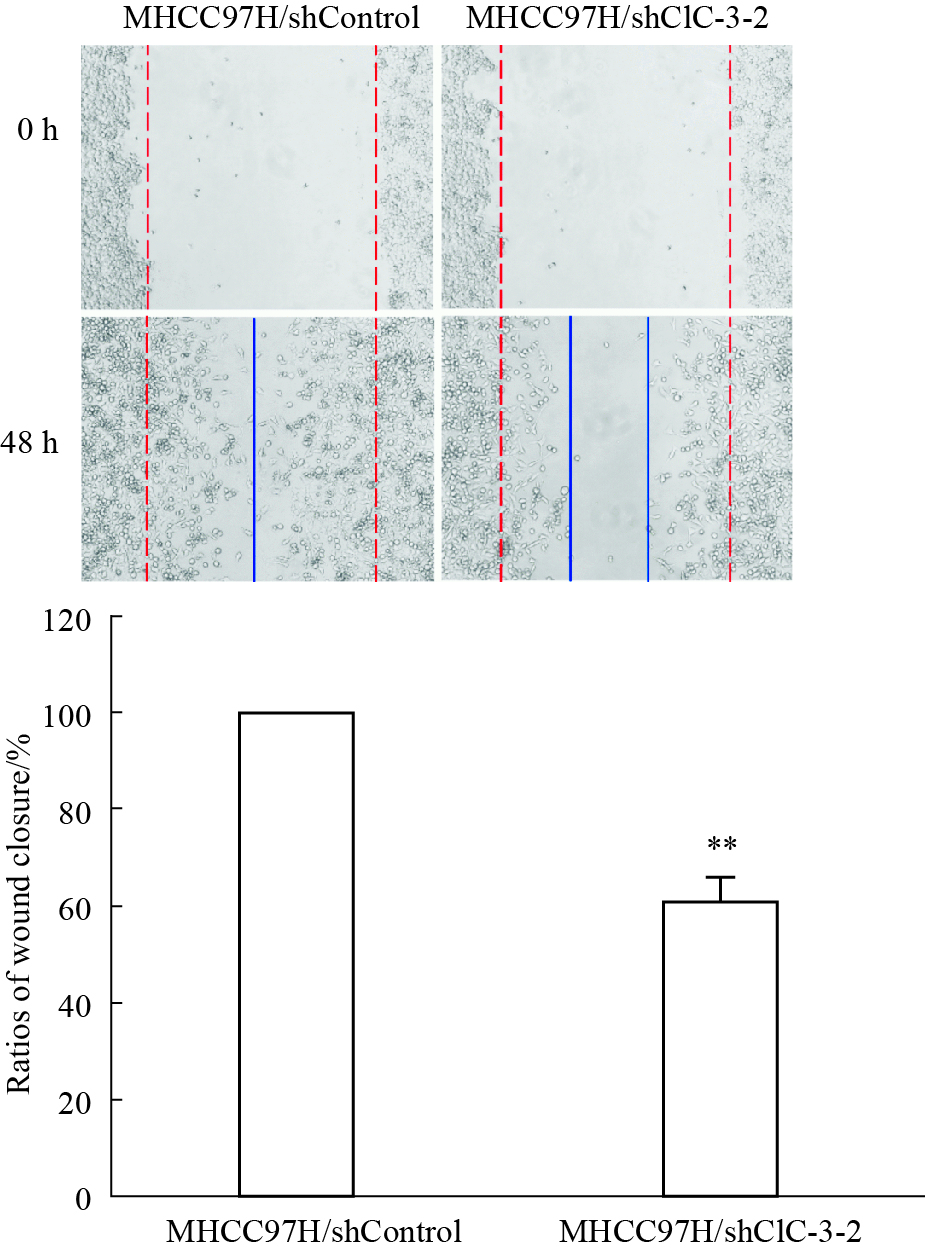
在细胞划痕实验中,细胞划痕后采用无血清培养基能排除细胞增殖的影响。结果显示MHCC97H/shClC-3-2细胞的迁移能力明显降低(Fig5)。划痕48 h后,MHCC97H/shControl细胞划痕闭合率为100%,而MHCC97H/shClC-3-2细胞只有(60.35±5.76)%,明显低于前者(P < 0.01)。
|
Fig 5
Effect of ClC-3 interference on migration of MHCC97H cells detected by cell scratch assay ( , n=4 ) (200×)
**P < 0.01 vs MHCC97H/shControl , n=4 ) (200×)
**P < 0.01 vs MHCC97H/shControl
|
ClC-3与肿瘤的发生和发展密切相关,可能参与了肿瘤细胞增殖、凋亡和耐药等重要过程[9, 10, 11]。肿瘤细胞迁移能力增强通常提示其转移能力增加,我们的前期研究中用反义寡核苷酸抑制鼻咽癌细胞中ClC-3的表达可使细胞迁移率下降[12],提示ClC-3可能在肿瘤转移过程中发挥了重要作用,但在后来的研究中发现此方法存在脱靶效应[13]。为了更深入地研究ClC-3在肿瘤侵袭转移中的作用,需要更好的细胞模型,而肝癌转移率很高,因此本研究采用人高转移肝癌细胞MHCC97H作为研究细胞。
为了确定ClC-3是否参与了肝癌转移,我们希望抑制MHCC97H细胞内源性ClC-3的表达来研究其对肿瘤的作用。目前,RNA干扰技术已成为研究基因功能的重要工具,但化学合成的siRNA存在转染效率低、转移到细胞内后半衰期短、对靶基因的表达抑制作用只能维持较短时间等缺陷[14]。而将shRNA载体导入细胞后,能在细胞内稳定地转录,并进一步生成靶基因特异性的siRNA,因此可以长期抑制靶基因表达的作用[15]。但普通shRNA仅可转染分裂期细胞且转染效率低。近年来发展的慢病毒技术,其免疫原性低、感染范围广,可整合到宿主细胞基因组稳定产生siRNA,高效抑制靶基因表达,而且可以浓缩,大大提高其转染效率,使得慢病毒介导的shRNA干扰成为稳定基因沉默的最常用选择[16]。本实验依据RNA干扰技术设计了特异性靶向ClC-3基因不同位点的3条不同干扰shRNA,通过慢病毒的介导转染MHCC97H细胞,经筛选获得了稳定干扰ClC-3基因表达的3株细胞。干扰效率最好的MHCC97H/shCLC-3-2细胞,其ClC-3 mRNA抑制效率为89.46%,ClC-3蛋白抑制效率高达92.14%。我们的前期研究中,利用反义寡核苷酸抑制鼻咽癌细胞CNZ2Z的ClC-3表达,在mRNA和蛋白水平的抑制率最高分别为77.5%和74.1%[12],这表明采用慢病毒介导的shRNA干扰技术来抑制ClC-3的表达是一种更好的研究方法。
肿瘤转移是一个非常复杂的过程,肿瘤细胞获得侵袭和迁移能力是肿瘤转移的关键因素之一。本研究显示,MHCC97H/shCLC-3-2细胞的穿膜能力在侵袭和迁移实验中比MHCC97H/shControl细胞明显降低,说明抑制ClC-3的表达可抑制肝癌细胞的侵袭和迁移,提示ClC-3在肝癌细胞侵袭和迁移中发挥了重要作用。细胞划痕实验进一步证实,抑制ClC-3的表达可明显抑制肝癌细胞迁移能力。非特异性ClC抑制剂NPPB可剂量依赖性的抑制子宫内膜癌细胞的侵袭和迁移[17],用反义寡核苷酸抑制鼻咽癌细胞ClC-3的表达可明显抑制其迁移能力[12],因此推测,ClC-3可能在实体瘤中普遍具有促进肿瘤细胞侵袭和迁移的作用。Lui等[18]研究发现,NPPB可以完全抑制胶质瘤细胞的侵袭,但单独使用ClC-3 siRNA和 ClC-3抑制剂或联合使用上述两者却都不能完全抑制细胞的侵袭,可见,可能有其他ClC家族成员在肿瘤细胞侵袭中也发挥了作用。但ClC-3是否参与了肿瘤的体内转移过程以及调控肿瘤细胞侵袭和迁移的具体机制有哪些,值得进一步的深入研究。
综上所述,我们应用慢病毒介导的shRNA干扰技术成功建立了稳定抑制ClC-3基因表达的肝癌细胞株,ClC-3表达抑制明显降低肝癌细胞MHCC97H的侵袭和迁移能力,但其具体的调控机制还有待进一步研究。
| [1] | Zhu L, Yang H, Zuo W, et al. Differential expression and roles of volume-activated chloride channels in control of growth of normal and cancerous nasopharyngeal epithelial cells[J]. Biochem Pharmacol, 2012, 83(3):324-34. |
| [2] | Xiong D, Heyman N S, Airey J, et al. Cardiac-specific, inducible ClC-3 gene deletion eliminates native volume-sensitive chloride channels and produces myocardial hypertrophy in adult mice[J]. J Mol Cell Cardiol, 2010, 48(1):211-9. |
| [3] | Dai Y P, Bongalon S, Hatton W J, et al. ClC-3 chloride channel is upregulated by hypertrophy and inflammation in rat and canine pulmonary artery[J]. Br J Pharmacol, 2005, 145(1):5-14. |
| [4] | Yoshikawa M, Uchida S, Ezaki J, et al. CLC-3 deficiency leads to phenotypes similar to human neuronal ceroid lipofuscinosis[J]. Genes Cells, 2002, 7(6):597-605. |
| [5] | 赵 维, 王 岩, 韩振国, 等. 氯离子通道CLC-3在乳腺癌中的表达及临床意义[J].中国实验诊断学, 2009, 13(3):350-2.Zhao W, Wang Y, Han Z G, et al. Expression of the CLC-3 in the breast cancer and its clinical significances[J]. Chin J Lab Diagn, 2009, 13(3):350-2. |
| [6] | Cuddapah V A, Sontheimer H. Molecular interaction and functional regulation of ClC-3 by Ca2+/calmodulin-dependent protein kinase II (CaMKII) in human malignant glioma[J]. J Biol Chem, 2010, 285(15):11188-96. |
| [7] | Ernest N J, Weaver A K, Van Duyn L B, Sontheimer H W. Relative contribution of chloride channels and transporters to regulatory volume decrease in human glioma cells [J]. Am J Physiol Cell Physiol, 2005, 288(6):C1451-60. |
| [8] | 赵 维, 白金锡, 韩振国, 等. 三苯氧胺(TAM)及靶向ClC-3反义核苷酸对MCF-7(ER+)增殖的影响[J].Zhao W, Bai J X, Han Z G, et al. The effects of the ClC-3 antisense strand and TAM on the proliferation of MCF-7 cell lines[J].中国实验诊断学, 2012, 16(10):1774-6. Chin J Lab Diagn, 2012, 16(10):1774-6. |
| [9] | Xu B, Mao J, Wang L, et al. ClC-3 chloride channels are essential for cell proliferation and cell cycle progression in nasopharyngeal carcinoma cells[J]. Acta Biochim Biophys Sin, 2010, 42(6):370-80. |
| [10] | Weylandt K H, Nebrig M, Jansen-Rosseck N, et al. ClC-3 expression enhances etoposide resistance by increasing acidification of the late endocytic compartment[J]. Mol Cancer Ther, 2007, 6(3):979-86. |
| [11] | 周 园, 周家国, 丘钦英, 等. ClC-3氯通道对H2O2诱导的大鼠主动脉平滑肌细胞凋亡的影响[J].Zhou Y, Zhou J G, Qiu Q Y, et al. Effects of ClC-3 chloride channel on H2O2-induced apoptosis in rat aortic vascular smooth muscle cells[J].中国药理学通报, 2006, 22(10):1175-9. Chin Pharmacol Bull, 2006, 22(10):1175-9. |
| [12] | Mao J, Chen L, Xu B, et al. Suppression of ClC-3 channel expression reduces migration of nasopharyngeal carcinoma cells[J]. Biochem Pharmacol, 2008, 75(9):1706-16. |
| [13] | Stessl M, Marchetti-Deschmann M, Winkler J, et al. A proteomic study reveals unspecific apoptosis induction and reduction of glycolytic enzymes by the phosphorothioate antisense oligonucleotide oblimersen in human melanoma cells[J]. J Proteomics, 2009, 72(6):1019-30. |
| [14] | Bakhtiyari S, Haghani K, Basati G, Karimfar M H. siRNA therapeutics in the treatment of diseases[J]. Ther Deliv, 2013, 4(1):45-57. |
| [15] | Rao D D, Vorhies J S, Senzer N, Nemunaitis J. siRNA vs. shRNA: similarities and differences[J]. Adv Drug Deliv Rev, 2009, 61(9):746-59. |
| [16] | Singer O, Verma I M. Applications of lentiviral vectors for shRNA delivery and transgenesis[J]. Curr Gene Ther, 2008, 8(6):483-8. |
| [17] | Li M, Wu D B, Wang J. Effects of volume-activated chloride channels on the invasion and migration of human endometrial cancer cells[J]. Eur J Gynaecol Oncol, 2013, 34(1):60-4. |
| [18] | Lui V C, Lung S S, Pu J K, et al. Invasion of human glioma cells is regulated by multiple chloride channels including ClC-3[J]. Anticancer Res, 2010, 30(11):4515-24. |

