


铝为地壳中含量最丰富的金属元素,人类日常生活中应用广泛,主要通过食物、化妆品及建筑材料等途径摄入。经证实,长期摄入大剂量铝会产生严重中枢神经系统毒性,表现为行为和认知功能障碍、神经元损伤,甚至神经退行性变,但其具体机制尚不完全清楚。
前列腺素(PGs)是一类多不饱和脂肪酸衍生物,由环氧化酶(COX)催化花生四烯酸(AA)代谢产生,介导一系列生理病理过程[1]。前列腺素D2(PGD2)是大脑中最丰富的PGs,其合酶(PGDS)有脑型PGDS(L-PGDS)和生血型PGDS(H-PGDS)两种亚型[2]。在中枢神经系统,除少突胶质细胞外,L-PGDS高表达于神经元[3]。PGD2与特异性受体DP1和DP2结合后,通过受体介导的信号传递机制而发挥广泛作用。DP1和DP2都是G蛋白偶联受体,分别偶联Gs和Gi蛋白,影响环磷酸腺苷(cAMP)水平而发挥不同作用。有研究报道,在PGD2致原代大鼠皮层神经元损伤模型中,DP2拮抗剂BAY-u3405未发挥保护作用,推测DP2可能不介导PGD2的神经毒性[4]。另也有研究报道,在谷氨酸致原代大鼠海马脑片损伤模型中,DP2激动剂DK-PGD2明显升高神经元的LDH漏出率及细胞死亡率,提示DP2介导PGD2的神经毒性[5]。出现此矛盾结果,可能与研究模型不同有关。DP2作为DP受体中的一员,在铝盐致原代培养大鼠海马神经元损伤过程中具体是如何变化的,尚未见报道。目前广泛研究的DP2选择性激动剂主要有DK-PGD2、15d-PGD2、15d-PGJ2,DP2选择性拮抗剂主要有CAY10471、AM-461、AZD1981。参考Yue等[6]的报道,我们选择DK-PGD2、CAY10471作为干预药物进行实验。
我们前期实验结果表明,铝负荷原代培养大鼠海马神经元损伤模型中,L-PGDS表达明显上调,DP2表达明显下调,PGD2含量明显升高,初步提示L-PGDS-PGD2-DP2信号通路可能参与了神经元损伤过程。在本实验中,我们采用DP2选择性激动剂和拮抗剂分别干预铝负荷神经元,进一步观察DP2在原代培养大鼠海马神经元中的作用。
1 材料与方法 1.1 材料 1.1.1 实验动物选取孕期18 d左右的SD大鼠,由重庆医科大学实验动物中心提供,合格证书号:SCXK(渝)2012-0002。
1.1.2 主要试剂与仪器麦芽酚(阿拉丁,上海),DMEM/F12、D-Hank′s(Hyclone,美国),B27、Neurobasal培养基、胎牛血清(Gibco,美国),左旋多聚赖氨酸、MTT试剂盒(Sigma,美国),青霉素-链霉素溶液、LDH试剂盒、Fluo-3 AM(碧云天,上海),山羊抗兔特异性烯醇化酶(NSE)多克隆抗体(博士德,武汉),SP试剂盒、DAB显色剂(中杉金桥,北京),苏木精染液、伊红染液(南京建成,南京),DK-PGD2、CAY10471(Cayman,美国),超净工作台(苏州净化设备有限公司),二氧化碳培养箱(Thermo Scientific,美国),超纯水系统(Millipore,美国),低温冷冻离心机(Thermo Scientific,美国),激光扫描共聚焦显微镜(Bio-Rad,美国),全自动酶标仪(BioTek,美国)。
1.2 方法 1.2.1 大鼠海马神经元原代培养取孕期18 d左右的SD大鼠,断颈后迅速剪开腹部皮肤和腹膜,将子宫完全暴露后剪断肌层和脐带,取出胎鼠并立即浸泡于装有75%乙醇的烧杯中。约30 s后,将消毒好的胎鼠移入事先准备的D-Hanks液中,断头取脑,迅速分离出两侧完整海马,放入冰浴的D-Hanks液中,用眼科剪将海马组织剪碎。加入组织体积5倍左右的0.125%胰酶,混匀,37 ℃培养箱内消化,10 min时拿出轻轻吹打数次。20 min后,加入同体积的含10%胎牛血清培养液终止消化。200目细胞网筛过滤,收集细胞悬液,800 r·min-1离心10 min。弃去上清,加入一定量的含10%胎牛血清培养液重悬细胞,制成细胞密度为1×106·L-1的细胞悬液。吸取不同体积细胞悬液分别接种于左旋多聚赖氨酸包被好的培养板、培养皿及培养瓶中,置于37 ℃、5% CO2的培养箱中培养。4 h后,待神经元贴壁,换含2% B27的Neurobasal培养液继续培养,以后每隔3 d半量换液1次。海马神经元培养至d 7时长到较好状态,可进行后续实验[7]。
1.2.2 原代培养大鼠海马神经元的免疫化学鉴定取6孔培养板中培养至d 7的海马神经元爬片(10 mm×10 mm),弃去细胞培养液用PBS漂洗3次;4%多聚甲醛固定30 min,PBS漂洗3次,每次2 min;3% H2O2孵育15 min,PBS漂洗3次,每次2 min;10%山羊血清封闭,37 ℃孵育20 min,吸干血清,不漂洗;NSE多克隆抗体 ∶抗体稀释液(1 ∶50),以PBS代替一抗设空白对照,4 ℃孵育过夜,PBS漂洗3次,每次5 min;生物素标记山羊抗兔二抗,37 ℃孵育30 min,PBS漂洗3次,每次5 min;辣根酶标记链霉素卵蛋白素工作液,37 ℃孵育30 min,PBS漂洗3次,每次5 min;避光条件下,DAB显色10 min,自来水终止反应;苏木精染液复染细胞核,3 min后自来水返蓝;95%乙醇脱水,二甲苯透明,中性树胶封片;晾干,镜下观察[8]。
1.2.3 MTT测定将96孔培养板中大鼠海马神经元培养至d 7进行实验分组,即空白对照组(300 μmol·L-1 maltol)、铝负荷模型组[100 μmol·L-1 Al(malt)3]、干预组(Al3++10-5、3×10-6、10-6 mol·L-1 DK-PGD2、CAY10471)。在加入处理因素后继续培养24 h,每孔加入20 μL的MTT溶液(5 g·L-1),37 ℃培养箱中孵育4 h。弃去孔内上清液,加入150 μL DMSO,摇床上避光震荡,以充分溶解结晶物,于570 nm波长处测定吸光度值(OD值)。
1.2.4 乳酸脱氢酶(LDH)漏出率测定将24孔培养板中大鼠海马神经元培养至d 7进行实验药物处理(分组同“1.2.3 ”),继续培养24 h后,根据LDH测定试剂盒说明书具体步骤操作,于490 nm波长处测定OD值。计算公式:细胞毒性或LDH漏出率/%=(处理样品OD值-样品对照孔OD值)/(细胞最大酶活性的OD值-样品对照孔OD值)×100。
1.2.5 海马神经元病理形态学观察将24孔培养板中大鼠海马神经元爬片(10 mm×10 mm)培养至d 7进行实验分组,即空白对照组(300 μmol·L-1 maltol)、铝负荷模型组[100 μmol·L-1 Al(malt)3]、干预组(Al3++10-5 mol·L-1 DK-PGD2、CAY10471)。在加入处理因素后继续培养24 h,弃去细胞培养液,PBS漂洗3次,每次1 min;4%多聚甲醛固定30 min,PBS漂洗3次;HE染色,镜下观察。
1.2.6 Ca2+荧光强度测定将共聚焦专用培养皿中大鼠海马神经元培养至d 7进行药物处理(分组同“1.2.5 ”),继续培养24 h。弃去培养皿中培养液,采用Ca2+荧光探针Fluo-3/AM标记活细胞内Ca2+,通过激光扫描共聚焦显微镜测定细胞内Ca2+荧光强度。
1.2.7 统计学分析所有实验结果均以 ± s表示,采用SPSS 17.0统计软件进行分析,组间比较采用单因素方差分析及Dunnett′s t检验。
± s表示,采用SPSS 17.0统计软件进行分析,组间比较采用单因素方差分析及Dunnett′s t检验。
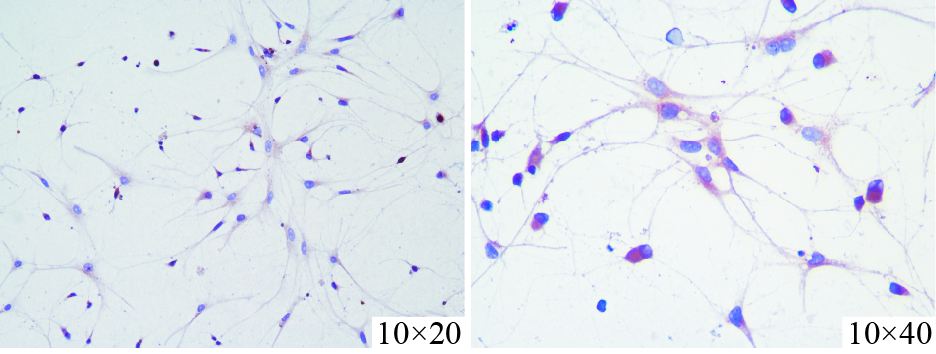
培养至d 7的神经元,在倒置光学显微镜下观察,其胞体饱满有光晕,轴突和树突明显,突起交错连接成网状。经NSE免疫细胞化学染色后,阳性细胞胞体及突起呈棕黄色;苏木精复染后,阳性细胞胞核呈蓝色。随机取6个视野,每个视野挑选100个细胞,计数NSE阳性细胞并计算其所占百分比。统计结果显示,超过95%为阳性细胞(Fig1)。
|
| Fig 1 NSE expression in primary cultured rat hippocampal neuron by immunocytochemistry |
与空白对照组比较,铝负荷模型组MTT值明显降低(P<0.01);与铝负荷模型组比较,DK-PGD2干预组MTT值明显降低,且有剂量依赖性(Tab1)。
( ± s,n=6) ± s,n=6) | |
| Group | OD |
| ##P<0.01 vs control;*P<0.05, **P<0.01 vs 100 μmol·L-1 Al(malt)3 | |
| Control | 0.63±0.02 |
| 100 μmol·L-1 Al(malt)3 | 0.40±0.03## |
| Al3+ + 10-5 mol·L-1 DK-PGD2 | 0.21±0.01** |
| Al3+ + 3×10-6 mol·L-1 DK-PGD2 | 0.25±0.02** |
| Al3++10-6 mol·L-1 DK-PGD2 | 0.33±0.02* |
与空白对照组比较,铝负荷模型组MTT值明显降低(P<0.01);与铝负荷模型组比较,CAY10471干预组MTT值明显升高,且有剂量依赖性(Tab2)。
( ± s,n=6) ± s,n=6) | |
| Group | OD |
| ##P<0.01 vs control;**P<0.01 vs 100 μmol·L-1 Al(malt)3 | |
| Control | 0.85±0.03 |
| 100 μmol·L-1 Al(malt)3 | 0.51±0.03## |
| Al3++10-5 mol·L-1 CAY10471 | 0.76±0.04** |
| Al3++3×10-6 mol·L-1 CAY10471 | 0.67±0.04** |
| Al3+ +10-6 mol·L-1 CAY10471 | 0.58±0.04** |
与空白对照组比较,铝负荷模型组LDH漏出率明显升高(P<0.01);与铝负荷模型组比较,DK-PGD2干预组LDH漏出率明显升高,10-5 mol·L-1、3×10-6 mol·L-1组差异有显著性(P<0.01)(Tab3)。
( ± s,n=6) ± s,n=6) | |
| Group | LDH leakage/% |
| ##P<0.01 vs control;**P<0.01 vs 100 μmol·L-1 Al(malt)3 | |
| Control | 4.03±0.34 |
| 100 μmol·L-1 Al(malt)3 | 21.90±0.89## |
| Al3++ 10-5 mol·L-1 DK-PGD2 | 43.38±1.56** |
| Al3+ + 3×10-6 mol·L-1 DK-PGD2 | 31.41±1.97** |
| Al3++10-6 mol·L-1 DK-PGD2 | 23.23±0.56 |
与空白对照组比较,铝负荷模型组LDH漏出率明显升高(P<0.01);与铝负荷模型组比较,CAY10471干预组LDH漏出率明显降低(P<0.01)(Tab4)。
( ± s,n=6) ± s,n=6) | |
| Group | LDH leakage/% |
| ##P<0.01 vs control;**P<0.01 vs 100 μmol·L-1 Al(malt)3 | |
| Control | 5.50±0.94 |
| 100 μmol·L-1 Al(malt)3 | 35.19±2.03## |
| Al3+ +10-5 mol·L-1 CAY10471 | 7.40±1.36** |
| Al3+ +3×10-6 mol·L-1 CAY10471 | 20.63±1.41** |
| Al3++10-6 mol·L-1 CAY10471 | 27.68±1.51** |
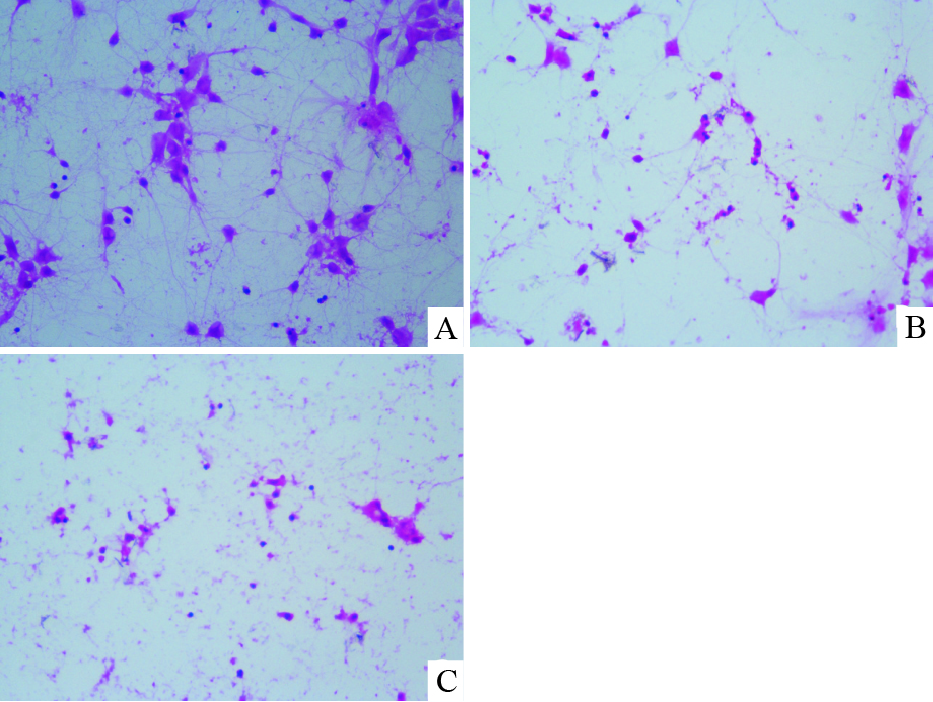
HE染色后,在正置光学显微镜下观察,空白对照组海马神经元结构清晰完整,胞体呈锥形或三角形,核仁明显,有双极或多极突起并相互交织成网;铝负荷模型组海马神经元细胞数目明显减少,突起萎缩,部分细胞核固缩;DK-PGD2 干预组海马神经细胞几乎全部核固缩、裂解;CAY10471干预组海马神经元较模型组神经元结构完整,胞体、胞核明显,裂解细胞明显减少(Fig2、3)。
|
| Fig 2 Effects of DK-PGD2 intervention on pathomorphology of primary cultured rat hippocampal neuron treated with aluminum overload (×400) A: control group; B: 100 μmol·L-1 Al(malt)3 group; C: 10-5 mol·L-1 DK-PGD2 group |

|
| Fig 3 Effects of CAY10471 intervention on pathomorphology of primary cultured rat hippocampal neuron treated with aluminum overload (×400) A: control group; B: 100 μmol·L-1 Al(malt)3 group; C: 10-5 mol·L-1 CAY10471 group |
空白对照组海马神经元的Ca2+荧光强度极其微弱,铝负荷模型组Ca2+荧光强度明显增强(P<0.01);与铝负荷模型组比较,DK-PGD2干预组Ca2+荧光强度有增强趋势,但差异无显著性;CAY10471干预组Ca2+荧光强度明显降低(P<0.01)(Tab5、Fig4)。
( ± s,n=10) ± s,n=10) | |
| Group | Fluorescence intensity |
| ##P<0.01 vs control; **P<0.01 vs 100 μmol·L-1 Al(malt)3 | |
| Control | 295.77±46.45 |
| 100 μmol·L-1 Al(malt)3 | 2 039.90±138.26## |
| Al3+ +10-5 mol·L-1 DK-PGD2 | 2 219.96±138.10 |
| Al3+ +10-5 mol·L-1 CAY10471 | 1 062.11±161.40** |

|
| Fig 4 Effects of DP2 intervention on Ca2+ fluorescence intensity change of primary cultured rat hippocampal neuron treated with aluminum overload (×200) A: control group; B: 100 μmol·L-1 Al(malt)3 group; C: 10-5 M DK-PGD2 group; D: 10-5 M CAY10471 group |
铝作为一种公认的神经毒剂,过量蓄积可严重影响人的认知功能,进而诱发一系列神经系统疾病[9]。与三氯化铝、葡萄糖酸铝等其他铝盐相比,麦芽酚铝[Al(malt)3]是一种中性含铝复合物,在生理pH条件能释放出大量Al3+,有利于进行铝负荷神经毒性的相关研究[10]。本实验采用Neurobasal培养基(含2% B27)进行海马神经元的原代培养,通过神经元胞质内特异性标志物NSE的鉴定,其纯度超过95%。参考Chen等[11]并通过我们的前期实验摸索,本实验采用100 μmol·L-1麦芽酚铝建立铝负荷大鼠原代海马神经元损伤模型。研究结果发现,与空白对照组比较,铝负荷原代培养大鼠海马神经元MTT值明显降低、LDH漏出率明显升高、Ca2+荧光强度明显增强,海马神经细胞数目明显减少、突起萎缩,部分细胞核固缩。Chen等[12]对麦芽酚铝致原代培养的大鼠皮层神经元损伤进行了研究,发现Al3+通过激活Rho-Rock信号通路诱导神经毒性。Johnson等[13]在原代培养的大鼠海马神经元中发现,麦芽酚铝可造成神经元呈时间和剂量依赖性凋亡,其作用机制可能与麦芽酚铝抑制脑源性神经生长因子(BDNF),导致细胞内Ca2+升高有关。
我们实验结果还发现,与铝负荷模型组相比,DK-PGD2 干预组MTT值明显降低、LDH漏出率明显升高、Ca2+荧光强度有增强趋势,海马神经细胞几乎全部核固缩、裂解;CAY10471干预组MTT值明显升高、LDH漏出率明显降低、Ca2+荧光强度明显减弱,海马神经元较模型组神经元结构完整,胞体、胞核明显,裂解细胞明显减少。有研究报道[14],DP2偶联Gi蛋白,通过激活磷脂酰肌醇3激酶(PI3K),磷酸化丝氨酸/苏氨酸蛋白激酶(Ser50/Thr145),激活糖原合成酶3(GSK-3),活化T 细胞核因子的转换,释放炎性介质。也有研究报道[15],DP2被激活后偶联Gi蛋白,抑制cAMP水平,促进Ca2+内流,上调CD11b表达,诱导嗜碱性粒细胞迁移和脱颗粒,促进IL-2、IL-4、IL-5、IL-13的释放。Liang等[5]对天冬氨酸(NMDA)致原代海马神经元损伤进行了研究,发现DK-PGD2加重神经元损伤。Schroder等[16]对炎性相关因子前列腺素H1(PGH1)进行了研究,发现CAY10471可抑制Th2细胞的迁移。结合本实验结果,DK-PGD2可能通过激动DP2,偶联Gi蛋白,增加细胞内Ca2+浓度,加重铝负荷原代培养大鼠海马神经元损伤;CAY10471可能通过抑制DP2活性,减少Ca2+流入,对铝负荷原代培养大鼠海马神经元损伤起一定保护作用。
综上所述,DP2激活表达可增加神经元对铝盐损伤的易感性,其机制可能涉及DP2下游Ca2+信号通路的调控,但由于作用复杂,在神经系统中的机制尚不完全清楚。因此,在本研究的基础上,可对DP2在神经系统中介导的下游Ca2+信号通路的具体调控机制进行深入研究。
(致谢:本实验在重庆医科大学生物化学与分子药理学重点实验室完成,非常感谢实验室提供的优越实验条件,使得本实验能顺利完成。再次呈上我诚挚的谢意!)
| [1] | Hao C M, Breyer M D. Physiologic and pathophysiologic roles of lipid mediators in the kidney[J]. Kidney Int, 2007,71(11): 1105-15. |
| [2] | Urade Y, Hayaishi O. Biochemical, structural, genetic, physiological, and pathophysiological features of lipocalin-type prostaglandin D synthase[J]. Biochim Biophys Acta, 2000,1482(1-2): 259-71. |
| [3] | Medani M, Collins D, Mohan H M, et al. Prostaglandin D2 regulates human colonic ion transport via the DP1 receptor[J]. Life Sci, 2015,122(2): 87-91. |
| [4] | Liu H, Li W, Rose M E, et al. Prostaglandin D2 toxicity in primary neurons is mediated through its bioactive cyclopentenone metabolites[J]. Neurotoxicology, 2013,39(12): 35-44. |
| [5] | Liang X, Wu L, Hand T, et al. Prostaglandin D2 mediates neuronal protection via the DP1 receptor[J]. J Neurochem, 2005,92(3): 477-86. |
| [6] | Yue L, Haroun S, Parent J L, et al. Prostaglandin D(2) induces apoptosis of human osteoclasts through ERK1/2 and Akt signaling pathways[J]. Bone, 2014,60(3): 112-21. |
| [7] | Liu X, Chen B, Chen L, et al. U-shape suppressive effect of phenol red on the epileptiform burst activity via activation of estrogen receptors in primary hippocampal culture[J]. PLoS One, 2013,8(4): e60189. |
| [8] | 黄 砚,杨俊卿,谢灵瑶. 咖啡酸对大鼠海马神经元铝盐损伤的保护作用[J].中国药理学通报,2009,25(12):1605-9. Huang Y,Yang J Q,Xie L Y. Protective effect of caffeicacid on damage induced by aluminum-overload in primary cultured rat hippocampal neuron [J]. Chin Pharmacol Bull,2009, 25(12):1605-9. |
| [9] | Molloy D W, Standish T I, Nieboer E, et al. Effects of acute exposure to aluminum on cognition in humans[J]. J Toxicol Environ Health A, 2007,70(23): 2011-9. |
| [10] | Bharathi, Shamasundar N M, Sathyanarayana Rao T S, et al. A new insight on Al-maltolate-treated aged rabbit as Alzheimer's animal model[J]. Brain Res Rev, 2006,52(2): 275-92. |
| [11] | Chen T J,Cheng H M,Wang D C,et al.Nonlethal aluminum maltolate can reduce brain-derived neurotrophic factor-induced Arc expression through interrupting the ERK signaling in SH-SY5Y neuroblastoma cells[J]. Toxicol Lett, 2011,200(1-2): 67-76. |
| [12] | Chen T J, Hung H S, Wang D C, et al. The protective effect of Rho-associated kinase inhibitor on aluminum-induced neurotoxicity in rat cortical neurons[J]. Toxicol Sci, 2010,116(1): 264-72. |
| [13] | Johnson V J, Kim S H, Sharma R P. Aluminum-maltolate induces apoptosis and necrosis in neuro-2a cells: potential role for p53 signaling[J]. Toxicol Sci, 2005,83(2): 329-39. |
| [14] | Hata A N, Breyer R M. Pharmacology and signaling of prostaglandin receptors: multiple roles in inflammation and immune modulation[J]. Pharmacol Ther, 2004,103(2): 147-66. |
| [15] | Arima M, Fukuda T. Prostaglandin D(2) and T(H)2 inflammation in the pathogenesis of bronchial asthma[J]. Korean J Intern Med, 2011,26(1): 8-18. |
| [16] | Schroder R, Xue L, Konya V, et al. PGH1, the precursor for the anti-inflammatory prostaglandins of the 1-series, is a potent activator of the pro-inflammatory receptor CRTH2/DP2[J]. PLoS One, 2012,7(3): e33329. |

