


2. 山东省中医药研究院, 山东 济南 250014
刘可春(1964-),男,博士,研究员,研究方向:药理学,通讯作者,Tel:0531-82605352,E-mail:hliukch@sdas.org
 ,
CHENG Li-fang2
,
CHENG Li-fang2
 ,
XU Xin-gang2,
LIU Ke-chun1
,
XU Xin-gang2,
LIU Ke-chun1
 ,
YAN Xue-sheng2,
WANG Xi-min1,
LIU Jin2, LI Ying2, HOU Hai-rong1,
SUN Dan-dan2,
HAN Li-wen1,
PENG Wei-bing1
,
YAN Xue-sheng2,
WANG Xi-min1,
LIU Jin2, LI Ying2, HOU Hai-rong1,
SUN Dan-dan2,
HAN Li-wen1,
PENG Wei-bing1 2. Shandong Research Academy of Traditional Chinese Medicine, Ji'nan 250014, China
新血管生成对于恶性肿瘤的生长和转移起着至关重要的作用[1, 2],抑制肿瘤新生血管生成已经成为肿瘤靶向治疗的重要方向,其中斑马鱼是公认的血管新生在体研究模型,由于其胚胎透明,生长初期主动脉及节间血管在镜下清晰可见,现已成为一种理想的抗血管生成高通量药物筛选的模型,并且在天然产物药理研究中也得到了应用[3]。熊果酸(ursolic acid,UA)是广泛存在于天然植物中的一种五环三萜类化合物,目前的研究发现其具有广泛的药理活性如:镇静、抗炎、抗菌、诱导肿瘤细胞凋亡等[4, 5]作用,本研究旨在考察UA对斑马鱼生理性和肿瘤诱导的血管生成的作用,及其对斑马鱼移植瘤模型的影响。
1 材料与方法 1.1 材料与试剂实验动物 AB 系野生斑马鱼(wild type,AB strain),血管荧光转基因斑马鱼Tg(VEGFR2: GFP)系山东省科学院斑马鱼药物筛选中心提供。肝癌SMMC-7721、结肠腺癌HT-29均为山东省医学科学院药物研究所惠赠。冻存HT-29和SMMC-7721分别复苏后,传代,备用。熊果酸(纯度≥99.0%)由山东省中医药研究院课题组提供;PTK787购自Sigma公司(纯度≥98.0 %);CM-DiL(C7000)活细胞染色剂购自Invitrogen;RPMI 1640培养基与新鲜牛血清(Gibco,批号1354643,1122050);0.25%胰酶-EDTA(Gibco,批号1535318);三卡因(Sigma-ALDRICH);脱膜剂pronase E(SOLARBIO)。
1.2 实验仪器微量注射仪ZGENEBIO PCO-1500(力钧生物科技有限公司);SZX16体式荧光显微镜、IX51倒置显微镜、激光扫描共聚焦显微镜FV-1000(Olympus);无菌操作台sw-cj-2fd(苏州AIRTECH);5804R离心机(Eeppendorf);ZSA302体视显微镜(重庆光学仪器公司);Forma 3111 CO2培养箱(Thermo),HPG-280BX光照培养箱(哈尔滨东联电子科技公司);斑马鱼养殖饲养设备(北京爱生科技公司)。
1.3 方法 1.3.1 斑马鱼胚胎的获取选用成熟♀♂斑马鱼分开喂养,照明14 h/黑暗10 h交替进行,定时饲喂人工饵料;采胚胎时,取性成熟斑马鱼按照♀:♂=1:1~2放入繁殖缸中,于次日10时获得受精卵。对受精卵进行纯净水清洗,移入加有亚甲基蓝(消毒)的斑马鱼胚胎培养用水(含5 mmol·L-1NaCl,0.17 mmol·L-1KCl,0.4 mmol·L-1CaCl2,0.164 mmol·L-1 MgSO4)中,置于28℃光照培养箱待用。
1.3.2 UA对TG斑马鱼节间血管生成的影响在受精卵发育至24 h时,使用1 g·L-1 Pronase E溶液脱去卵膜。在体视显微镜下挑选正常的斑马鱼胚胎,移入24孔板中,每孔10枚。用二甲基亚砜(DMSO)将UA配制成2 g·L-1母液,取一定体积至24孔中,使UA的终浓度为1.25、2.5、5、10 mg·L-1 4组;阳性药物选用终浓度为2 mg·L-1的酪氨酸酶抑制剂PTK787;对照组为含0.1%DMSO培养水,加药后置于光照培养箱28℃ 24 h。于48 hpf时,荧光显微镜下观察并计算斑马鱼节间血管长度,拍照,利用IPP计算背部中段血管长度,计算抑制率。
抑制率/%=(正常对照组节间血管长度-给药组节间血管长度)/正常对照组节间血管长度×100%。
1.3.3 UA对斑马鱼肝癌移植细胞的影响制备微量注射癌细胞悬液:按照Yong等[6]报道的实验方法进行,略有改动。无菌条件下在操作台将培养瓶中SMMC-7721细胞除去培养基,PBS清洗1次后,加入0.25%胰酶消化1 min,后加入培养基终止消化,离心后换新的RPMI 1640培养基,细胞悬液加入CM-DiL活细胞染色剂,37℃孵育5 min,然后4℃孵育15 min,随后离心除去上清液,PBS清洗2次后,加入培养基,镜下调整细胞密度达到2×109·L-1,备用。
给药条件及处理方法:新生斑马鱼胚胎用蒸馏水清洗2次,随后用含有亚甲基蓝培养水灭菌处理,加入终浓度0.03%二苯硫脲(PTU)孵育48 h(除斑点),斑马鱼胚胎加入适量1%三卡因轻度麻醉,放置在体式显微镜下,用微量注射仪将CM-Dil染色后的肝癌细胞注射于胚胎卵黄下,约0.1μL(约200个癌细胞),微量注射条件:压力0.12psi,注射时间:0.08s,注射后斑马鱼按照每组12条分组,随机分4组:模型组、低浓度组、中浓度组、高浓度组;正常对照组仅做穿刺注射处理,不注射细胞;UA用DMSO配制成2 g·L-1母液,取一定体积无菌水至24孔中,使UA的终浓度为0、5、10、15 mg·L-1放入28℃培养箱。在48 h后,将各组麻醉后的胚胎于共聚焦镜下拍照,用40倍镜拍摄,波长为550 nm,X、Y行2个方向的逐层扫描,拍摄整体斑马鱼。并用FV-10软件计算红色肿瘤细胞OD值,进行统计。抑制率/%=(模型组OD-给药组OD)/模型组OD×100%。
1.3.4 UA对HT-29诱导斑马鱼肠下静脉血管生成的影响 1.3.4.1 制备微量注射悬液移植癌选用增殖期HT-29,操作参照“1.3.3”。
1.3.4.2 微量注射方法操作参考“1.3.3”,斑马鱼胚胎与UA共同孵育了48 h后观察结果,将麻醉后的胚胎放置于共聚焦镜下,波长为480 nm,分别拍摄整体与肠下静脉,沿X、Y行2个方向的逐层扫描拍照,并用FV-10软件分析肠下静脉OD,并进行统计学处理。
1.4 统计学分析实验数据采用SPSS 13.0统计学软件工具进行分析,数据均用 ± s表示,组间比较采用t检验。
± s表示,组间比较采用t检验。
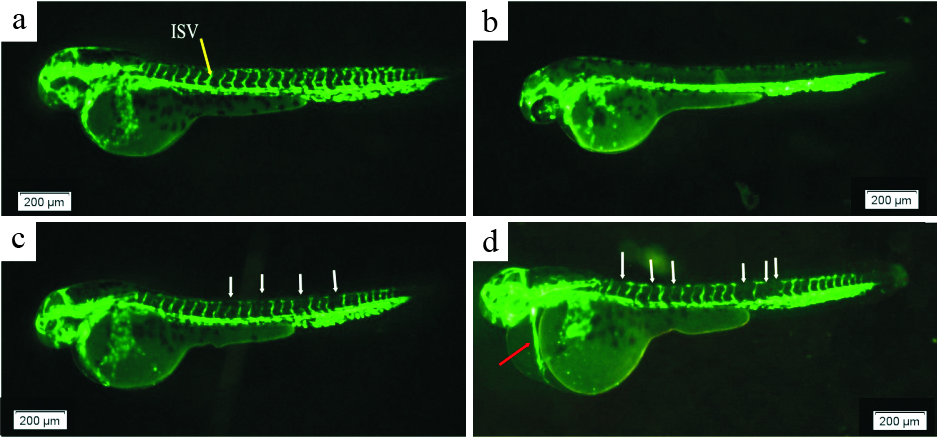
斑马鱼节间血管的发育起始时间24hpf,本实验观察的现象与文献相同[7];对照组斑马鱼节间血管生长良好,节间血管呈均匀纵向排列,完整无缺失,无断裂,荧光强。PTK787组的斑马鱼ISV缺失明显,荧光消失;UA处理组的中、高剂量组荧光缺失明显:出现血管变细、部分缺失,5与10 mg·L-1UA组节间血管长度与对照组比较差异有显著性(P<0.01),抑制率分别达到了20.25%、26.65% (Fig1,2),同时镜下可见节间血流明显减少,并且高浓度UA具有延迟胚胎发育,心脏线性畸形等现象。

|
| Fig.1 ISV of VEGFR2 zebrafish after treatment of different concentrations of UA **P<0.01 vs control (0.1%DMSO) |
|
| Fig.2 Lateral view of TG(VEGFR2:GFP) zebrafish showing ISV after treatment with UA for 24h a: Control (0.1%DMSO) at 48hpf; b: Zebrafish larva treated with 2 mg·L-1 PTK787; c: Zebrafish larva treated with 5 mg·L-1 UA; d: Zebrafish larva treated with 10 mg·L-1 UA. Yellow arrow indicates ISV, white arrow indicates missing ISV, red arrow shows lineheart. |
胚胎经微量注射SMMC 7721细胞48 h后,各组死亡率介于25.0%~41.7%,与文献报道相似[8];显微镜下可见:空白对照组生长良好,模型组镜下可见红色肿瘤细胞在胚胎各个器官均有分布,较集中于卵黄部、卵黄延伸部及尾段主动脉,在头部及眼睛也有少量分布;UA组红色肿瘤细胞全身分布的情况消失,10及15 mg·L-1组红色细胞数量减少,且分布区域有限,仅局限于卵黄延伸部和尾段主动脉(Fig3),15 mg·L-1组胚胎出现体色变浅、生长缓慢等变化;各组OD值显示,10及15 mg·L-1组与模型组比较均差异具有显著性(P<0.01),UA各组对SMMC 7721的抑制率分别为38.01%、54.69%、61.88%,具有明显的剂量依赖性(Tab1)。

|
| Fig.3 Zebrafish showing SMMC-7721 xenografts after treatment with UA for 48h a:Control(0.1%DMSO). b:SMMC-7721 xenograft zebrafish at 96hpf(model group); c. d. e:SMMC-7721 xenograft Zebrafish larvas treated with 5mg·L-1UA, 10mg·L-1UA,15mg·L-1UA. White arrow indicates SMMC-7721 cell. |
 ± s)
± s)
| Group | n | OD | Inhibition rate of tumor growth/% |
| **P<0.01 vs model group | |||
| 0.1%DMSO | 10 | 0 | |
| Model | 9 | 67822.67±20905.33 | |
| UA 5 mg·L-1 | 8 | 42235.25±19003.75 | 38.01 |
| UA 10 mg·L-1 | 8 | 30732.75±14051.63** | 54.69 |
| UA 15 mg·L-1 | 7 | 25852.86±14722.43** | 61.88 |
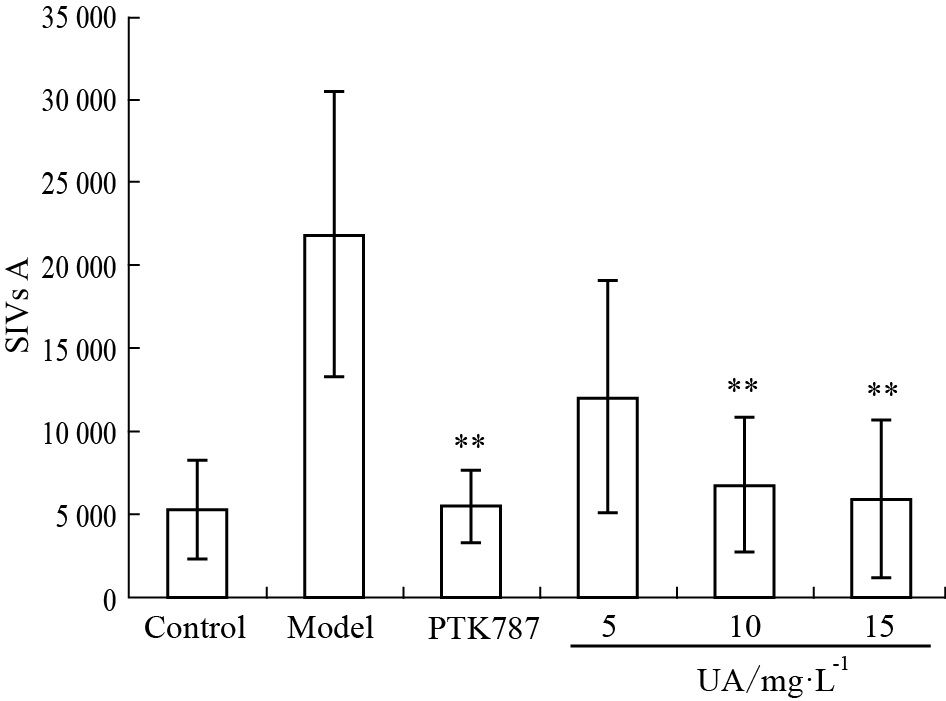
共聚焦镜下观察显示:空白对照组斑马鱼胚胎SIVs呈半月形,呈栅栏状,连续无分支,无侧枝及出芽;HT-29荷瘤模型组SIVs显示有明显增生,静脉弯曲延长,出现侧枝与分支,部分区域呈网状结构;与模型组比较,UA组显示出肠下静脉丛OD值随浓度增加减少,出芽及侧枝数量减少(Fig5),其作用具有明显剂量依赖性,UA组与模型组比较,10 mg·L-1UA与15 mg·L-1UA组差异有显著性(P<0.01,Fig4)。
|
| Fig.4 Effect of UA on SIVs in HT-29 xenografts in zebrafish after treatment for 48h **P<0.01 vs model group |

|
| Fig.5 Effect of UA on SIVs in HT-29 xenografts in zebrafish after treatment for 48h a:Control at 96hpf (0.1%DMSO); b:HT-29 xenografts zebrafish at 96hpf.; c.d.e:xenogrsfts zebrafish larvas treated with PTK787 2mg·L-1; UA 10mg·L-1; UA 15mg·L-1 at 96hpf. |
斑马鱼移植瘤模型属于国际上新型移植肿瘤动物模型,相对于实验鼠移植肿瘤模型,斑马鱼移植肿瘤模型具有成本较低、实验周期短(4~7 d),样品用量少,移植癌细胞在镜下清晰可见等优点,有利于肿瘤细胞体内迁移与新生血管的研究,目前斑马鱼胚胎肿瘤移植模型常常被用于癌细胞迁移相关基因功 能与抑制血管生成的药物筛选研究[6, 8];研究发现,不同的肿瘤细胞在斑马鱼体内的表现有差异,MDA-231、DU-145等肿瘤细胞具有较强的迁移性,会在胚胎多个部位有出现;而T-47D、HT-29等肿瘤细胞迁移则不明显,主要在卵黄区域注射部位聚集,该部位的肿瘤细胞分泌的生长因子可刺激肠下静脉SIVs明显增殖[9],因而非常适合药物初期筛选实验,在本实验我们采用了SMMC-7721与HT-29分别注射建模。
现代研究发现,UA对前列腺癌、膀胱癌、结肠癌等多种肿瘤细胞均具有抑制作用,其作用靶点广泛:有报道[10, 11, 12, 13]UA对Wnt/β-catenin、Akt/NF-κB、AMPK、STAT3等重要信号通路均有抑制作用,本项研究考察UA对斑马鱼生理性节间血管及对移植瘤环境下的血管生成的作用,应用斑马鱼移植癌模型探讨UA抗肿瘤活性在国内属首次报道。
本实验所使用的转基因斑马鱼为血管内皮生长因子Ⅱ型受体(VEGFR2)标记绿色荧光蛋白的斑马鱼,UA处理后的斑马鱼节间血管荧光减弱或者消失,镜下血流数量减少,说明UA对于斑马鱼生理状态下血管生成有抑制作用,同时也提示UA的作用机制与抑制VEGFR2的表达有关;体外研究结果表明:UA在4.57 mg·L-1 浓度时对HT-29增殖有明显抑制作用[14],本实验表明10 mg·L-1时可明显抑制HT-29引起的斑马鱼SIVs增生,说明UA抗肿瘤作用既有抗增殖作用,同时具有抑制血管生成的作用,揭示了UA的抗肿瘤作用具有多个靶点作用特点。
UA针对肝癌体外实验结果显示:UA对SMMC-7221细胞体外增殖有抑制作用,其机制为将肝癌细胞周期阻滞于S期,使DNA合成受阻,细胞丧失增殖能力[15],本实验结果表明UA对于斑马鱼胚胎体内SMMC-7221细胞数量同样具有抑制作用;并且从UA处理后斑马鱼移植瘤癌细胞分布的部位来看,其具有抑制癌细胞迁移的倾向,说明熊果酸的抗迁移作用也是其抗肿瘤活性作用,但是该现象还需要更深入的实验研究。综上,本研究证明了UA对斑马鱼体内移植癌以及移植癌诱导的血管新生均有明显的抑制作用,表明UA具有良好的抗癌活性,证明其具有较好的应用前景。
| [1] | Carmeliet P, Jain R K. Angiogenesis in cancer and other diseases[J]. Nature, 2000, 407(6801):249-57. |
| [2] | Folkman J, Angiogenesis in cancer, vascular, rheumatoid, and other diseases[J]. Nature Med, 1995,1:27-31. |
| [3] | 陈 磊, 刘 怡, 梁生旺.模式生物斑马鱼在中药研究中的应用[J].药学学报, 2012, 47(4):434-9. Chen L, Liu Y, Liang S W. Application of zebrafish model organism in the research of Chinese materia medical[J]. Acta Pharm Sin, 2012, 47 (4):434-9. |
| [4] | 王博龙.乌索酸对人肝星状细胞凋亡及TGFβ1mRNA表达的影响[J].中国药理学通报, 2010,26(3):417-8. Wang B L. Effect of ursolic acid on apoptosis and expression of TGFβ1 mRNA in human hepatic stellate cells[J].Chin Pharmacol Bull, 2010, 26(3):417-8. |
| [5] | 孟艳秋,陈 瑜,王 趱,等. 熊果酸的研究进展 [J].中国新药杂志,2007,16(1):25-9.Meng Y Q, Chen Y, Wang Z, et al. Research advance of ursolic acid [J].Chin J New Drugs, 2007,16(1):25-9. |
| [6] | Stefania N, Marco P. The zebrafish/tumor xenograft angiogenesis assay[J]. NAT protocols, 2007, 2 (11):2918-23. |
| [7] | 夏小燕, 刘可春, 王思锋, 等.大青叶靛玉红的抗血管生成活性研究[J]. 中国药学杂志, 2010, 45(3):187-9. Xia X Y, Liu K C, Wang S F, et al.Studies on anti-angiogenesis activity of indirubin from folium isatidis [J]. Chin Pharm, 2010, 45(3):187-99. |
| [8] | Yong T, Xie X Y, Steven W, et al. Evaluating human cancer cell metastasis in zebrafish [J]. BMC Cancer, 2013, 13:453-65. |
| [9] | Karni S M, Karine F L, Jamil H, et al. Discriminating different cancer cells using a zebrafish in vivo assay[J]. Cancers, 2011, 3:4102-13. |
| [10] | Park J H, Kwon H Y, Sohn E J, et al. Inhibition of Wnt/β-catenin signaling mediates ursolic acid-induced apoptosis in PC-3 prostatecancer cells [J]. Pharmacol Rep, 2013, 65(5):1366-74. |
| [11] | Gai L, Cai N, Wang L, et al. Ursolic acid induces apoptosis via Akt/NF-κB signaling suppression in T24 human bladder cancercells [J]. Mol Med Rep, 2013, 7(5):1673-7. |
| [12] | Chen M B, Zhang Y, Wei M X, et al. Activation of AMP-activated protein kinase (AMPK) mediates plumbagin-induced apoptosis and growth inhibition in cultured human colon cancer cells [J].Cell Signal, 2013, 25(10):1993-2002. |
| [13] | 唐 丹,李剑萍,郑锡凤,等. 熊果酸通过STAT3通路调控胃癌细胞增殖和凋亡[J].中国药理学通报, 2012,28(2):179-84. Tang D, Li J P, Zheng X F, et al. Regulatory effect of ursolic acid on proliferation and apoptosisof gastric cancer cells via STAT3 signaling pathway[J].Chin Pharmacol Bull, 2012, 28(2):179-84. |
| [14] | Prasad S,Yadav V R, Sung B, et al. Ursolic acid inhibits growth and metastasis of human colorectal cancer in an orthotopic nude mouse model by targeting multiple cell signaling pathways:chemosensitization with capecitabine[J].Clin Cancer Res, 2012,15,18(18):4942-53. |
| [15] | 崔兵兵, 程丽芳, 侯立静, 等. 熊果酸抑制人肝癌SMMC-7721细胞生长及凋亡的实验研究[J]. 中国实验方剂学杂志, 2013, 19(18):181-4.Cui B B, Cheng L F, Hou L J, et al. Effect of ursolic acid on inhibiting growth and apoptosis in human hepatoma SMMC-7721[J]. Chin J Exp Tradit Med Formul, 2013, 19(18):181-4. |