


机械性脑损伤是一种常见的中枢神经系统损伤性疾病,致死和致残率非常高。近些年,机械性脑损伤患者正逐年增加,严重影响患者的工作能力及生活质量,给患者及家属造成严重的精神及经济压力。机械性颅脑损伤的病理过程包括原发性损伤和继发性损伤,原发性损伤是与外界直接作用导致;继发性损伤包括炎症反应、氧自由基的增多和神经元坏死凋亡等[1, 2]。
近些年,中药在中枢神经系统方面的作用越来越受到重视,有研究表明,氧化苦参碱能够减少大鼠缺血性脑损伤后神经细胞凋亡,修复神经功能;山茱萸环烯醚萜苷能够抑制大鼠创伤性脑损伤后炎症因子的释放,减轻了继发性损伤[4]。近年来发现蛇床子素(osthole,Ost)在中枢神经系统中具有广泛的药理作用,具有抗炎、抗凋亡、抗氧化以及神经营养作用[5, 6, 7],但是Ost对创伤性脑损伤小鼠的抗炎抗凋亡作用,还未见报道。本实验主要探讨Ost对小鼠脑损伤后炎症细胞浸润及细胞凋亡的影响。
1 材料与方法 1.1 材料 1.1.1 动物昆明种小鼠,购于大连医科大学实验动物中心,许可证号: SCXK(辽) : 2008-0002。
1.1.2 试剂蛇床子素(中国药品检验所,纯度>98%,批号:110822-200407);DMSO (Sigma公司);RevertAidTM First Strand cDNA Synthesis Kit (Thermo);PCR Master Mix Kit (Thermo);冰冻切片包埋剂(美国樱花);兔抗Caspase-3多克隆抗体、兔MPO多克隆抗体、兔抗Iba-1多克隆抗体(北京博奥森);Cy3标记驴抗兔IgG二抗、FITC标记羊抗兔IgG二抗 (Jackson);抗荧光淬灭剂 (碧云天);其他试剂均为国产分析纯。
1.1.3 仪器Ti-S型荧光显微镜(日本尼康公司);ST-5ND型脑立体定位仪(成都仪器厂);MG96G型PCR仪(杭州朗基);水平核酸电泳仪(Bio-Rad);4100型凝胶成像系统(UVP);CM-1850型冰冻切片机 (德国徕卡)。
1.2 方法 1.2.1 实验分组将40只小鼠(体质量30 g±5 g)随机分为5组,每组8只,分别为(1)假手术组(Sham);(2)模型组(SWI);(3)10 mg·kg-1蛇床子素组;(4)20 mg·kg-1蛇床子素组;(5)30 mg·kg-1蛇床子素组。
1.2.2 开放性脑损伤模型的制备根据以往文献报道的开放性脑刺伤模型的制备方法[8],利用10%乌拉坦对小鼠腹腔注射麻醉,麻醉起效后,将其固定于脑立体定位仪中,消毒、切开头皮、分离骨膜,确定损伤位点:距颅骨中线左侧2 mm、人字缝前2 mm处。利用牙钻将小鼠颅骨钻开直径约1.5 mm的圆孔,但不伤及大脑皮层。利用直径为1.3 mm探针垂直插入脑组织中,为了减小误差,控制脑立体定位仪进针手柄,使其进针速度与深度一致,深度为2 mm,停留30 min,然后拔出探针,止血,缝合切口,消毒。将损伤后的小鼠置于鼠笼中,待其苏醒。假手术组只钻孔,不刺伤皮层。损伤1 h后根据文献记载的方式采用腹腔注射给药(药物浓度为1 g·L-1)[6],每天1次;Sham组给予等量含DMSO(<0.1%)的蒸馏水,最后1次注射后4 h后处死小鼠,取脑。包埋,置于-20℃冰冻切片机中做连续冠状切片,片厚8 μm。
1.2.3 针刺伤开放性脑损伤模型评价方法利用神经功能缺损评分(neurological severity scores,NSS)对造模方法进行评价[9],NSS评分包括了力量、运动、感知及平衡能力测评,NSS评分包含了评分大于6说明脑损伤模型制作成功。
1.2.4 脑组织含水量的检测取损伤后3 d的小鼠,根据文献报道的脑组织含水量的检测方法进行实验[10, 11],将各组小鼠麻醉后取脑,将取好的脑组织沿中线分为两部分,取损伤侧脑组织置于锡箔纸上测量其重量(湿重),将其置于烘箱中100℃ 24 h后测量重量(干重)。
脑组织含水量/%=(湿重-干重)/湿重×100%
1.2.5 逆转录PCR检测凋亡相关基因表达情况取蛇床子素治疗7 d后各组小鼠脑组织,TRIzol法提取各组细胞总RNA,取各组总RNA 3μg,按照试剂盒说明书合成cDNA[12]。取2 μL cDNA为模板,按照RT-PCR试剂盒说明书进行体外扩增,DNA引物由北京赛诺科为生物科技有限公司合成,序列为内参β-actin上游引物:5′-GGGAAATCGTGCGTGACAT-3′;下游引物:5′-TCAGGAGGAGCAATGATCTTG-3′,Bcl-2上游引物:5′-CGCTGGGAGAACAGGGTA-3′;下游引物:5′-GGGCTGGGAGGAGAAGAT-3′,Bax上游引物:5′-CTGACATGTTTTCTGACGGC-3′;下游引物:5′-TCAGCCCATCTTCTTCCAGA-3′;Caspase-3上游引物:5′-AGATACCGGTGGAGGCTGACT-3′;下游引物:5′-TCTTTCGTGAGCATGGACACA-3′。琼脂凝胶电泳,凝胶成像仪拍照,Image J图像分析系统进行分析。结果用相对光密度表示,相对光密度=光密度目的基因/光密度β-actin。
1.2.6 免疫组织化学染色方法利用免疫组织化学染色法检测MPO、Iba-1、Caspase-3细胞表达情况。将8 μm厚脑冰冻冠状切片置于室温晾干,PBS洗;4%多聚甲醛固定30 min,PBS洗×3次;1% Triton X-100透化30 min,PBS洗×3次;5% BSA封闭30 min;兔抗MPO、Iba-1、Caspase-3多克隆抗体(1:150) 4℃孵育过夜,次日滴加Cy3标记驴抗兔、FITC标记羊抗兔二抗(1:300)室温孵育1 h,DAPI染核15 min,滴加少量抗荧光淬灭剂,盖玻片封片,置于荧光显微镜下观察各组MPO、Iba-1、Caspase-3细胞的表达变化。
1.2.7 统计学处理采用SPSS 13.0统计软件进行统计学分析,数据以 ± s表示,对所得数据进行单因素方差分析和t检验。
± s表示,对所得数据进行单因素方差分析和t检验。
各组小鼠清醒后,分别于损伤后12 h进行NSS评分检测,假手术组各只小鼠NSS评分少许增加,说明假手术对小鼠造成了轻微的神经损伤,其余各组小鼠清醒后均出现了不能行走或者偏瘫、感知反射等能力丧失的现象,其余各组与假手术组相比,NSS评分明显增加,见表1(P<0.01),并且各组NSS评分均大于6,说明机械性脑损伤模型制备成功,能够用于以后的实验。
| Group | 12 h |
| ##P<0.01 vs sham group | |
| Sham | 3.67±1.15 |
| SWI | 16.33±1.53## |
| Ost 10 mg·kg-1 | 15.33±1.53 |
| Ost 20 mg·kg-1 | 15.67±0.58 |
| Ost 30 mg·kg-1 | 15.00±1.00 |
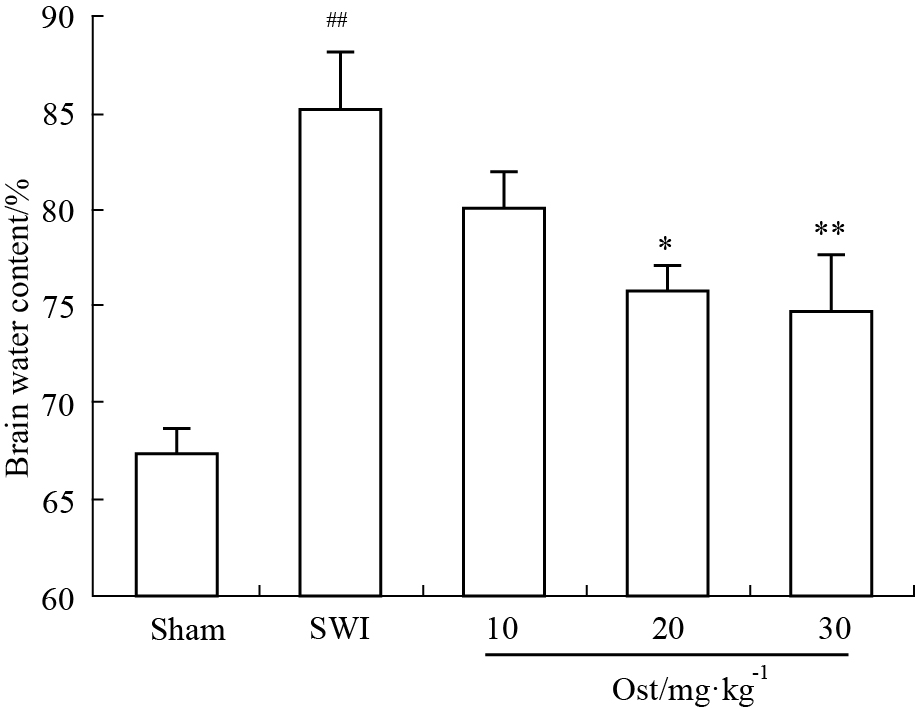
为了验证不同剂量的蛇床子素能否降低脑组织含水量,减轻水肿程度,我们于损伤后3d进行了脑组织含水量的测定。结果显示,SWI组与Sham组相比,脑组织含水量明显增加(P<0.01),20 mg·kg-1与30 mg·kg-1蛇床子素组脑组织含水量与SWI组相比,均能够降低脑组织含水量,减少水肿,且差异具有显著性(P<0.05,P<0.01);20 mg·kg-1与30 mg·kg-1蛇床子素组差异并没有显著性(P>0.05)。而10 mg·kg-1蛇床子素组则无明显作用(P>0.05)。Sham组、SWI组、10、20、30 mg·kg-1 Ost组脑组织含水量分别为:(67.36±1.39)%、(85.27±2.92)%、(80.18±1.85)%、(75.89±1.30)%、(74.86±2.87)%,见Fig1。
|
| Fig.1 Effect on brain water content with Ost treatment ##P<0.01 vs sham group; *P<0.05,**P<0.01 vs SWI group |
我们于损伤后7 d进行了RT-PCR实验,检测蛇床子素对脑组织损伤后凋亡的影响,结果显示,SWI组与Sham组相比,凋亡因子Bax/Bcl-2 mRNA比率,caspase-3 mRNA表达量明显增加(P<0.01),20与30 mg·kg-1蛇床子素组与SWI组相比,均能够降低Bax/Bcl-2 mRNA比率,caspase-3 mRNA表达量且差异具有显著性(P<0.05,P<0.01);20与30 mg·kg-1蛇床子素组并没有显著性差异(P>0.05)。而10 mg·kg-1蛇床子素组则无明显作用(P>0.05)。Sham组、SWI组、10、20、30 mg·kg-1 Ost组Bax/Bcl-2 mRNA比率分别为:(0.34±0.10)%、(1.64±0.20)%、(1.26±0.12)%、(0.78±0.19)%、(0.62±0.18)%; Sham组、SWI组、10、20、30 mg·kg-1 Ost组caspase-3 mRNA表达量分别为:(0.24±0.04)%、(0.53±0.06)%、(0.41±0.06)%、(0.35±0.05)%、(0.31±0.03)%,见Fig2。

|
| Fig.2 Effect of osthole on apoptotic cytokines mRNA in injuryed mice brains 1: Sham; 2: SWI; 3: Ost 10 mg·kg-1; 4: Ost 20 mg·kg-1; 5: Ost 30 mg·kg-1. ##P<0.01 vs sham group; *P<0.05,**P<0.01 vs SWI group |
我们于损伤后7 d利用免疫组织化学染色法,测定caspase-3阳性细胞数量,研究蛇床子素对机械性脑损伤小鼠的抗凋亡作用。结果显示,SWI组与Sham组相比,caspase-3阳性细胞数量明显增加(P<0.01),30 mg·kg-1蛇床子素组与SWI组相比,能够明显降低caspase-3阳性细胞数量 (P<0.05)。Sham,SWI,30 mg·kg-1 Ost组脑组织含水量分别为:(19.67±4.16) cells/mm2,(115.33±17.21) cells/mm2,(64.00±4.58) cells/mm2,见图3。

|
| Fig.3 Effect on apoptotic cytokine caspase-3 with Ost treatment ##P<0.01 vs sham group; **P<0.01 vs SWI group |
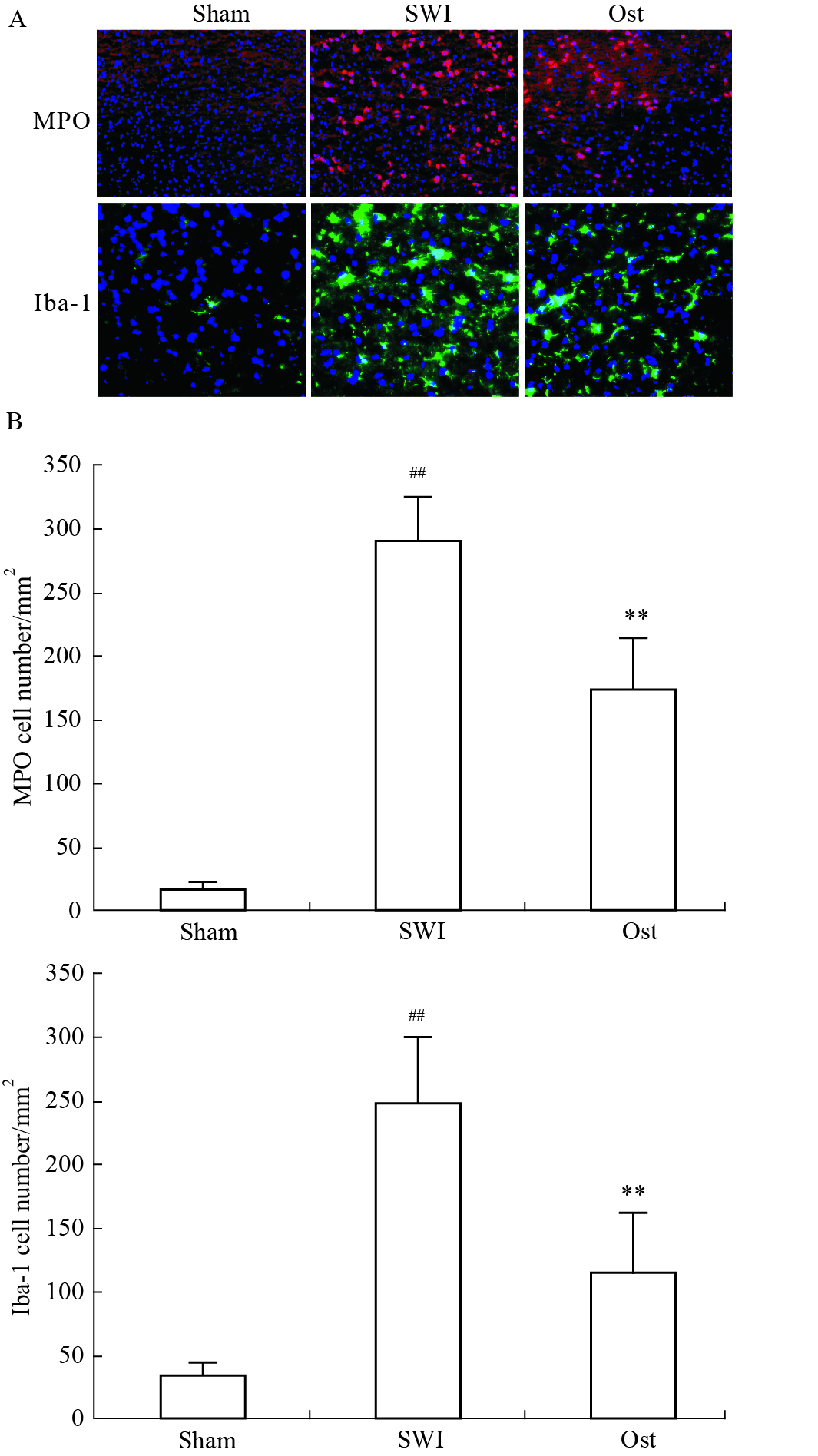
为了研究蛇床子素是否能够减轻脑损伤后伤口周围炎症细胞的浸润现象,我们于损伤后3 d利用免疫组织化学方法检测了损伤皮层中性粒细胞(MPO),小胶质细胞(Iba-1)阳性细胞的表达情况。结果显示,未损伤组MPO,Iba-1阳性细胞数量非常少,而SWI组与Sham组相比,MPO明显增加(P<0.01),30 mg·kg-1蛇床子素组与SWI组相比,能够明显减轻中性粒细胞浸润情况,差异具有显著性(P<0.01)。Sham组、SWI组、30 mg·kg-1 Ost组MPO细胞数量分别为:(18.83±6.37) cells·mm-2、(290.67±34.89) cells·mm-2、(176.00±39.48) cells·mm-2。损伤后Iba-1数量也明显增加(P<0.01),经30 mg·kg-1蛇床子素治疗后其数量明显降低(P<0.01)。Sham组、SWI组、30 mg·kg-1 Ost组Iba-1细胞数量分别为:(34.67±10.78) cells·mm-2、(247.83±52.29) cells·mm-2、(115.33±47.96) cells·mm-2,见图4。
|
| Fig.4 Effect of osthole on inflammatory cytokines in injuryed mice brains ##P<0.01 vs sham group; **P<0.01 vs SWI group |
蛇床子素是独活和蛇床子等中药的主要活性成分,属于香豆素类化合物[13]。具有神经营养作用的中药单体蛇床子素能够保护由Aβ损伤的大脑皮层神经元;在实验性自身免疫性脑脊髓炎动物模型中,蛇床子素能够通过改善病处微环境,促进外源性NSCs存活与分化,促进髓鞘与轴突再生,并发挥神经营养等作用[14, 15]。本实验通过建立小鼠开放性脑刺伤模型,我们证实了这种模型制备方法能够造成小鼠神经功能的损伤,能够用于实验。血脑屏障被破坏,脑内含水量升高,继而导致脑水肿[16],本实验证明20、30 mg·kg-1蛇床子素能够减轻损伤后脑组织含水量,有利于水肿的消除和血脑屏障的恢复。
细胞凋亡主要是线粒体损伤,导致线粒体功能改变或丧失,激活caspase凋亡级联反应,最终导致凋亡[17]。 Bcl-2家族基因是细胞内一种重要的抗凋亡因子,凋亡发生过程中,Bcl-2表达降低;Bax则是Bcl-2家族中一种促凋亡因子,Bcl-2和Bax基因可以形成二聚体,当Bcl-2表达量多时抑制细胞凋亡,当Bax表达多时促进细胞凋亡。本实验证实20、30 mg·kg-1蛇床子素能够降低损伤后脑组织内Bax/Bcl-2的比率及caspase-3 mRNA的表达,并且30 mg·kg-1蛇床子素能够减少caspase-3阳性细胞的数量,因此蛇床子素能够抑制损伤后神经细胞的凋亡。
脑损伤导致的炎症反应可能会引起并加重继发性脑损伤,如中性粒细胞浸润会导致脑水肿,形成恶性循环[18]。中性粒细胞及小胶质细胞是脑损伤发生后比较常见的炎症细胞,所以本实验利用免疫组织化学染色法检测了脑内MPO、Iba-1的表达量,结果发现,脑损伤后脑内MPO、Iba-1的表达量明显增多,当给予蛇床子素后脑内MPO、Iba-1的表达量明显减少,炎症细胞浸润现象减轻。这充分说明了蛇床子素对炎症反应的抑制作用,也进一步证明了蛇床子素通过减轻炎症因子和炎症反应而减轻脑损伤程度。
综上所述,蛇床子素可以减轻小鼠机械性脑损伤,并且证实蛇床子素发挥的治疗作用是通过抑制细胞凋亡,抑制炎症细胞,减轻炎症反应,发挥治疗作用。为有效修复治疗脑损伤等神经系统难治性疾病开辟新的思路与途径,具有广阔的临床应用前景和重大的社会经济价值。
(以上实验内容在辽宁中医药大学药学院药理实验室完成)。
| [1] | Lu X Y, Wang H D, Xu J G, et al. NADPH oxidase inhibition improves neurological outcome in experimental traumatic brain injury[J].Neurochem Intern,2014, 69:14-9. |
| [2] | Povlishock J T, Katz D I. Update of neuropathology and neurological recovery after traumatic brain injury[J]. J Head Trauma Rehabil, 2005, 20:76-94. |
| [3] | 程 钢, 秦媛媛, 程 迪, 等. 氧化苦参碱对大鼠局灶性脑缺血损伤的保护作用及其抑制凋亡的作用机制[J]. 中国药理学通报, 2013, 29(3):387-92. Chen G, Qin Y Y, Cheng D, et al. Protection of oxymatrine on focal crerebral ischemic injury in rats and its mechanism of inhibition of apoptosis[J]. Chin Pharmacol Bull, 2013, 29(3):387-92. |
| [4] | 王 娜, 李 林. 山茱萸环烯醚萜苷对创伤性脑损伤模型大鼠脑内炎症反应的影响[J]. 中国临床药理学与治疗学, 2010, 15(3):255-9.Wang N, Li L. Effects of cornel iridoid glycoside on inflammatory reaction in the brain of traumatic brain injury rat model[J]. Chin J Clin Pharmacol Ther, 2010, 15(3):255-9. |
| [5] | Chao X, Zhou J, Chen T, et al. Neuroprotective effect of osthole against acute ischemic stroke on middle cerebral ischemia occlusion in rats[J]. Brain Res, 2010, 1363:206e211. |
| [6] | Ji H J,Hu J F,Wang Y H,et al.Osthole improves chronic cerebral hypoperfusion induced cognitive deficits and neuronal damage in hippocampus[J].Eur J Pharmacol,2010,636(1-3):96-101. |
| [7] | Chen X, Pi R, Zou Y, et al. Attenuation of experimental autoimmune encephalomyelitis in C57 BL/6 mice by osthole, a natural coumarin[J]. Eur J Pharmacol, 2010, 629(1-3):40-6. |
| [8] | Robel S, Bardehle S, Lepier A, et al. Genetic deletion of cdc42 reveals a crucial role for astrocyte recruitment to the injury site in vitro and in vivo[J]. J Neurosci, 2011, 31:12471-82. |
| [9] | Chen J, Li Y, Wang L, et al. Therapeutic benefit of intravenous administration of bone marrow stromal cells after cerebral ischemia in rats[J]. Stroke, 2001, 32(4):1005-11. |
| [10] | Taya K, Marmarou C R, Okuno K, et al. Effect of secondary insults upon aquaporin-4 water channels following experimental cortical contusion in rats[J]. J Neurotrauma, 2010, 27:229-39. |
| [11] | Zhang R, Liu Y, Yan K, et al. Anti-inflammatory and immunomodulatory mechanisms of mesenchymal stem cell transplantation in experimental traumatic brain injury[J]. J Neuroinflamm, 2013, 10(1):106. |
| [12] | Zhang N, Wen Q, Ren L, et al. Neuroprotective effect of arctigenin via upregulation of P-CREB in mouse primary neurons and human SH-SY5Y neuroblastoma cells[J]. Int J Mol Sci, 2013, 14(9):18657-69. |
| [13] | 胡 昱, 赵 丹, 张晓丹, 等. 独活不同提取部位抑制H2O2诱导的SH-SY5Y细胞损伤[J]. 中国实验方剂学杂志, 2013, 19(24):184-8.Hu Y, Zhao D, Zhang X D, et al. Different extracts of Angelica pubescens inhibit H2O2-induced SH-SY5Y cells injury[J]. Chin J Exp Tradit Med Formul, 2013, 19(24):184-8. |
| [14] | Hu Y, Wen Q, Liang W, et al. Osthole reverses beta-amyloid peptide cytotoxicity on neural cells by enhancing cyclic AMP response element-binding protein phosphorylation[J]. Biol Pharm Bull, 2013, 36(12):1950-8. |
| [15] | Gao Z, Wen Q, Xia, Y, et al. Osthole augments therapeutic efficiency of neural stem cells-based therapy in experimental autoimmune encephalomyelitis[J]. J Pharmacol Sci, 2014, 124(1):54-65. |
| [16] | Li M, Li F, Luo C, et al. Immediate splenectomy decreases mortality and improves cognitive function of rats after severe traumatic brain injury[J]. J Trauma, 2011,71:141-7. |
| [17] | Sins N R, Muydeman H. Mitochondria, oxidative metabolian and cell death in sroke[J]. Biochim Biophys Acta, 2010, 1802(1):80-91. |
| [18] | Bareyre F, Wahl F, McIntosh T K, et al. Time course of cerebral edema after traumatic brain injury in rats:effects of riluzole and mannitol[J]. J Neurotrauma, 1997, 14(11):839-49. |

