


2. 河北省心脑血管病中医药防治重点实验室, 河北 石家庄 050200;
3. 河北医科大学第三医院, 河北 石家庄 050052;
4. 河北医科大学, 河北 石家庄 050017

 , FANG Ming-xing3, GUO Qian-yu4, LI Yun-feng1, XU Bing-yuan1, LAI Shao-hong4, ZHANG Shang-yue1, LIU Yu1, LI Ai-ying1
, FANG Ming-xing3, GUO Qian-yu4, LI Yun-feng1, XU Bing-yuan1, LAI Shao-hong4, ZHANG Shang-yue1, LIU Yu1, LI Ai-ying1 2. Hebei Key Laboratory of Chinese Medicine Research on Cardiocerebrovascular Disease, Shijiazhuang 050200 China;
3. The Third Hospital of Hebei Medical University, Shijiazhuang 050052, China;
4. Hebei Medical University, Shijiazhuang 050017, China
血管平滑肌细胞是构成血管壁组织结构及维持血管张力的主要细胞成分,其结构及功能的改变是导致高血压、动脉粥样硬化和血管成形术后再狭窄等多种心血管病的细胞病理学基础。损伤诱导的血管平滑肌细胞(vascular smooth muscle cell,VSMC)由中膜向内膜下迁移、增殖、合成和分泌大量细胞外基质等事件是导致血管重构的主要病理机制[1]。PCNA是VSMC增殖的重要标志,其表达水平的高低可反映细胞的增殖活性。血小板源性生长因子(platelet-derived growth factor,PDGF)是激活VSMC的主要因素之一[2],它通过与VSMC膜上受体结合,逐级激活丝裂原活化蛋白激酶(mitogen activated protein kinases,MAPK)通路,促进细胞的有丝分裂[3, 4],从而引起细胞的增殖。因此,基于已知的VSMC增殖调节机制,寻找药物干预与此相关的病理过程已经成为目前防治心血管疾病的重要策略之一。
羟基红花黄色素A(hydroxysafflor yellow A,HYSA)是从活血化瘀中草药红花中分离出来的黄酮类化合物,具有抗氧化、清除自由基、抗炎、增强机体免疫功能多种药理作用,对免疫、心脑血管、神经等系统均有保护效应[5, 6]。大量研究发现,HYSA对心血管疾病具有很好的治疗作用[7, 8],但该化合物对血管增生性疾病的防治机制还不清楚。本实验探讨HYSA对VSMC增殖的影响及其机制,旨在为HYSA在防治血管重塑性疾病中的应用提供实验依据。
1 材料与方法 1.1 材料清洁Ⅱ级♂ SD大鼠,体质量80~100 g,由河北省实验动物中心(合格证号:10061783)提供。DMEM培养基、胎牛血清(R&D Systems公司);抗体(Santa Cruz公司);羟基红花黄色素A由西安森冉生物工程有限公司提供,高效液相色谱法测定其纯度为99 %;PDGF-BB(Gibco产品);其他试剂盒(南京建成生物公司)。
1.2 方法 1.2.1 细胞培养取大鼠胸腹主动脉,用贴块法分离培养VSMC,取3~6代细胞进行实验。待细胞生长至汇合70%~80%后换用无血清培养液饥饿培养24 h,使细胞同步于静止期,分别加入不同浓度HYSA(0、5、10、20及40 μmol·L-1)预孵育24 h,加入PDGF(10 μg·L-1)处理24 h,收集细胞用于部分实验。
1.2.2 MTT分析将处于对数生长期的VSMC接种于96孔板中,每孔150 μL (约3×100个细胞),培养24 h后,换用无血清2% FBS培养液培养24 h,使VSMC同步化,然后换用2% FBS培养液,每组设6个复孔,分别加入不同浓度 (0、1、5、10、20、40、60 μmol·L-1) 的HYSA预孵育24 h,再用PDGF (10 μg·L-1) 刺激24 h后,各孔加入MTT (5.5 g·L-1) 20 μL,37℃孵育4 h,弃去上层培养基,每孔各加DMSO 150 μL,摇床低速振荡至蓝紫色结晶溶解,然后在酶标仪上于570 nm波长处测吸光度,实验重复3次。
1.2.3 免疫细胞化学染色将VSMC接种于盖玻片上,待生长至60%~70% 融合时,换用2% FBS培养液培养24 h使细胞同步化,之后加入20 μmol·L-1的HYSA 预孵育24 h,而后用PDGF (10 μg·L-1)刺激24 h。取出玻片,冷PBS清洗两次,4 %多聚甲醛固定20 min,1% Triton X-100处理20 min,10%山羊血清室温封闭15 min,分别加入大鼠抗PCNA单克隆抗体 (1 ∶ 150) 37℃孵育30 min。经PBS充分漂洗后,依次滴加生物素标记的二抗、辣根过氧化物酶标记的链霉卵白素进行结合反应,DAB显色,80%甘油封片后,照相分析结果。
1.2.4 Western blot分析收集各组细胞,用冷PBS洗涤2次后,将细胞重悬于细胞裂解液 (1 % NP40,150 mmol·L-1 NaCl,50 mmol·L-1 Tris-HCl,pH 7.5,10 % 甘油,1 mmol·L-1 Na3VO4,1 mmol·L-1 PMSF,1 mmol·L-1 DTT) 中,冰浴40 min,使细胞充分裂解。4℃,8 000 r·min-1离心10 min,收集上清,用改良的 Lowry 法进行蛋白定量。取等量的VSMC蛋白的提取液,进行SDS-PAGE电泳,电转移至PVDF膜上,随后与相应的一抗及二抗反应,用化学发光法检测抗原抗体结合的显色区带。用数码成像分析系统软件对电泳条带进行密度扫描,以β-actin为内参照进行定量分析。
1.2.5 统计学处理数据以 ± s表示,组间资料应用单因素方差(one way ANOVA)分析,各项统计均用SPSS 13.0统计软件进行处理。
± s表示,组间资料应用单因素方差(one way ANOVA)分析,各项统计均用SPSS 13.0统计软件进行处理。
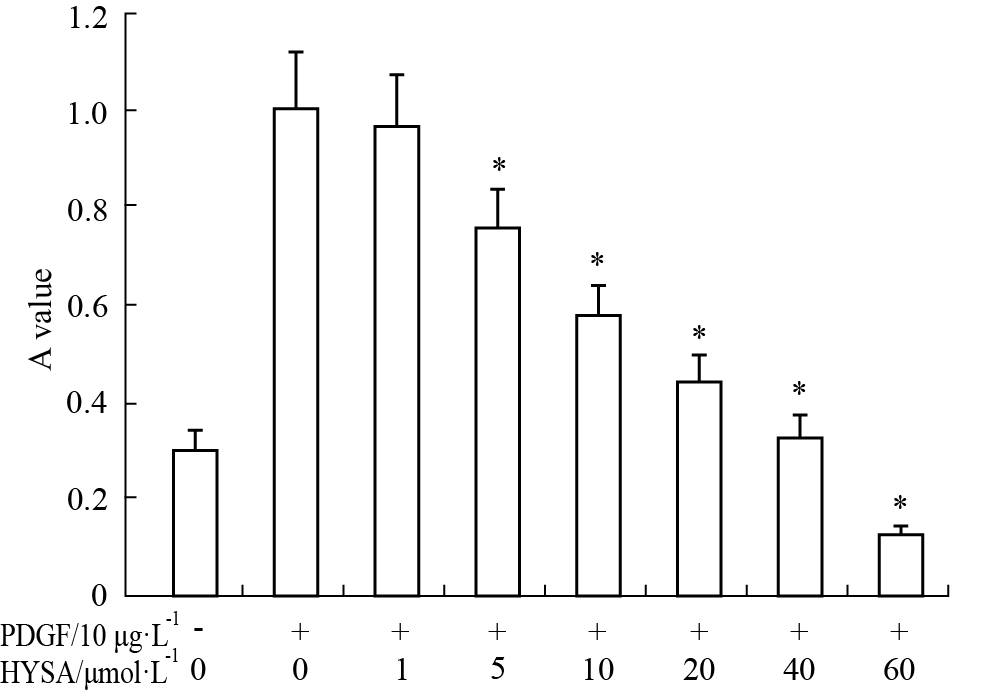
MTT结果显示,在HYSA浓度为5至60 μmol·L-1的范围内,随着HYSA浓度增加,VSMC增殖活力下降,呈剂量依赖性(P<0.05,Fig1)。其中当用20 μmol·L-1 HYSA刺激时,细胞生长状态良好,抑制程度明显,故以下实验采用20 μmol·L-1 的HYSA作为实验条件。
|
| Fig 1 Inhibition of hydroxysafflor yellow A on VSMC proliferation induced by PDGF (n=6) *P<0.05 vs group of PDGF stimulation. |
实验采用Western blot、免疫细胞化学实验方法,观察了HYSA对增殖标志基因PCNA表达的影响。Western blot分析显示,在蛋白水平,随着HYSA浓度的增加,PCNA表达逐渐降低。免疫细胞化学结果显示,20 μmol·L-1 HYSA刺激24 h后,PCNA表达明显低于对照组(Fig2)。

|
| Fig 2 Hydroxysafflor yellow A inhibition of VSMC proliferation induced by PDGF (n=6) A: Western blot; B: Densitometric scanning;C: Immunocytochemistry,**P<0.01 vs PDGF stimulation. |
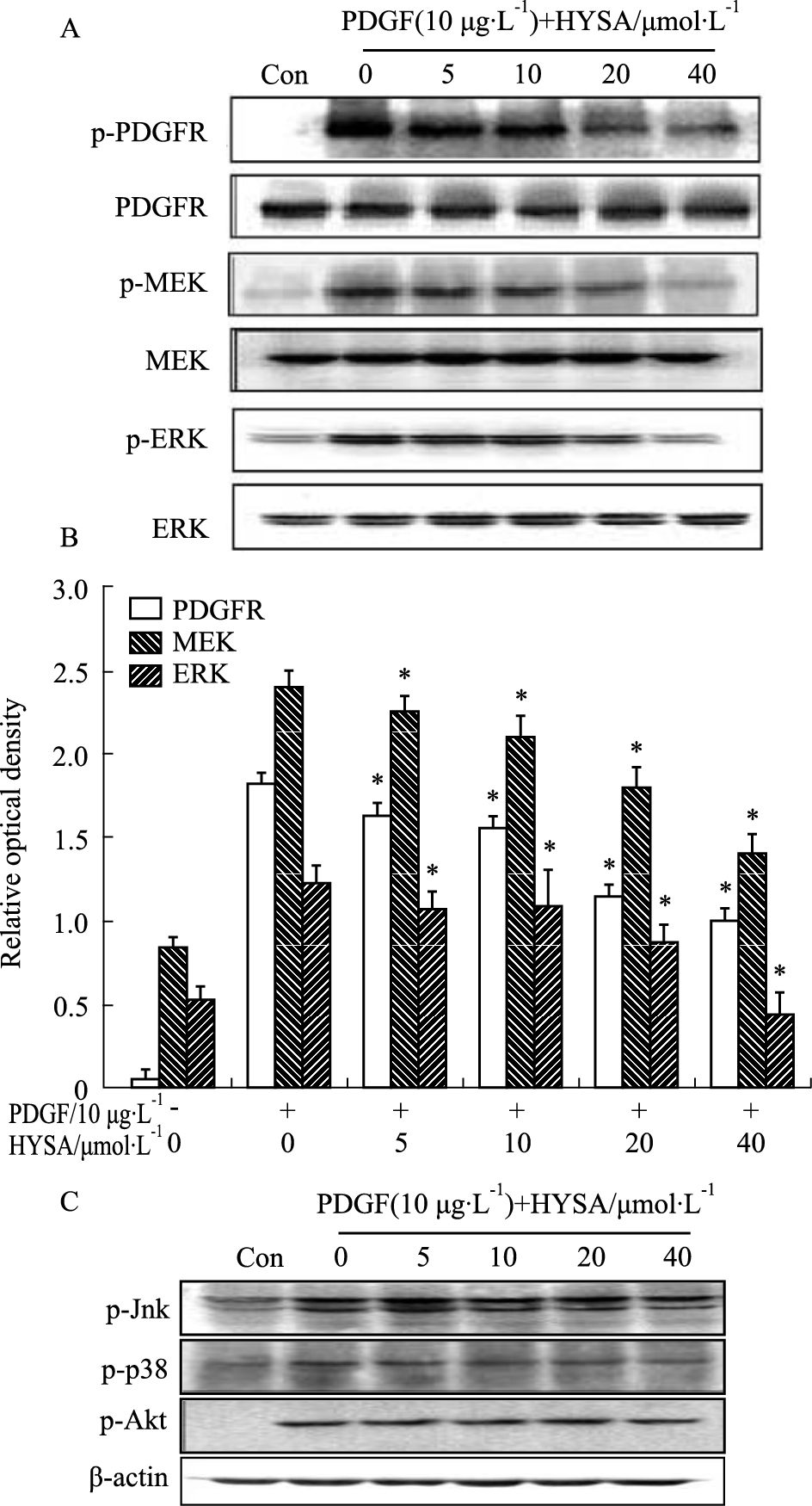
实验采用Western blot方法,观察到PDGF刺激细胞15 min,PDGFR磷酸化水平明显升高;而经HYSA预处理的VSMC,磷酸化的PDGFR呈浓度依赖性地降低;MEK和ERK1/2磷酸化程度也随着药物浓度的增加逐渐降低;但对JNK、p38及Akt的磷酸化没有影响(Fig3)。
|
| Fig 3 Inhibition of hydroxysafflor yellow A on PDGF-induced tansmembrane signal transduction in VSMC A: Western blot; B: Densitometric scanning; C: Western blot. *P<0.05 vs PDGF stimulation. |
血管平滑肌细胞异常增殖是高血压、动脉粥样硬化和血管成形术后再狭窄等血管重塑性疾病发生、发展的重要细胞病理学基础[9, 10]。当血管内膜受损伤后,局部暴露的中膜VSMC发生表型转化,并向内膜下迁移、增殖和分泌细胞外基质,最终导致血管重塑,管腔狭窄。流行病学调查发现,PTCA术后由于血管重塑导致的再狭窄率严重限制了其临床疗效。因此,寻找可抑制血管平滑肌细胞增殖、迁移的有效药物,已成为当前防治血管重塑性疾病的重要策略之一[11]。
细胞增殖活力是反映VSMC增殖程度的重要指标。MTT结果显示,在羟基红花黄色素A 浓度在1~60 μmol·L-1范围内,随着HYSA浓度增加,VSMC增殖活力不断下降,呈剂量依赖性。其中浓度为5~60 μmol·L-1时,与对照组相比,分别下降了25%、41%、52%和63%,差异有显著性(Fig1)。MTT检测结果表明,HYSA可明显抑制PDGF诱导的VSMC增殖,并具有明显的量-效依赖关系。
PCNA是细胞增殖的重要标志基因,其表达水平的高低可反映VSMC的增殖活性。本实验采用Western blot和免疫组化分析的方法,观察了HYSA对增殖标志基因PCNA表达的影响。如Fig2所示,在蛋白水平,Western blot结果表明,随着HYSA浓度的增加,PCNA表达逐近降低;免疫细胞化学结果显示,20 μmol·L-1HYSA刺激24 h后,PCNA表达明显低于对照组。上述结果进一步说明了MTT分析的结果的正确性(Fig1),即HYSA能抑制体外培养的VSMC的增殖。
MAPK属于蛋白丝/苏氨酸激酶类,是接受膜受体转换和传递信号并将其带入细胞膜内的一类重要分子,在许多细胞增殖分化相关的信号通路中具有关键的作用。该信号转导通路在未受刺激时,处于静止状态;在受到生长因子的刺激时,在上游激酶的作用下,发生级联磷酸化而激活,MAPK被激活后进入细胞核,使一些转录因子磷酸化,改变细胞基因的表达状态,参与细胞的生长、分化、增殖、凋亡、存活等多种生理过程的调控[12, 13]。哺乳动物MAPK家族主要包括ERK1/2、p38和JNK 3个亚家族[13]。其中ERK包括ERK1和ERK2,主要参与细胞增殖与分化的调控,多种生长因子受体都需要ERK的活化而完成信号转导过程; p38蛋白激酶是一种分子质量38 ku磷酸化蛋白激酶,在各种应激或细胞因子等的刺激下,其分子中的苏氨酸、酪氨酸位点发生磷酸化而被激活,主要参与介导抗凋亡、增生和细胞生存信号的转导;JNK由JNK1、JNK2、JNK3组成,分别由JNK激酶1,2 (也分别称为MKK4、MKK7) 激活,在细胞应激反应中起重要作用。大量实验表明,MAPK通路在血管再狭窄中具有重要的作用,血管内皮损伤可以引起VSMC中MAPK通路信号分子的高表达。以往研究证明,HYSA对细胞的增殖和氧化应激等都有明显的抑制作用,临床中广泛应用于心血管疾病的治疗[5, 15, 16, 17]。但HYSA对心血管疾病作用的分子机制尚不清楚,对VSMC增殖的影响鲜有报道。本课题组采用PDGF诱导VSMC增殖,利用HYSA干预其增殖过程,观察了MAPK 3个亚家族介导的信号传导对VSMC增殖的影响,我们观察了HYSA阻断PDGFR活化后对MAPK信号通路的影响。 结果显示(Fig3),HYSA可选择性抑制PDGF诱导的MEK/ERK1/2的磷酸化活化,但不影响JNK、p38MAPK及Akt的磷酸化活性。该结果提示,HYSA 抑制VSMC增殖与其特异性阻断MEK/ERK1/2信号通路有关,而与JNK和p38MAPK介导的信号通路无关。
综上所述,HYSA是一种具有抗VSMC增殖作用的天然单体,通过降低细胞增殖标志基因PCNA表达和MEK-ERK1/2信号通路抑制大鼠血管平滑肌细胞增殖,能够明显抑制PDGF诱导的VSMC增殖,为该药物在防治血管重塑性疾疗中的应用提供了实验依据。
(致谢:该研究课题在河北省心脑血管病中医药防治重点实验室、河北中医学院基础医学院生物化学与生物学教研室完成,在此感谢)
| [1] | Fernández-Mariño A I, Cidad P, Zafra D, et al. Tungstate-targeting of BKαβ1 channels tunes ERK phosphorylation and cell proliferation in human vascular smooth muscle [J]. PLoS One, 2015,10(2):118148. |
| [2] | Nurminskaya M, Beazley K E, Smith E P, Belkin A M. Transglutaminase 2 Promotes PDGF-Mediated activation of PDGFR/Akt1 and β-Catenin signaling in vascular smooth muscle cells and supports neointima formation [J]. J Vasc Res, 2014,51(6):418-28. |
| [3] | Simões M R, Aguado A, Fiorim J, et al. MAPK pathway activation by chronic lead-exposure increases vascular reactivity through oxidative stress/cyclooxygenase-2-dependent pathways [J]. Toxicol Appl Pharmacol, 2015,283(2):127-38. |
| [4] | Chang H J, Park J S, Kim M H, et al. Extracellular signal-regulated kinases and AP-1 mediate the up-regulation of vascular endothelial growth factor by PDGF in human vascular smooth muscle cells [J]. Int J Oncol, 2006,28(1):135-41. |
| [5] | 万先惠,秦亚利,颜 涛.红花注射液药理作用研究进展[J].中医药学报,2011,39(6):109-11. Wan X H, Qin Y L, Yan T. pharmacologic actions of HONGHUA injection in research progress[J].Acta Chin Med Pharmacol,2011,39(6):109-11. |
| [6] | 张 前,牛 欣,闫 妍,等.羟基红花黄色素A 抑制新生血管形成的机制研究[J].北京中医药大学学报, 2004,27(3):25-9. Zhang Q, Niu X, Yan Y, et al. Research on the Mechanism of Hydroxysafflor Yellow A in Inhibiting Angiogenesis[J]. J Beijing Univer TCM,2004,27(3):25-9. |
| [7] | Wei X, Liu H, Sun X. Hydroxysafflor yellow A protects rat brains againstischemia-reperfusion injury by antioxidant action [J]. Neurosci Lett, 2005,386:58-62. |
| [8] | He H, Liu Q, Shi M, et al. Cardioprotective effects of hydroxysafflor yellow A on diabetic cardiac insufficiency attributed to up-regulation of the expression of intracellular calcium handling proteins of sarcoplasmic reticulum in rats [J]. Phytother Res, 22(3):1107-14. |
| [9] | Yoshiyama S, Chen Z, Okagaki T,et al. Nicotine exposure alters human vascular smooth muscle cell phenotype from a contractile to a synthetic type [J]. Atherosclerosis, 2014,237(2):464-70. |
| [10] | Kudryavtseva O, Herum K M, Dam V S. et al. Downregulation of L-type Ca2+ channel in rat mesenteric arteries leads to loss of smoothmuscle contractile phenotype and inward hypertrophic remodeling [J]. Am J Physiol Heart Circulat Physiol, 2014, 306(9):1287-1301. |
| [11] | Magalhaes M A, Minha S, Chen F, et al. Clinical presentation and outcomes of coronary in-stent restenosis across 3-stent generations[J]. Circ Cardiovasc Interv, 2014,7(5):768-76. |
| [12] | Park B, Yim J, Lee H, et al.Ramalin inhibits VCAM-1 expression and adhesion of monocyte to vascular smooth muscle cellsthrough MAPK and PADI4-dependent NF-κB and AP-1 pathways[J]. Biosci Biotechnol Biochem, 2014,15(12):1-14. |
| [13] | Wang Z, Niu Q, Peng X, et al. Mitofusin 2 ameliorates aortic remodeling by suppressing ras/raf/ERK pathway and regulating mitochondrial function in vascular smooth muscle cells [J]. Int J Cardiol, 2015,178(1):165-7. |
| [14] | 钟良瑞,魏克民. 三叶青黄酮对肺癌A549 细胞生长抑制与MAPKs 通路关系的研究[J].中国药理学通报,2014,30(1):101-4. Zhong L R, Wei K M. Radix tetrastigma hemsleyani flavone suppresses human lung carcinoma A549 cell by regulating MAPKs pathway[J].Chin Pharmacol Bull, 2014,30(1):101-4. |
| [15] | Samarakoon R, Higgins C E, Higgins S P, et al.Differential requirement for MEK/ERK and SMAD signaling in PAI-1 and CTGF expression in response to microtubule disruption [J]. Cell Signal, 2009,21(6):986-95. |
| [16] | Yuan W, Yang D, Sun X, et al. Effects of hydroxysafflor yellow A on proliferation and collagen synthesis of rat vascular adventitial fibroblasts induced by angiotensin Ⅱ [J]. Int J Clin Exp Pathol, 2014,7(9):5772-81. |
| [17] | Zhang X P, Zhang L, Yang P, et al. Protective effects of hydroxysafflor yellow A and octreotide on multiple organ injury in severe acute pancreatitis [J]. Dig Dis Sci, 2008,53(2):581-91. |