


2. 辽宁医学院附属第一医院, 辽宁 锦州 121000;
3. 中国医科大学, 辽宁 沈阳 110001
2. The First Affiliated Hospital of Liaoning Medical University, Jinzhou Liaoning 121000, China;
3. The China Medical University, Shenyang 110001, China
吗啡等阿片类药物反复应用可造成耐受、依赖和成瘾,中断给药出现戒断综合征、强迫觅药行为及戒断后焦虑等精神神经系统症状。在阿片类药物的成瘾过程中,中脑腹侧被盖区(ventral tegmental area,VTA)起到重要的作用[1]。VTA靠近黑质与红核,含有大量DA能神经元。针对吗啡强化和依赖效应主要通过VTA的DA系统介导,VTA神经元的异常兴奋是吗啡成瘾的关键环节,但目前机制尚不清楚[2]。神经内分泌活性肽UCN是近年来发现的促皮质激素释放因子(coticortropin-releasing factor,CRF) 肽类家族的一个新成员[3]。UCN 具有与CRF 相似的生物活性,通过下丘脑-腺垂体-肾上腺轴,促进腺垂体分泌肾上腺皮质激素,调节应激、应急反应、抗焦虑、镇静等作用。UCN作为一种新型的小分子神经活性肽,通过自分泌和(或)旁分泌途径,其作用是广泛的,相应作用机制也是多方面的[4]。有少量报道表明,UCN参与酒精成瘾及戒断后焦虑和觅药等行为的应激性反应[5]。但UCN对吗啡成瘾VTA神经元电活动及DA系统的影响未见报道,且机制也不明确。因此,本实验采用七管玻璃微电极细胞外记录方法,微电泳UCN2及CRF2受体抑制剂AST对VTA 神经元放电情况的影响,同时也观察了UCN2对VTA中DA能神经递质传递的影响,以探讨VTA内存在的复杂的神经纤维联系及各种神经递质之间的相互作用,从而为VTA神经元放电异常及发作性疾病的诊治提供电生理学方面的依据。
1 材料与方法 1.1 实验动物♂ Sprague-Dawley(SD)大鼠,50只,体质量180~220 g,由辽宁医学院实验动物中心提供,动物合格证号:SCXK(辽) 2003-0007。随机分为吗啡成瘾模型组40只和对照组10只。模型组采用剂量序贯递增法腹腔注射盐酸吗啡(Tab1)建立大鼠吗啡成瘾模型,对照组在相同条件下给予生理盐水,12 d后采用纳洛酮(5 mg·kg-1)诱导吗啡成瘾戒断模型[6]。
| Time | d1 | d2 | d3 | d4 | d5 | d6 | d7 | d8 | d9 | d10 | d11 | d12 |
| Morning/mg·kg-1 | 0 | 5 | 10 | 15 | 20 | 25 | 35 | 45 | 55 | 65 | 75 | 85 |
| Afternoon/mg·kg-1 | 0 | 5 | 10 | 15 | 20 | 25 | 35 | 45 | 55 | 65 | 75 | 85 |
| Evening/mg·kg-1 | 5 | 10 | 15 | 20 | 25 | 30 | 40 | 50 | 65 | 70 | 80 | 90 |
细胞外记录及微电泳采用51-217 型微管拉制仪(美国STOELTING公司)所拉制的7管玻璃微电极。中心管尖端直径在4~8 μm,电阻为5~12 MΩ,管内灌注含1%滂胺天蓝的NaCl溶液(3.0 mol·L-1)作为神经元放电活动的引导电极;外周管电阻为20-100MΩ,外周管内灌注下列药物,包括:UCN2(10-6 mol·L-1);astressin2B-AST-2B(CRF-2受体阻断剂,10-6 mol·L-1);DA及其非选择性阻断剂α-flupenthixol(FLU,10-5 mol·L-1),蛋白激酶A(protein kinase A,PKA)及抑制剂(H-89,10-5 mol·L-1)。
1.3 实验方法上述实验动物用20%乌拉坦(1 g·kg-1)麻醉后,于脑立体定位仪上行常规开颅。根据Paxions Watson大鼠脑图谱,确定VTA核团位置,坐标为前囟后5.20~6.80 mm,中线旁开0.20~0.80 mm,脑表下7.0~8.0 mm。应用微电极推进器将七管微电极缓慢插入VTA,神经元单位放电经DAM80 微电极放大器采集及滤波后显示于示波器上,再经Spike2 生物信号采集系统(英国CED公司)输入计算机并处理,生成序列密度直方图。观察吗啡成瘾大鼠VTA神经元放电情况,之后观察UCN2及AST-2B对VTA神经元放电影响。另外,微电泳DA及其阻断剂期间,给予UCN2对VTA神经元多巴胺能神经传递的影响;微电泳PKA及抑制剂H-89,进一步观察UCN2对吗啡成瘾大鼠VTA神经元影响是否通过PKA发挥作用。为排除可能发生的电流影响,只要注入生理盐水引起的任何放电改变,则该资料不列入统计之内。
1.4 数据处理及统计记录微电泳药物前、后VTA神经元放电频率改变,微电泳药物后放电频率变化/%=(微电泳药物期间放电频率-微电泳前20s放电频率)/微电泳前20s 放电频率×100%,电泳药物后放电变化超过±30%为有效临界值。
采用SPSS 13.0 统计软件进行统计学处理。所有数据以用 ± s表示。组间比较采用单因素方差分析及LSD-t检验进行统计学处理。
± s表示。组间比较采用单因素方差分析及LSD-t检验进行统计学处理。
实验中,共计观察了52个吗啡成瘾大鼠VTA神经元的自发放电活动,其自发放电频率快而且不规则,VTA神经元放电频率在10~25Hz之间,多为单个爆发式放电。
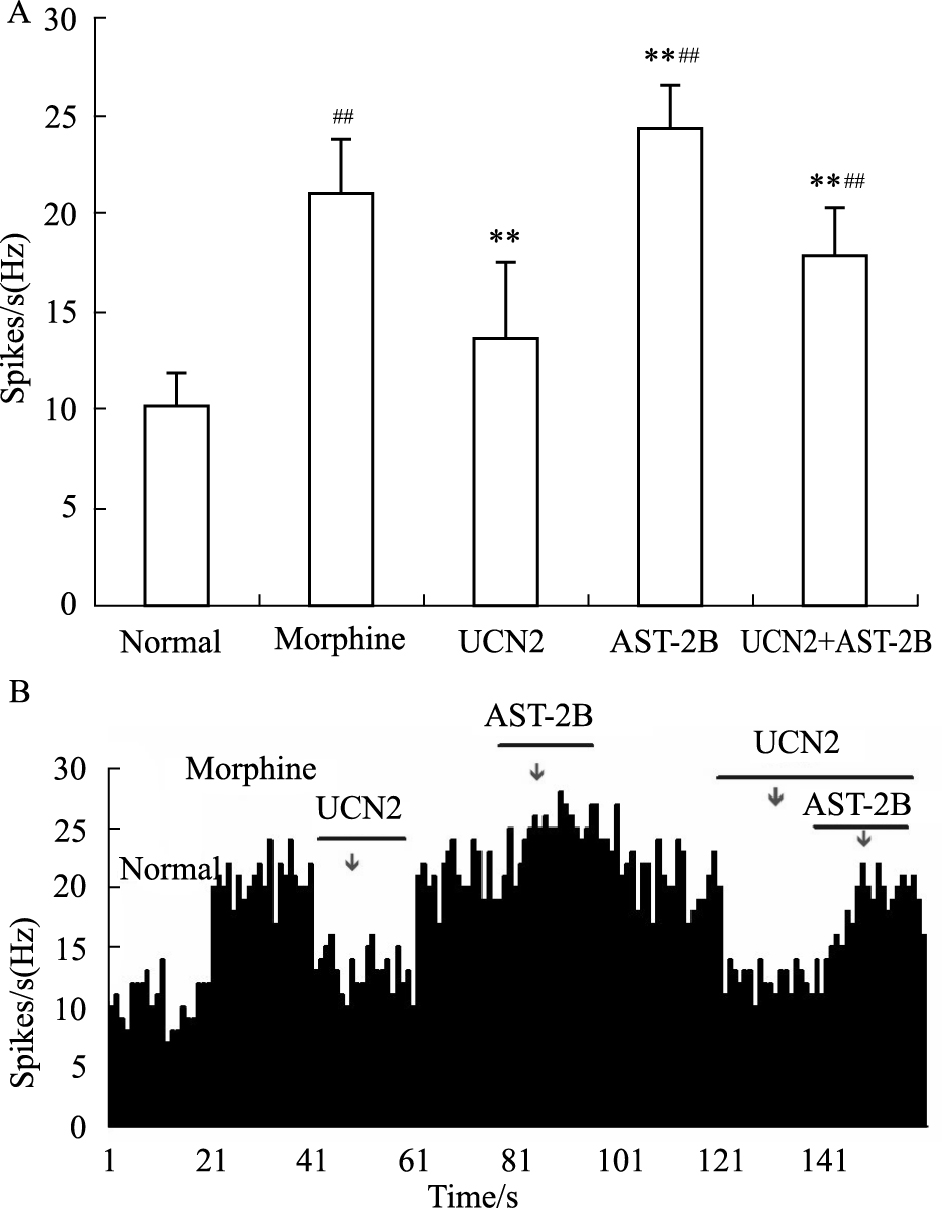
2.1 微电泳UCN2及AST对VTA神经元自发放电的影响本结果中,共观察了38个吗啡成瘾大鼠的VTA神经元。微电泳UCN2(10-6 mol·L-1,20nA,20s)使82%(31/38)神经元自发放电频率减慢,对7个神经元无作用。38个受试VTA神经元的平均放电频率由微电泳前的(20.89±2.86)Hz减少到(13.66±3.93)Hz,给药前后放电频率降低具有显著性(P<0.01)。实验中发现,UCN2的抑制作用较明显,几乎没有潜伏期,但存在后作用。此外,在22个VTA神经元中单独微电泳AST(10-6 mol·L-1,20nA,20s),可使73%(16/22)VTA神经元自发放电频率升高。受试VTA神经元放电频率由微电泳前的(21.64±2.82)Hz升高到(24.25±2.30)Hz(P<0.01),在微电泳UCN2造成抑制效应的20个神经元中,微电泳UCN2(20nA,40s)期间给予AST(20nA,20s)可拮抗UCN2 的抑制效应,使80%(16/20)对UCN2产生抑制效应的神经元放电频率明显加快,放电频率由微电泳AST前的(13.35±1.89)Hz增加到(17.80±2.53)Hz,微电泳前后平均放电频率改变具有显著性(P<0.01)。AST的起效迅速,无潜伏期,可引起爆发式放电,并可见双向动作电位增加(Fig1A,1B)。
|
| Fig 1 Effects of UCN2 on VTA neuron A:Effects of UCN2 (10-6 mol·L-1, 20nA, 20s) and AST-2B on VTA neuron. **P<0.01 vs normal group; ##P<0.01 vs UCN2 group,B:Effects of UCN2 on VTA neuron spontaneous firing rates. AST-2B was administrered during the period of UCN2. |
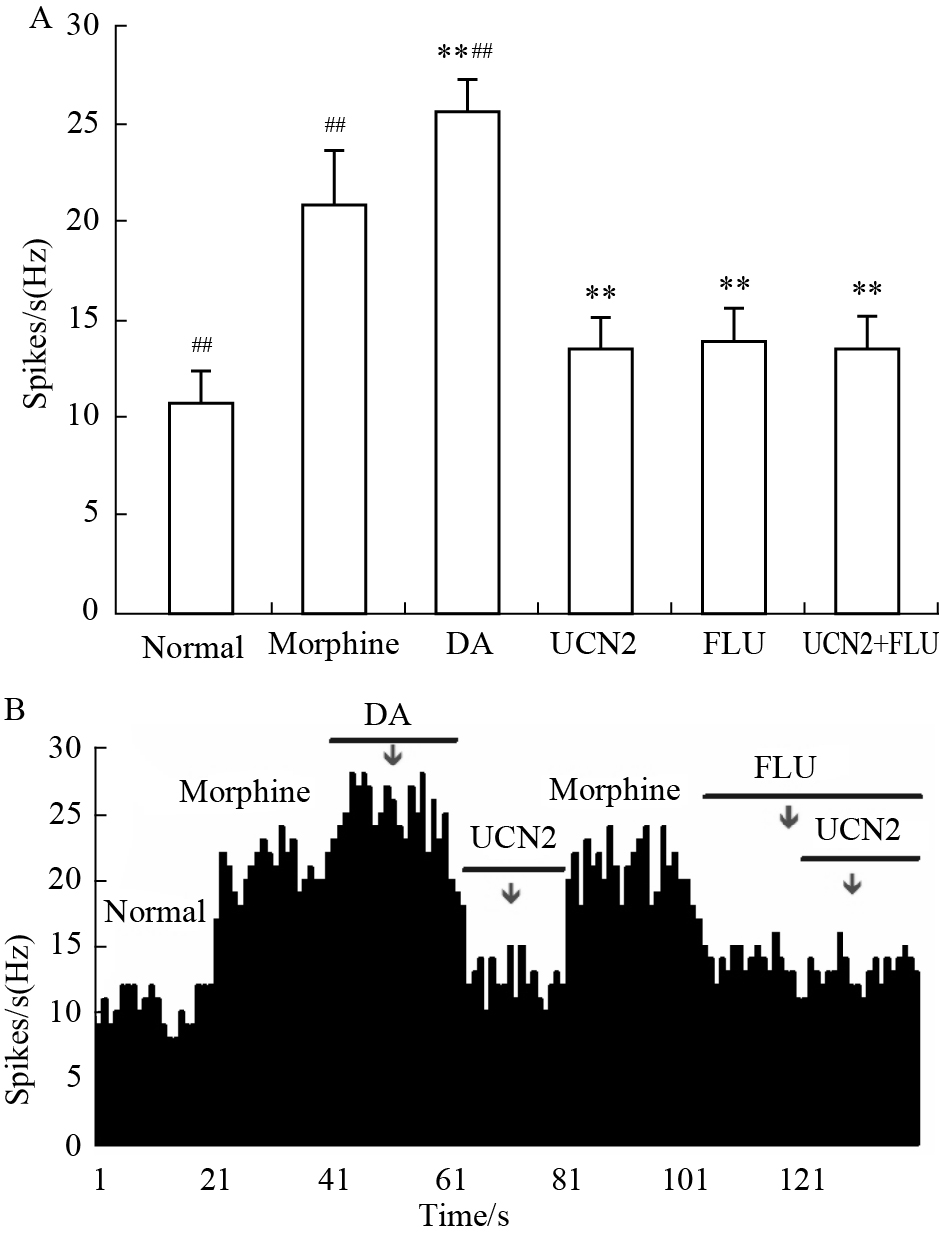
微电泳DA可使吗啡成瘾大鼠VTA神经元兴奋性进一步升高,而给予DA非选择性阻断剂可拮抗其兴奋效应。选取对DA产生兴奋效应的24个VTA神经元进行研究。在微电泳DA(20nA,40s)期间,在第20s微电泳UCN2(20nA,20s),使受试神经元中的79%(19/24)的放电频率明显降低。受试VTA中DA神经元的放电频率由微电泳UCN2前(25.57±1.64)Hz减少到(13.42±1.60)Hz,给药前后放电频率差异有显著性(P<0.01)。微电泳DA的阻断剂FLU可使DA神经元放电频率明显降低,在微电泳期间给予UCN2(20nA,20s),对受抑制的VTA神经元中放电频率无明显影响,平均放电频率由微电泳UCN2前的(13.88±1.80)Hz变化到(13.46±1.78)Hz,给UCN2前后差异无显著性(P>0.05)(Fig2A,2B)。
|
| Fig 2 Effects of UCN2 on DA neuron A:Effects of UCN2 (10-6 mol·L-1, 20nA, 20s) on VTA′s DA neuron; **P<0.01 vs normal group; ##P<0.01 vs UCN2 group. B:Effects of UCN2 on VTA′s dopaminergic neuron spontaneous firing rates. FLU could inhibit VTA neuron spontaneous firing rates, and UCN2 was administrered during the microiontophoresis of FLU. |
对DA产生兴奋效应的19个VTA神经元进行研究。在微电泳DA(20nA,80s)期间,在第20s微电泳H89 (20 nA,40s),使受试神经元中的79%(15/19)的放电频率由微电泳H89前(25.50±1.58)Hz减少到(16.17±1.47)Hz,给药前后放电频率差异有显著性(P<0.05)。在微电泳H89的第20 s,再微电泳UCN2(20nA,20 s),受试的VTA神经元中的52%(10/19)放电频率略降低,由(15.80±2.41)Hz改变为(15.45±1.28)Hz但给药前后差异无显著性(P>0.05)(Fig3A,3B)。

|
| Fig 3 Effects of UCN2 on PKA pathway A: Effects of UCN2 (10-6 mol·L-1, 20nA, 20s) and H89 on VTA′s DA neuron.**P<0.01 vs normal group; ##P<0.01 vs h89 group;B: Effects of UCN2 on VTA′s dopaminergic neuron spontaneous firing rates via PKA pathway. |
实验中发现,吗啡成瘾大鼠VTA 神经元放电频率明显增加,呈爆发式放电,而神经肽UCN2 能使其神经元放电频率明显减慢,提示UCN2对吗啡成瘾大鼠VTA神经元的放电起抑制作用。研究表明[7],阿片类药物能直接或间接刺激VTA,产生神经元异常高频放电,VTA是愉悦系统或奖赏系统的重要部分,当产生奖赏行为时,能够刺激VTA神经元兴奋性放电,产生药物依赖成瘾,本实验结果进一步提示,UCN2可以通过抑制VTA神经元异常高频放电,对阿片类药物成瘾起到抑制及治疗作用。
实验中单独微电泳选择性CRF2R阻断剂AST-2B可增加受试VTA神经元的放电频率。微电泳UCN2 期间,其抑制作用可被AST-2B所拮抗,结果提示UCN2 对吗啡成瘾大鼠VTA 神经元的抑制效应可能是通过与CRF2R结合后而产生。UCN有3种形式:UCN1、UCN2、UCN3。CRF 受体主要有CRF-1R、CRF-2R两种 ,新近发现的非哺乳动物CRFR3受体,均为7 次跨膜的G 蛋白偶联受体,CRFR1 受体能高亲和力地与CRF、UCN1 肽结合。而UCN2、UCN3只对CRFR2 受体有特异结合特征。UCN与CRF-R2 结合后,具有抗氧化、抗衰老、抗焦虑、忧郁等多种生理作用及药理功能[8, 9]。有研究表明,Urocortin在脑损伤过程中具有神经保护作用,特别是在药物成瘾、神经退行性疾病中发挥重要调节作用,但目前机制尚不十分明确[10]。因此,本实验结果进一步提示,UCN2在对吗啡类药物成瘾中主要是通过与CRF-R2 结合发挥抑制作用。
实验结果表明,DA能投射纤维对VTA 神经元有兴奋作用,UCN2 可以拮抗DA的兴奋效应,且给予AST 对DA兴奋效应具有一定协同作用,提示UCN2 与VTA 神经元中CRF2 受体结合后,拮抗DA在吗啡成瘾中的兴奋毒性。有报道表明[11],VTA 中的DA神经元异常兴奋,诱发VTA神经元过度爆发式放电,产生药物依赖性。UCN2是CRF肽类家族的成员,有研究表明,UCN2可增加实验鼠的迷宫探索能力,增强学习和记忆能力,具有抗焦虑作用及很强的镇静效应。UCN2与酒精成瘾有密切关系,微量核团注射UCN2能减少小鼠自我供给酒精的量,在酒精戒断过程中发挥作用。吗啡是通过阿片受体作用于VTA上的DA能神经元,从而引起DA释放增加,减弱或消除GABA能神经元对DA神经元的抑制作用,进一步促进DA释放。因此,本实验结果进一步提示,UCN2能够抑制VAT中DA神经元活动的物质将有望成为减轻吗啡成瘾的有效药物。
UCN2与CRF-2R 结合后是如何引起效应的呢?其保护VTA神经元作用的机制,很可能与阻断了神经递质DA的兴奋毒性作用有关。有限的研究资料也表明:UCN与酒精成瘾有密切关系,微量核团注射UCN能减少小鼠自我供给酒精的量[10];可卡因戒断引起的长时程增强可被CRFR1和CRFR2受体拮抗剂阻断[11];在酒精戒断过程中,大鼠杏仁核细胞外CRF明显升高。上述结果均提示:UCN可能通过CRF-R2受体参与酒精成瘾及戒断后焦虑和觅药等行为的应激性反应[12]。另外,VTA的DA能神经元成簇放电导致其突触末梢DA释放量瞬时大量增加,已被公认是编码奖赏效应的功能信号,但诱发DA能神经元产生簇放电的神经机制尚不完全清楚[7]。在本实验中证实,微电泳PKA阻断剂H89后,再给予UCN2,可使VTA中DA神经元的放电频率略降低,但给药前后差异无显著性,该结果提示,UCN2与CRF-2R 结合后,进而通过激活蛋白激酶A引起效应。
本实验结果表明,UCN2 可以通过作用于CRF-2R能够抑制VTA神经元放电活动,降低神经元的过度兴奋性,并且降低DA能兴奋毒性,提示在吗啡成瘾病理情况下,UCN2可以起到神经元保护作用,研究结果为药物成瘾机制提供新的实验依据,对临床防治提供新的思路。
| [1] | Charalampopoulos I, Androulidaki A, Minas V, et al. Neuropeptide urocortin and its receptors are expressed in rat Kupffer cells [J]. Neuroendocrinology, 2006,84(1):49-57. |
| [2] | 胡蓉蓉, 宋 睿, 苏瑞斌, 等.多巴胺 D3 受体与阿片成瘾研究进展[J]. 国际药学研究杂志,2013, 10(40):5525-6. Hu R R, Song R, Su R B, et al. Dopamine D3 receptor and opioid addiction:researeh advances[J]. J Int Pharm Res, 2013, 10(40):5525-6. |
| [3] | Walczewska J,Dzieza-Grudnik A,Siga O,Grodzicki T. The role of urocortins in the cardiovascular system [J]. J Physiol Pharmacol, 2014, 65(6):753-66. |
| [4] | Voltolini C, Battersby S, Novembri R, et al. Urocortin 2 role in placental and myometrial inflammatory mechanisms at parturition [J]. Endocrinology, 2015,156(2):670-9. |
| [5] | Ryabinin A E, Yoneyama N, Tanchuck M A, et al. Urocortin 1 microinjection into the mouse lateral septum regulates the acquisition and expression of alchhol consumption [J]. Neuroscience, 2008, 151(3):780-90. |
| [6] | 郑久明, 张 迪, 刘新宇, 刘春娜. 神经肽 urocortin Ⅱ 对吗啡成瘾大鼠中脑腹侧被盖区神经元自发放电的影响[J]. 中国药理学通报, 2014,30(5):735-6. Zheng J M, Zhang D, Liu X Y, Liu C N. Effects of neuropeptide urocortinⅡ on spontaneous discharge of ventral tegmental area in morphineaddicted rats[J]. Chin Pharmacol Bull, 2014,30(5):735-6. |
| [7] | 汤贤春, 杨培润, 吴明松, 等. 吗啡精神依赖大鼠奖赏环路多巴胺递质含量和 D2 受体表达的变化[J].中国药物依赖性杂志, 2014, 23(1):19-23. Tang X C, Yang P R, Wu M S, et al. Changes of dopamine content and D2 receptor expression in reward circuit in morphine dependent rats[J]. Chin J Drug Depend, 2014, 23(1):19-23. |
| [8] | Lawrence K M, Jackson T R, Jamieson D, et al. Urocortin-from Parkinson's disease to the skeleton [J]. Int J Biochem Cell Biol, 2014,23(60C):130-8. |
| [9] | Stengel A, TachéY. CRF and urocortin peptides as modulators of energy balance and feeding behavior during stress [J]. Front Neurosci,2014,18(8):52. |
| [10] | Pan W, kastin A J. Urocortin and the brain [J]. Pregr Neurobiol, 2008,84(2):148-56. |
| [11] | Guan X, Zhang R, Xu Y, Li S. Cocaine withdrawal enhances long-term potentiation in rat hippocampus via changing the activity of corticotrophin-releasing factor receptor subtype 2 [J]. Nuroscience, 2009,161(3):665-70. |
| [12] | Valdez G R, Sabino V, Koob G F. Increased anxiety-like behavior and ethanol self-administration in dependent rats:reversal via corticotrophin-releasing factor-2 receptor activation [J]. Alcohol Clin Exp Res, 2004, 28(6):865-72. |

