


2. 江苏省药用植物生物技术重点实验室, 江苏 徐州 221116
陆军(1974-),男,博士,教授,硕士生导师,研究方向:神经退行性疾病作用机制,E-mail:lu-jun75@163.com
郑元林(1961-),男,博士,教授,博士生导师,研究方向:神经退行性疾病作用机制,E-mail:ylzheng@jsnu.edu.cn
2. Key Laboratory for Biotechnology on Medicinal Plants of Jiangsu Province, Xuzhou Jiangsu 221116, China
海马属于大脑的边缘系统,其在学习记忆过程中发挥关键性作用[1]。研究表明[2],海马是最容易受损的脑区之一。而在认知失常患者中海马损伤严重,其可能的机制与神经元丢失有关[2]。 利用遗传[3]或者药物干预方法[4]可增强海马神经的存活环路,在一定程度上减轻神经元的丢失,改善模型组动物的学习记忆能力。
帕金森病(Parkinson’s disease,PD) 是一种常发于中老年人的中枢神经系统退行性疾病之一[5, 7]。其典型的病理特征是中脑黑质致密部多巴胺能神经元变性、坏死,皮质基底节环路失控[6, 7]。临床表现出严重的运动障碍[7]。此外,研究发现PD患者还患有认知功能障碍[8]。
神经生长因子(nerve growth factor,NGF)是一种多亚基蛋白组成的靶组织源性细胞因子,它在神经保护、突触再生、神经损伤后功能重建等方面发挥了重要作用[9]。Lim等[4] 研究证明,生姜提取物可使东莨菪碱诱导的认知障碍小鼠的海马区NGF表达增加,促使突触再生,修复受损的海马区。临床和实验证据表明[10],PD患者及PD模型的血清中NGF水平明显降低。由此,我们推测NGF可能在PD认知障碍的病理学发生、发展过程中发挥重要作用。本实验初步探索PD模型小鼠海马区NGF mRNA的表达变化。
1 材料与方法 1.1 实验动物及处理15周龄C57BL/6 ♂小鼠36只(北京维通利华实验动物技术有限公司),体质量25-35 g。将其均分为实验组和对照组,在自然昼夜节律光照条件下,置于清洁代谢笼,每笼6只,自由进食饮水,控制室温于(20±2)℃。小鼠适应环境48 h后,剪趾标记,称量体重。按MPTP(Sigma) 20 mg·kg-1的给药量对模型组腹腔注射MPTP,对照组注射等量生理盐水。每隔2 h注射一次,共注射4次,7 d后造模完成。
1.2 实验方法 1.2.1 行为学检验 1.2.1.1 足迹分析法(foot print analysis)[11, 12, 13]参考Simon d和Oliver等研究,自制大小为50 cm×9 cm×6 cm的足印测试装置。测试时,在测试盒底部垫一张白纸,小鼠两后足蘸取适量无毒碳素墨水后,放入盒中从一端走向另一端,形成一连串脚印,如Fig1-A所示。3个连续的脚印形成1个三角形,记录以下参数:a是从右侧脚印中点做的一条与盒子长轴垂直的直线,相邻两右侧脚印之间的连线与a之间所形成的锐角用α表示,α的平均变异值用Δα表示;b是相邻两左脚印或右脚印之间的距离,用δ表示b的平均变异值;c是左右两脚印之间的距离;e是步宽,即一侧脚印到对侧相邻两脚印连线的垂直距离; β是步态变异率,即β=0.5-c/b。步长=总共步行的距离/右(左)侧脚印数目,步长、步宽、Δα、δ、β 5个指标反映试验小鼠的共济运动,若有共济失调,则表现为步态不稳,Δα、δ、β增大。

|
| Fig 1 Foot print analysis for detection of mouse ataxia A is the foot print test analysis; B,C and D are ataxic analysis results of delta alpha, sigma, beta respectively.**P < 0.01 vs saline |
实验装置分为大小均为13.6 cm×15.3 cm×25.0 cm的明室和暗室。两室之间有一直径约为5 cm的拱形洞。两室底部均以铜栅铺设,其中暗室底部中间位置铜栅通交流电,实验在微暗的环境进行。实验前1 d将小鼠放入明室,待其进入暗室后,关闭通道使其适应新环境3 min。次日进行实验,将小鼠背对洞口放入明室测定潜伏期。小鼠有嗜暗的习性,很快会穿过拱洞进入暗室。小鼠从放入明室到进入暗室的时间称为潜伏期。记录潜伏期,然后关闭拱洞通以0.3 mA,50Hz的电流电击5 s,停止分析取出小鼠放回笼内。24 h后重复实验(不予电击),记录潜伏期,时间上限设为300 s。
1.2.2 PD模型生化及形态学检测[14]取各组小鼠中脑黑质区于组织匀浆液T-PER(Thermo)中使用球磨仪(Retsch)匀浆,4℃,12 000 r·min-1离心30 min,取上清,采用BCA法定量。加热变性蛋白质至同等浓度。SDS-PAGE电泳,每孔加等量蛋白样品,电泳后湿转至PVDF膜上。5%脱脂奶粉TBST缓冲液室温震荡封闭1h后洗膜,加入TBST稀释的多克隆抗体一抗(β-actin 抗体1 ∶ 1 000 稀释,Santa Cruz;TH抗体1 ∶ 1 000 稀释,Millipore),在4℃下低速摇床过夜,洗膜,加入TBST稀释的辣根过氧化物酶标记的山羊抗兔抗体(1 ∶ 2 000),室温孵育1 h,洗膜后滴加ECL发光剂于化学发光凝胶成像系统(Protein Simple) 显影。并对各组TH蛋白与相应内参条带进行灰度扫描,测其相对表达量。
灌流固定,取全脑制作12 μm冰冻切片,储存于-70℃。切片取出37℃烘干20 min,滴加5%BSA PBST缓冲液室温封闭1 h,洗片,滴加PBST稀释的TH抗体(1 ∶ 500),4℃过夜,洗片,滴加PBST稀释的二抗(1 ∶ 500),洗片,加DAPI孵育5 min,盖片镜检。
1.2.3 RT-PCR检测[3]用TRIzol [15](Sigma)法分别提取实验组和对照组小鼠海马体总RNA,并用ND-2000(Nanodrop)分别测定核酸浓度。取同等量的总RNA,根据逆转录试剂盒说明书以Oligo(dT)18(Promega) 为引物分别合成cDNA第一条链。以β-actin为内参,各引物序列通过Vector NTI Advance 11.5软件设计,经GenBank BLAST 同源性检索后,由上海生工生物技术工程有限公司合成。β-actin基因上游引物:5′-TGTGCCCATCTACGAG-3′;下游引物:5′-AGGATTCCATACCCAAG-3′,合成329bp产物。NGF基因上游引物:5′-AGACGAATTCGCCCACTGGACTAAACT-3;下游引物:5′-AGACAAGCTTCAGCCTGCTTCTCATCT-3′,合成553bp产物。用捷达凝胶成像系统对各组NGF基因扩增电泳条带与相应内参条带进行灰度扫描,测其相对含量。
1.2.4 原位杂交检测 [10, 16]利用RT-PCR扩增的NGF基因片段、PGEM-3Z质粒载体及大肠杆菌DH5α克隆构建NGF/PGEM-3Z重组质粒,以SP6和T7聚合酶转录合成酶(Roche)体外转录合成地高辛标记的RNA探针,参照罗氏原位杂交及信号检出方法处理各组含海马区的组织切片。从-70℃取出切片,于37℃烘干20 min,蛋白酶K缓冲液孵育30 min,含甘氨酸的PBS缓冲液孵育10 min,洗片,4%多聚甲醛4℃后固定10 min,洗片,三乙酸酐缓冲液孵育10 min,预杂交缓冲液37℃孵育2 h。滴加含DIG标记的RNA探针杂交缓冲液于切片上,55℃孵育16 h。4×SSC于42℃洗片15 min,2×SSC、1×SSC和0.1×SSC分别于37℃各洗15 min,2%绵羊血清封闭液封闭1 h,弃液,加1 ∶ 1 000稀释的碱性磷酸酶偶联抗DIG抗体孵育2 h,PBS洗片,NBT/BCIP显色液显色,PBS洗片,水溶性树胶封片,镜检拍照。
1.2.5 数据统计分析统计学处理使用SPSS 17.0软件,采用单因素方差分析结合t检验。
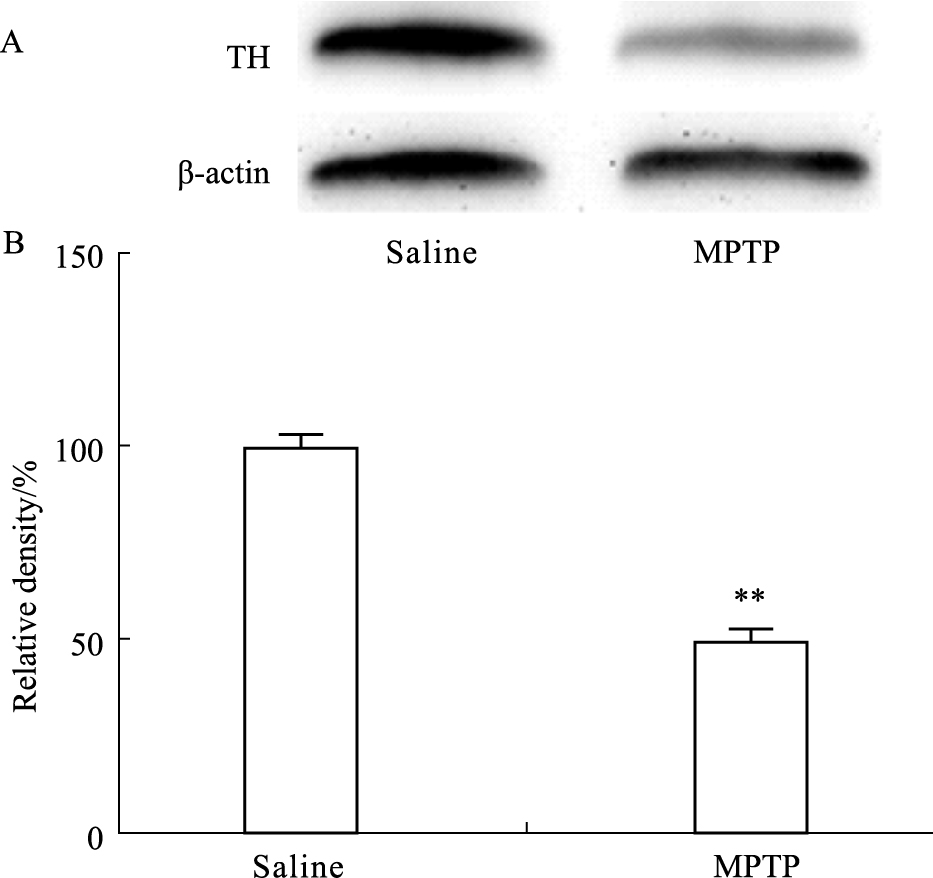
2 结果 2.1 PD模型建立MPTP是常用的建立PD模型的药物。腹腔注射该药物后,会形成类帕金森症状及多巴胺神经元减少。酪氨酸羟化酶(Tyrosine hydroxylase,TH)是DA前体生物合成的限速酶。研究表明,PD动物模型及PD患者中脑TH 表达下调。我们的免疫印迹结果(Fig3-A)发现,与注射生理盐水的对照组相比,注射MPTP的模型组TH条带灰度值明显降低,P < 0.01(Fig3-B)。TH免疫荧光结果(Fig4-A)显示,与注射生理盐水的对照组相比,模型组阳性细胞数量减少,胞质亮度变暗,P < 0.01(Fig4-B)。这些结果表明我们成功建立了PD模型。
|
| Fig 3 Detection on expression of TH protein A is the result of TH Western blot; B is the relative content of TH.**P < 0.01 vs saline |

|
| Fig 4 Detection of TH-positive cells in the substantia nigra A is the immunofluorescence test of TH in the substantia nigra; B is the relative content of TH positive cells in the substantia nigra. **P < 0.01 vs saline |
目前,行为学评估的内容主要包括肌力及协调运动能力、学习与记忆能力[11]。足迹分析法是分析肌力及运动协调能力的一种,常用来评估动物的运动功能。实验发现,与注射生理盐水的对照组相比,注射MPTP的模型组小鼠的Δα、δ、β均明显增大,P< 0.05(Fig1-B、C、D),表明PD模型小鼠的共济运动失调,出现步态不稳症状,即其运动能力出现障碍。
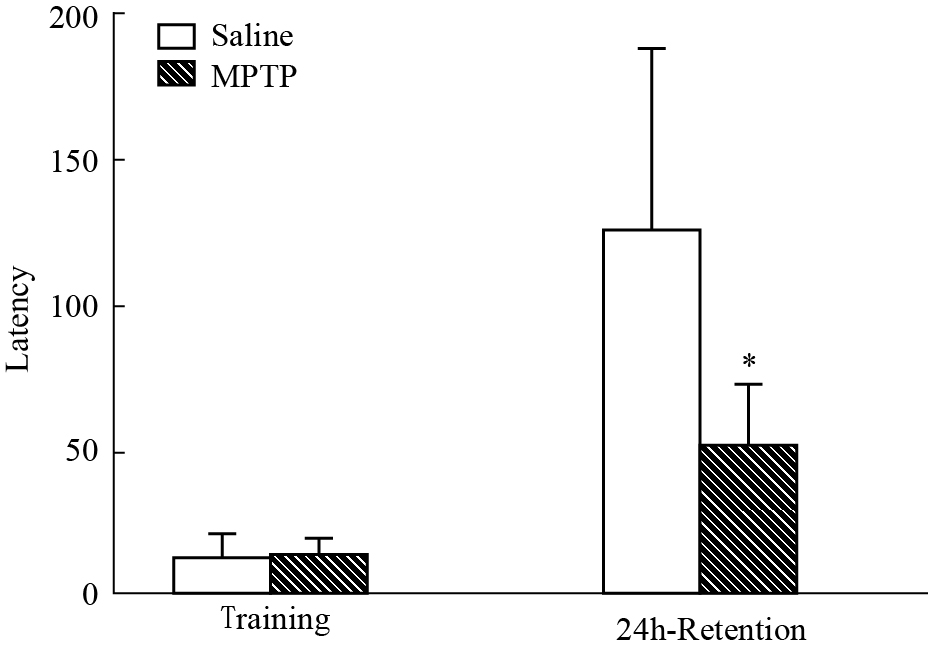
避暗法实验是评估动物获得性记忆的有效方式之一。在暗室电击处理24 h后记录的记忆保持潜伏期越长,学习记忆能力越好。在该检测实验中发现,训练前,两组不同处理的小鼠进入暗室的自然潜 伏期没有差异。在暗室电击处理24 h后记录的记忆保持潜伏期结果发现,与注射生理盐水的对照组比较,注射MPTP的PD模型组小鼠的记忆保持潜伏期明显减少,P < 0.05(Fig2),这表明该组小鼠的学习记忆能力减弱,其神经系统在一定程度上可能受损。
|
| Fig 2 Result of step-through test *P<0.05 vs saline |
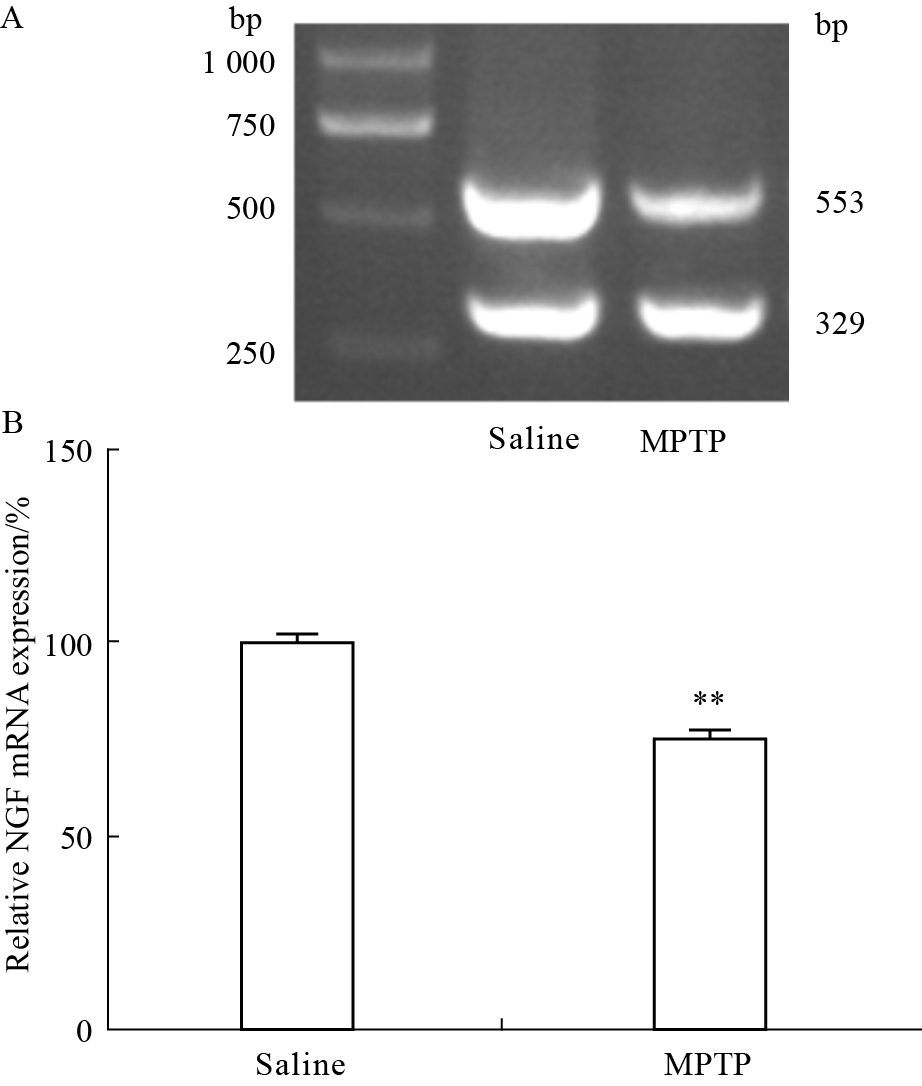
RT-PCR即反转录-聚合酶链反应,它是以反转录酶合成的cDNA为模板,扩增合成目的片段,用于检测基因的表达水平。根据引物设计,扩增长度为553 bp的NGF目的片段和长度为329 bp的β-actin内参片段,其琼脂糖凝胶电泳结果如Fig5-A所示。与注射生理盐水的对照组相比,注射MPTP的模型组海马区NGF扩增片段电泳条带灰度值明显降低,P < 0.01(Fig5-B)。这表明模型组海马区NGF mRNA含量明显降低。
|
| Fig 5 Expression level of NGF mRNA A is the amplification result of NGF and β-actin gene; B is the relative content of NGF gene.**P < 0.01 vs saline |
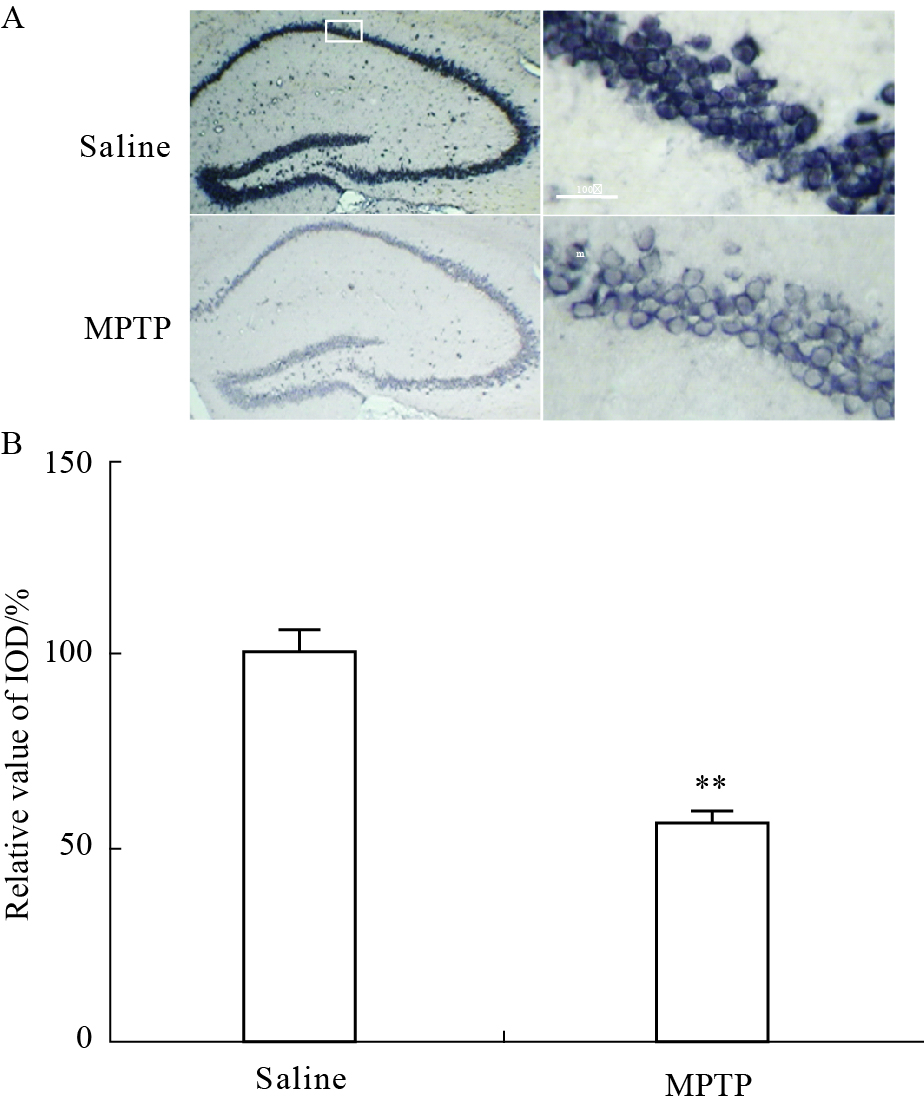
原位杂交是将特定标记的核酸探针与细胞或者组织切片中核酸进行杂交,从而对特定核酸进行定量定位的过程。我们的实验结果发现,与注射生理盐水的对照组相比,注射MPTP的模型组阳性细胞色浅,光密度分析,P < 0.01(Fig6)。这表明与对照组相比,模型组海马区NGF mRNA水平明显降低。
|
| Fig 6 Detection on the expression of NGF mRNA in hippocampus A is the results of in situ hybridization of NGF mRNA in hippocampus; B is the analysis of the integral optical density value(IOD) of NGF mRNA in hippocampus.**P < 0.01 vs saline |
帕金森病是常见的神经退行性疾病之一[2, 5, 10, 15]。临床表现出严重的运动障碍[7]。进一步研究发现[8],部分患者患有认知障碍。腹腔注射MPTP是常用的建立帕金森动物模型之一[14]。造模后,行为学评价发现,模型组动物出现运动功能和认知功能障碍。
NGF是一种多亚基蛋白组成的靶组织源性细胞因子,不仅对正常神经细胞有营养作用,而且对损伤神经的修复机能有调节作用[9]。大量研究证据表明,NGF在促进脑损伤修复及增强认知功能中发 挥重要作用。在PD模型的研究中,Chaturvedi等[18]发现,联合移植NGF和胎儿腹侧中脑细胞于模型鼠纹状体,多巴胺神经元和神经纤维增加明显,且其运动能力恢复到正常水平。此外,有相关证据显示,NGF含量高的动物学习记忆能力强[19],且当抑制NGF表达时,其学习记忆能力减弱[20]。在鹅膏蕈氨酸致痴呆模型研究中,耿劲松等[17]发现,与模型组相比,脑益康治疗组海马区NGF mRNA表达明显上调,且其认知能力恢复到正常水平。而在我们建立的PD模型行为学评价中,我们检测到其出现认知障碍。为此,我们通过RT-PCR检测NGF mRNA的表达,发现PD模型组NGF mRNA 表达下调。进一步利用原位杂交技术发现,模型组海马区NGF基因表达也出现明显下调。这在一定方面可能支持认知功能障碍与NGF表达下调有关。
进一步,我们将阐明NGF在PD模型动物认知功能障碍中的作用机制。
| [1] | Lu J, Wu D M, Zheng Y L, et al. Ursolic acid improves high fat diet-induced cognitive impairments by blocking endoplasmic reticulum stress and IκB kinase β/nuclear factor-κB-mediated inflammatory pathways in mice[J]. Brain Behav Immun, 2011, 25(8):1658-67. |
| [2] | 刘加强, 童 卫. 海马神经发生障碍与阿尔兹海默病发病机制[J].神经解剖学杂志, 2014, 30(2):244-8.Liu J Q, Tong W.The disorders of hippo-campal neurogenesis and pathogenesis of Alzheimer's disease[J]. Chin J Neuroanat, 2014, 30(2):244-8. |
| [3] | Birch A M, Kelly Á M. Chronic intracerebroven-tricular infusion of nerve growth factor improves recognition memory in the rat[J]. Neuropharmacology, 2013, 75:255-61. |
| [4] | Lim S, Moon M, Oh H, et al. Ginger improves cognitive function via NGF-induced ERK/CREB activation in the hippocampus of the mouse[J]. J Nutr Biochem, 2014, 25(10):1058-65. |
| [5] | 宋玫香,张 岩,王 芳,等. 丁酸钠通过维持乙酰化平衡改善帕金森病模型鼠认知功能和情感障碍[J].中国药理学通报,2012,28(7):988-93.Song M X,Zhang Y, Wang F,et al. Sodium butyrate improved cognitive and affective disorder of PD model mice mainly via maintenance of histone acetylation homeostasis[J]. Chin Pharmacol Bull,2012,28(7):988-93. |
| [6] | 周 东. 神经病学(供双语教学使用) [M]. 北京:高等教育出版社, 2011:250-64. |
| [7] | 王晓民, 梁希彬. 帕金森病因学研究[J].世界科技研究与发展, 1999, 21 (6):52-5. Wang X M,Liang X B. Studies on The etiology of Parkinson's disease[J]. World Sci Tech R & D, 1999, 21(6):52-5. |
| [8] | 吴 斌, 王晓平. 第二届国际神经退行性疾病学术研讨会 (上海) 纪要[J].中华脑科疾病与康复杂志 (电子版), 2012, 2(3):182-4.Wu B, Wang X P.Summary of 2ed International conference of cognitive movement disorders & degeneration (Shanghai)[J].Chin J Brain Dis Rehab (Elec-tonic Edition), 2012, 2(3):182-4 . |
| [9] | 毕 波, 刘 力, 金魁和, 等. 慢性应激对大鼠海马 NGF, NT-3 表达的影响及应激停止后的变化[J].中国行为医学科学, 2007, 16(6):490-2.Bi B, Liu L, Jin K H,et al. Effects of chronic stress on the expression of NGF,NT-3 in hippocampus of the rats [J]. Chin J Behav Med Brain Sci, 2007, 16(6):490-2. |
| [10] | Lorigados P L, Pavón F N, Alvarez G L, et al. Nerve growth factor levels in Parkinson disease and experimental parkinsonian rats[J]. Brain Res, 2002, 952(1):122-7. |
| [11] | 曾 莉, 张 旻, 卜碧涛. 实验啮齿类动物行为学评估[J].神经损伤与功能重建, 2008, 3(5):352-6.Zeng L, Zhang M, Bu B T. The behavior assessment of experimental rodent animal[J]. NIFR, 2008, 3(5):352-6. |
| [12] | Simon D, Seznec H, Gansmuller A, et al. Friedreich ataxia mouse models with progressive cerebellar and sensory ataxia reveal autophagic neurodegeneration in dorsal root ganglia [J]. J Neurosci, 2004, 24(8):1987-95. |
| [13] | Oliver P L, Keays D A, Davies K E. Behavioural characterisation of the robotic mouse mutant[J]. Behav Brain Res, 2007, 181(2):239-47. |
| [14] | Jackson-Lewis V, Przedborski S. Protocol for the MPTP mouse model of Parkinson's disease[J]. Nat Protoc, 2007, 2(1):141-51. |
| [15] | Dag A, Kjeld A, Larsen J P, et al. Prevalence and characteristics of dementia in Parkinson disease:an 8-year prospective study[J]. Arch Neurol, 2003, 60(3):387-92. |
| [16] | Perry J C, Cunha C D, Anselmo-Franci J, et al. Behavioural and neurochemical effects of phosphatidylserine in MPTP lesion of the substantia nigra of rats[J]. Eur J Pharmacol, 2004, 484(2):225-33. |
| [17] | 耿劲松, 周爱玲, 茅家慧, 等. 脑益康对AD大鼠学习记忆及海马NGF-TrkA mRNA表达的影响[J].中国老年学杂志, 2009, 29(2);152-5.Geng J S, Zhou A L, Mao J H, et al. Effects of Naoyikang on both learning and memory ability and expression of NGF-TrkA mRNA in rats with Alzheimer's disease[J].Chin J Gerontol, 2009, 29 (2):152-5 . |
| [18] | Chaturvedi R K, Shukla S, Seth K, Agrawal A K. Nerve growth factor increases survival of dopamin-ergic graft, rescue nigral dopaminergic neurons and restores functional deficits in rat model of Parkinson's disease[J]. Neurosci Lett, 2006, 398(1):44-9. |
| [19] | Henriksson B G, Söderström S, Gower A J, et al. Hippocampal nerve growth factor levels are related to spatial learning ability in aged rats[J]. Behav Brain Res, 1992, 48 (1):15-20. |
| [20] | Conner J M, Franks K M, Titterness A K, et al. NGF is essential for hippocampal plasticity and learning[J]. J Neurosci, 2009, 29(35):10883-9. |
