


2. 中国医学科学院北京协和医学院药用植物研究所, 北京 100193
陈素红(1973-),女,研究员,博士生导师,研究方向:中药药效学与中药新产品开发,通讯作者,Tel/Fax:0571-86613601,E-mail:chensuhong06@yahoo.com.cn
2. Institute of Medicinal Plant Development, Chinese Academy of Medical Sciences and Peking Union Medical College, Beijing 100193, China
冠状动脉粥样硬化性心脏病是指冠状动脉粥样硬化使血管腔狭窄或阻塞,导致心肌缺血、缺氧而引起的心脏病。随着生活方式的改变,肥胖和吸烟人群的增加,高血压病、糖尿病、高脂血症发病率的增加,冠心病发病率不断增高,越来越多的学者开始关注于冠心病的发病机制研究。氧化应激损伤被认为是重要的发病机制之一。氧化应激损伤主要来自于缺血部位的心肌细胞在再灌注过程中(急性),或长期低氧条件下(慢性)产生的过量活性氧自由基(reactive oxygen species,ROS)。这些ROS会攻击心肌细胞的脂质、DNA及蛋白质等生物大分子,使已经损伤的心肌细胞情况更加恶化[1]。Nrf2/ARE信号通路是人体内重要的抗氧化通路,调控着细胞对氧化应激的抵抗能力。Nrf2/ARE信号通路可以诱导细胞内的二相抗氧化酶来清除多余的ROS,保持细胞内氧化还原状态的平衡,并减轻ROS对细胞的损伤[2]。有研究表明在冠状动脉粥样硬化的治疗中Nrf2/ARE信号通路发挥着重要的作用[3]。
异鼠李素(isorhamnetin,ISO)属于黄酮类化合物,并广泛存在于植物界中。其具有较好的抗肿瘤、降血脂、降血压、抗氧化,以及扩张冠脉等多种药理作用,在心血管系统疾病防治中具有广泛的应用前景[4]。然而,目前关于异鼠李素对心肌细胞保护作用的研究还比较少,本研究将通过建立H9C2心肌细胞氧化应激损伤模型,探索异鼠李素对心肌细胞氧化应激损伤的保护作用以及其对Nrf2/ARE信号通路的影响,以期了解异鼠李素的作用机制并对临床做出指导。
1 材料与方法 1.1 实验材料DMEM(dulbecco′s modified eagle medium,批号:8114057)培养基购自Gibco公司,MTT(批号:2399B477)和胰酶(批号:3049B047)购自Amresco公司,FBS(fetal bovine serum,批号:090722)购自四季青公司,ROS检测试剂(批号:1275755)及凋亡检测试剂(批号808365)购自Invitrogen公司,JC-1试剂(批号:30MYL0)购自ENZO公司,DMSO(dimethyl sulphoxide,批号:089K1407V)购自Sigma公司,细胞核蛋白与细胞质蛋白抽提试剂盒(批号:P0028)购自碧云天公司,Western blot一抗(批号:cytochrome,c-sc-13560;caspase-9,sc-7885;caspase-3,sc-7148;bcl-2,sc-492;Nrf2,G1916;HO-1,F0216;β-actin,sc-1616;lamin B,sc-374015)购自Santa Cruz公司,Western blot二抗(批号:105134)购自中杉金桥公司。考马斯亮蓝蛋白质定量试剂盒(A045-2),过氧化氢酶(catalase,CAT)测定试剂盒(A007-1),谷胱甘肽过氧化物酶(glutathione peroxidase,GSH-Px)测定试剂盒(A005),丙二醛(malondialdehyde,MDA)测定试剂盒(A003-1),总超氧化物歧化酶(total superoxide dismutase,T-SOD)测试盒(A001-1)购自南京建成生物工程研究所。
1.2 仪器流式细胞仪(美国BD公司),电泳仪(美国Bio-Rad公司),荧光显微镜(日本Olympus公司),荧光酶标仪(瑞士Tecan公司)。
1.3 细胞存活率实验MTT法用无血清DMEM将异鼠李素配制成不同浓度,并与H9C2细胞共孵育12 h,然后向正常组以外的实验组加入无血清DMEM配制的300 μmol·L-1 H2O2孵育4 h(在异鼠李素的细胞毒性实验中省略H2O2孵育)。吸弃所有实验组的上清,加入200 μL 1 g·L-1 MTT溶液,孵育4 h。加入200 μL DMSO,混匀后在570 nm波长下测定吸光度。细胞存活率/%=(实验组光吸收值/对照组光吸收值)×100%。
1.4 流式细胞术检测凋亡及活性氧自由基水平变化实验组分为正常组(N)、模型组(M)、治疗组(M+ISO)、单给药组(ISO)。用步骤“1.3”中确定的最佳异鼠李素浓度,与治疗组及单给药组的H9C2细胞预孵育12 h,其他组用无血清DMEM预孵育。预孵育结束后,用300 μmol·L-1 H2O2溶液对模型组与治疗组造模,其他两组换成新鲜无血清DMEM。4 h后消化细胞,用凋亡试剂盒内的200 μL binding buffer重悬各组细胞,再用5 μL FITC标记的Annexin V工作液与1 μL PI工作液共同孵育细胞悬液15 min,然后用流式细胞仪检测;在检测ROS过程中,向培养板中加入用无血清DMEM配制的25 μmol·L-1的ROS探针,将各组H9C2细胞于37℃下避光孵育0.5 h,再用PBS洗两次,然后用流式细胞仪检测。
1.5 荧光显微镜检测线粒体膜电位变化对各组H9C2细胞进行预给药并造模后,向培养板中加入用无血清DMEM配制的2μmol·L-1 JC-1探针,于37℃下避光孵育0.5 h,再用PBS洗两次。用荧光显微镜进行观察拍照。统计结果由image-pro plus软件分析得出。
1.6 细胞内MDA、SOD、CAT、GSH-Px的测定对各组H9C2细胞进行预给药并造模后,消化并收集细胞,用-80℃冰箱将各组细胞反复冻融3次,提取细胞内容物,并按照检测MDA、SOD、CAT、GSH-Px试剂盒的说明书进行操作。
1.7 Western blot检测细胞内蛋白表达 1.7.1 胞质蛋白提取对各组H9C2细胞进行预给药并造模后,用PBS洗涤细胞1次并消化,400×g 10 min离心细胞,并加入细胞裂解液400 μL重悬,于4℃裂解1 h。800×g离心15 min,收集上清液,BCA法测定蛋白浓度。
1.7.2 核蛋白提取收集“1.7.1”中的沉淀,并加入50 μL核蛋白抽提试剂,剧烈震荡5 min,于4℃静置30 min。800×g 15 min离心,收集上清液,BCA法测定蛋白浓度。
1.7.3 Western blot步骤每组取20 μg的总蛋白,12% SDS-PAGE分离蛋白,用电转移法将蛋白质转移至PVDF膜,5%脱脂奶粉室温封闭3 h,分别加入细胞质cytochrome C、caspase-9、caspase-3、bcl-2、Nrf2、HO-1、β-actin、lamin B、Nrf2、HO-1一抗(1 ∶ 200稀释),4℃过夜;TBST溶液洗涤3次(×15 min),加入辣根素过氧化酶标记的二抗,室温孵育4 h,TBST溶液洗膜3次(×15 min),化学发光法显影。在检测Nrf2及HO-1的实验中,未对细胞进行造模。所检测的蛋白表达为异鼠李素对正常细胞抗氧化通路的作用。
1.8 统计学分析所有实验均重复3次,数据采用SPSS 17.0统计软件进行分析,计量资料先进行正态性检验,正态分布资料采用单因素方差分析,非正态分布资料转成正态分布后再采用单因素方差分析;计数资料采用非参数秩和检验。
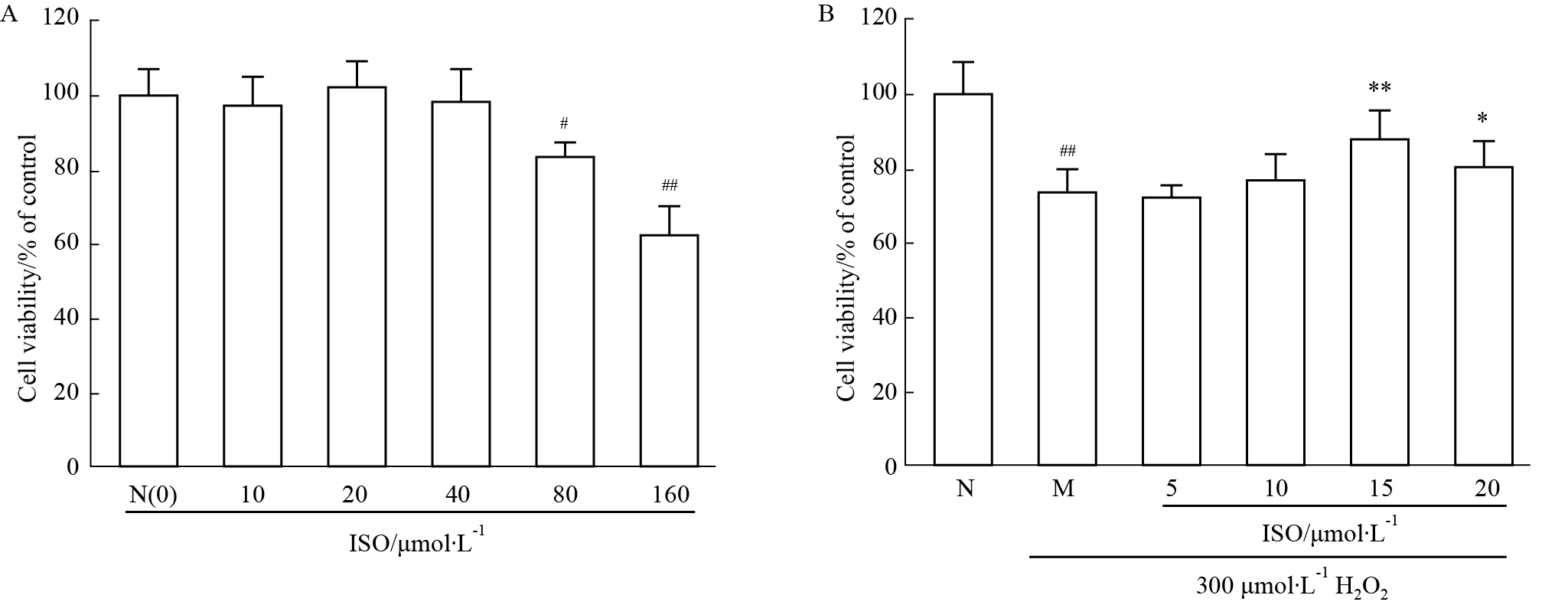
2 结果 2.1 异鼠李素的毒性作用以及对H2O2引起的H9C2细胞损伤的保护作用MTT结果(Fig1A)显示,0~40 μmol·L-1的异鼠李素溶液与H9C2细胞共孵育12 h未见毒性作用,各组活率与正常组的差异无统计学意义(P>0.05)。80(P<0.05)与160 μmol·L-1(P<0.01)的异鼠李素则使H9C2细胞的活率明显下降。异鼠李素的保护作用结果则表明(Fig1B),15 μmol·L-1的异鼠李素对H2O2致H9C2细胞损伤的保护作用较好,其与模型组M相比差异有统计学意义(P<0.01)。20 μmol·L-1的异鼠李素也具有保护作用,差异有显著性(P<0.05)。与模型组相比,其他浓度的作用没有统计学意义(P>0.05),由于这些浓度还未至异鼠李素的毒性作用浓度,因此,保护作用的降低并非是由于异鼠李素毒性的原因。
|
| Fig 1 Toxicity of isorhamnetin and its protective effect on oxidatively injured H9C2 cell line A:H9C2 cells were treated with a series of concentrations of isorhamnetin for 12h, then cell viability was detected by MTT assay; B: H9C2 cells were pretreated with different concentrations of ISO and injured by 300 μmol·L-1 H2O2, then cell viability was detected by MTT assay. The concentrations of 15 and 20 μmol·L-1 ISO were considered to protect H9C2 cells significantly. All experiments were repeated 3 times, and the most representative result was given. #P<0.05,##P<0.01 vs N group; *P<0.05, **P<0.01 vs M group. |
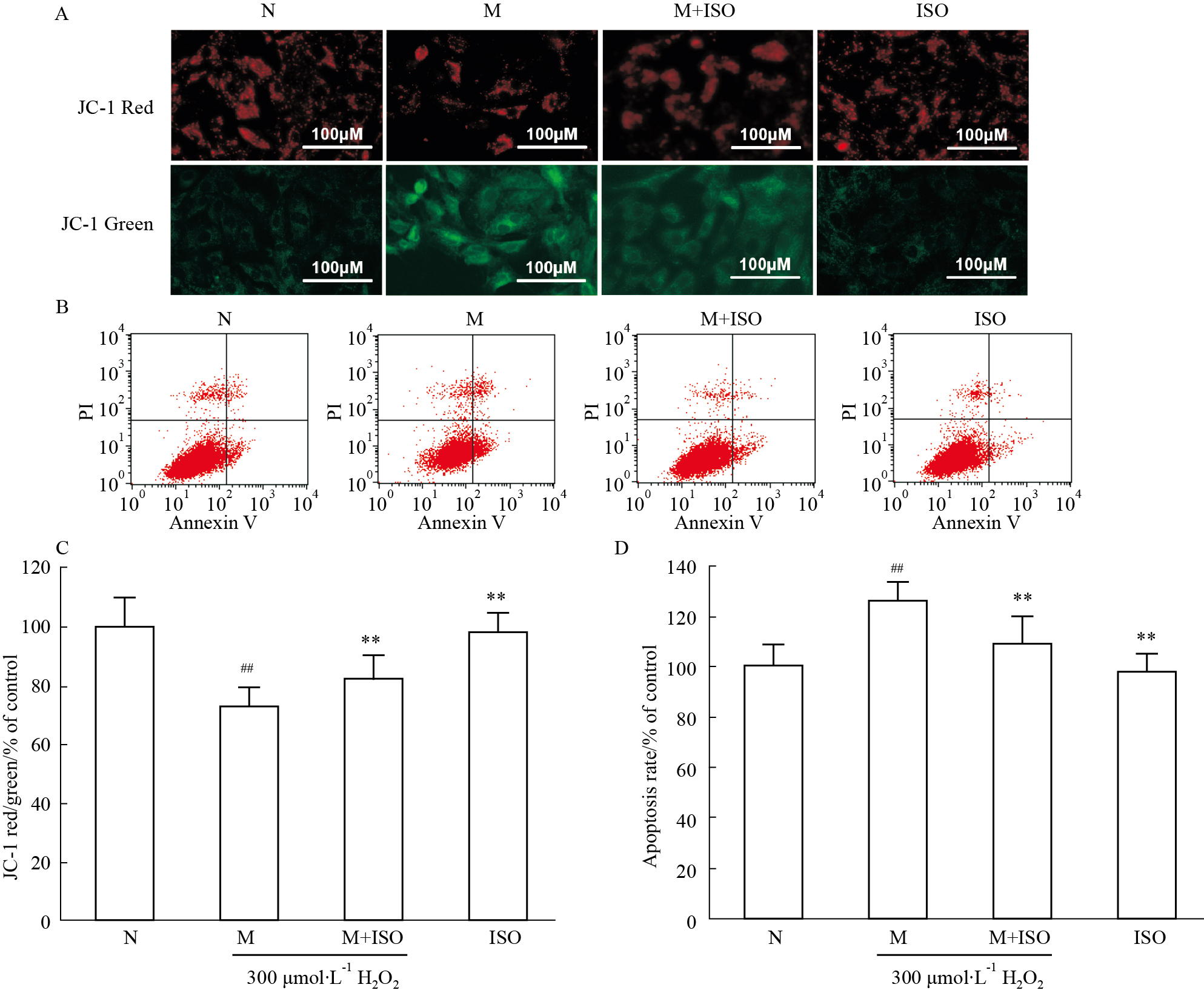
在检测线粒体膜电位的实验当中,本实验利用红绿荧光的比例来体现线粒体膜电位去极化的程度。红色荧光表达越强,或者表达比例越高,说明去极化程度越弱。由Fig2A,C可知,与正常组相比,模型组的线粒体膜电位去极化明显(P<0.01)。15 μmol·L-1异鼠李素可缓解治疗组H9C2细胞的MMP去极化(P<0.01)。对凋亡水平(Fig2B,D)的检测也呈现出类似的结果,与模型组相比,治疗组的凋亡细胞比例明显降低(P<0.01)。而与正常组相比,单给药组的MMP去极化与细胞凋亡水平均没有差异(P>0.05)。因此,15 μmol·L-1的异鼠李素对于H2O2引起H9C2的MMP去极化、细胞凋亡都有抑制的作用。
|
| Fig 2 Effects of isorhamnetin on apoptosis of oxidatively injured H9C2 cell line A:MMP was detected using fluorescence microscope, H9C2 cells were injured by 300 μmol·L-1 H2O2 with or without pretreatment with 15μmol·L-1 ISO; B:The apoptotic rate of H2O2-injured H9C2 cells were measured by flow cytometry. H9C2 cells were injured by 300 μmol·L-1 H2O2 with or without pretreatment with 15μmol·L-1 ISO; C:Statistical analysis was shown from (A) indicating 15 μmol·L-1 ISO ameliorated the depolarization of MMP of H2O2-injured H9C2 cells significantly; D:Statistical analysis was shown from (B) indicating ISO rescued H2O2- induced H9C2 cells apoptosis significantly. All experiments were repeated 3 times, and the most representative result was given. ##P<0.01 vs N group; **P<0.01 vs M group. |
如Fig3所示,与模型组相比,异鼠李素可以明显降低治疗组H9C2的Bax、胞质细胞色素C、caspase-9与caspase-3的表达(P<0.01),并能够提高由于损伤而降低的Bcl-2的表达(P<0.01)。这些结果提示,异鼠李素治疗组可以抑制氧化应激引起的H9C2细胞凋亡,而这种保护作用是通过抑制线粒体凋亡通路来实现的。

|
| Fig 3 Effect of isorhamnetin on apoptotic signal pathway of oxidatively injured H9C2 cell line 1:N;2:M;3:M+ISO;4:ISO. H9C2 cells were pretreated with or without ISO, followed by H2O2 injury. The expressions of apoptosis related proteins were observed and the statistical results were given below. All experiments were repeated 3 times, and the most representative result was given. ##P<0.01 vs N group;**P<0.01 vs M group. |
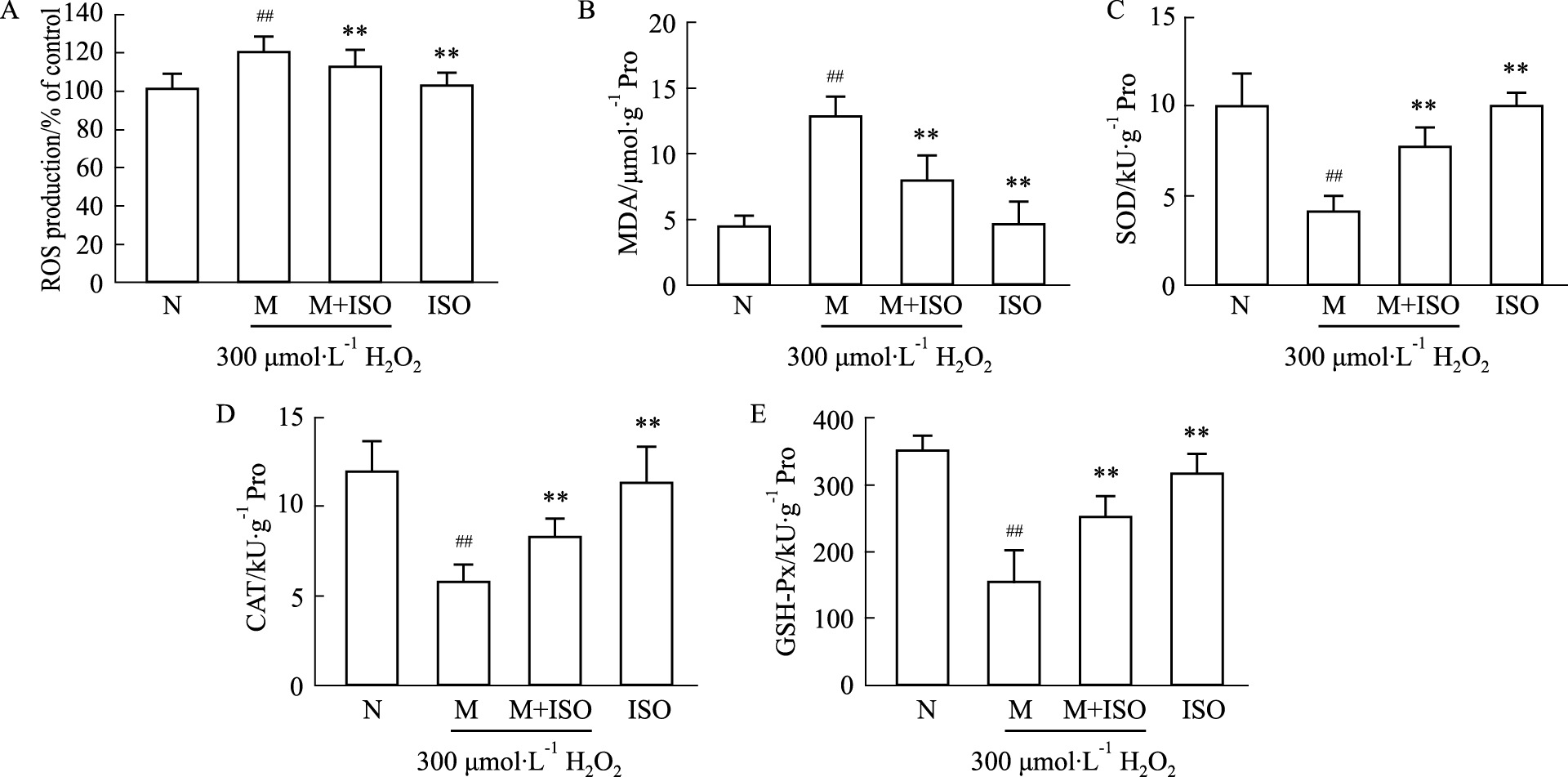
为了研究异鼠李素对H9C2细胞抗氧化能力的影响,本实验检测了细胞内ROS、丙二醛(MDA)、超氧化物歧化酶(SOD)、过氧化氢酶(CAT)与谷胱甘肽过氧化物酶(GSH-Px)产生的变化。本实验首先研究了异鼠李素对H2O2造成H9C2细胞产生过量ROS的影响。结果表明(Fig4A)异鼠李素可以保护H9C2细胞,抑制H2O2造成的过量ROS产生。与模型组相比,治疗组ROS的产生明显降低(P<0.05)。MDA是细胞内的脂质过氧化物,其含量可以反映出细胞损伤的程度,SOD、CAT与GSH-Px是细胞内的抗氧化酶,对细胞的氧化损伤起着重要的保护作用[5]。如Fig4B所示,模型组的MDA含量较正常组明显升高(P<0.01),经异鼠李素预孵育后则使MDA明显降低(P<0.01)。另一方面,与正常组相比,模型组的抗氧化酶SOD、CAT与GSH-Px都明显下降(Fig4C,D,E,P<0.01)。而治疗组的抗氧化酶产量均较模型组明显增加(P<0.01)。单独给予异鼠李素处理组的ROS、MDA、SOD、CAT与GSH-Px较正常组差异均无显著性(P>0.05)。
|
| Fig 4 Effects of isorhamnetin on ROS, MDA, SOD, CAT, GSH-Px generations of oxidatively injured H9C2 cell line A:The production of ROS was detected by flow cytometry, and the statistical result was given. 15 μmol·L-1 ISO inhibited ROS production of damaged H9C2 dramatically; B:Effects of ISO on activities of MDA in H9C2 injured by H2O2; C:Effects of ISO on activities of SOD in H9C2 injured by H2O2; D:Effects of ISO on activities of CAT in H9C2 injured by H2O2; E:Effects of ISO on activities of GSH-Px in H9C2 injured by H2O2. All experiments were repeated 3 times, and the most representative result was given. ##P<0.01 vs N group; **P<0.01 vs M group. |
接下来,本实验研究了异鼠李素对抗氧化信号通路的影响。由于Nrf2/ARE信号通路是体内重要的抗氧化信号通路,本研究推测异鼠李素的抗氧化应激作用可能与该通路相关。根据Western blot的结果(Fig5)可知,在4~24 h这段时间内,异鼠李素逐渐增加Nrf2的核转位以及抗氧化 酶HO-1的表达,抗氧化作用不断增强。这表明异鼠李素对H9C2细胞的保护至少部分是通过Nrf2/ARE信号通路来发挥作用的。

|
| Fig 5 Effect of isorhamnetin on Nrf2/ARE signal pathway of H9C2 cell line H9C2 cells were pretreated with or without ISO, followed by H2O2 injury. The expressions of Nrf2/ARE pathway related proteins were observed and the statistical results were given below. All experiments were repeated 3 times, and the most representative result was given. ##P<0.01 vs 4h group; **P<0.01 vs 8h group; ΔΔP<0.01 vs 12h group. |
在冠状动脉粥样硬化性心脏病发生及发展的过程中,氧化应激损伤起着重要的作用。氧化应激是指体内氧化与抗氧化作用失衡,倾向于氧化,导致大量氧化中间产物的产生。ROS包括超氧阴离子(·O2-)、羟自由基(·OH)和过氧化氢(H2O2)等。氧化应激损伤中产生的过量ROS会损伤心肌细胞线粒体,刺激线粒体释放细胞色素C,继而活化caspase家族,如caspase-9、caspase-3等,并最终导致心肌细胞死亡[6]。除此之外,ROS还能够引起炎症反应及低密度脂蛋白氧化,导致巨噬细胞成为泡沫细胞,血管平滑肌细胞增生,促使冠状动脉内斑块形成[7]。有研究表明,异鼠李素可以缓解ox-LDL对内皮细胞产生的损伤[8]。本实验利用H2O2损伤H9C2细胞的模型来模拟过量ROS损伤心肌细胞,并探索异鼠李素对心肌细胞的保护作用。结果表明,15 μmol·L-1的异鼠李素可以保护H9C2细胞,对抗H2O2造成的氧化应激损伤。而其他浓度没有改善效果,毒性实验的结果表明,在孵育时间相同的条件下,异鼠李素从80 μmol·L-1的浓度才开始出现H9C2的细胞毒性作用。这些结果提示,异鼠李素能够降低H2O2对H9C2心肌细胞的损伤,并且在 15 μmol·L-1的浓度下具有最佳的保护作用。随着 浓度的增加,异鼠李素的保护作用逐渐减弱,而这种减弱并非是由于细胞毒作用造成的。
心肌细胞的凋亡是心肌损伤的重要机制。在心肌细胞的凋亡中,线粒体起着重要的作用。在线粒体内膜上,存在着名为线粒体通透性转换孔的孔道(mPTP)。氧化应激等损伤会促使mPTP开放,而mPTP的持续开放会导致线粒体膜电位去极化,并释放线粒体内的促凋亡物质如细胞色素C至细胞质中[9],继而导致caspase-9、-3的活化,最终引起细胞凋亡[6]。线粒体同时也是Bcl-2基因家族发挥作用的场所,Bcl-2基因家族包括抗凋亡基因Bcl-2、Bcl-lx与促凋亡基因Bax、Bad、Bid、Bnip3。Bax转位至线粒体中则会导致细胞色素C的释放,而抗凋亡蛋白Bcl-2能够保持线粒体膜的完整性、稳定性,并与Bax形成二聚体,减少细胞色素C的释放[10]。因此本实验研究了异鼠李素对线粒体膜电位以及细胞凋亡的影响。实验结果表明,H2O2促进H9C2细胞线粒体膜电位去极化,使线粒体内的细胞色素C释放至细胞质内,并使caspase-9与caspase-3相继活化,导致心肌细胞凋亡。Bcl-2的表达下调与Bax上调也同样表明线粒体受到损伤,线粒体凋亡通路被活化。而异鼠李素逆转了治疗组细胞的上述指标,这表明异鼠李素能够作用于心肌细胞的线粒体凋亡通路,抑制H2O2对心肌细胞的损伤,降低了心肌细胞凋亡。
ROS的作用是复杂的。一方面,ROS是机体正常功能所必需的,是线粒体呼吸作用的正常副产物[11]。它还可以作为一种信号分子,活化细胞内的信号通路,维持细胞正常机能与氧化还原状态,甚至还会参与组织的再生与修复[12];另一方面,ROS又与心肌细胞的氧化应激损伤存在着密切的关系,过量的ROS可以损伤心肌细胞的脂质、DNA及蛋白质等生物大分子,从而加重心脏的损伤[13]。在冠状动脉粥样硬化性心脏病的缺血阶段,细胞内抗氧化物活性降低,ROS产生增加。而当再灌注发生时,线粒体受到氧化应激损伤,会产生过量的ROS,这些ROS会再次损伤线粒体,形成恶性循环,最终导致细胞的死亡[11]。实验结果表明,单给药组的ROS产生与正常组相比不存在差异,这说明异鼠李素并未对生理水平的ROS产生影响。而H2O2则会引起H9C2心肌细胞ROS产量增加,抗氧化酶SOD、CAT、GSH-Px产量降低,造成过量的ROS得不到有效的清除。这些过量的ROS会氧化生物膜的磷脂、酶和膜受体相关的生物大分子,并产生有害的脂质过氧化产物丙二醛(MDA)[14],因此H9C2细胞内MDA明显增加。由于ROS也会损伤线粒体,如线粒体膜、DNA、蛋白质等[11],因此过量的ROS能够造成线粒体氧化还原状态失衡,引起线粒体凋亡通路活化,并导致细胞凋亡。这也可能是H2O2导致H9C2细胞凋亡的原因。而异鼠李素能够缓解治疗组H9C2细胞的氧化应激负荷,抑制细胞内ROS产生与脂质过氧化,并提高细胞内的抗氧化酶水平。凭借这些作用,异鼠李素能够抑制H9C2心肌细胞的线粒体凋亡途径,达到保护心肌细胞的作用。
Nrf2/ARE信号通路是抗氧化的重要通路,Nrf2与Keap1以无活性的二聚体形式存在于细胞质内,当受到外界氧化应激刺激后,Nrf2与Keap1分离,转位进入细胞核。在细胞核内Nrf2与Maf、抗氧化反应元件(Antioxidant responsive element,ARE)结合并调控二相抗氧化酶如HO-1等的表达[15]。在某些情况下,例如血管老化,Nrf2不能对ROS做出反应,这将导致血管及心脏的氧化应激损伤[16]。由Western blot的结果可知,随着孵育时间的增加,异鼠李素可以逐渐增加Nrf2的核转位以及其所调控的二相抗氧化酶HO-1的表达。这表明异鼠李素可以活化Nrf2/ARE信号通路,并增加其下游二相抗氧化酶的表达。有研究表明,Nrf2能够上调抗凋亡蛋白Bcl-2的表达,来实现抗氧化,抗细胞凋亡的作用[17]。本研究结果提示,异鼠李素可以通过促进Nrf2的核转位,活化Nrf2/ARE通路,并抑制细胞凋亡与氧化应激负荷,促进细胞存活。
综上所述,本研究采用H2O2诱导的H9C2氧化损伤模型,探索异鼠李素对心肌细胞的保护作用。研究的结果表明,异鼠李素具有抗氧化、抗凋亡作用,其机制是通过活化Nrf2通路来提高心肌细胞的抗氧化能力,抑制心肌细胞凋亡。上述实验结果为临床应用异鼠李素治疗冠状动脉粥样硬化性心脏病提供了支持,也为开发治疗冠状动脉粥样硬化性心脏病药物提供了依据。
(致谢:本研究于中国医学科学院北京协和医学院药用植物研究所药理毒理中心完成。感谢实验室的各位老师与同学给予的大力支持和无私帮助。)
| [1] | Rodrigo R, Libuy M, Feliu F, et al. Molecular basis of cardioprotective effect of antioxidant vitamins in myocardial infarction[J]. Biomed Res Int, 2013, 2013:437613. |
| [2] | Lee J H, Khor T O, Shu L, et al. Dietary phytochemicals and cancer prevention:Nrf2 signaling, epigenetics, and cell death mechanisms in blocking cancer initiation and progression[J]. Pharmacol Ther, 2013, 137(2):153-71. |
| [3] | Bozaykut P, Karademir B, Yazgan B, et al. Effects of vitamin E on peroxisome proliferator-activated receptor gamma and nuclear factor-erythroid 2-related factor 2 in hypercholesterolemia-induced atherosclerosis[J]. Free Radic Biol Med, 2014, 70:174-81. |
| [4] | 赵增光, 刘应才. 异鼠李素的心血管保护作用[J]. 医学综述, 2008 (15):2321-3. Zhao Z G, Liu Y C. Cardiovascular protective effect of isorhamnetin[J]. Med Recap, 2008 (15):2321-3. |
| [5] | Meng X B, Sun G B, Wang M, et al. P90RSK and Nrf2 Activation via MEK1/2-ERK1/2 pathways mediated by Notoginsenoside R2 to prevent 6-hydroxydopamine-induced apoptotic death in SH-SY5Y cells[J]. Evid Based Complement Alternat Med, 2013, 2013:971712. |
| [6] | Rajendran P, Nandakumar N, Rengarajan T, et al. Antioxidants and human diseases[J]. Clin Chim Acta, 2014, 436C:332-47. |
| [7] | Vichova T, Motovska Z. Oxidative stress:Predictive marker for coronary artery disease[J]. Exp Clin Cardiol, 2013, 18(2):e88-91. |
| [8] | Bao M, Lou Y. Isorhamnetin prevent endothelial cell injuries from oxidized LDL via activation of p38MAPK[J]. Eur J Pharmacol, 2006, 547(1-3):22-30. |
| [9] | Solesio M E, Saez-Atienzar S, Jordan J, et al. 3-Nitropropionic acid induces autophagy by forming mitochondrial permeability transition pores rather than activating the mitochondrial fission pathway[J]. Br J Pharmacol, 2013, 168(1):63-75. |
| [10] | 谢 飞, 魏 珂, 闵 苏, 等. 神经生长因子对H9c2心肌细胞缺氧/复氧后凋亡的保护作用及其机制[J]. 中国药理学通报, 2014, 30(4):506-10. Xie F,Wei K,Min S, et al. Anti-apoptotic effect of NGF on H9c2 cardiac myocytes in a hypoxia/reoxygenation injury model[J]. Chin Pharmacol Bull, 2014, 30(4):506-10. |
| [11] | Dai D F, Chiao Y A, Marcinek D J, et al. Mitochondrial oxidative stress in aging and healthspan[J]. Longev Healthspan, 2014, 3:6. |
| [12] | Urao N, Ushio-Fukai M. Redox regulation of stem/progenitor cells and bone marrow niche[J]. Free Radic Biol Med, 2013, 54:26-39. |
| [13] | Rodrigo R, Prieto J C, Castillo R. Cardioprotection against ischaemia/reperfusion by vitamins C and E plus n-3 fatty acids:molecular mechanisms and potential clinical applications[J]. Clin Sci (Lond), 2013, 124(1):1-15. |
| [14] | Han S, Zhang H, Qin L, et al. Effects of dietary carbohydrate replaced with wild rice (Zizania latifolia (Griseb) Turcz) on insulin resistance in rats fed with a high-fat/cholesterol diet[J]. Nutrients, 2013, 5(2):552-64. |
| [15] | Kansanen E, Kuosmanen S M, Leinonen H, et al. The Keap1-Nrf2 pathway:Mechanisms of activation and dysregulation in cancer[J]. Redox Biol, 2013, 1(1):45-9. |
| [16] | Cho Y H, Cha M J, Song B W, et al. Enhancement of MSC adhesion and therapeutic efficiency in ischemic heart using lentivirus delivery with periostin[J]. Biomaterials, 2012, 33(5):1376-85. |
| [17] | Fan J, Xu G, Jiang T, et al. Pharmacologic induction of heme oxygenase-1 plays a protective role in diabetic retinopathy in rats[J]. Invest Ophthalmol Vis Sci, 2012, 53(10):6541-56. |

