


2. 南京中医药大学药学院, 江苏 南京 210023
2. College of Pharmacy, Nanjing University of Chinese Medicine, Nanjing 210023, China
磷脂转运蛋白(phospholipid transfer protein,PLTP)属于脂质转移/脂多糖结合蛋白家族LTP/LBP,可以介导磷脂在脂蛋白间的交换,参与高密度脂蛋白(high density lipoprotein,HDL)亚类的组成,影响HDL代谢[1]。流行病学及动物体内研究均表明,PLTP的高表达已成为冠心病的独立危险因子,因而抑制PLTP的表达已成为抗动脉粥样硬化(atherosclerosis,AS)的主要手段[2]。我们在前期临床观察中发现,冠心病患者血清中PLTP表达水平较正常人明显升高[3],为了进一步研究PLTP的功能以及观察药物能否通过PLTP途径抑制AS的发生发展,我们建立了ApoE-/-小鼠AS模型,观察半枝莲活性成分半枝莲总黄酮(total flavonoids of scutellaria barbata,TFSB)对高脂饲养的ApoE-/-小鼠早期AS病变形成的影响,旨在研究和揭示TFSB抗AS的作用机制,为探讨中药抗AS的研究提供新的思路和实验依据。
1 材料与方法 1.1 实验动物♂ ApoE-/-小鼠(品系C57BL/6J),40只,清洁级,11周龄,体质量(22.3±2.7)g,由北京市维通利华实验动物中心提供。
1.2 药品、试剂及仪器TFSB(由扬州大学医学院药学实验室提供,总黄酮含量为24.12%);辛伐他汀(40 mg/片,5片/盒,杭州默沙东制药有限公司,批号:100260);PLTP ELISA试剂盒(USCNLIFE公司,货号080527);VE ELISA试剂盒(USCNLIFE公司,货号081012);PLTP一抗为兔抗小鼠单克隆抗体(USCNLIFE公司,货号HZ55321);PLTP二抗为人抗兔多克隆抗体(BioVision公司,货号3595-100);免疫组化染色SABC试剂盒(武汉博士德公司,货号:SA1073);内参蛋白GAPDH一抗为兔抗小鼠多克隆抗体(武汉博士德公司,货号:BA2913),二抗为抗兔多克隆抗体(武汉博士德公司,货号:BM1623)。BX51系统显微镜(Olympus公司);JEDA801D形态学图像分析系统(江苏捷达科技发展有限公司)。
1.3 实验方法 1.3.1 动物分组及给药♂ ApoE-/-小鼠40只,给予普通饲料适应性饲养1周,室温保持在22~24℃,相对湿度为50%,光照时间为7 ∶ 00~19 ∶ 00。1周后,将小鼠随机分成5组:模型组、TFSB低、中、高剂量组和辛伐他汀组,每组8只。另取11周龄正常C57BL/6J小鼠8只作为正常对照组。模型组以高脂饲料喂饲12周,各给药组给予高脂饲料4周后,开始灌胃给药,每日1次。按照体表系数折算人和小鼠的用药量,换算得给药剂量:辛伐他汀组3.3 mg·kg-1·d-1;根据课题组前期实验结果,TFSB低、中、高有效给药剂量分别为100、200、400 mg·kg-1·d-1。正常对照组、模型组每天给予等容量的0.5%CMC-Na。连续给药8周,末次给药后24 h处死。
1.3.2 指标检测模型组以高脂饲料连续喂饲12周后,禁食12 h,眼眶取血0.5 mL,静置1 h后3 000 r·min-1离心10 min,取血清待用;处死动物,眼眶取血,肝素抗凝,采用LBY-N6 型血液流变仪测全血黏度(低切、高切)、血浆黏度,用温氏法测红细胞比容。无菌条件下取心脏主动脉根部,10%福尔马林固定,常规脱水,石蜡包埋并切片,苏木精-伊红(hematoxylin-eosni,HE)染色观察AS程度。采用全自动生化分析仪检测血清总胆固醇(total cholesterol,TC)、甘油三酯(triglyceride,TG)、低密度脂蛋白-胆固醇(low density lipoprotein-cholesterol,LDL-C)、HDL-C的表达水平。采用ELISA方法检测血清PLTP及VE的表达水平,操作步骤严格按照说明书进行。提取肝组织中PLTP及FXR总蛋白,配制上样蛋白样品,经12%的SDS-PAGE电泳分离。转于PVDF膜上,5%脱脂奶粉封闭,以TBST 1 ∶ 200稀释的兔抗鼠一抗4℃孵育过夜,二抗孵育后PBS清洗,DAB显色,用 Image-Pro Plus 软件扫描作积分吸光度值(integral absorbance,IA)分析。以目的蛋白PLTP或FXR与内参蛋白(GAPDH)条带的IA比值评定 PLTP的表达水平。
1.4 统计学处理计量资料以 表示,多组间比较采用单因素方差分析,变量间采用Pearson相关分析方法,采用SPSS 15.0统计软件完成。
表示,多组间比较采用单因素方差分析,变量间采用Pearson相关分析方法,采用SPSS 15.0统计软件完成。
HE染色后光镜下观察发现,正常组主动脉平滑肌层较薄,内膜光滑且连续、结构完整、内皮细胞完整,弹性膜无断裂,无动脉粥样硬化病灶。而模型组的主动脉管壁内膜则呈明显增厚,可见丘状斑块。平滑肌纤维数量增多,内膜含有较多泡沫细胞。TFSB组主动脉内壁内皮层结构完好,管壁三层结构分层清楚,偶见泡沫细胞,其形态结构较模型组明显改善。模型组红细胞比容、血浆黏度、全血黏度(低切、高切)明显高于正常对照组,经统计学检验差异有显著性(P<0.01);TFSB低、中、高剂量组均可明显降低红细胞比容、血浆黏度及全血黏度(低切、高切),与模型组相比,差异均有显著性(P<0.01);TFSB中剂量及高剂量效果优于阳性对照药辛伐他汀组。见Tab1。
经One-way ANOVA分析,模型组的TC、LDL-C、TG表达水平明显升高,HDL-C水平明显降低,与正常对照组比较,差异具有显著性(P<0.01),提示造模成功。TFSB各剂量组的TG、TC水平明显降低,与模型组相比,差异具有显著性(P<0.01);TFSB各剂量组的LDL-C水平明显降低,与模型组相比,差异具有显著性(P<0.05或P<0.01);TFSB各剂量组的HDL-C水平明显升高,与模型组比较,差异有显著性(P<0.01)。TFSB高剂量组降低TC、TG、LDL-C的作用及升高HDL-C的作用均优于阳性对照药辛伐他汀。见Tab2。
经 One-way ANOVA 分析,模型组PLTP的水平均明显高于正常对照组,VE水平明显低于正常对照组,差异均具有显著性(P<0.01)。TFSB中、高剂量组的PLTP表达水平较模型组明显降低(P<0.01),VE水平较模型组明显升高(P<0.01),差异亦具有显著性,且作用优于辛伐他汀组。经 Linear Regression 相关性分析,PLTP水平与VE水平呈负相关(r=-0.675,P<0.01)。见Tab3。
各组小鼠肝组织中PLTP均有不同程度的表达,经One-way ANOVA分析,以模型组表达为最高,与正常组相比,差异有显著性(P<0.01);TFSB中、高剂量组能抑制小鼠肝组织PLTP的蛋白表达水平,与模型组相比,差异有显著性(P<0.01),且高剂量组抑制肝组织PLTP蛋白表达的作用强于辛伐他汀(P<0.01)。见Fig1。

|
| Fig 1 Effects of TFSB on expression of PLTP in liver of mice ##P<0.01 vs control group; **P<0.01 vs model group; ▲▲P<0.01 vs SIM group. |
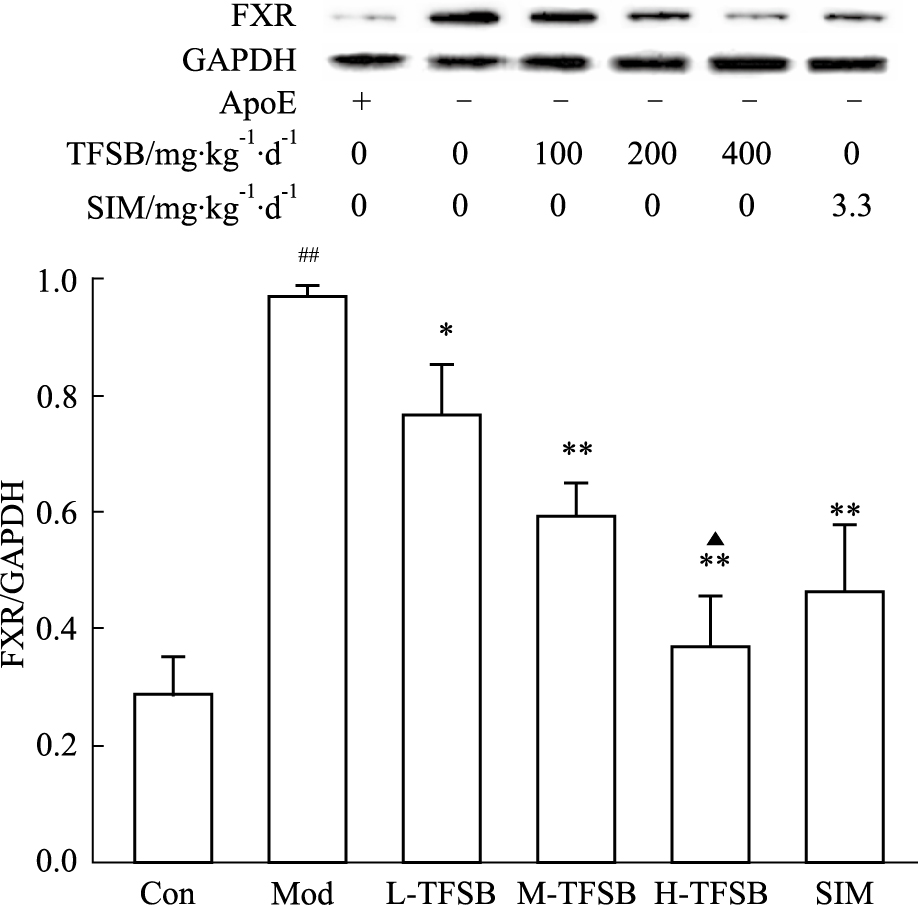
各组小鼠肝组织中FXR均有不同程度 的表达,经One-way ANOVA分析,模型组FXR表达最高,与正常组相比,差异有显著性(P<0.01);药物干预组小鼠肝组织FXR蛋白表达水平均明显下降,与模型组比较,差异有显著性(P<0.05或P<0.01),TFSB各浓度组能抑制小鼠肝组织FXR的蛋白表达水平,其中,中浓度及高浓度TFSB的作用效果与模型组相比,差异有显著性(P<0.01),且抑制肝组织FXR蛋白表达的作用强于辛伐他汀(P<0.05)。见Fig2。
|
| Fig 2 Effects of TFSB on expression of FXR in liver of ApoE-/- mice ##P<0.01 vs control group; *P<0.05; **P<0.01 vs model group;▲P<0.05 vs SIM group. |
AS是冠心病、脑卒中等心血管疾病的基础病变,决定疾病的预后与转归。AS的形成原因非常复杂,脂质转运蛋白的表达调控在脂蛋白代谢和AS中的作用成为国内外研究新的热点。PLTP是一种重要的脂质转运蛋白,参与重构HDL并调节HDL颗粒的大小和亚类组成,影响HDL的功能,从而发挥影响AS发生发展的作用[4]。研究发现,PLTP在人类组织如卵巢、胸腺、胎盘、肺、肝脏和小肠中高表达[5, 6, 7, 8],同时在动脉硬化病变组织和巨噬细胞中也高表达[9, 10]。已有研究表明,冠心病患者血清PLTP活性增加[11]。本课题组前期研究也显示,与正常人群相比,冠心病患者的血清PLTP表达水平也明显升高[3]。由于全身PLTP表达增高是AS动物模型的一个危险因素,因而PLTP过度表达则会诱发AS[12, 13]。因此,降低血浆PLTP的水平对于AS的治疗可能是有益的。
中药抗AS有着多靶点、作用持久、副作用小的独特优势。目前,中药抗AS常用黄酮类化合物,主要包括黄酮及黄酮醇类、二氢黄酮及二氢黄酮醇类、黄烷醇类、异黄酮及二氢异黄酮、双黄酮类等,该类成分能够调节脂质代谢紊乱、保护内皮细胞[14]、抗炎、抗血小板凝集[15]及抗氧化低密度脂蛋白[16]等作用,但对其研究较少涉及到酶、受体、蛋白转导通路等信号机制。本课题组前期研究已经证实TFSB具有调节血脂、抗炎及抗氧化等抗AS的作用,但其作用机制如何,尚不清楚。因此,本研究基于建立的AS[J]小鼠模型,探讨半枝莲活性成分是否通过脂蛋白途径发挥抗AS的作用及其作用机制。
我们选择了ApoE-/-小鼠作为模型动物,由于ApoE是清除乳糜微粒和极低密度脂蛋白受体的配体,因此缺乏ApoE会导致血液循环中富含胆固醇的物质累积,易引起AS病灶形成[17]。在本实验中,11周龄的ApoE-/-小鼠在高脂饮食喂饲12周后,HE染色光学显微镜下可见主动脉管壁内膜增厚,可见隆起丘状斑块。弹性膜有明显断裂现象,血管平滑肌纤维数量增多,细胞质中可见大量脂质,内膜含较多的泡沫细胞。与正常对照组比较,模型组TC、TG、LDL-C水平明显升高,HDL-C水平明显降低,表明造模成功。TFSB干预ApoE-/-小鼠8周后,能够明显降低模型小鼠的TC、TG、LDL-C水平,升高HDL-C水平,表明TFSB有减轻AS病变程度、调节血脂的作用。TFSB能够明显降低红细胞比容、血浆黏度、全血黏度(低切、高切),表明TFSB对ApoE-/-小鼠的血液流变学指标的异常变化具有明显的改善作用。由于VE可延缓或抑制LDL的氧化、抑制平滑肌细胞增殖、抑制血小板黏连、抑制黏着分子的表达和功能,具有预防AS的作用,而PLTP 参与VE代谢,具有转运VE的活性,能够维持组织和血浆VE的表达水平。因此,本研究同时研究了TFSB对ApoE-/-小鼠血清PLTP和VE的影响以及血清PLTP与VE水平的相关性,结果显示,模型组小鼠血清VE水平较正常对照组明显降低,TFSB能明显升高小鼠血清VE水平,血清PLTP水平与VE水平呈负相关,这与部分研究结果一致[12]。已有研究表明,法尼酯衍生物X 受体(farnesoid X receptor,FXR)在AS疾病的过程中起重要作用,AS血脂的改变与FXR活化有关[18, 19, 20]。而PLTP又是FXR的靶基因之一,FXR可上调PLTP转录水平,诱导PLTP的表达[21, 22]。因此,我们进一步研究了不同浓度TFSB对于PLTP的调控作用机制,结果显示,模型组小鼠肝脏FXR及PLTP的蛋白表达水平均明显升高,而不同剂量的TFSB能明显降低小鼠肝脏FXR及PLTP的蛋白表达水平,提示TFSB可能参与调控PLTP信号通路,通过调节PLTP的上游蛋白FXR的表达,下调PLTP的表达,调节血清脂质、降低LDL过氧化,提高VE的表达水平而发挥抗AS的作用。
尽管PLTP在AS中的分子机制还有待于进一步探索,但可以肯定的是,PLTP在AS疾病的过程中起着重要作用,PLTP有望成为治疗AS药物的新型靶点。选择性调控PLTP靶基因的新药正等待我们去探索和发现。
| [1] | Bruce C, Beamer L J, Tall A R. The implications of the structure of the bactericidal/permeability-increasing protein on the lipid-transfer function of the cholesteryl ester transfer protein [J].Curr Opin Struct Biol, 1998, 8(4):426-34. |
| [2] | Schlitt A, Bickel C, Thumma P, et al. High plasma phospholipid transfer protein levels as a risk factor for coronary artery disease [J]. Arterioscler Thromb Vasc Biol, 2003, 23(10):1857-62. |
| [3] | 祝娉婷,卜 平,孙 云,等.冠心病患者血清磷脂转运蛋白及胆固醇脂转运蛋白水平与中医证型相关性研究[J].中国中西医结合杂志,2011, 31(6):749-52. Zhu P T, Bo P, Sun Y, et al. Study on the correlation between chinese medical syndrome types and serum levels of PLTP and CETP in coronary heart disease patients[J]. Chin J Int Tradit West Med, 2011, 31(6):749-52. |
| [4] | 秦树存,叶 平. 磷脂转运蛋白的生物学特性及其与脂蛋白代谢相关疾病的关系[J].中华老年心脑血管病杂志, 2008, 10(8):633-5. Qin S C, Ye P. The relationship between biological characteristics of phospholipid transfer proteinand lipoprotein metabolism related diseases[J].Chin J Geriatr Heart Brain Vessel Dis,2008, 10(8):633-5. |
| [5] | Day J R, Albers J J, Lofton-Day C E, et al. Complete cDNA encoding human phospholipid transfer protein from human endothelial cells[J].J Biol Chem, 1994, 269(12):9388-91. |
| [6] | Cao G, Beyer T P, Yang X P, et al. Phospholipid transfer protein is regulated by liver X receptors in vivo[J].J Biol Chem,2002, 277(42):39561-5. |
| [7] | Valenta D T, Ogier N, Bradshaw G, et al. Atheroprotective potential of macrophage-derived phospholipid transfer protein in low-density lipoprotein receptor-deficient mice is overcome by apolipoprotein AI overexpression[J]. Arterioscler Thromb Vasc Biol, 2006, 26(7):1572-8. |
| [8] | Lee-Rueckert M, Vikstedt R, Metso J, et al. Absence of endogenous phospholipid transfer protein impairs ABCA1-dependent efflux of cholesterol from macrophage foam cells[J].J Lipid Res, 2006,47(8):1725-32. |
| [9] | Desrumaux C M, Mak P A, Boisvert W A, et al. Phospholipid transfer protein is present in human atherosclerotic lesions and is expressed by macrophages and foam cells[J].J Lipid Res,2003, 44(6):1453-61. |
| [10] | O'Brien K D, Vuletic S, McDonald T O, et al. Cell-associated and extracellular phospholipid transfer protein in human coronary atherosclerosis [J]. Circulation, 2003, 108(3):270-4. |
| [11] | Cavusoglu E, Marmur J D, Chhabra S, et al. Relation of baseline plasma phospholipid transfer protein (PLTP) activity to left ventricular systolic dysfunction in patients referred for coronary angiography [J]. Atherosclerosis, 2009, 207(1):261-5. |
| [12] | Yang X P, Yan D, Qiao C, et al. Increased atherosclerotic lesios in apoE mice with plasma phospholipid transfer protein overexpression[J].Arterioscler Thromb Vasc Biol, 2003, 23(9):1601-7. |
| [13] | van Haperen R, van Tol A, van Gent T, et al. Increased risk of atherosclerosis by elevated plasma levels of phospholipid transfer protein[J].J Biol Chem, 2002, 277(50):48938-43. |
| [15] | 刘连亮,吴晓琴,张 英.类黄酮化合物防治动脉粥样硬化的研究进展[J].天然产物研究与开发, 2012, 24(5):708-13. Liu L L,Wu X Q, Zhang Y. Research advances in mechanism of flavonoids against atherosclerosis[J].Nat Prod Res Dev,2012, 24(5):708-13. |
| [16] | 姜秀娟,王旭辉,李 奕,等.木贼总黄酮对ox-LDL损伤内皮细胞保护作用的形态学观察[J].时珍国医国药,2012, 23(3):637-8. Jiang X J,Wang X H, Li Y, et al. The protective effect of horsetail flavonoids on ox-LDL damage of endothelial cell[J]. Lishenzhen Med Mat Med Res, 2012, 23(3):637-8. |
| [17] | 王 磊,王宏涛,魏 聪,等.通心络联合阿托伐他汀、阿司匹林对ApoE-/-小鼠动脉粥样硬化病变的影响[J]. 中国药理学通报, 2014, 30(1):135-9. Wang L, Wang H T, Wei C, et al. Effects of Tongxinluo combined with atorvastatin and aspirin on atherosclerotic lesions in ApoE-/- mice[J].Chin Pharmacol Bull,2014, 30(1):135-9. |
| [18] | Hu T, Chouinard M, Cox A L, et al. Farnesoid X receptor agonist reduces serum asymmetric dimethylarginine levels through hepatic dimethylarginine dime-thylaminohydrolase-1 gene regulation[J].J Biol Chem, 2006, 281(52):39831-8. |
| [19] | Li Y T, Swales K E, Thomas G J, et al. Farnesoid x receptor ligands inhibit vascular smooth muscle cell inflammation and migration [J]. Arterioscler Thromb Vasc Biol, 2007, 27(12):2606-11. |
| [20] | Shih D M, KASt-Woelbern H R, Wong J. A role for FXR and human FGF-1-9 in the repression of paraoxonase-1 gene expression by bile acids [J].J Lipid Res, 2006, 47 (2):384-92. |
| [21] | Urizar N L, Dowhan D H, Moore D D. The farnesoid X-activated receptor mediates bile acid activation of phospholipid transfer protein gene expression [J].J Biol Chem, 2000, 275(50):39313-7. |
| [22] | Cai S Y,He H,Nguyen T,et al. Retinoic acid represses CYP7A1 expression in human hepatocytes and HepG-2 cells by FXR/RXR-dependent and independent mechanisms[J]. J Lipid Res, 2010, 51(8):2265-74. |




