


2. 南华大学药物药理研究所, 湖南 衡阳 421001;
3. 湘南学院, 湖南 郴州 423000;
4. 西安交通大学医学院实验动物中心, 陕西 西安 710061
2. Institute of Drug and Pharmacology, University of South China, Hengyang Hunan 421001, China;
3. Xiangnan University, Chenzhou Hunan 423000, China;
4. Xi'an Jiaotong University, Medical College, Xi'an 710061, China
弱氧化低密度脂蛋白(minimally modified low density lipoprotein,mmLDL)是氧化程度轻微的LDL,脂质部分被氧化,载脂蛋白B结构完整,可以损伤内皮细胞,增强单核细胞与内皮细胞黏附,促进oxLDL产生。mmLDL是动脉粥样硬化(atherosderosis,AS)的危险因子,AS是心脑血管病的重要病理基础,mmLDL引起AS的致病机制尚未研究清楚。AS是一种多因素共同参与的慢性炎症性疾病,内皮细胞损伤、平滑肌细胞迁移增殖在AS的发生和发展中有重要作用。心脑血管疾病与血管收缩功能异常息息有关,交感神经系统对血管的活动有重要的调节作用。交感神经兴奋释放去甲肾上腺素,主要通过兴奋血管平滑肌α1受体,引起血管收缩。受体是传递生物信息、介导生物效应关键因素。受体本身会因新陈代谢而动态变化,其数量、亲和力和效应会受生理、病理因素的影响而增多或减少。受体的调节是机体维持内环境稳定的重要因素。有文献报道[1, 2],在高血压大鼠和高血压患者血管平滑肌α肾上腺素受体的反应性增强。研究mmLDL对在体肠系膜动脉α受体的作用,对阐明mmLDL致病机制有重要意义。
1 材料与方法 1.1 主要试剂LDL,去甲肾上腺素(noradrenaline,NA)、5-羟色胺 (5-hydroxytryptamine,5-HT)、普萘洛尔(propranolol,Prop)、乙酰胆碱(acetylcholine,ACh)、哌唑嗪(prazosin)及育亨宾(yohimbine)均购于Sigma公司,试剂用超纯化水溶解,均用Krebs稀释,浓度以浴槽中最终药物的浓度表示。 α1受体抗体 (Proteintech Biotechnology,Inc of USA)、α2受体抗体 (American Research Products,Inc.),辣根过氧化物酶标记的山羊抗兔和山羊抗小鼠二抗 (Pierce Biotechnology,Inc of USA),GAPDH单克隆抗体(Proteintech Biotechnology,Inc of USA)。新鲜动物组织和细胞总RNA抽提试剂盒、通用逆转录工具包、SYBR Green试剂盒(Shanghai Novland Co.,Ltd.)。
1.2 仪器DMT 620M微小血管张力测定仪(Danish Myo Technology A/S,DMT,丹麦)、Powerlab生物信号采集分析系统(AD instruments Co,Australia)、Zeiss-2000系列生物显微镜(德国蔡司光电仪器有限公司)、显微手术解剖工具(World Precision Instruments,WPI,美国),电子天平(BP211D,Startorius公司)、微量移液器(Dragonmed,芬兰)、HH-2型电热恒温水浴锅(北京科伟永兴仪器有限公司),LG冰箱、优普纯水机(成都优普纯水设备有限公司),SW-CJ-2FD-超净无菌工作台(苏州安泰空气技术公司),美国Bio-RAD 电泳仪,MX3000P实时荧光定量PCR仪(Stratagene,U.S.),Image Gauge Ver. 4.0 (Fuji Photo Film Co.,Ltd,日本)。
1.3 实验动物与分组8~11 周龄SPF级的ICR小鼠,体质量20~24 g,♀♂各半,从西安交通大学医学院动物实验中心购买,动物使用许可证编号:SYXK (陕)2012-005。 实验组尾静脉注射mmLDL 1 mg·kg-1,第1次注射开始计时,每隔12 h重复1次,在处死动物的时间点不给药(比如 24 h 组给药时间为0、12 h),分别于24、48、72、96、120 h将小鼠颈部脱臼处死,浓度累加法加入NA,观察mmLDL对血管α受体介导的收缩功能的影响。考察mmLDL对血管α受体作用的量效关系时,设立mmLDL (0.5、1及1.5 mg·kg-1) 组。实验设对照组,分别为尾静脉注射生理盐水(normal saline,NS)组和LDL组[3]。
1.4 血管收缩功能检测小鼠脱臼处死,立即取出包含有肠系膜的组织,浸入预冷的Na+-Krebs 液 (含mmol·L-1:NaHCO3 15、NaCl 119、MgCl2 1.2、NaH2PO4 1.2、无水CaCl2 1.5、KCl 4.6和葡萄糖5.5) 中,显微镜下剥离血管周围组织,0.1% Triton X-100血管内灌注10 s,去除血管内皮,再用缓冲液冲洗10 s,20 μmol·L-1的5-HT预收缩,当乙酰胆碱(acetylcholine,ACh)引起的舒张率<10%,认为内皮已被去除。将处理好的血管切成1~2 mm长的血管环,在显微镜下穿入两根直径为40 μm大小的金属丝上,一根连接在可调负荷张力的微调装置上,另一根连接张力换能器,张力换能器与PowerLab系统相连,详细记录血管环的收缩曲线。将血管环放置于充满 Na+-Krebs液的37℃恒温浴槽中,为使氧饱和,持续通入含(95% O2+5% CO2)的混合气体,pH保持在7.4左右[4, 5, 6]。保持静息张力为1.5 mN,每隔20 min 更换1次Krebs液,平衡1.5 h。加 K+-Krebs 液 (含mmol·L-1: NaHCO3 15、NaH2PO4 1.2、 CaCl2 1.5、KCl 63.5、MgCl2 1.2、NaCl 60、和葡萄糖5.5) 以检测血管环的活性,Na+-Krebs 液冲洗血管环3次,重复上述步骤。两次K+-Krebs液引起的收缩幅度均大于1 mN并且两次收缩幅度差在10%以内,才可进行后续实验。用Prop(10-9 mol·L-1)于浴槽中孵育血管0.5 h阻断β受体,再浓度累加法加入NA(10-11~10-4 mol·L-1),考察α受体功能。先分别用Prop与不同浓度α1受体拮抗剂哌唑嗪(10-11~10-9 mol·L-1)或不同浓度α2受体拮抗剂育亨宾 (10-7~10-5 mol·L-1) 孵育血管0.5 h,再浓度累加法加入NA,分别考察α1和α2受体在NA引起的收缩量效曲线的作用。
1.5 RT-PCR总的RNA提取使用RNA抽提试剂盒,按照使用说明书提取。检测260 nm、280 nm吸光度,考察总RNA浓度和纯度。按说明书逆转录成cDNA。RT-PCR在MX3000P实时荧光定量PCR仪中进行,使用基因扩增的SYBR Green试剂盒,以cDNA为模版。设立对照组,除不加cDNA外,余平行操作。引物根据基因数据库应用引物表达-2软件设计,α1受体前引物:5′-ATCCTCTCGGTGGCCTGTCATC -3′;后引物:5′- AGATGGCAGAGAAGGGCA GCAC-3′ (115 bp)。α2受体前引物:5′- AGGTGACACTGACGCTGGTTTG -3′;后引物:5′- AAGAGGTTTTGGGGAGCTTTGAG-3′ (121 bp)。管家基因β-actin mRNA,在细胞内连续恒定表达,作为mRNA定量的参照。β-actin前引物:5′- AAGATCAAGATCATTGCTCCTCC -3′;后引物:5′- GACTCATCGTACTCCTGCTTGC-3′ (119 bp)。反应体系为25 μL,开始在95℃反应3 min,94℃反应12 s,62℃反应40 s,完成40个PCR 循环。反应结束后采用分离曲线分析法以确定PCR反应产物的特异性。mRNA定量分析采用PCR循环阈值(CT)比较法,以 β-actin 的 CT 值为内对照,计算α1受体、α2受体mRNA 相对表达量。
1.6 Western blot由于1只小鼠肠系膜动脉提取的蛋白不足以开展Werstern blot研究,因此,每个样本由3根小鼠肠系膜动脉组成,加入含有蛋白酶抑制剂的细胞提取变性缓冲液RIPA裂解液,匀浆。使用BCA 蛋白分析试剂盒蛋白定量。提取的蛋白用SDS-PAGE凝胶电泳进行分离并转移到PVDF膜上,5%脱脂牛奶(T-TBS缓冲液配置)封闭。一抗α1受体抗体(1 ∶ 1 000稀释),α2受体抗体(1 ∶ 1 000稀释)和GAPDH抗体(1 ∶ 1 000稀释),稀释液为含2%牛血清白蛋白的PBS;二抗为辣根过氧化物酶标记的山羊抗兔和山羊抗小鼠IgG(1 ∶ 5 000 稀释)。图像经Image Gauge Ver. 4.0 (Fuji Photo Film Co.,Ltd,日本),对光密度进行分析,并且均采用自身灰度值校正,以目的基因的条带灰度与管家基因的灰度比值表示蛋白的表达水平。
1.7 统计学分析数据以 表示,血管环的收缩反应以相对于63.5 mmol·L-1 钾引起收缩的百分数表达,反应特征表述为Emax(最大收缩百分率)和pEC50(产生一半最大收缩时所需要受体激动剂浓度的负对数)。采用Arunlakshana和Schild (1959)描述的方法[7]计算拮抗剂pA2值。统计分析及作图使用Prism 5.0 软件及SPSS 18.0。Students′t检验用来比较两组间的数据,单因素双向方差分析(ANOVA)或双因素ANOVA和Dunnett’s 后检验(GraphPad Prism)用来比较两组以上的数据。统计分析及作图使用Prism 5.0 软件。
表示,血管环的收缩反应以相对于63.5 mmol·L-1 钾引起收缩的百分数表达,反应特征表述为Emax(最大收缩百分率)和pEC50(产生一半最大收缩时所需要受体激动剂浓度的负对数)。采用Arunlakshana和Schild (1959)描述的方法[7]计算拮抗剂pA2值。统计分析及作图使用Prism 5.0 软件及SPSS 18.0。Students′t检验用来比较两组间的数据,单因素双向方差分析(ANOVA)或双因素ANOVA和Dunnett’s 后检验(GraphPad Prism)用来比较两组以上的数据。统计分析及作图使用Prism 5.0 软件。
将LDL(0.2 g·L-1) 置于不含EDTA,含1 μmol·L-1 FeSO4磷酸盐缓冲液 (phosphate buffered saline,PBS)中,在4℃透析96 h,再用0.25 mmol·L-1 EDTA终止氧化反应,生成mmLDL[8, 9, 10, 11]。将mmLDL浓缩成1 g·L-1。mmLDL的氧化程度采用硫代巴比妥酸反应物质法(thiobarbituric acid-reactive substances,TBARS)进行检测,结果显示,丙二醛样结构浓度为(10.47±1.13) μmol·g-1 LDL(mmLDL的TBARS检测值为5-20 μmol·g-1 LDL)。同时0.8%琼脂糖胶电泳结果显示,mmLDL的电泳迁移率是LDL的1.69倍(倍数值为1.50-2.00时为合格)。制备好的mmLDL存放于4℃,避光,两周内用完。
2.2 血管环对K+的收缩反应、动脉内皮去除及血清oxLDL水平测定使用mmLDL尾静脉注射,血管环对63.5 mmol·L-1 K+的收缩值在各组间的差异没有统计学意义[如:NS 组(2.58±0.47) mN,mmLDL组(2.87±0.49) mN,n=8,P>0.05]。用20 μmol·L-1的5-HT预收缩血管环,再用10 mmol·L-1 ACh舒张,舒张率低于预收缩值的5%,表明内皮去除完全。我们对血清中oxLDL的浓度水平进行了测定,结果表明,mmLDL组血清中oxLDL浓度水平较生理盐水组略有升高,但差异无显著性[mmLDL组(317±39) μg·L-1,NS 组(276 ± 31)μg·L-1,n=8,P>0.05]。
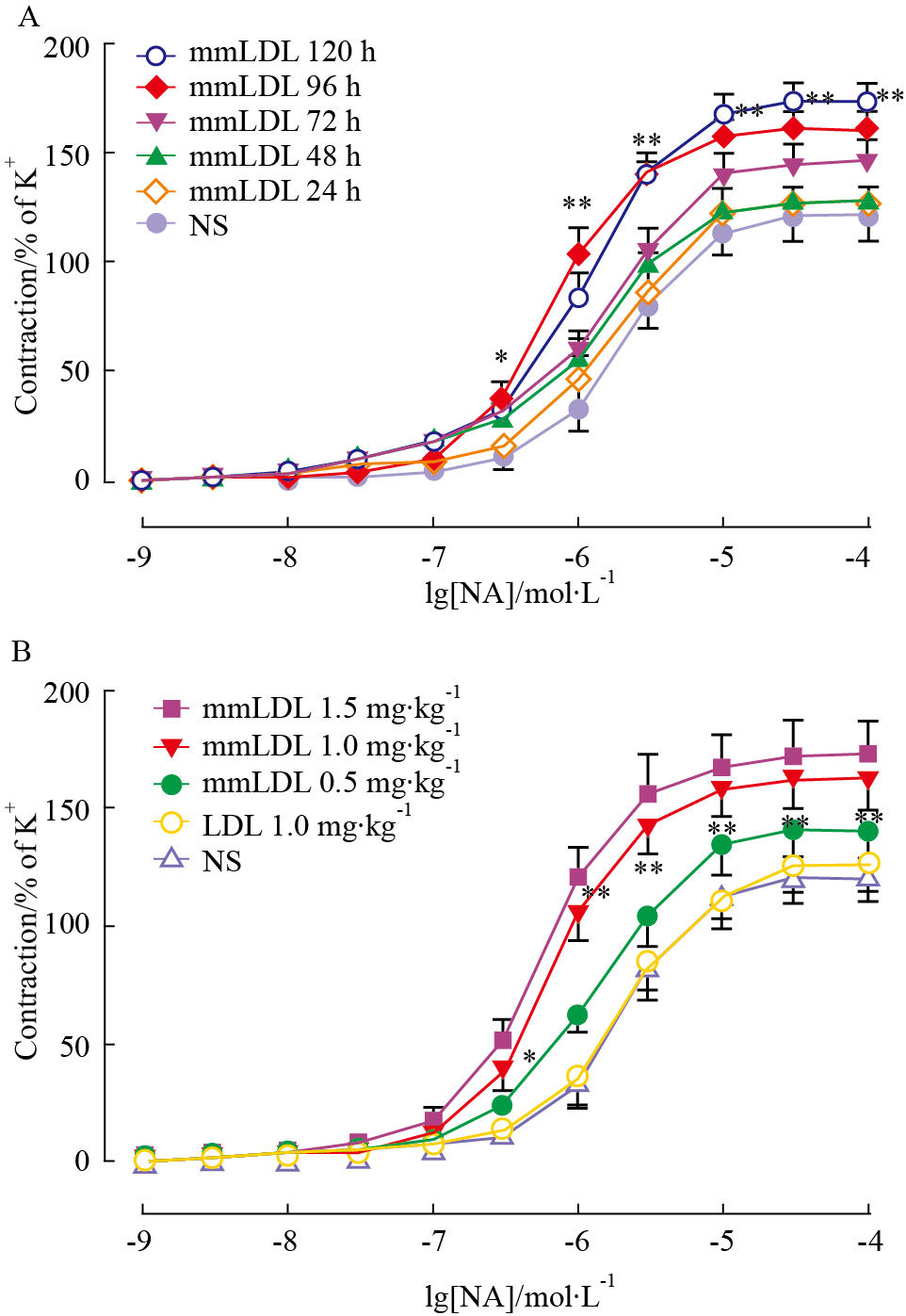
2.3 mmLDL 影响α受体介导收缩反应的时效和量效关系考察mmLDL影响肠系膜动脉α受体介导收缩反应的时间-效应关系,实验组按1 mg·kg-1的剂量尾静脉注射mmLDL。结果显示,与对照组相比,随着时间的延长,mmLDL提高α受体介导收缩反应的作用逐渐增强,表明mmLDL提高血管α受体收缩反应的作用呈时间依赖性。在24 h及48 h,α受体介导收缩量效曲线变化不明显;72 h时,α受体收缩效应出现上升,但与NS组比差异无统计学意义;96h时,α受体介导的收缩曲线明显上升伴随明显左移;120 h时,α受体收缩量效曲线与96 h比较略有升高(Fig1A)。考察mmLDL (剂量分别为0.5、1 及1.5 mg·kg-1) 96 h后对肠系膜动脉α受体收缩量效曲线的剂量-效应关系,结果显示,实验组中尾静脉注射mmLDL对α受体收缩作用的影响随着剂量增大而加强,表明mmLDL对血管α受体收缩作用的影响呈剂量依赖性。与对照组相比,0.5 mg·kg-1剂量组α受体介导的收缩量效曲线出现了升高 (P>0.05);1 mg·kg-1剂量组出现明显上升;1.5 mg·kg-1剂量组较1 mg·kg-1略有上升,差异无统计学意义(Fig1B)。故选择剂量为1 mg·kg-1、时间点为96 h来考察mmLDL对小鼠肠系膜动脉α受体收缩反应的影响,实验结果Emax值由NS组的(120.75±3.44) %上升为mmLDL组的(161.00±6.87) % (P<0.01),pEC50值由NS组的(5.65±0.05)上升为mmLDL组的(6.20±0.08) (P<0.01),表明量效曲线出现了明显增高伴明显左移。实验结果还显示尾静脉注射1 mg·kg-1 LDL,96 h时α受体介导的收缩量效曲线与NS组比基本上没有改变。
|
Fig 1
Effects of mmLDL on concentration-contractile curves induced by noradrenalin in a time-dependent(A) and concentration-dependent(B) manner ( , n=8)
NS:Normal saline.*P<0.05, **P<0.01 vs NS group. , n=8)
NS:Normal saline.*P<0.05, **P<0.01 vs NS group.
|
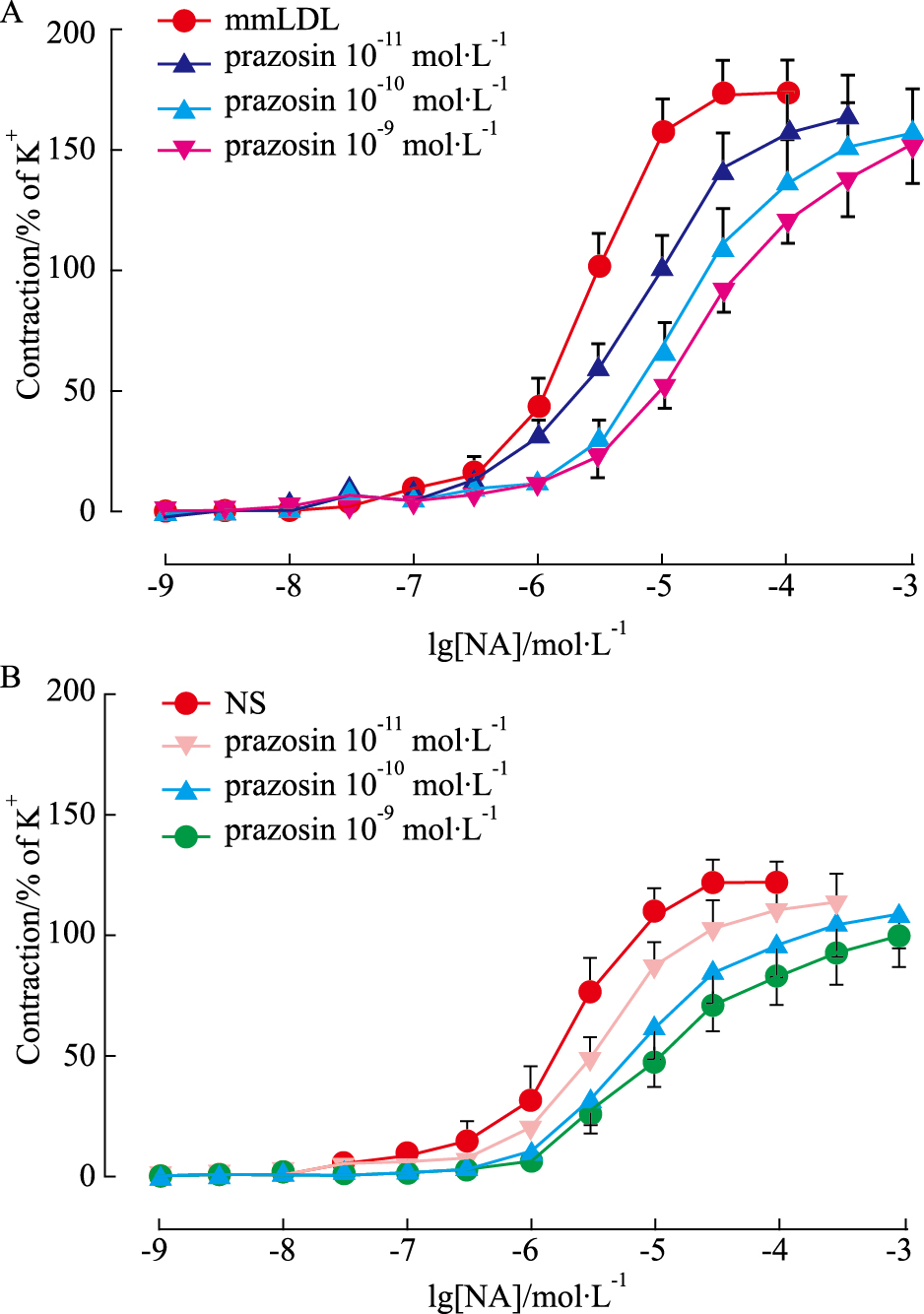
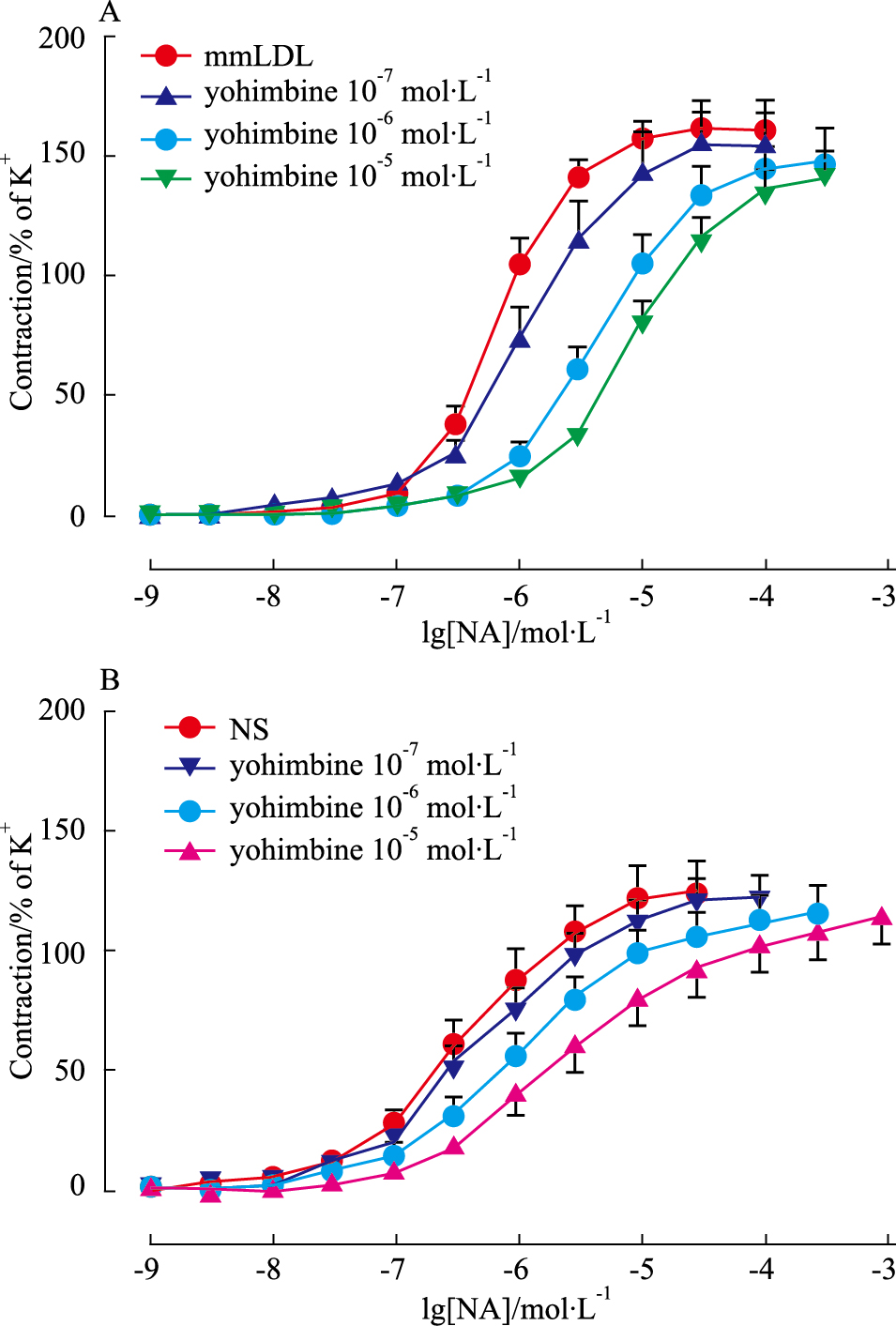
考察α受体亚型,使用选择性α1受体拮抗剂哌唑嗪(10-11~10-9 mol·L-1)使NA量效曲线平行右移,pA2值在mmLDL组和NS组分别为10.54±0.77和9.85±0.64(Fig2)。选择性α2受体拮抗剂育亨宾 (10-7~10-5 mol·L-1)使NA量效曲线平行右移,pA2值在mmLDL组和NS组分别为7.51±0.40和7.13±0.76(Fig3)。
|
Fig 2
Concentration-contraction curves of mmLDL (A) and NS (B) in mouse mesenteric arteries induced by noradrenalin ( , n=8)
In the presence of selective α1-adrenoceptor antagonist prazosin, the data of pA2 were 10.54±0.77 (A) and 9.85±0.4 (B), NS means normal saline. , n=8)
In the presence of selective α1-adrenoceptor antagonist prazosin, the data of pA2 were 10.54±0.77 (A) and 9.85±0.4 (B), NS means normal saline.
|
|
Fig 3
Concentration-contraction curves of mmLDL (A) and NS (B) in mouse mesenteric arteries induced by noradrenalin ( , n=8)
In the presence of selective α2-adrenoceptor antagonist yohimbine, the data of pA2 were 7.51±0.40 (A) and 7.13±0.76 (B). NS means normal saline. , n=8)
In the presence of selective α2-adrenoceptor antagonist yohimbine, the data of pA2 were 7.51±0.40 (A) and 7.13±0.76 (B). NS means normal saline.
|
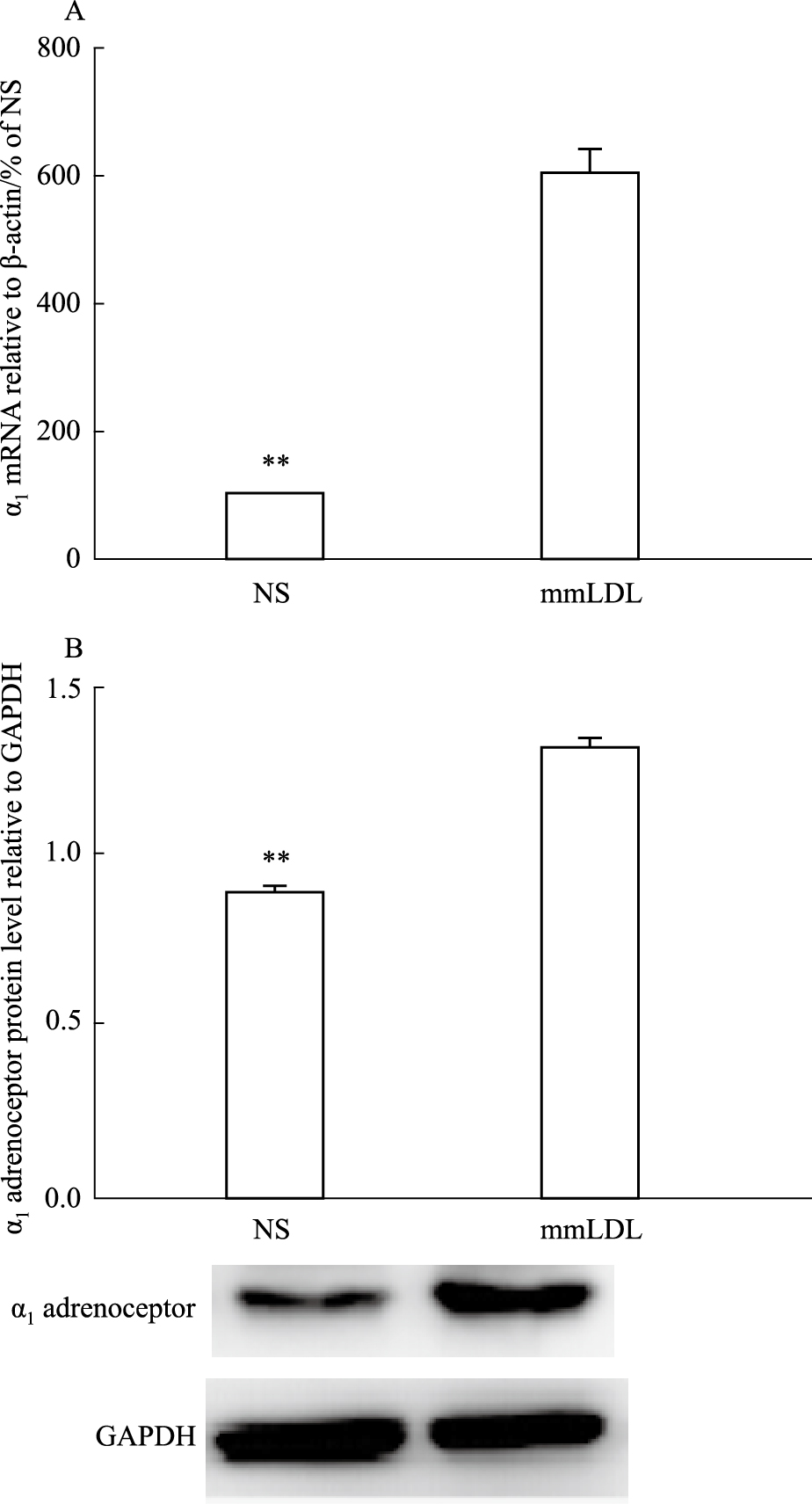
mmLDL引起α1受体表达增加。尾静脉注射mmLDL后,α1受体mRNA水平相对于NS组升高为 (603±38)% (P<0.01);α1受体蛋白水平由NS组的0.90±0.02升高为1.31±0.03 (P<0.01) (Fig4)。
|
Fig 4
Effect of mmLDL on expressions of α1 adrenoceptor in mouse mesenteric arteries( )
A: The expression of α1 adrenoceptor mRNA level is presented relative to β-actin and shown as percentage of NS group (n=6). B: The expression of α1 adrenoceptor protein level (n=3-4 samples), **P<0.01 vs mmLDL. NS means normal saline. )
A: The expression of α1 adrenoceptor mRNA level is presented relative to β-actin and shown as percentage of NS group (n=6). B: The expression of α1 adrenoceptor protein level (n=3-4 samples), **P<0.01 vs mmLDL. NS means normal saline.
|
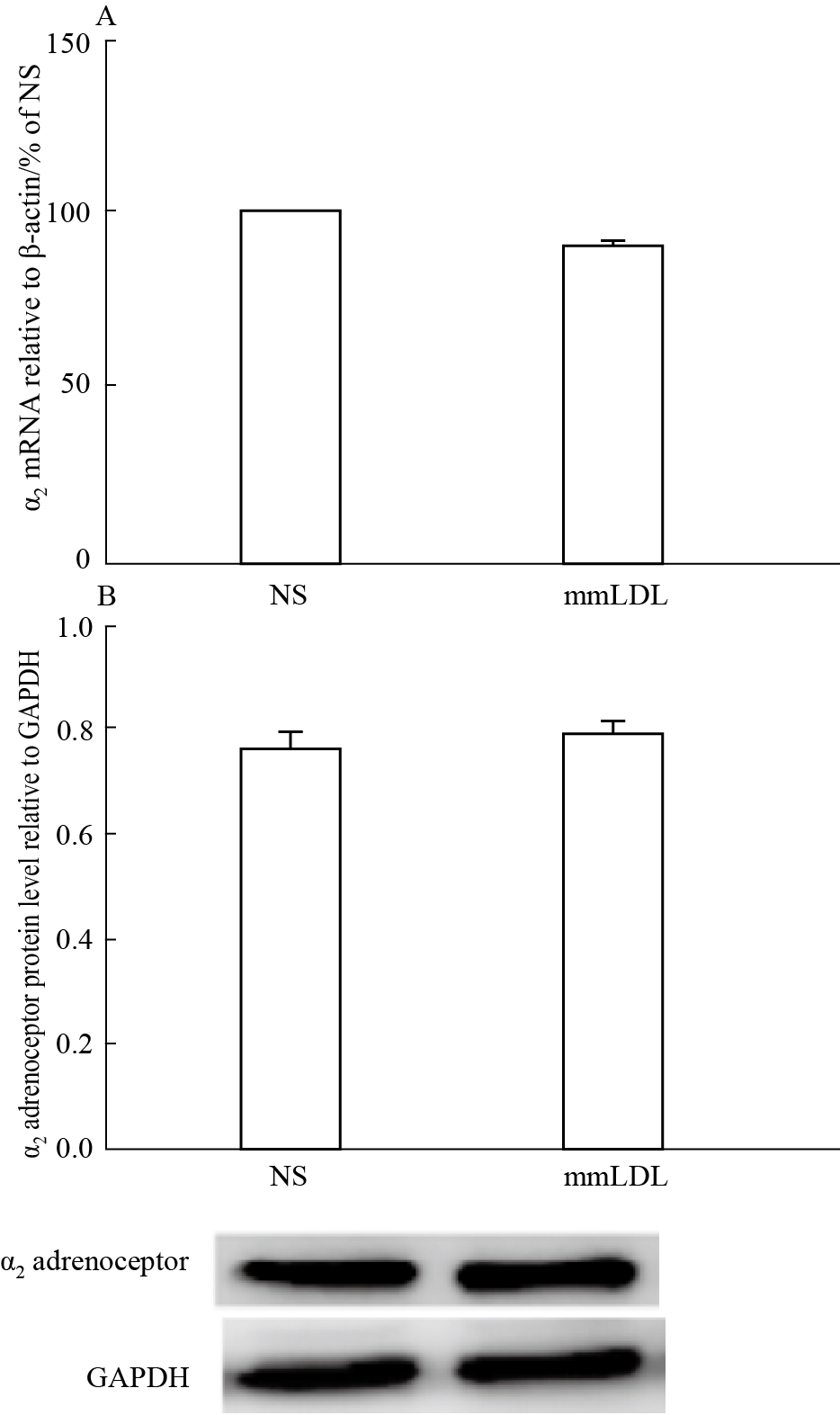
尾静脉注射mmLDL后,α2受体表达几乎没有变化。α2受体mRNA水平由NS组略降低为(89±3)% (P>0.05);α2受体蛋白水平由NS组的0.76±0.04略升高为0.78±0.02 (P>0.05)(Fig5)。
|
Fig 5
Effect of mmLDL on expressions of α2 adrenoceptor in mouse mesenteric arteries( )
A: The expression of α2 adrenoceptor mRNA level is presented relative to β-actin and shown as percentage of NS group (n=6). B: The expression of α2 protein level (n=3-4 samples). NS means normal saline. )
A: The expression of α2 adrenoceptor mRNA level is presented relative to β-actin and shown as percentage of NS group (n=6). B: The expression of α2 protein level (n=3-4 samples). NS means normal saline.
|
mmLDL是AS等心脑血管疾病的危险因子,AS是一种慢性炎症性疾病,早期表现为内皮损伤,血管平滑肌迁移增殖。近期课题组研究发现,mmLDL 可以上调离体大鼠冠状动脉和脑基底动脉内皮素B(endothelin B,ETB)受体,血管收缩性增强[12, 13];尾静脉注射mmLDL能损伤血管内皮细胞超微结构,损伤血管内皮依赖性舒张[3]。我们的研究结果显示,mmLDL损伤血管内皮细胞,此作用是AS的诱发因素;mmLDL上调血管平滑肌细胞ETB受体,增加了血管张力,表明mmLDL对血管平滑肌有影响。本研究结果进一步证实尾静脉注射mmLDL可以上调在体小鼠肠系膜动脉的α1受体,我们首次从整体动物实验证实了mmLDL可以对血管平滑肌受体产生作用。
心脑血管疾病的发生常常与血管的收缩、舒张功能失调有关。交感神经兴奋,末梢释放NA,NA激动血管平滑肌细胞膜上的α1受体,强烈收缩血管。血管平滑肌的收缩功能是影响血管阻力的重要因素,危险因子与机体相互作用,改变平滑肌的收缩功能,这种变化可能与疾病互为因果,成为疾病的基础。本研究观察mmLDL对在体血管平滑肌的影响,实验过程中去除血管内皮,因为血管内皮可以释放NO、ET-1等影响血管张力的血管活性物质,干扰血管环张力测定。使用β受体拮抗剂普萘洛尔孵育血管环,再浓度累加法加入NA,消除β受体对收缩曲线的干扰。预实验中我们测定血清中oxLDL的浓度水平显示,mmLDL组血清中oxLDL浓度水平较生理盐水组略有升高,但差异无显著性,表明血管平滑肌收缩功能增强与oxLDL无关。在实验中发现尾静脉注射mmLDL可以时间依赖性和剂量依赖性的增加α受体收缩反应性。给予剂量为1 mg·kg-1 mmLDL,72 h内α受体收缩反应性逐渐增强,但是与生理盐水组比差异无显著性,96 h后可以引起的NA收缩功能较生理盐水组明显增强,量效曲线明显左移,表明mmLDL增强NA引起血管的收缩功能。考察α1受体、α2受体在NA引起收缩反应的作用时,分别在mmLDL组和生理盐水组加入α1受体拮抗剂哌唑嗪和α2受体拮抗剂育亨宾。在mmLDL组和生理盐水组,α1受体拮抗剂哌唑嗪的pA2值分别为10.54±0.77和9.85±0.64,α2受体拮抗剂育亨宾的pA2值分别为7.51±0.40和7.13±0.76,与早期的文献报道一致[14]。mmLDL组我们观察到α1受体拮抗剂哌唑嗪在浓度为10-11 mol·L-1 时引起量效曲线的明显右移,而α2受体拮抗剂育亨宾产生类似作用需要的浓度为10-6 mol·L-1,是哌唑嗪浓度的100 000倍,表明mmLDL引起的NA收缩反应增强主要是由α1受体介导,这与文献报道高血压患者与α1受体表达上调有关相一致[15]。在RT-PCR和Western blot的实验结果中,我们发现mmLDL能明显增加的α1受体mRNA水平和蛋白表达,对α2受体的蛋白表达没有明显影响,这与功能实验结果一致。mmLDL引起α2受体mRNA水平略为降低,可能是由于mmLDL明显升高α1受体表达的一种反馈调节。结果显示mmLDL引起NA收缩量效曲线增强并伴随明显左移主要是由于增加了α1受体在血管平滑肌的表达,增加了α1受体介导的收缩功能。
综上所述,尾静脉注射mmLDL对肠系膜动脉平滑肌有作用,增加了动脉α1受体的mRNA水平、蛋白表达,并且增加小鼠肠系膜动脉α受体的收缩反应主要由α1受体介导。mmLDL可以通过上调α1受体增加血管平滑肌的收缩功能,此作用是否参与了血管平滑肌细胞迁移到内皮下还需要进一步研究。
(致谢:本研究功能学实验部分在西安交通大学医学院贺浪冲教授实验室完成,在此特别感谢。)
| [1] | 李洁,刘浩,曹永孝,等. 高血压大鼠和高血压患者血管平滑肌α肾上腺素受体的反应性增强作用[J].药学学报,2006,41(10):973-7. Li J,Liu H,Cao Y X,et al.Hypersensitization of α-adrenoreceptor of artery smooth muscle in hypertensive rats and hypertensive patients[J].Acta Pharmaceut Sin,2006,41(10):973-7. |
| [2] | Yan L,Tan X,Chen W,et al. Enhanced vasoconstriction to α1 adrenoceptor autoantibody in spontaneously hypertensive rats[J]. Sci China Life Sci,2014,57(7):681-9. |
| [3] | 陈根,秦旭平,李洁,等. 弱氧化低密度脂蛋白对小鼠肠系膜动脉内皮依赖性舒张功能的影响及机制[J].药学学报,2013,48(11):1657-64. Chen G,Qin X P,Li J,et al.Minimally modified LDL induced impairment of endothelium-dependent relaxation in mesenteric arteries of mice[J].Acta Pharmaceut Sin,2013,48(11):1657-64. |
| [4] | Cao Y X,He L C, Xu C B,et al. Enhanced transcription of contractile 5-hydroxytryptamine 2A receptors via extracellular signal-regulated kinase 1/2 after organ culture of rat mesenteric artery[J].Basic Clin Pharmacol Toxicol,2005,96(4):282-8. |
| [5] | Cao L, Zhang Y,Cao Y X, et al.Cigarette smoke upregulates rat coronary artery endothelin receptors in vivo[J].PloS One,2012,7(3):e33008. |
| [6] | Cao L,Cao Y X, Xu C B,et al.Altered endothelin receptor expression and affinity in spontaneously hypertensive rat cerebral and coronary arteries[J].PloS One, 2013,8(9):e73761. |
| [7] | Arunlakshana O, Schild H O. Some quantitative uses of drug antagonists[J]. Br J Pharmacol Chemother,1959.,14(1):48-58. |
| [8] | Itabe H,Mori M,Fujimoto Y,et al.Minimally modified LDL is an oxidized LDL enriched with oxidized phosphatidylcholines[J]. J Biochem,2003,134(3):459-65. |
| [9] | Chávez-Sánchezl L,Chávez-Rueda K, Legorreta-Haquet1 M V,et al. The activation of CD14,TLR4, and TLR2 by mmLDL induces IL-1b,IL-6,and IL-10 secretion in human monocytes and macrophages[J].Lipids Health Dis,2010,9:117. |
| [10] | Heusch G.Alpha-adrenergic coronary vasoconstriction in humans[J].J Am Coll Cardiol,2010,55(12):1278-9. |
| [11] | Li J, Cao L, Xu C B, et al.Minimally modified LDL upregulates endothelin type A receptors in rat coronary arterial smooth muscle cells[J].Mediators Inflamm,2013,2013:656570. |
| [12] | Li J,Cao Y X, Liu Y,et al.Minimally modified LDL upregulates endothelin type B receptors in rat basilar artery[J].Microvascul Res,2012,83(2):178-84. |
| [13] | Li J,Cao Y X,Yang Z Y,et al. Minimally modified LDL upregulates endothelin type B receptors in rat coronary artery via ERK1/2 MAPK and NF-kappaB pathways[J]. Biochim Biophys Acta,2012,1821(4):582-9. |
| [14] | Li J,Cao Y X,Liu H, et al.Enhanced G-protein coupled receptors-mediated contraction and reduced endothelium-dependent relaxation in hypertension[J].Eur J Pharmacol,2007,557(2-3):186-94. |
| [15] | 林杰, 李洁,曹永孝,等.高血压机体外周动脉G-蛋白偶联受体对缩血管物质的反应[J].中华高血压杂志,2007,15(7):587-94. Lin J,Li J,Cao Y X,et al.Enhanced G-protein coupled receptors mediated vasoconstrictor effect in human and rat arterioles[J].Chin J Hyper,2007,15(7):587-94. |

