


2. 军事医学科学院毒物药物研究所, 北京 100850
徐江平(1967-),男,博士,教授,博士生导师,研究方向:神经药理与新药临床前评价,通讯作者,Tel:020-61648236,E-mail:jpx@fimmu.com
 , XUE Rui2, YU Neng-jiang2, WANG Yu-lu2, HU Xiao-xu2, QIU Zhi-kun1, 2, ZHAO Nan2, LI Yun-feng2, XU Jiang-ping1
, XUE Rui2, YU Neng-jiang2, WANG Yu-lu2, HU Xiao-xu2, QIU Zhi-kun1, 2, ZHAO Nan2, LI Yun-feng2, XU Jiang-ping1
 , ZHANG You-zhi2
, ZHANG You-zhi2

2. Institute of Pharmacology and Toxicology, Academy of Military Medical Sciences, Beijing 100850, China
抑郁症(depression)以明显而持久的心境低落为主要特征,是情感性精神障碍(mood disorders)的主要类型,因其逐年升高的患病率和死亡率,已经成为一种影响人类健康的重大精神类疾病。下丘脑-垂体-肾上腺轴(hypothalamic-pituitary-adrenocortical axis,HPA轴)功能亢进是较为公认的抑郁症的发病机制之一,长期应激能够导致糖皮质激素(glucocorticoids,GC)水平升高,中枢神经系统糖皮质激素受体受损、密度下调,HPA轴呈脱抑制状态,皮质酮(CORT)、促肾上腺皮质激素(ACTH)等应激激素水平持续性升高,进而造成对海马等脑区的结构功能损伤,该病理生理现象是导致抑郁的机制之一[1, 2, 3]。
小补心汤(代号XBXT)出自敦煌莫高窟遗书、陶弘景所著的《辅行诀脏腑用药法要》,该方由代赭石、旋复花、竹叶和淡豆豉4味中药组成。小补心汤原用于气血不足导致心包络虚,中医理论认为心包虚损不足则其人善悲,原方主治症亦有“时悲泣”的七情郁证表现。本课题组前期发现小补心汤及其总黄酮提取物(代号XBXT-2 黄酮含量>70%)在多种抑郁模型上具有明显的抗抑郁行为学效应[4, 5, 6, 7]。在此基础上,本研究采用小鼠获得性无助模型,进一步评价XBXT-2的抗抑郁活性,并检测其对模型小鼠血清CORT水平、ACTH水平、海马糖皮质激素受体(glu-cocorticoids receptor,GR)蛋白和BDNF表达的影响,探讨XBXT-2对应激状态下HPA轴功能的调节作用及对海马的保护作用。
1 材料与方法 1.1 实验动物ICR小鼠,♂,体质量20~22 g,购自北京斯贝福实验动物中心,动物合格证号:SCXK(京)2011-0004。小鼠自由摄食饮水,实验前适应性饲养7 d。
1.2 药品与主要试剂XBXT-2由军事医学科学院毒物药物研究所植物化学研究室提供。中药饮片均购自北京同仁堂药店,代赭石∶旋覆花∶竹叶∶淡豆豉以2 ∶ 2 ∶ 1 ∶ 1(W/W,6 kg)混合后,用70%乙醇回流,石油醚萃取,并经AB-8大孔树脂柱进行吸附,70%乙醇洗脱、浓缩、冷冻干燥后得到总黄酮部位(XBXT-2)。 芦丁为标准,比色法测定XBXT-2中的黄酮含量为76.0%[8] ;盐酸度洛西汀(duloxetine hydrochlorate,Dlx)由浙江海翔药业股份有限公司惠赠,批号:30091080701,药品均溶于蒸馏水;皮质酮酶联免疫分析试剂盒,美国Enzo公司;ACTH酶联免疫分析试剂盒,美国Phoenix Pharmaceuticals公司;兔抗小鼠GR多克隆抗体,美国Sant Cruz公司;兔抗人脑源性神经营养因子(human brain-derived neurotrophic factor,BDNF)多抗,美国Sigma 公司;鼠抗人β-肌动蛋白(β-actin)单克隆抗体、辣根过氧化物酶(horseradish peroxidase,HRP)标记的山羊抗兔IgG、HRP标记的山羊抗鼠IgG,购于北京中杉金桥生物技术有限公司;其他化学试剂均为国产分析纯。
1.3 主要仪器微机程序控制小鼠穿梭箱反应仪(美国Med Associate公司);电子分析天平(德国 Sartrious 公司);超声细胞和组织破碎仪(美国Sonic公司);Victor3多功能酶标仪(美国 Perkin Elmer公司);蛋白电泳装置(美国Bio-Rad公司);HIMAC CR 20B2型低温高速离心机(日本HITACHI公司);荧光/化学发光成像分析系统 (美国Sonic公司)。
1.4 小鼠获得性无助抑郁模型的制备[9, 10] 1.4.1 获得性无助模型诱导期穿梭箱中间门关闭,将小鼠放入箱内,左右小室各1只,不可逃避性电击组(inescapable shock,IS)动物连续4 d、每日给予360次不可逃避的足底电击(电流强度0.3mA,每次持续15s,间歇期伴随机化,总时程1 h),d 5给予电击180次,程序与前4 d相同,正常对照组[无不可逃避性电击(no inescapable shock,NIS)]动物放入实验箱内同样的时间,但不给予足底电击。
d 5电击诱导训练结束后进行动物筛选分组测试。连续进行10个周期的测试程序,每个运行周期的时间为30 s,依次为3 s条件刺激(灯光)、3 s条件刺激+非条件刺激(电击0.3mA)、24 s间歇(不给任何刺激)。当小鼠在仅有灯光的条件刺激期穿梭到箱的另一侧以免遭电击时,记为回避反应(avoid response);当小鼠在同时具有灯光和电击刺激的情况下穿梭到箱的另一侧以躲避电击时,则记为逃避反应(escape response)。观测指标为逃避失败(escape failure,EF)次数=[10-(回避次数+逃避次数)]。根据动物EF得分筛选模型动物(筛选标准为EF次数≥6),按EF次数随机均衡分为各IS组。分组后当天给药1次。
1.4.2 条件性回避反应测试期d 6~9进行条件性回避反应测试,每天测试1次,在灌胃给药1 h后进行,测试连续进行30个周期,每个运行周期依次为5 s条件刺激(灯光),条件刺激+非条件刺激(电击0.3 mA),当小鼠穿梭到箱的另一侧以躲避电击时,电击和灯光刺激同时结束,否则光电刺激持续25 s结束。前5个周期,中间门持续开放,后25个周期,中间门在电击开始2 s后自动开启,在电击结束后关闭。测试指标为逃避失败(escape failure,EF)次数和逃避潜伏期(escape latency,EL)。
1.5 实验分组及给药动物购入后首先按体重均衡随机分为正常对照组(NIS)和不可逃避电击(IS)组,经过穿梭箱回避程序筛选后,将不可逃避电击组动物按筛选测试得分均分为模型组(IS+Vehicle)、度洛西汀组(IS+Dlx 20 mg·kg-1)和XBXT-2(IS+XBXT-2 25,50mg·kg-1)4组。采用灌胃给药(ig),d 5~9,每天给药1次,给药体积10 ml·kg-1,每组12只动物。
1.6 ELISA 法检测血清CORT和ACTH水平行为测试结束后,小鼠断头取血,血样静置1 h后离心(3 000 r·min-1,30 min),取上清并分装,于-80 ℃冰箱保存。采用 ELISA 法,按照试剂盒说明流程检测血清CORT和ACTH水平。
1.7 Western blot法检测海马GR和BDNF的表达水平取小鼠双侧海马,提取总蛋白,BCA法测定蛋白浓度。加入2×上样缓冲液,沸水浴变性5 min,-80℃冰箱保存备用。10%SDS-聚丙烯酰胺凝胶电泳分离出目标蛋白后,将凝胶湿法电转印至硝酸纤维素膜(NC膜)上,取出NC膜,浸于含5%脱脂奶粉的Tris缓冲液(Tris buffered saline,TBS)中室温轻摇封闭2 h,用含0.05% 吐温-20的TBS(TBS-T)缓冲液漂洗干净,浸入含5%BSA(牛血清白蛋白)的TBS-T稀释的一抗(GR 1 ∶ 1 000,β-actin 1 ∶ 1 000),4℃孵育过夜,用TBS-T漂洗NC膜3次,每次室温轻摇10 min,在TBS-T稀释的辣根过氧化物酶标记的二抗(山羊抗兔IgG 1 ∶ 3 000; 山羊抗鼠IgG 1 ∶ 3 000)中室温孵育1 h,二抗杂交后的NC膜在TBS-T中漂洗2次,TBS中漂洗1次,每次室温轻摇10 min,凝胶成像仪显影,采用GR、BDNF分别与β-actin的积分吸光度比值表示蛋白的相对表达量。
1.8 统计学分析采用GrphPadprism 5.0统计软件,两组间比较采用t检验,多组间比较采用单因素方差分析 (one-way ANOVA,post hoc test 选用Dunnett’t检验)。
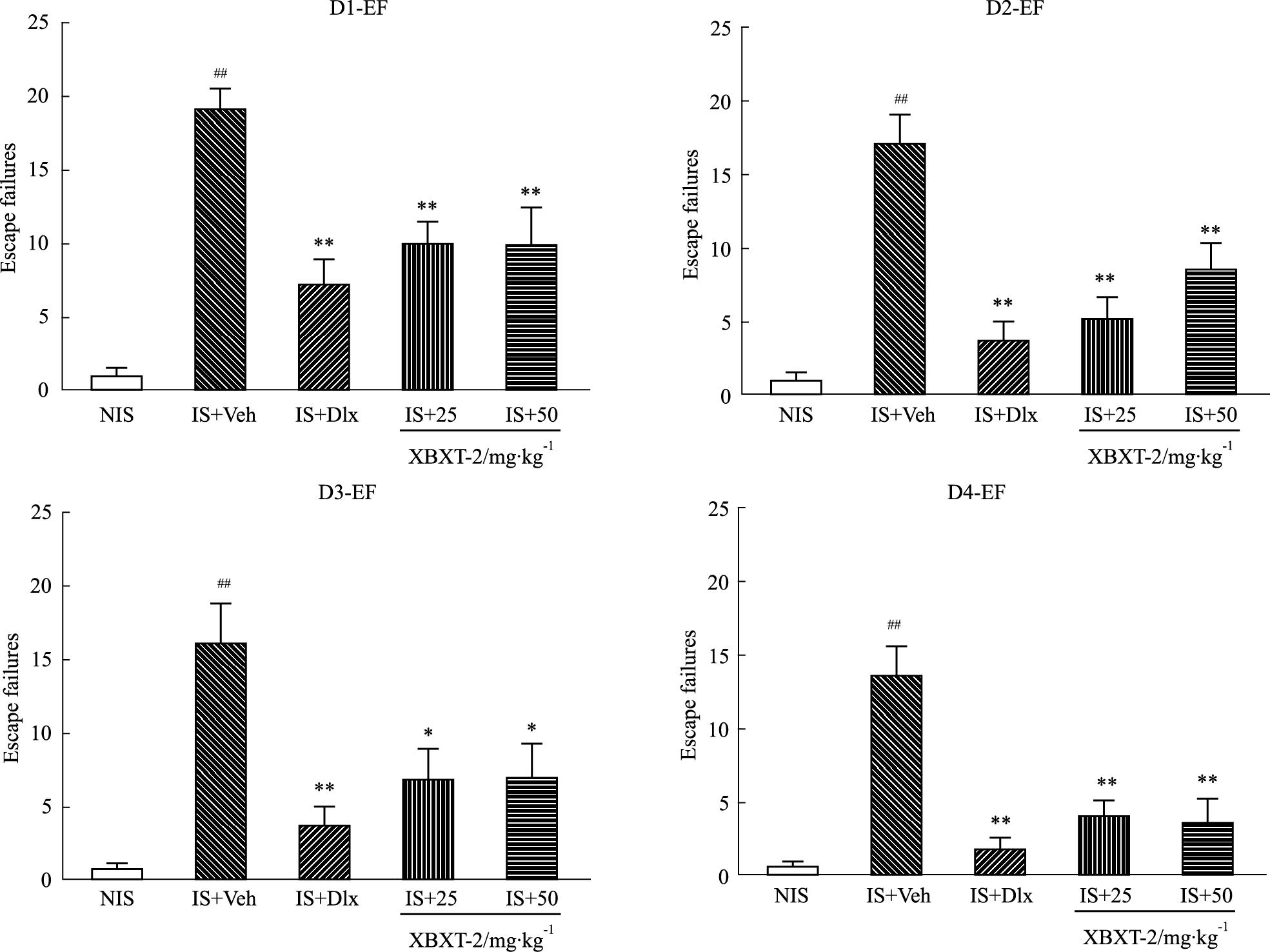
2 结果 2.1 XBXT-2对无助小鼠逃避失败次数的影响与NIS组比较,模型组小鼠在IS诱导后测试1~4 d逃避失败次数明显增加(P<0.01)。与模型组比较,XBXT-2 25mg·kg-1在测试d 1~4均可明显减少无助小鼠的逃避失败次数(分别P<0.01,P<0.01,P<0.05,P<0.01),XBXT-2 50 mg·kg-1同样在测试d 1~4可明显减少逃避失败次数(分别P<0.01,P<0.01,P<0.05,P<0.01),阳性药度洛西汀在测试d 1~4均明显降低逃避失败次数(P<0.01),如Fig1所示。
|
Fig 1
Effect of XBXT-2 on escape failures in mouse learned helplessness model( , n=12)
NIS: Non inescapable shock; IS: Inescapable shock; Veh: Vehicle; Dlx: Dulxetine. ##P<0.01 vs NIS; *P<0.05, **P<0.01 vs IS+Veh. , n=12)
NIS: Non inescapable shock; IS: Inescapable shock; Veh: Vehicle; Dlx: Dulxetine. ##P<0.01 vs NIS; *P<0.05, **P<0.01 vs IS+Veh.
|
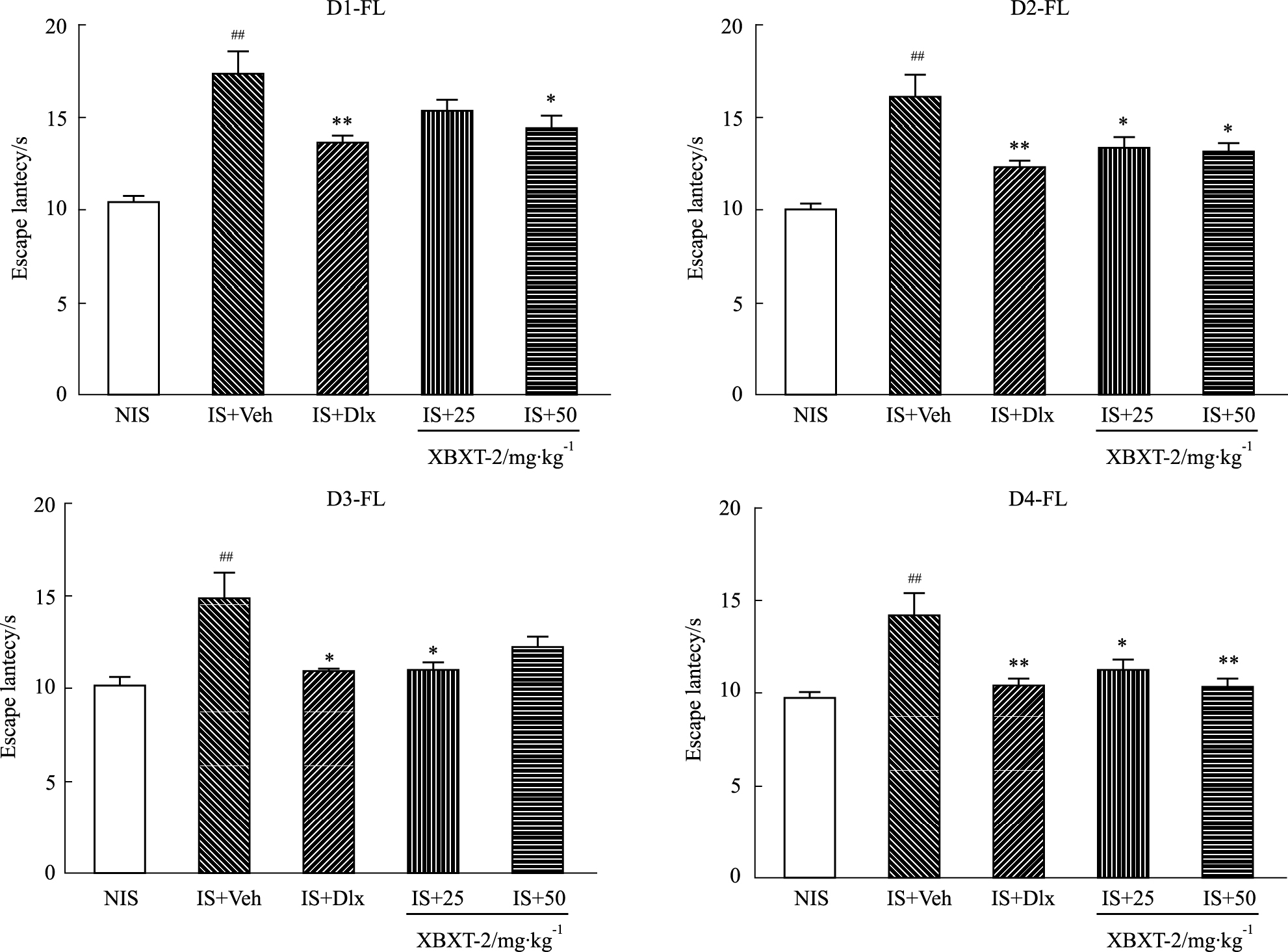
与NIS组比较,模型组小鼠在IS诱导后测试1~4 d逃避失败潜伏期明显延长(P<0.01)。XBXT-2 25 mg·kg-1从d 2开始明显缩短无助小鼠逃避潜伏期(P<0.05),XBXT-2 50 mg·kg-1在d 1、d 2和d 4可明显缩短逃避潜伏期P<0.05,P<0.05,P<0.01),d 3有缩短逃避潜伏期的趋势,但没有统计学意义,阳性药度洛西汀从d 1就表现出明显缩短逃避潜伏期的作用(P<0.01),如Fig2所示。
|
Fig 2
Effect of XBXT-2 on failure lantencys in mouse learned helplessness mode( ,n=12)
NIS: Non inescapable shock; IS: Inescapable shock; Veh: Vehicle; Dlx: Dulxetine. ##P<0.01 vs NIS; *P<0.05, **P<0.01 vs IS+Veh. ,n=12)
NIS: Non inescapable shock; IS: Inescapable shock; Veh: Vehicle; Dlx: Dulxetine. ##P<0.01 vs NIS; *P<0.05, **P<0.01 vs IS+Veh.
|
与NIS组比较,模型组小鼠血清皮质酮水平明显升高(P<0.01)。与模型组比较,XBXT-2 25、50 mg·kg-1亚慢性给药在减少模型小鼠逃避失败次数的 同时明显降低皮质酮水平(P<0.05)。阳性药度洛西汀也明显降低了血清皮质酮的水平(P<0.01),如Fig3所示。

|
Fig 3
Effect of XBXT-2 on serum corticosterone level in mouse learned helplessness model( ,n=4~5)
Serum corticosterone concentration was detected using a commercial ELISA kit. NIS: Non inescapable shock; IS: Inescapable shock; Veh: Vehicle; Dlx: Dulxetine. ##P<0.01 vs NIS; *P<0.05, **P<0.01 vs IS+Veh. ,n=4~5)
Serum corticosterone concentration was detected using a commercial ELISA kit. NIS: Non inescapable shock; IS: Inescapable shock; Veh: Vehicle; Dlx: Dulxetine. ##P<0.01 vs NIS; *P<0.05, **P<0.01 vs IS+Veh.
|
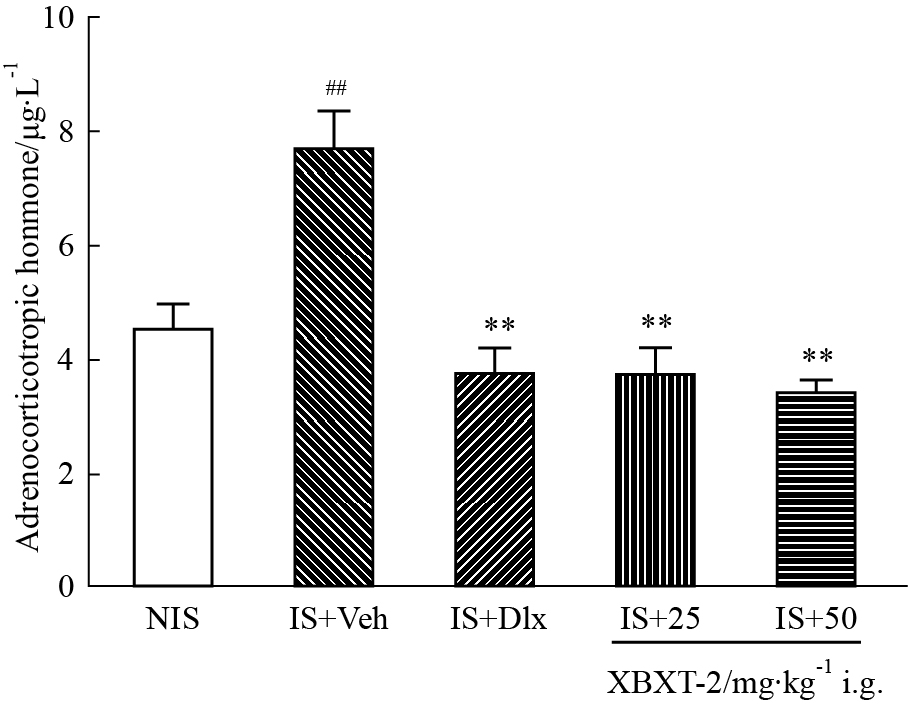
与NIS组比较,模型组小鼠血清皮质酮水平明显升高(P<0.01)。与模型组比较,XBXT-2(25、50 mg·kg-1)亚慢性给药均能分别明显降低ACTH水平(P<0.01,P<0.01)。阳性药度洛西汀也明显降低了血清皮质酮的水平(P<0.01),如Fig4所示。
|
Fig 4
Effect of XBXT-2 on serum ACTH level in mouse learned helplessness model( , n=6)
Serum ACTH concentration was detected using a commercial ELISA kit. NIS: Non inescapable shock; IS: Inescapable shock; Veh: Vehicle; Dlx: Dulxetine. ##P<0.01 vs NIS; **P<0.01 vs IS+Veh. , n=6)
Serum ACTH concentration was detected using a commercial ELISA kit. NIS: Non inescapable shock; IS: Inescapable shock; Veh: Vehicle; Dlx: Dulxetine. ##P<0.01 vs NIS; **P<0.01 vs IS+Veh.
|
糖皮质激素受体GR主要分为α、β两个亚型,与NIS组比较,无助模型组小鼠海马总的GR表达水平明显降低(P<0.01),XBXT-2 25 mg·kg-1(P<0.05)和50 mg·kg-1(P<0.01)慢性给药均可明显增加GR的表达量,阳性药度洛西汀也明显增加了GR的表达量(P<0.01),如Fig5所示。

|
Fig 5
Effect of XBXT-2 on hippocampal GRs expression in mouse learned helplessness model( , n=3)
1: NIS; 2: IS+Veh; 3: IS+Dlx (20 mg·kg-1); 4: IS+XBXT-2 (25 mg·kg-1); 5: IS+XBXT-2 (50 mg·kg-1). ##P<0.01 vs NIS; *P<0.05,**P<0.01 vs IS+Veh. , n=3)
1: NIS; 2: IS+Veh; 3: IS+Dlx (20 mg·kg-1); 4: IS+XBXT-2 (25 mg·kg-1); 5: IS+XBXT-2 (50 mg·kg-1). ##P<0.01 vs NIS; *P<0.05,**P<0.01 vs IS+Veh.
|
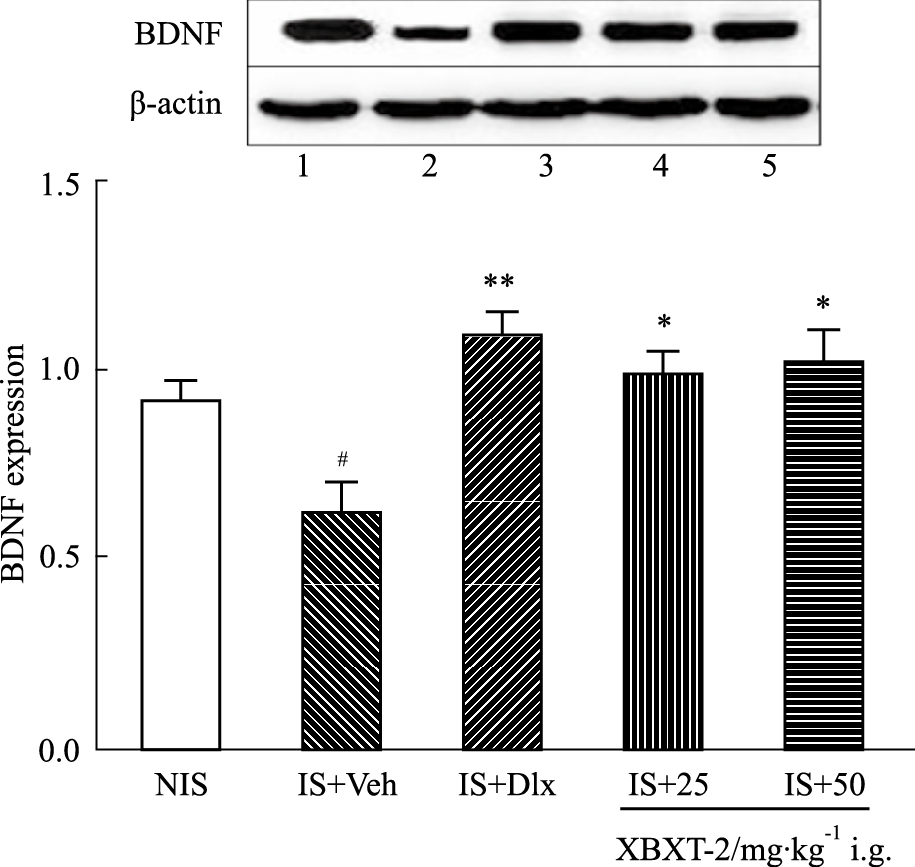
与NIS组比较,无助模型组小鼠海马BDNF表达水平明显降低(P<0.05),XBXT-2 25、50 mg·kg-1(P<0.05)慢性给药均可明显增加BDNF的表达量,阳性药度洛西汀具有相似的作用(P<0.01),如Fig6所示。
|
Fig 6
Effect of XBXT-2 on hippocampal BDNF expression in mouse learned helplessness model( , n=3)
1: NIS; 2: IS+Veh; 3: IS+Dlx (20 mg·kg-1); 4: IS+XBXT-2 (25 mg·kg-1); 5: IS+XBXT-2 (50 mg·kg-1). #P<0.05 vs NIS;*P<0.05, **P<0.01 vs IS+Veh. , n=3)
1: NIS; 2: IS+Veh; 3: IS+Dlx (20 mg·kg-1); 4: IS+XBXT-2 (25 mg·kg-1); 5: IS+XBXT-2 (50 mg·kg-1). #P<0.05 vs NIS;*P<0.05, **P<0.01 vs IS+Veh.
|
本课题组前期研究发现,XBXT-2在大、小鼠强迫游泳试验、小鼠悬尾试验和大鼠慢性应激模型等多个抑郁模型中具有明确的抗抑郁作用;并且发现XBXT-2对中枢5-HT神经系统功能具有明显的增强作用,能够提高慢性应激模型小鼠的脑组织5-HT含量[4, 5, 11]。
“获得性无助”是动物在接受无法逃避的厌恶性刺激后表现出的逃避能力缺失的一种行为现象,这种行为现象与临床抑郁症患者的症状表现具有相似性。有研究表明,啮齿类动物在经历不可逃避的应激刺激(如电击)后,会出现操作行为缺失,如逃避(escape)行为障碍、自发活动减少等,并且可伴有同临床抑郁症病人相似的生理生化和激素水平等改变[12]。本研究选用小鼠获得性无助模型评价XBXT-2的抗抑郁行为效应。采用连续5 d给予不可逃避地足底电击诱导小鼠获得性无助模型,行为检测结果表明,模型组小鼠在测试d 1~d 4均表现出逃避潜伏期和逃避失败次数的明显增加,提示造模成功;XBXT-2(25、50 mg·kg-1)可以明显逆转动物逃避潜伏期延长和逃避失败次数增加的无助样行为,阳性药度洛西汀(20 mg·kg-1)具有相似的作用。
HPA轴功能亢进已经成为抑郁症发病的神经内分泌机制研究中较为公认的改变[2]。临床研究表明,抑郁症患者的唾液、血浆及尿液等代谢产物中的CORT明显升高,BDNF表达下降,海马体积缩小[13]。机体长期处于应激状态时,持续升高的糖皮质激素会损伤海马(BDNF的表达下降),严重时甚至会导致海马神经元萎缩、凋亡及神经再生减少等一系列的可塑性损伤,使HPA轴的负反馈调节作用不能正常发挥,进而造成HPA轴功能亢进,ACTH分泌代偿性增加,海马GR表达下调,升高的GC会对HPA轴负反馈作用减弱,使其功能更为亢进,从而形成恶性循环[14, 15]。并且有研究表明,皮质酮损伤与5-HT能神经传导活性低下密切相关,皮质酮可以通过海马的盐皮质激素受体(mineralocorlicoid reccptos,MR)及GR调节着缝核-海马系统5-HT神经元活性,长期应激能持续升高血中CORT水平,可以引起5-HT传导系统功能受损[16]。本研究中,XBXT-2(25、50 mg·kg-1)亚慢性给药能明显逆转获得性无助模型组小鼠血清CORT和ACTH的增加,以及海马GR和BDNF表达的减少。本结果提示,XBXT-2能够抑制应激状态下HPA轴功能的过度亢进及对海马的损伤。
结合前期研究结果,我们认为XBXT-2亚慢性或慢性给药在多种抑郁模型中具有明确的抗抑郁作用,其可能作用机制与抑制应激状态下HPA轴功能亢进有关,但关于XBXT-2抗抑郁作用精细机制仍有待进一步深入研究。
(致谢:本研究在军事医学科学院毒物药物研究所新药评定研究室张有志研究员课题组完成,研究工作得到该研究室诸多同仁的帮助,在此一并表示感谢!)
| [1] | Pariante C M, Lightman S L. The HPA axis in major depression:classical theories and new developments[J]. Trends Neurosci, 2008, 31(9):464-8. |
| [2] | 柴 丽,赵 博.抑郁症与HPA轴关系及中药干预的研究进展[J].中国实验方剂学杂志, 2011, 17(12):268-71. Chai L, Zhang B. Relationship between depression and HPA axis and intervention by traditional chinese medicine[J]. Chin J Exp Tradit Med Formul, 2011, 17(12):268-71. |
| [3] | 陈 姣,楚世峰,陈乃宏. 糖皮质激素与抑郁发病相关机制研究进展[J].中国药理学通报, 2013, 29(11):1493-5. Chen J, Chu S F, Chen N H. Research progress in glucocorticoid and pathophysiology of depression[J]. Chin Pharmacol Bull, 2013, 29(11):1493-5. |
| [4] | Zhang Y Z, Li Y F, Yu N J, et al. Antidepressant-like effects of the ethanolic extract of XiaobuxinTang, a traditional Chinese herbal prescription in animal models of depression[J]. Chin Med, 2007, 120(20):1792-6. |
| [5] | Zhang Y Z, Yu N J, Yuan L, et al. Antidepressant effect of total flavonoids extracted from Xiaobuxin-Tang in forced swimming tests and learned helplessness in rats and mice[J]. Chin J Pharmacol Toxicol, 2008, 22(1):1-8. |
| [6] | An L, Zhang Y Z, Yu N J, et al. The total flavonoids extracted from Xiaobuxin-Tang up-regulate the decreased hippocampal neurogenesis and neurotrophic molecules expression in chronically stressed rats[J]. Prog Neuropsychopharmacol Biol Psychiatry, 2008, 32(6):1484-90. |
| [7] | An L, Zhang Y Z, Yu N J, et al. Role of serotonin in the antidepressant-like effect of a flavonoid extract of Xiaobuxin-Tang[J]. Pharmacol Biochem Behav, 2008, 89(4):572-80. |
| [8] | Xu G, Zhang H, Hu J. Leaching method of flavone from Bamboo leaves[J]. Chin J Anal Chem, 2000, 28(7):857-9. |
| [9] | Anisman H, Merali Z. Rodent models of depression:Learned helplessness induced in mice[J]. Curr Protoc Neurosci, 2001, 8:unit 8.10C.Chapter. |
| [10] | Bougarel L, Guitton J, Zimmer L, et al. Behaviour of a genetic mouse model of depression in the learned helplessness paradigm[J]. Psychopharmacology (Berl), 2011, 215(3):595-605. |
| [11] | 安 磊,田 燕,李 静,等. 小补心汤总黄酮对慢性应激小鼠脑内单胺递质水平的影响[J]. 大连医科大学学报, 2011, 33(3):208-11. An L, Tian Y, Li J, et al. Effect of the total flavonoids extracted from Xiaobuxin-Tang on monoamine neurotransmitter in chronically stressed mice[J]. J Dalian Med Univ, 2011, 33(3):208-11. |
| [12] | Willner P. Validation criteria for animal models of human mental disorders:learned helplessness as a paradigm case[J]. Prog Neuro Psycho Pharmaeol Biol Psyehiatry, 1986, 10(6):677-90. |
| [13] | 陈 嘉, 董文心. 抗抑郁药物对海马神经元保护作用的研究进展[J].中国新药杂志, 2008,17(6):441-5. Chen J, Dong W X. Research advance of protection of antidepressants on hippocam pus[J]. Chin J New Drugs, 2008,17(6):441-5. |
| [14] | Lueassen P J, Muller M B, Holsboer F, et al. Hippoeampal apoptosis in maor depression is a minor event and absent from subareas at risk for glucoeortieoid overexposure[J]. Am J Pathol, 2001, 158(2):453-68. |
| [15] | 董瑞婕, 吴爱勤. 糖皮质激素受体在抑郁症病理机制中的地位[J]. 上海精神医学, 2008, 20(4):243-4. Dong R J, Wu A Q. Role of glucocorticoid receptors in the pathogenesis of depression[J]. Shanghai Arch Psychiatry, 2008,20(4):243-4. |
| [16] | Takeda H, Tsuii M, Matsumiya T. Formation mechanisms of stress adaptation:role of functional coupling of glucocortieoids and brain serotortenergic nervous system[J]. Nihon Shinkei Seishin Yakurigaku Zasshi, 2000, 20:83-91. |