


2. 安徽医科大学 生物药物研究所, 安徽 合肥 230032;
3. 解放军第306医院心血管内科, 北京 100010
沈玉先(1965-),女,博士,教授,博士生导师,研究方向:功能性蛋白与药物作用靶点,通讯作者,Tel:0551-65113750,E-mail:shenyx@ustc.edu.cn
2. Institute of Biopharmaceutical Research, Anhui Medical University, Hefei 230032, China;
3. Dept of Cardiology, the 306th Hospital of PLA, Beijing 100101, China
组织器官在缺血后进行血液再灌注时可能导致缺血/再灌注损伤的发生。缺血缺氧可导致细胞膜通透性增加、线粒体及溶酶体损伤。再灌注时期由于氧自由基大量释放、细胞内钙超载、炎症细胞浸润等多种因素作用,可引起细胞代谢和功能障碍,发生形态和结构改变,甚至导致细胞死亡。内质网(ER)应激是启动细胞凋亡的重要途径之一,研究表明ER应激参与了心、脑、肾等重要器官缺血再灌注损伤的病理生理过程[1, 2, 3]。中脑星形胶质细胞来源的神经营养因子(mesencephalic astrocyte-derived neurotrophic factor,MANF)在ER应激时特异的表达上调[4],在脑缺血、糖尿病、缺血性心脏病等多种病理状态下发挥保护作用[5, 6, 7, 8, 9],但MANF的保护作用机制尚不十分明确。本研究发现,MANF蛋白可明显改善OGD/R诱导损伤的SH-SY5Y细胞状态,并对ER应激相关蛋白的改变有抑制作用,尤其是减少促凋亡蛋白CHOP及cleaved caspase-3的表达。本研究将为理解MANF在缺血/再灌注损伤中的保护作用提供实验依据。
1 材料与方法 1.1 材料 1.1.1 细胞及主要试剂SH-SY5Y细胞为本实验室保存。高糖DMEM培养基购自美国Gibco公司,胎牛血清购自杭州四季青公司。甲基偶氮唑盐(MTT)、DAPI、PI染料购自美国Sigma公司。ECL底物发光试剂盒购自美国Thermo公司。CHOP/GADD153抗体购自美国Santa Cruz 生物公司,MANF、GRP78/BiP、p-IRE1、p-eIF2α、cleaved caspase-3抗体购自美国Abcam公司,α-tubulin抗体购自美国Sigma公司。重组人MANF蛋白由本实验室自备。Galaxy 170R三气培养箱购自德国Eppendorf公司,荧光倒置显微镜购自日本OLYMPUS公司,Synergy HT型多功能酶标仪购自美国BioTek公司。
1.2 方法 1.2.1 细胞培养SH-SY5Y细胞培养于含10%胎牛血清,100 kU·L-1青霉素及100 mg·L-1链霉素的DMEM培养基中,置于5% CO2,37℃培养箱,隔日换液1次,3~4 d传代1次。
1.2.2 缺血/再灌注损伤模型的建立收集对数生长期SH-SY5Y细胞,分为NC组和OGD/R组。待细胞贴壁后OGD/R组在糖氧剥夺期更换为预热的无葡萄糖平衡盐溶液(a glucose-free Earle’s balanced salt solution,BSS):NaCl 116 mmol·L-1,KCl 5.4 mmol·L-1,MgSO4·7H2O 0.8 mmol·L-1,NaH2PO4·2H2O 1 mmol·L-1,NaHCO3 26.2 mmol·L-1,Glycine 0.01 mmol·L-1,CaCl2·2H2O 1.8 mmol·L-1,pH 7.4,放入含1% O2,5% CO2,94% N2,37℃饱和温湿三气培养箱中,初以5 L·min-1,30 min后培养箱内O2浓度降至1%,持续充入缺氧混合气体,维持培养箱内O2浓度低于1%,并开始计时,进行糖氧剥夺6 h。之后两组细胞分别更换为含有2 μmol·L-1重组人MANF蛋白的DMEM培养基,在5% CO2,37℃,饱和湿度培养箱中再灌注12 h。使用倒置显微镜观察细胞的形态,并检测细胞存活率及死亡率,以及ER应激相关蛋白和促凋亡相关蛋白的表达。
1.2.3 MTT法检测细胞存活率接种于96孔板的SH-SY5Y细胞,在OGD/R处理结束后加入5 g·L-1 MTT溶液10 μL(终浓度为0.5 g·L-1)作用4 h。之后加入150 μL DMSO溶液,使结晶物甲臜溶解,室温震荡10 min,使用酶联免疫检测仪,测量吸光度(optical density,OD)570 nm处各孔的吸光值。各组细胞存活率/%=(该组OD值均值-空白对照OD值均值) / (NC组OD值均值-空白对照OD值均值)×100%。
1.2.4 PI染色检测细胞死亡率SH-SY5Y细胞培养于24孔板内,预先加入含有5 mg·L-1 DPAI的DMEM培养基过夜培养,衬染细胞核,避光操作。待OGD/R处理结束后,各孔加入50 mg·L-1 PI染料2 μL,室温孵育5 min,轻混匀后在荧光倒置显微镜下观察,细胞核为蓝色荧光,死亡细胞核为红色荧光。随机选取5个视野(100×),Image-Pro Plus软件计算各视野细胞数,计算细胞死亡率。
1.2.5 免疫印迹法检测经OGD/R处理后MANF蛋白、ER应激及凋亡相关蛋白的表达SH-SY5Y细胞接种于6孔板,OGD/R处理结束后,使用RIPA裂解液(Tris,pH 7.4;150 mmol·L-1 NaCl,1% NP-40,0.25% sodium deoxycholate)提取细胞总蛋白,煮沸变性后,用15% SDS-PAGE凝胶分离,转移蛋白至PVDF膜,5%脱脂奶粉室温封闭1 h,加入适当稀释度的一抗,4 ℃孵育过夜,加入辣根过氧化物酶标记的二抗室温孵育1 h,PBS-Triton洗涤后ECL化学发光显色,Adobe Photoshop CS5 Extended软件计算灰度值并进行统计学分析。
1.3 统计学处理采用SPSS 16.0统计软件对实验数据进行分析,计量资料以 表示,组间数据的显著性检验采用单因素方差分析,两两比较采用SNK检验。
表示,组间数据的显著性检验采用单因素方差分析,两两比较采用SNK检验。
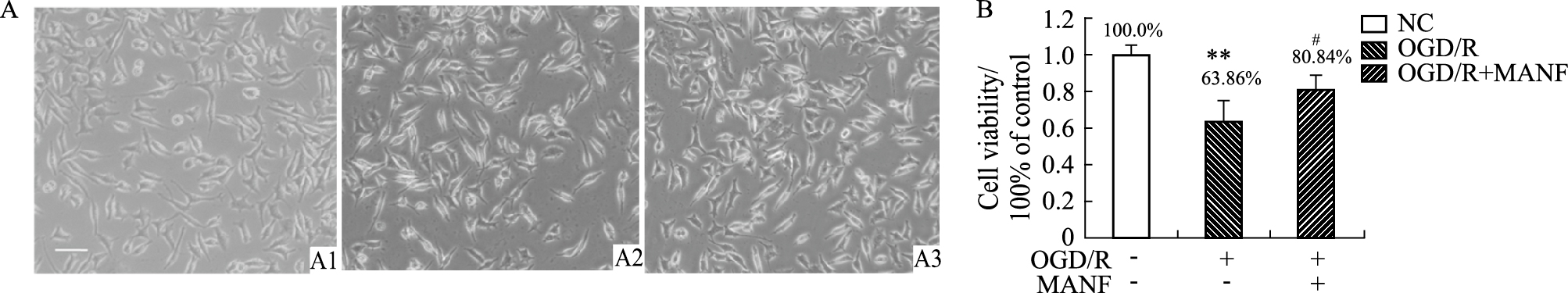
光镜下可见NC组SH-SY5Y细胞呈单层贴壁生长,多有突起(Fig1 A1)。OGD/R组细胞体积变小,突触变短或消失(Fig1 A2),MANF明显改善该细胞的状态(Fig1 A3)。MTT 结果显示,OGD/R组SH-SY5Y细胞增殖能力下降,明显低于NC组(P<0.01),OGD+MANF组细胞增殖活性明显高于OGD/R组(P<0.05) (Fig1B)。该结果表明重组人MANF蛋白对OGD/R诱导的细胞损伤有抑制作用。
|
| Fig 1 Recombinant human MANF inhibits the decrease of OGD / R-induced cell proliferation A: SH-SY5Y cell morphology was observed under an optical microscope, A1: NC group, A2: OGD/R group, A3: OGD/R+MANF group. The cells exposed to OGD/R became smaller and round, and the neurites of the cells were shortened or disappeared. Scale bar=50 μm。B: MTT results revealed that the cell survival rate decreased to (63.86±0.11) % in OGD/R-treated cells, recombinant human MANF protein promoted the cell viability of SH-SY5Y cells. **P<0.01 vs untreated controls; ##P<0.05 vs OGD/R treated group. |
PI染色可见NC组及NC+MANF组仅有少量PI染色阳性细胞(Fig2 A2,A5),而OGD/R组PI染色阳性细胞明显多于NC组(P<0.01)(Fig2 A8)。OGD/R+MANF组较OGD/R组死亡细胞数明显减少,死亡率下降 (P<0.05)(Fig2 A11)。该结果表明,重组人MANF蛋白能抑制OGD/R诱导的细胞死亡。

|
| Fig 2 Recombinant human MANF inhibits OGD / R-induced cell death A: PI staining was performed to detect the number of dead cells. A1-3: NC group, A4-6: NC+MANF group, A7-9: OGD/R group; A10-12: OGD/R+MANF group. PI stained positive cells showed red (A2, 5, 8, 11), the nuclei were stained with DAPI (blue, A1, 4, 7, 10). Scale bar = 50 μm. B: The quantitative analysis of the PI-positive cells. **P<0.01 vs untreated control group. #P<0.05 vs OGD/R treated group. |
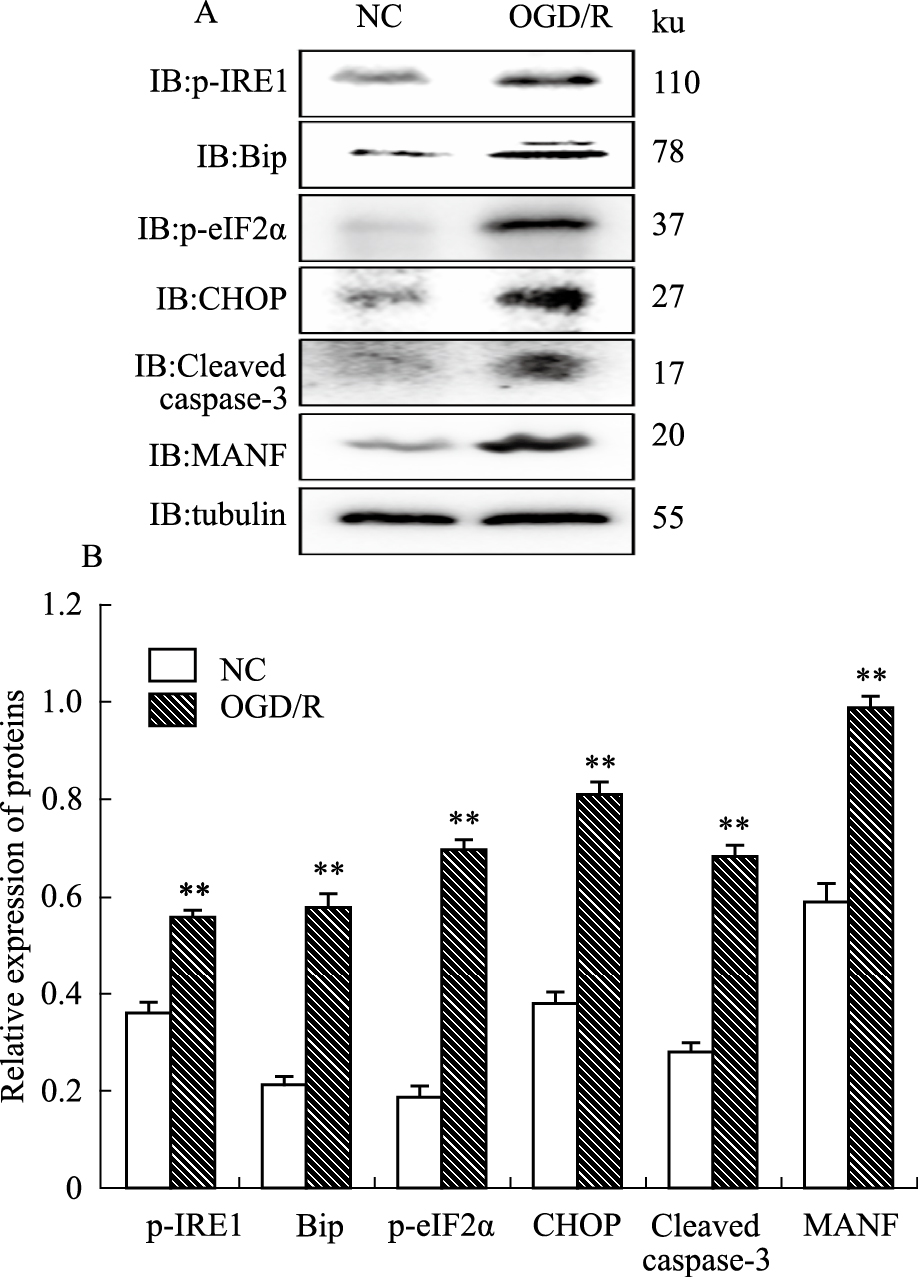
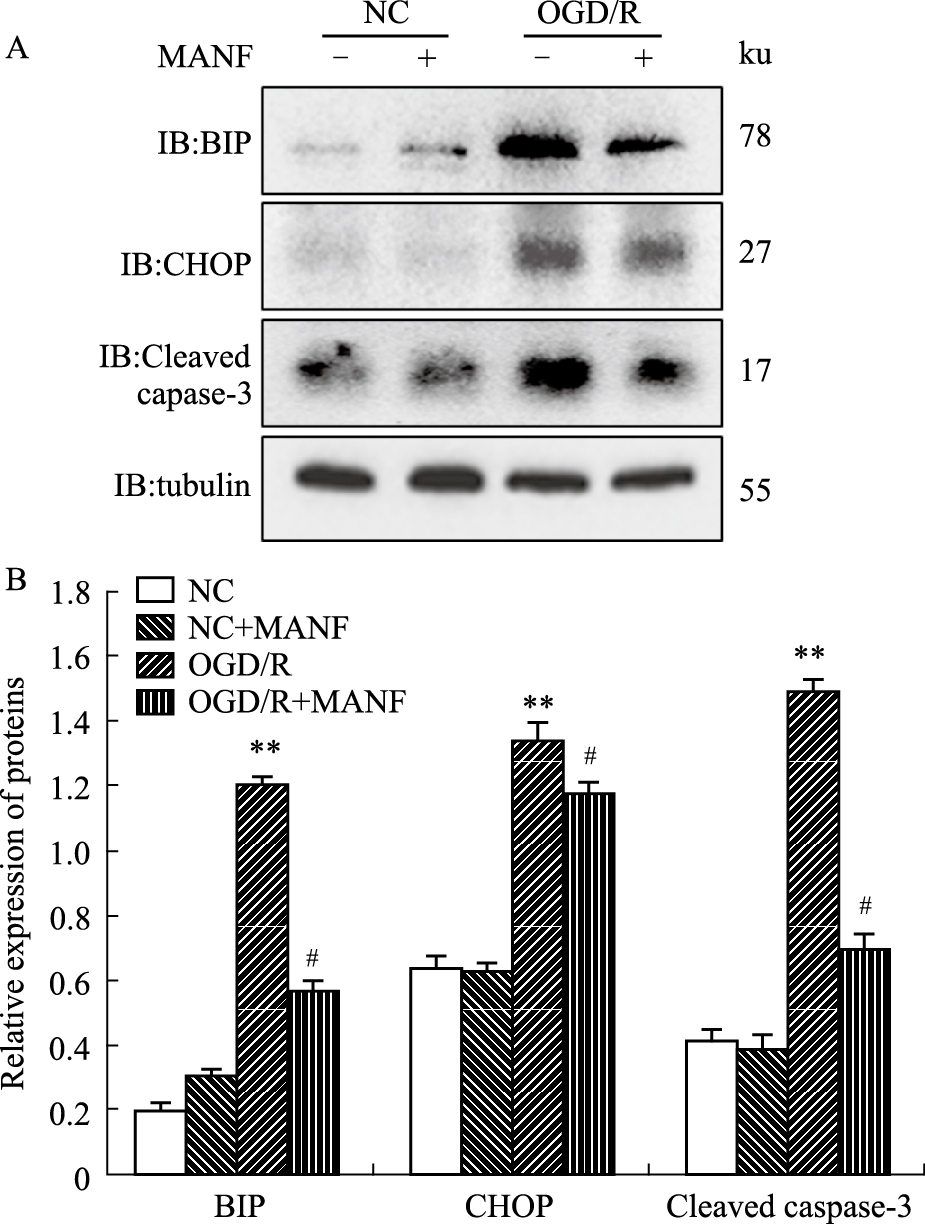
用免疫印迹方法检测ER应激相关蛋白时发现,OGD/R组SH-SY5Y细胞ER应激相关蛋白GRP78/BiP、p-IRE1、p-eIF2α、MANF的表达均明显高于NC组(P<0.01)(Fig3),提示OGD/R可诱导SH-SY5Y细胞发生ER应激。给予重组人MANF蛋白处理后,由OGD/R 上调的GRP78/BiP和CHOP的表达量均有所降低(Fig4)。
|
Fig 3
Protein levels of endogenous MANF, ER stress-associated proteins, and apoptosis-associated proteins(performed by Western blot)
A: Western blotting assay showed that endoplasmic reticulum (ER) stress-associated proteins GRP78/BiP, p-IRE1, p-eIF2α, and MANF were increased significantly after OGD/R treatment, compared with the untreated controls. Meanwhile, OGD/R treatment increased the levels of apoptosis-associated proteins CHOP and cleaved caspase - 3; B: Quantitative data from A were shown as the  . **P<0.01 vs the untreated controls. . **P<0.01 vs the untreated controls.
|
|
| Fig 4 Recombinant human MANF inhibits the expression of ER stress associated proteins and pro-apoptotic protein induced by OGD/R A: Western blot was performed to determine the protein levels; B: Quantitation of proteins normalized to tubulin levels (bottom). **P<0.01 vs the untreated control. #P<0.05 vs OGD/R treated group. |
在检测ER应激相关蛋白时发现,OGD/R组促凋亡蛋白CHOP表达增加,该结果提示OGD/R可能诱导了凋亡性的ER应激。为了进一步验证该结果,我们对caspase-3进行了检测,结果发现,与NC组比较,激活性的caspase-3水平也明显增加(P<0.01)。这些结果提示OGD/R可诱导凋亡性ER应激(Fig3)。同时发现,给予重组人MANF蛋白干预后,由OGD/R上调的CHOP和cleaved caspase-3的水平被抑制(P<0.05)(Fig4)。
3 讨论现已证实,心、脑、肝、肾及胃肠道等多种组织器 官都存在缺血/再灌注损伤的现象。缺血/再灌注的发生机制尚未阐明,目前认为自由基的作用、细胞内钙超载和白细胞的激活是缺血/再灌注损伤的主要发病环节。近年来的研究表明,ER应激在缺血/再灌注导致的细胞凋亡中具有重要作用[1, 2, 10]。
ER应激是启动凋亡的主要途径之一。ER应激触发了一个复杂的信号网络和细胞内非折叠蛋白反应(unfolded protein response,UPR)过程。UPR主要通过3种跨膜效应蛋白(PERK、IRE1和ATF6)的活化,调节蛋白质的合成、修饰及降解,维持ER内环境稳定,促进细胞存活。在生理状态下,PERK、IRE1和ATF6与GRP78/BiP结合而处于抑制状态。发生ER应激时,PERK、IRE1和ATF6与GRP78/BiP解离,GRP78/BiP与未折叠或错误折叠的蛋白质结合,以促进蛋白质正确折叠,同时PERK、IRE1和ATF6被激活[11]。PERK激活后催化其底物eIF2α发生磷酸化,使蛋白质合成暂停。IRE1α具有激酶和核糖核酸内切酶活性,可对XBP1进行剪切,生产XBP1的活性形式XBP1s,XBP1s促进蛋白质正确折叠后由ER输出,并加强错误折叠及未折叠蛋白的降解,维持ER的稳态[12]。本研究发现,OGD/R可上调ER应激标志蛋白GRP78/BiP的表达及激活UPR通路效应蛋白IRE1和PERK,提示 OGD/R可诱导ER应激,导致PERK/eIF2α和IRE1/ XBP1s通路激活,模拟体外缺氧缺血诱导的SH-SY5Y细胞损伤过程。
ER应激是机体应对损伤的一种保护性的反应,故称为适应性ER应激。但当刺激因素过强,或ER应激持续存在而超过机体的代偿能力,则ER应激变得不可逆,从而出现凋亡性ER应激。CHOP是ER应激特异的转录因子,属于转录因子家族成员[13],PERK、ATF6以及IRE1都能诱导CHOP的转录。在正常情况下 CHOP 主要存在于细胞质中,含量很低,细胞处于应激状态时,CHOP的表达量大大增加并聚集在细胞核内,过量表达的CHOP 能促进细胞凋亡[14]。caspase-3是凋亡的关键蛋白,caspase-3经剪切后成为活化型caspase-3(cleaved caspase-3),水解其蛋白底物,导致细胞凋亡。本研究发现OGD/R可上调CHOP 和cleaved caspase-3的水平,提示OGD/R在凋亡性的ER应激中发挥重要作用。
MANF是神经营养因子(neurotrophic factors,NTFs)家族成员,是1种分泌蛋白,在ER应激时特异性的表达上调,分子伴侣GRP78/BiP与MANF相互作用,并能调节MANF的分泌[1]。近年来的一些研究结果显示,MANF作为1个新型的神经保护因子,可进入细胞内与凋亡相关蛋白结合发挥细胞保护作用[5]。MANF包括两个结构域:氨基末端的鞘脂激活蛋白样结构域,可与脂质膜相互作用,其羧基末端结构域可能具有保护细胞应对ER应激的作用。越来越多的证据表明MANF是1个ER应激反应蛋白,在体外实验中MANF能够保护细胞应对ER应激反应诱导的细胞死亡[4]。晶体结构表明MANF可以帮助蛋白质在ER内折叠。MANF的C-末端结构域,模体127CKGC130有两个半胱氨酸形成,一个C-末端二硫键可能有助于形成半胱氨酸桥并帮助蛋白质折叠,从而减少未折叠或错误折叠的蛋白质引起的ER应激[15]。本研究探讨MANF对OGD/R诱导的SH-SY5Y细胞损伤的保护作用。研究结果表明,再灌注时期给予MANF处理能够抑制OGD/R诱导的SH-SY5Y细胞的细胞活力下降,减少OGD/R诱导的SH-SY5Y细胞死亡率增加,表明MANF能够减轻OGD/R诱导的SH-SY5Y细胞损伤。此外,Western blot显示,经MANF蛋白处理之后,OGD/R诱导的ER应激标志物GRP78增加能够被MANF明显抑制,并且MANF能够减少ER应激特异的促凋亡蛋白CHOP和凋亡执行分子cleaved caspase-3的表达,表明MANF通过抑制SH-SY5Y细胞ER应激抑制凋亡。因此,MANF在SH-SY5Y细胞应对ER应激诱导的损伤中起着重要的作用。本研究为理解低氧诱导的损伤机制以及MANF在缺血/再灌注损伤中的保护作用提供了实验依据。
| [1] | Glembotski C C, Thuerauf D J, Huang C, et al. Mesencephalic astrocyte-derived neurotrophic factor protects the heart from ischemic damage and is selectively secreted upon sarco/endoplasmic reticulum calcium depletion[J]. J Biol Chem, 2012,287(31):25893-904. |
| [2] | Zhu C, Wang X, Huang Z, et al. Apoptosis-inducing factor is a major contributor to neuronal loss induced by neonatal cerebral hypoxia-ischeinia[J]. Cell Death Diffe,2007,14(4):775-84. |
| [3] | Yang J R, Yao F H, Zhang J G, et al. Ischemia-reperfusion induces renal tubule pyroptosis via the CHOP-caspase-11 pathway[J]. Am J Physiol Renal Physil,2014,306(1):F75-84. |
| [4] | Apostolou A, Shen Y, Liang Y, et al.Armet, a UPR-upregulated protein, inhibits cell proliferation and ER stress-induced cell death[J]. Exp Cell Res,2008, 314(13):2454-67. |
| [5] | Hellman M, Arumäe U, Yu L Y, et al. Mesencephalic astrocyte-derived neurotrophic factor (MANF) has a unique mechanism to rescue apoptotic neurons[J]. J Biol Chem, 2011,286(4):2675-80. |
| [6] | Yang W, Shen Y, Chen Y, et al. Mesencephalic astrocyte-derived neurotrophic factor prevents neuron loss via inhibiting ischemia-induced apoptosis[J]. Neurol Sci,2014,344(1-2):129-38. |
| [7] | Lindahl M, Danilova T, Palm E, et al. MANF is indispensable for the proliferation and survival of pancreatic β cells[J]. Cell Rep,2014,7(2):366-75. |
| [8] | Voutilainen M H, Bäck S, P rsti E, et al.Mesencephalic astrocyte-derived neurotrophic factor is neurorestorative in rat model of Parkinson's disease[J]. Neurosc, 2009,29(30):9651-9. |
| [9] | 李 静,王 涛,沈玉君,等.MANF对神经细胞中tau蛋白过度磷酸化的抑制作用[J].中国药理学通报,2012,28(8):1111-5. Li J, Wang T, Shen Y J, et al. MANF inhibits tau hyperphosphorylation in cultured neuronal cells[J]. Chin Pharmacol Bull, 2012,28(8):1111-5. |
| [10] | Nakka V P, Gusain A, Raghubir R. Enddoplasinic reticulum stress plays critical role in brain damage after cerebral ischemia/reperfusion in rats[J]. Neurotox Res,2010,17(2):189-202. |
| [11] | Oyadomari S, Mori M. Roles of CHOP/GADD153 in endoplasmic reticulum stress [J]. Cell Death Differ, 2004,11:381-9. |
| [12] | Calfon M, Zeng H, Urano F, et al. IRE1 couples endoplasmic reticulum load to secretory capacity by processing the XBP-1 mRNA[J]. Nature, 2002,415(6867):92-6. |
| [13] | Fels D R, Koumenis C. The PERK/elF2/ATF4 module of the UPR in hypoxia resistance and tumor growth[J]. Cancer Biol Ther, 2006,5(7):723-8. |
| [14] | Mccullough K D, Martindale J L, Klotz L O, et al. Gadd153 sensitizes cells to endoplasmic reticulum stress by down-regulating Bcl2 and perturbing the cellular redox state [J]. Mol Cell Biol, 2001,21(4):1249-59. |
| [15] | Lindholm P, Voutilainen M H, Laurén J, et al. Novel neurotrophic factor CDNF protects and rescues midbrain dopamine neurons in vivo[J]. Nature,2007,448(7149):73-7. |

