


脑胶质瘤亦称神经胶质细胞瘤,由神经上皮组织衍化而来,具有发病率高、病死率高和治愈率低的特点,手术切除是当前最主要的临床治疗手段。由于胶质瘤本身固有的浸润性生长的病理特点,手术后的复发仍不可避免,采用安全有效的方法进行胶质瘤的治疗成为亟待解决的问题。天然药物单体化合物可通过抑制肿瘤细胞增殖、诱导肿瘤细胞分化或凋亡从而发挥抗肿瘤作用。牛蒡子为菊科植物牛蒡(Arctium Lappa L.)的干燥成熟果实。癌细胞体外及体内实验证明,牛蒡子具有抗癌性[1]。米靖宇等[2]经过归纳总结认为,牛蒡子中具有抗肿瘤和免疫活性的有效成分主要为牛蒡子苷元(arctigenin,ARG)。牛蒡子苷元体内外试验表明,其可抑制多种肿瘤细胞的生长,其抗肿瘤作用主要集中在促进肿瘤细胞凋亡、抑制肿瘤细胞增殖等方面[1]。检索国内外文献尚未发现有关牛蒡子苷元对脑胶质瘤相关作用的报道。本试验采用大鼠脑内注射C6胶质瘤细胞建立大鼠脑瘤模型,研究牛蒡子苷元及联合抗脑胶质瘤药物替莫唑胺对大鼠C6胶质瘤的作用,同时观察其对脑瘤组织中的增殖细胞核抗原(proliferating cell nuclear antigen,PCNA)、胶质纤维蛋白(glial fibrillary acidic protein,GFAP)及CD40表达的作用。
1 材料与方法 1.1 药物和试剂牛蒡子苷元注射液(山东新时代药业有限公司); 大鼠C6脑胶质瘤细胞株系(中国科学院上海生命科学研究院细胞资源中心);替莫唑胺原料(北京嘉瑞时代科技有限公司);免疫组化PCNA和CD40试剂盒(Santa Cruze);免疫组化GFAP试剂盒(北京中杉金桥有限公司)。
1.2 仪器超净工作台(SW-CJ-1BU型,苏净集团安泰公司制造);倒置荧光显微镜(CKX41型,日本奥林巴斯公司);组织包埋机(Tissue-Tek® TECTM 5.,日本樱花科技);全封闭组织脱水机(Tissue-Tek® VIPTM 5Jr,日本樱花科技)。
1.3 动物健康♂ SD大鼠,SPF级,90只,体质量(200±20) g。鲁南制药集团股份有限公司试验动物中心提供,动物许可证号:SCXK(鲁)2012 0002;质量合格证号:0015264。
1.4 细胞培养及处理大鼠C6脑胶质瘤细胞,取对数期细胞,消化,分散均匀,浓度为1×1011 ·L-1,C6细胞使用含有10%小牛血清的RPMI 1640培养液于37℃、5%的CO2培养箱中常规培养。当细胞处于对数生长期时,用胰蛋白酶适量消化3~5 min后,弃去消化液。用PBS液吹打冲洗1~2次形成细胞悬液,调整细胞浓度为1×1010·L-1的悬液用于接种[3]。
1.5 大鼠脑胶质瘤模型的建立SD大鼠尾静脉注射1%戊巴比妥钠(40 mg·kg-1)后,脱去大鼠头顶部毛发,头顶双侧眼裂连线后大约1.5 cm处横向切开头皮,暴露前囱颅骨标志,前囱中点前1 mm,矢状缝旁开3 mm处用自制牙钻钻一骨孔,微量注射器抽取C6细胞悬液10 μL,垂直固定于试验台上,经原骨孔处进针硬脑膜下6 mm,后退1 mm,于10 min内将细胞悬液注完(2 μL·min-1),注射完毕后留针5 min,缓慢退针,骨蜡封闭骨孔,1号丝线缝合头皮切口[4, 5, 6]。
1.6 动物分组及给药90只大鼠随机分为6组,分别为模型组(M)、低剂量牛蒡子苷元组(ARG 0.05,0.05 mg·kg-1)、高剂量牛蒡子苷元组(ARG 0.1,0.1 mg·kg-1)、替莫唑胺组(TMZ,20 mg·kg-1)、低剂量牛蒡子苷元+替莫唑胺组(TMZ/ARG 0.05)、高剂量牛蒡子苷元+替莫唑胺组(TMZ/ARG 0.1),每组15只。牛蒡子苷元于术后d 2开始皮下给药[0.1 mL·(100 g)-1],连续给药15 d,替莫唑胺于接种后d 5开始灌胃给药,1 mL·(100 g)-1连续给予5 d,其余各组灌胃给予相同体积的质量分数为0.5% 的CMC-Na。
1.7 结果判定标准术后d 16以过量戊巴比妥钠麻醉处死实验动物,断头取脑,全脑于3%甲醛中固定1周,沿进针点作冠状切口,测量肿瘤的长短径,计算肿瘤体积V=πab2/6(b为短径)。抑瘤率/%=(模型组的肿瘤体积 - 实验组的肿瘤体积)/模型组肿瘤的平均体积×100%,抑制率>30%为肿瘤对药物敏感。同时石蜡切片,行PCNA、GFAP和CD40免疫组织化学染色检测,染色操作过程按照试剂盒说明书进行。将已染好的切片在显微镜下观察并拍照,采用IPP病理图像分析软件计算GFAP阳性表达的光密度及CD40阳性细胞的IOD值和面密度;PCNA结果以胞核或(和)胞质中出现棕黄色或褐色颗粒为阳性,光镜高倍视野下(400倍)阳性细胞数所占总肿瘤细胞数的百分率为 PCNA 阳性指数。
1.8 统计学方法数值用 表示,试验数据用SPSS 17.0进行统计分析,组间差异用ANOVA检验。
表示,试验数据用SPSS 17.0进行统计分析,组间差异用ANOVA检验。
由Tab1可以看出,与模型组相比,低、高剂量牛蒡子苷元组和替莫唑胺组的肿瘤体积降低(P<0.05),联合用药组的肿瘤体积明显降低(P<0.01)。表明牛蒡子苷元单用及联用均对大鼠脑胶质瘤有抑制作用,并且牛蒡子苷元与替莫唑胺联用具有协同作用。所有给药组的抑瘤率均>40.65%,显示大鼠C6胶质瘤对牛蒡子苷元及联合用药敏感。
PCNA阳性细胞的胞核呈黄色或棕黄色,400倍镜下计数肿瘤内5个视野的阳性细胞。由Fig1可以看出,模型组大鼠肿瘤细胞表现为阳性细胞密度高,胞核呈阳性,数量多。与模型组相比,低剂量及高剂量牛蒡子苷元的PCNA阳性表达率明显降低(P<0.05);牛蒡子苷元联合替莫唑胺组的PCNA阳性表达率也明显降低(P<0.01),并且联合用药优于单独牛蒡子苷元和替莫唑胺。表明牛蒡子苷元可以明显抑制大鼠C6胶质瘤细胞增殖,并且与替莫唑胺联用可以协同抑制C6胶质瘤增殖。

|
| Fig 1 Expression of PCNA on rat tumor issue(×400) *P<0.05, **P<0.01 vs model group |
GFAP免疫组化阳性染色定位于细胞质,呈棕黄色,400倍镜下计数肿瘤内3个视野的阳性细胞,计数肿瘤内GFAP阳性表达。低剂量牛蒡子苷元组的GFAP表达与模型组相比有升高的趋势,但差异无显著性。除低剂量牛蒡子苷元组外,其余给药组GFAP阳性表达,瘤内光密度值较模型组均明显增强(P<0.05)。表明牛蒡子苷元单用及联用均可以明显增强GFAP表达,见Fig2。

|
| Fig 2 Expression of GFAP on rat tumor issue (×400) *P<0.05 vs model group |
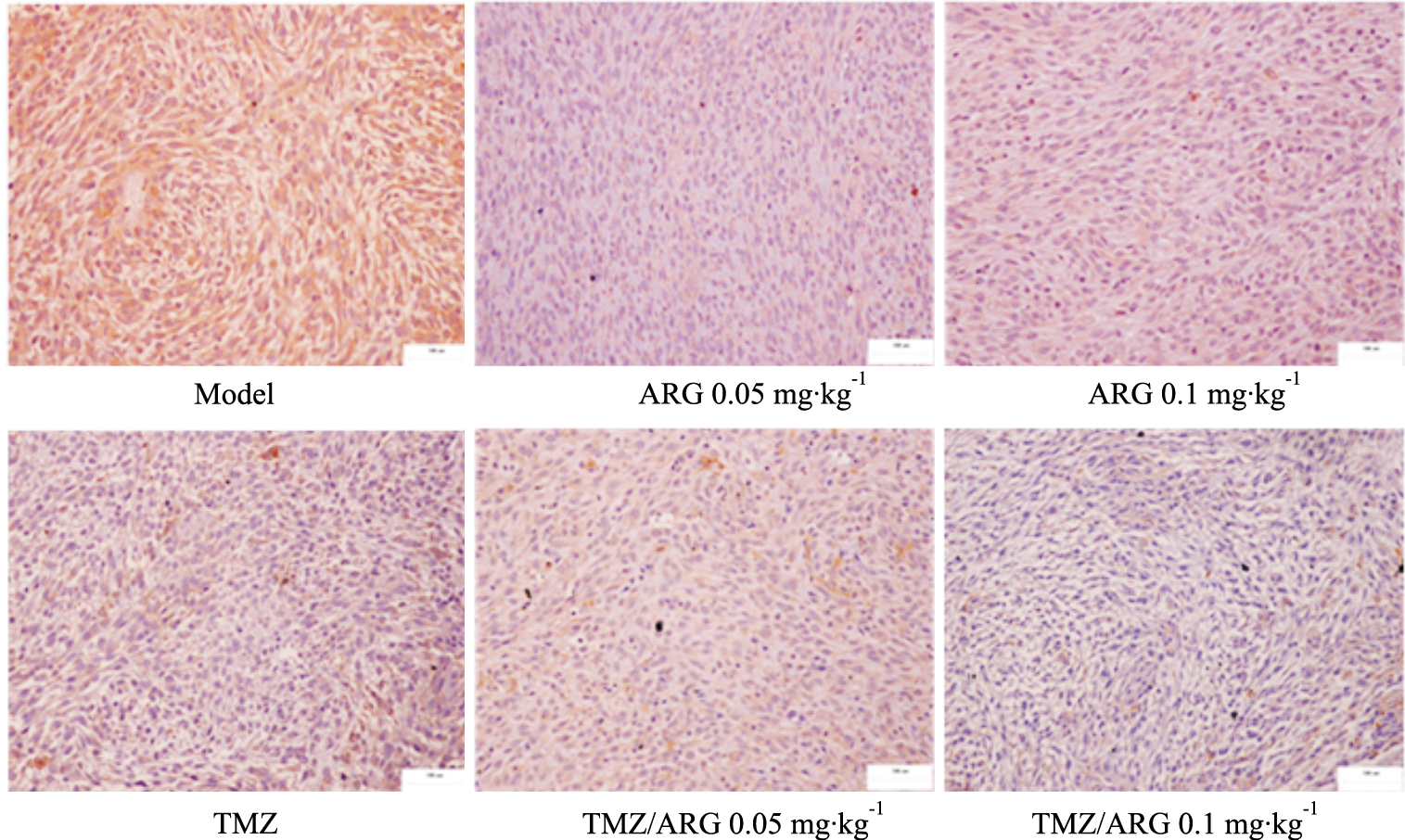
CD40免疫组化阳性染色定位于细胞膜、细胞质。由Tab2及Fig3可以看出,牛蒡子苷元IOD值(P<0.01)和面密度值(P<0.05)均明显低于模型组;联合用药组的IOD值(P<0.01)和面密度值(P<0.01)也明显低于模型组,并且好于单独牛蒡子苷元和替莫唑胺。表明牛蒡子苷元可以明显抑制CD40表达,并且同替莫唑胺联用具有协同作用。
|
| Fig 3 Expression of CD40 on rat tumor issue (×400) |
脑胶质瘤是最常见的原发性脑肿瘤,占原发性中枢神经系统肿瘤的32%。2012年,中国肿瘤登记报告指出中国脑及中枢神经系统恶性肿瘤死亡率约 为3.87 /10万,位列十大高病死率肿瘤之第9位。
替莫唑胺是国际上治疗脑胶质瘤的一线药物,但是其作为化疗药物,全身毒性反应较大,对患者的免疫力影响较大。几十年来,天然产物一直是药物和药物先导化合物的重要来源。天然抗肿瘤药物以其作用机制独特、效果明显、毒副作用小在临床广泛使用。目前临床使用量已占到肿瘤治疗药物的74%。
脑胶质瘤中PCNA和GFAP的表达水平呈负相关,PCNA的过度表达导致了细胞周期调节紊乱,影响胶质瘤的增殖和分化,参与了胶质瘤的恶性进展,它的表达与胶质瘤的恶性行为相关[7, 8]。而GFAP是星形胶质细胞及其发生肿瘤的最佳特征性标记物[9]。研究发现,GFAP强阳性表达往往标志着瘤细胞趋于成熟,分化良好,预后较好[10]。观察PCNA与GFAP的表达是评价胶质瘤增殖、生长、分化及恶性程度的主要指标。CD40信号的高表达与胶质瘤的发生发展、微血管形成等存在正相关性。CD40信号可直接刺激肿瘤细胞和肿瘤微环境中的多种细胞,产生IL-6、MMP、VEGF等一系列利于肿瘤生长和促进肿瘤新生血管形成的细胞因子[11, 12]。
本实验表明,牛蒡子苷元能明显减少C6胶质瘤大鼠的肿瘤体积,并且牛蒡子苷元作为天然产物单体,其抗肿瘤作用并非类似于替莫唑胺单纯依靠其对肿瘤细胞的特异性杀灭,而是同时发挥对荷瘤大鼠的全面调节作用,如改善机体免疫功能,调节机体内环境,拮抗替莫唑胺和肿瘤本身对机体功能的损害。同时本实验还观察了牛蒡子苷元对PCNA、GFAP和CD40表达的影响,研究结果显示,牛蒡子苷元可以明显降低PCNA、CD40表达,升高GFAP表达,表明牛蒡子苷元抑制胶质瘤大鼠肿瘤的生长,作用机制可能与影响相关蛋白(降低PCNA、升高GFAP)表达和调节机体免疫(抑制CD40表达)相关。
此外,本研究还观察了牛蒡子苷元与替莫唑胺合用对大鼠C6胶质瘤是否具有协同作用。结果显示,牛蒡子苷元与替莫唑胺合用可以协同抑制大鼠C6胶质瘤生长,无论低剂量牛蒡子苷元,还是高剂量牛蒡子苷元联合替莫唑胺的肿瘤抑制率均高于单独的牛蒡子苷元和替莫唑胺,并且两者联用能协同抑制PCNA表达和增强GFAP表达,同时其CD40的IOD和面密度值均低于单独用药,表明牛蒡子苷元和替莫唑胺合用在影响胶质瘤相关蛋白表达和免疫调节(抑制CD40表达)作用机制方面也具有协同作用。
综上所述,牛蒡子苷元能明显抑制大鼠C6脑胶质瘤生长;同时牛蒡子苷元(0.05和0.1 mg·kg-1)和抗胶质瘤药替莫唑胺(20 mg·kg-1)合用具有协同作用,作用机制可能与抑制PCNA和CD40的表达、增强GFAP的表达相关。脑胶质瘤细胞生长增殖是一个极其复杂的生物学过程,影响因素很多,目前牛蒡子苷元抑制胶质瘤细胞生长相关机制目前尚无定论,更多详细的机制需要进一步研究。牛蒡子苷元已经作为中药一类新药上报到国家食品药品监督管理局,本次试验为牛蒡子苷元作为一类新药上报提供临床前药理实验支持。
(本实验在鲁南制药集团股份有限公司/中药制药共性技术国家重点实验室完成,感谢实验室提供的技术资金支持,感谢实验室同事提供的大力帮助。)
| [1] | 郑国灿.牛蒡子提取液的抗癌性研究[J].东南大学学报(医学版),2003,22(5):319-22. Zheng G C.The study of antitumor to the extract of Arctium lappa L[J].J Southeast Univ (Med Sci Edit), 2003,22(5):319-22. |
| [2] | 米靖宇,宋纯清.牛蒡子中木脂素类化合物的抗肿瘤及免疫活性[J].时珍国医国药, 2002,13(3):168. Mi J Y,Song C Q.The anti-tumor and immunity activities of lignans compound from Arctium lappa L[J]. Lishizhen MED Mat Med Res,2002,13(3):168. |
| [3] | 王天路,陆利霞,孙涛,谭关子.聚乳酸——替莫唑胺微胶囊对大鼠C6脑胶质瘤体外和体内抑瘤试验[J].江苏医药, 2008,34(5):478-80. Wang T L,Lu L X,Sun T,Tan G Z.Growth inhibition of polylactic acid temozolomide microspheres on SD rat brain in vitro and in vivo[J]. Jiangsu Med J,2008,34(5):478-80. |
| [4] | 邱大胜,徐丽莹,尹明媛,等. 注射后留置时间对大鼠C6脑胶质瘤模型的影响[J].重庆医科大学学报,2008,33(10):1260-3. Qiu D S,Xu L Y,Yin M Y,et al.The effect of detaining time after injection in rat brain C6 glioma[J].J Chongqing Med Univ, 2008,33(10):1260-3. |
| [5] | 余永强,陈骏,钱银锋,等.立体定向建立大鼠C6胶质瘤模型[J].中国药理学通报, 2003,19(2):222-5. Yu Y Q,Chen J,Qian Y F,et al. Establishment of rat C6 glioma model by intracranial injection[J]. Chin Pharmacol Bull,2003,19(2):222-5. |
| [6] | 李蓉,刘国龙,牛道立,等.建立大鼠C6/SD脑胶质瘤放射剂量效应模型的实验研究[J].解剖学研究,2011,33(1):4-9. Li R,Liu G L,Niu D L,et al. Experimental study of radiation on C6 glioma rats model[J].Anat Res,2011,33(1):4-9. |
| [7] | 张进华,游枫慧,杨卫忠,等.榄香烯抑制人脑胶质瘤U251细胞增殖和PCNA基因表达的研究[J].中国药理学通报, 2008,24(10):1348-51. Zhang J H,You F H,Yang W Z,et al. Study on the inhibiti on of cell pro liferation and the expression of PCNA gene of human glioma U251 by elemene[J]. Chin Pharmacol Bull,2008,24(10):1348-51. |
| [8] | 陈罡,罗殿中,侯巧燕,郭芳.PCNA和GFAP在脑星形胶质细胞瘤中表达的双重染色研究[J].中国临床神经外科杂志, 2005,10(4):252-4. Chen G,Luo D Z,Hou Q Y,Guo F.Study of PCNA and GFAP expressions in human brain astrocytomas by double immunohistochemical staining[J].Chin J Clin Neurosurg,2005,10(4):252-4. |
| [9] | 杨金庆,于耀宇,陶胜忠,等.GFAP,Vimentin,VEGF和p53的表达与星形细胞瘤预后的相关性研究[J].中国临床神经外科杂志, 2006,11(9):535-7. Yang J Q,Yu Y Y,Tao S Z,et al. Expressions of GFAP, Vimentin, VEGF and p53, and their relationship with prognosis in astrocytoma[J].Chin J Clin Neurosurg,2006,11(9):535-7. |
| [10] | 张建平,付银根,刘大全.人参皂苷Rg3对大鼠脑胶质瘤GFAP,Vimentin表达的影响[J].第四军医大学学报, 2009,30(13):1173-6. Zhang J P,Fu Y G,Liu D Q. Effects of Ginsenoside Rg3 on GFAP and vimentin expression in rat glioma[J].J Fourth Mil Med Univ,2009,30(13):1173-6. |
| [11] | 蔡文治,王卓,谢炜,等. CD40基因特异性沉默对脑胶质瘤细胞株U87增殖和迁移的影响[J].苏州大学学报(医学版), 2012,32(1):36-40. Cai W Z,Wang Z,Xie W,et al.The effect of CD40 gene silencing on proliferation and migration of glioma cell line U87[J]. J Soochow Univ Med Sci Edit,2012,32(1):36-40. |
| [12] | Futagami S, Hiratsuka T,Shindo T,et al.COX-2 and CCR2 induced by CD40 ligand and MCP-1 are linked to VEGF production in endothelial cells[J].Prostaglandins Leukot Essent Fatty Acids,2008,78(2):137-46. |



