2. 重庆医科大学药理学教研室, 重庆 400016
2. Dept of Pharmacology, Chongqing Medical University, Chongqing 400016, China
脑缺血是导致成年人认知功能障碍的主要原因之一。神经发生在脑缺血后脑组织修复和认知功能恢复中发挥重要作用[1]。成年哺乳动物中枢神经系统内的神经发生主要分布在海马齿状回(dentate gyrus,DG)和侧脑室室管膜下区(subventricular zone,SVZ)。中药单体黄芩苷(baicalin),是从黄芩的干燥根中提取分离出来的一种黄酮类化合物,具有抗炎、抗过敏、抗氧化等多方面的药理作用[2]。研究表明,黄芩苷能够在体外促进神经前体细胞(neural precursor cells,NPCs)增殖,诱导间充质干细胞分化为神经元,但其机制仍不清楚[3, 4]。环氧化酶-2 (cyclooxygenase-2,COX-2)是脑损伤后脑内炎症反应的重要标志物,可在某些炎症介质的诱导下表达。近年研究发现,使用抗炎类药物可以逆转脑缺血损伤后炎症反应导致的脑内神经细胞增殖减弱[5, 6]。因此,我们设想黄芩苷能否通过抑制脑缺血后脑组织内产生的过度炎症反应,维持内源性NPCs增殖相对稳定的小生境(niche),从而改善脑缺血后的神经功能缺损。本实验拟研究黄芩苷对全脑缺血/再灌注大鼠认知功能的影响及其可能机制是否与调控脑组织COX-2蛋白表达,促进内源性NPCs增殖有关。
1 材料与方法 1.1 材料 1.1.1 实验动物与分组60只成年♂ SD大鼠(SPF级),体质量(230±20) g,由重庆医科大学实验动物中心提供。术前12 h 禁食,自由饮水,并随机分为3组:假手术组(S组)、全脑缺血/再灌注组(I/R组)、全脑缺血/再灌注+黄芩苷组(I/RB组),每组20只。其中Morris水迷宫实验6只,BrdU免疫组化10只,Western blot检测4只。
1.1.2 药品与试剂黄芩苷(西安原生植物技术有限公司,纯度98%);小鼠抗BrdU 单克隆抗体(Sigma,美国);兔抗鼠COX-2 多克隆抗体(Cayman,美国);鼠β-actin单克隆IgG (Santa Cruz,美国);5-溴脱氧尿嘧啶核苷(5-Bromo-2-deoxyUridine,BrdU)购自美国Sigma公司。
1.1.3 主要仪器Morris水迷宫系统(淮北正华生物仪器设备有限公司);凝胶成像系统 (Bio-Rad,美国);光学显微镜(Nikon,日本);全自动酶标仪(Spectra Max M2公司,美国)。
1.2 方法 1.2.1 模型制备采用双侧颈总动脉夹闭合并低血压建立大鼠全脑缺血/再灌注模型[7]。水合氯醛(400 mg·kg-1,ip)麻醉后,分离左、右颈总动脉及右侧颈总静脉,静脉插管,输入肝素化生理盐水,缓慢抽取大鼠总血容量体积分数0.3的血液后,夹闭双侧颈总动脉20 min,再缓慢回输血液,缝合。S组仅分离双侧颈总动脉和右侧颈总静脉。
1.2.2 黄芩苷给药及BrdU标记用生理盐水将黄芩苷稀释成浓度10 g·L-1。I/RB组大鼠造模后12 h行黄芩苷(100 mg·kg-1)灌胃,每天两次,连续7 d。S组和I/R组大鼠在相同时间点给予相应体积的生理盐水灌胃。用于标记脑内NPCs增殖的大鼠于处死前1 d腹腔注射BrdU(50 mg·kg-1),共3次,每次间隔4 h,最后一次注射12 h后处死大鼠。
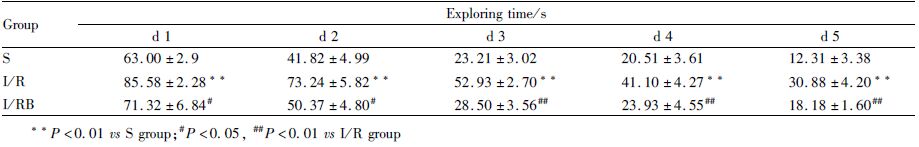
1.2.3 行为学测试[8]造模7 d后行Morris水迷宫试验。Morris 水迷宫直径150 cm、高60 cm,内含直径12 cm平台一个,置于水面下1 cm。实验全程实时监控,电脑记录数据。训练d 1,先将大鼠放于平台适应2 min,再由任意象限池壁放入水中让其自由游泳至平台,90 s 内未找到平台者,将其引导至平台停留15 s 后终止试验。d 2~d 4大鼠分别从4个象限沿池壁放入水中进行训练,逃避潜伏期超过90 s 按90 s计算,d 5时,撤去平台,随机选定一个象限将大鼠放入水池,记录大鼠逃避潜伏期、目标象限滞留时间以及穿越平台次数。
1.2.4 BrdU免疫组化造模7 d后,大鼠进行在体灌流固定。石蜡切片常规脱蜡、脱水、修复,山羊血清封闭。加入BrdU一抗(1 ∶ 1 000)4℃过夜(PBS阴性对照),加入二抗37℃ 30 min,再滴加SABC试剂盒检测试剂,DAB显色。显微镜下观察海马DG和侧脑室SVZ增殖的阳性细胞,细胞核呈深棕黄色的颗粒为增殖阳性细胞。每只大鼠分别取3张切片(切片间隔为400 μm),每张切片取5个高倍视野进行细胞计数,计算出每只大鼠所要分析部位的平均BrdU阳性细胞数,并应用Image-pro plus 6.0进行图像分析。
1.2.5 Western blot检测造模7 d后新鲜大鼠脑组织经RIPA裂解液裂解提取全蛋白。BCA法测定蛋白浓度,经电泳、转膜、封闭后加入COX-2和β-actin一抗(1 ∶ 1 000 ),4 ℃孵育过夜,加入二抗 37℃孵育2 h后,凝胶成像仪成像,Quantity One软件分析蛋白表达水平。
1.3 统计学方法采用SPSS 17.0统计软件包进 行统计分析,数据用 表示,多组比较采用单因素方差分析。
表示,多组比较采用单因素方差分析。
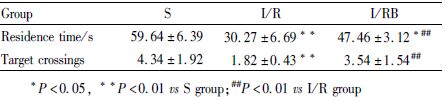
航行试验中,各组大鼠随着训练时间的延长,平均逃避潜伏期均缩短。与S组相比,I/R组大鼠平均潜伏期明显延长(P<0.01),表明I/R组大鼠的空间学习能力受损明显;与I/R组相比,I/RB组大鼠平均逃避潜伏期明显缩短(P<0.05),表明黄芩苷能够改善全脑缺血/再灌注大鼠的空间学习能力(Tab1)。空间探索实验中,I/RB组大鼠在原平台所在象限的停留时间和穿越平台次数明显高于I/R组大鼠(P<0.01),说明撤除平台后,黄芩苷能够明显改善全脑缺血/再灌注对大鼠空间记忆能力的损害(Tab2)。
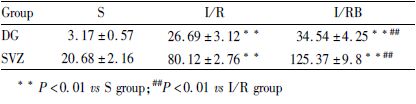
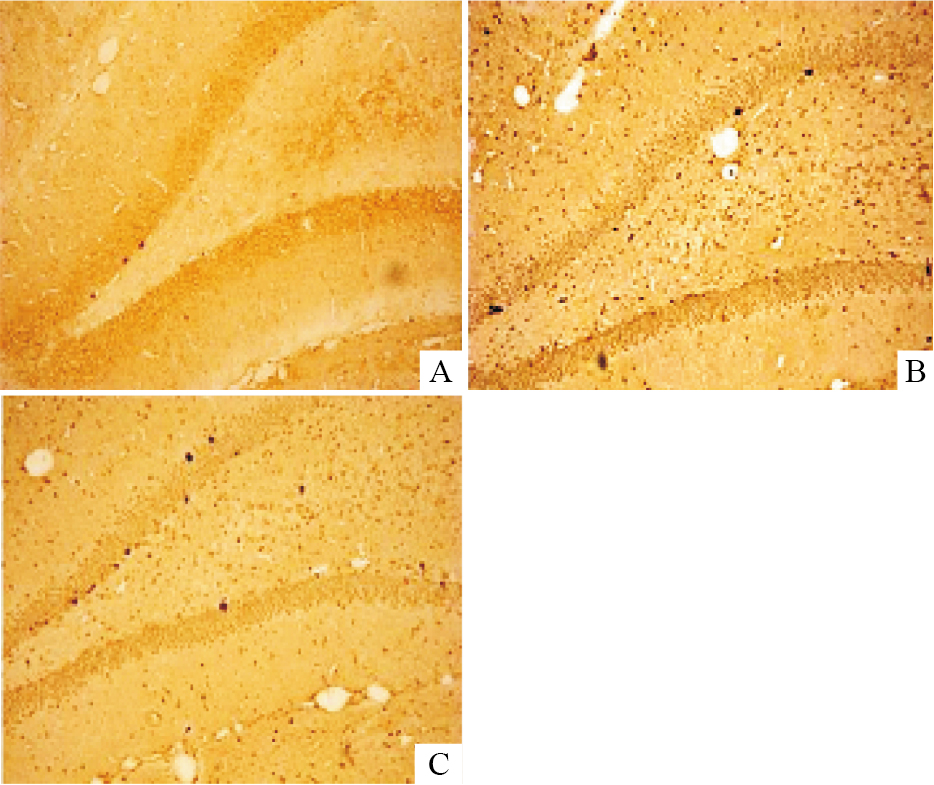
造模7 d后,免疫组化检测的阴性对照组未见BrdU阳性细胞,S组大鼠海马DG和侧脑室SVZ仅见少量的BrdU阳性细胞;而I/R组和I/RB组大鼠可见BrdU阳性细胞单个或成群地出现在海马DG和侧脑室SVZ。统计结果显示,与S组相比,I/R组和I/RB组大鼠在海马DG和侧脑室SVZ的BrdU阳性细胞数均明显增加(P<0.01,Tab3,Fig1,2),且与I/R组相比,I/RB组大鼠在海马DG和侧脑室SVZ的BrdU阳性细胞数仍呈明显增多趋势(P<0.01,Tab3,Fig1,2),提示黄芩苷可促进脑内内源性NPCs增殖。
|
| Fig 1 Effects of baicalin on the number of BrdU-positive cells in DG area 7 days after surgery(×200) A:S group; B: I/R group; C: I/RB group |

|
| Fig 2 Effects of baicalin on the number of BrdU-positive cells in SVZ area 7 days after surgery(×200) A:S group; B: I/R group; C: I/RB group |
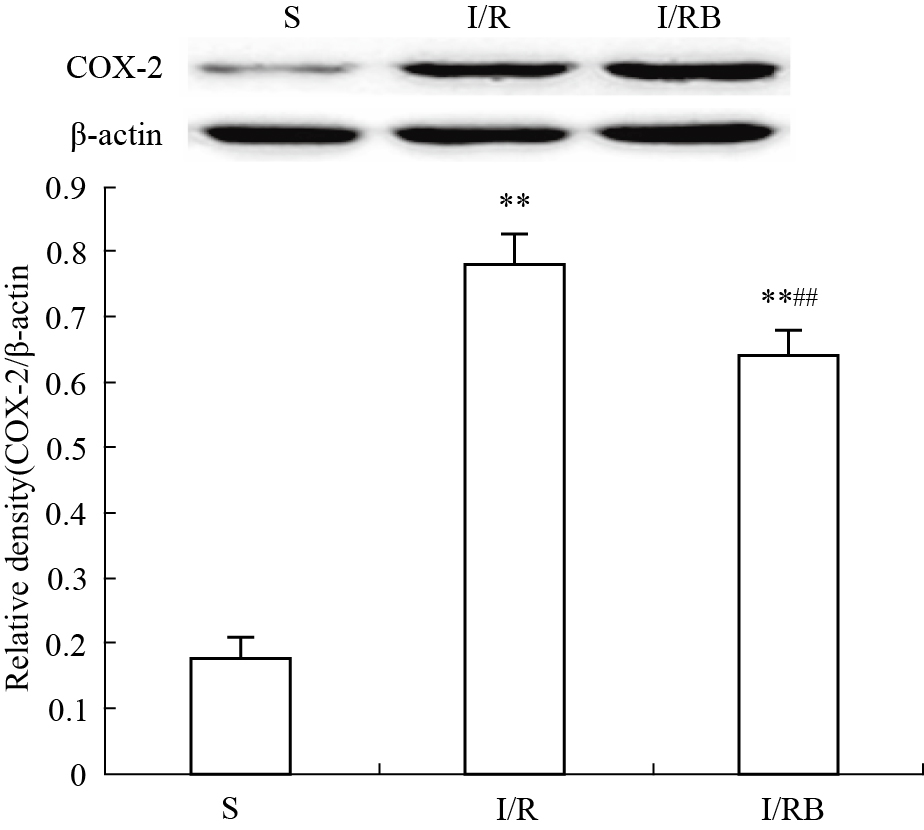
统计结果显示,造模7 d后,I/R组大鼠脑组织COX-2蛋白的表达与S组相比明显增加(P<0.01),表明全脑缺血/再灌注后脑组织内炎症反应明显。使用黄芩苷干预后,I/RB组大鼠脑组织COX-2蛋白的表达水平较I/R组明显降低(P<0.01),提示黄芩苷可抑制全脑缺血/再灌注后脑组织COX-2蛋白的表达(Fig3)。
|
Fig 3
Effects of baicalin on expression of COX-2 in the brain of rats 7 days after surgery( , n=4)
**P<0.01 vs S group;##P<0.01 vs I/R group , n=4)
**P<0.01 vs S group;##P<0.01 vs I/R group
|
大量研究证实,位于海马DG和侧脑室SVZ的神经发生在成年哺乳动物认知功能的修复过程中发挥重要作用[9]。病理状态如脑缺血能诱导脑内内源性NPCs增殖、向缺血周边区域迁移、分化与残存的神经元形成突触联系,通过神经环路发挥生理功能[10]。脑内内源性NPCs的增殖、迁移、分化等活动主要依赖于其周围独特而相对稳定的微环境,即小生境[11]。活化的小胶质细胞是脑内神经发生小生境的重要组成部分,过度活化的小胶质细胞可以产生一系列炎症介质,引发脑内过度炎症反应,从而减弱脑内NPCs的增殖和分化[12, 13]。有研究发现,使用抗炎类药物可以逆转脑缺血/再灌注后炎症反应,导致的脑内神经细胞增殖减弱[5, 6]。此外,Bastos等[14]使用脂多糖诱导大鼠脑组织的神经性炎症反应,结果发现脂多糖降低了大鼠海马DG新生细胞的存活率,应用COX-2的选择性抑制剂NS398干预后,海马DG新生细胞的存活率得到改善,提示脂多糖降低新生细胞存活率的机制可能与其提高了COX-2的表达有关。中药单体黄芩苷,具有抗炎、清除氧自由基、神经保护等药理功能,而且体外研究中已发现其可以促进NPCs增殖,诱导间充质干细胞分化为神经元。本研究观察黄芩苷对全脑缺血/再灌注大鼠认知功能的影响,探讨其可能机制是否与抑制脑组织COX-2蛋白的表达,维持脑内NPCs增殖相对稳定的小生境有关。
采用Morris水迷宫试验观察大鼠的学习记忆功能,结果显示,I/RB组大鼠平均逃避潜伏期比I/R组大鼠明显缩短(P<0.05),且I/RB组大鼠在目标象限的滞留时间和穿越平台次数比I/R组大鼠明显增多(P<0.01),表明黄芩苷能够改善全脑缺血/再灌注大鼠的学习记忆功能障碍。为进一步证实黄芩苷促进认知功能的恢复是否与其促进脑内NPCs增殖有关,本研究采用BrdU腹腔注射法标记海马DG和侧脑室SVZ增殖的NPCs。BrdU是胸腺嘧啶脱氧核苷类似物,可以在注射BrdU的时间内,被正在进行DNA合成的NPCs摄取,加入到新的DNA核苷酸链中,标记具有增殖能力的NPCs[15]。结果显示,I/RB组大鼠海马DG和侧脑室SVZ的BrdU阳性细胞个数均明显多于I/R组大鼠(P<0.01),表明黄芩苷能够促进全脑缺血/再灌注大鼠脑内内源性NPCs增殖。同时Western blot 结果显示,I/RB组大鼠脑组织COX-2蛋白的表达水平较I/R组大鼠明显降低(P<0.01),提示黄芩苷能够抑制全脑缺血/再灌注大鼠脑组织内产生的过度炎症反应,维持内源性NPCs增殖小生境的相对平衡。
总之,我们的研究结果显示,黄芩苷可能通过抑制全脑缺血/再灌注后脑组织COX-2蛋白的表达,促进脑内内源性NPCs的增殖,从而改善全脑缺血/再灌注大鼠的认知功能障碍,其具体机制需要进一步深入研究。
(致谢:本实验在重庆医科大学附属第一医院实验中心完成,感谢实验中心各位老师的指导和帮助。)
| [1] | Aridsson A, Collin T, Kirik D, et al. Neuronal replacement from endogenous precursors in the adult brain after stroke [J]. Nat Med, 2002, 8(5):491-500. |
| [2] | 迟戈夫, 丁丽常, 丽 敏. 目前国内黄芩苷药理研究进展 [J].内蒙古民族大学学报(自然科学版),2005,20(2):207-9. Chi G F, Ding L C, Li M. The present domestic pharmacological advance on scutellaria baicalensis [J].J Inner Mongolia Univ Nationalit,2005, 20(2):207-9. |
| [3] | Jia Y, Yang Y, Zhou Y, et al. Differentiation of rat bone marrow stromal cells into neuron induced by baicalin [J]. Nat Med J China, 2002, 82(19):1337-41. |
| [4] | Yan X H, Huang R B. Differentiation of human umbilical cord blood mesenchymal stem cells toward neurons induced by baicalin in vitro [J]. Chin J Pediatr, 2006,44(3):214-9. |
| [5] | Hoehn B D, Palmer T D, Steinberg G K. Neurogenesis in rats after focal cerebral ischemia is enhanced by indomethacin [J]. Stroke, 2005,36(12):2718-24. |
| [6] | Liu Z, Fan Y, Won S J, et al. Chronic treatment with minocycline preserves adult new neurons and reduces functional impairment after focal cerebral ischemia [J].Stroke, 2007,38(1):146-52. |
| [7] | Cheng O, Li Z H, Han Y, et al. Baicalin improved the spatial learning ability of global ischemia/reperfusion rats by reducing hippocampal apoptosis [J]. Brain Res, 2012,1470:111-8. |
| [8] | Vorhees C V, Williams M T. Morris water maze:procedures for assessing spatial and related forms of learning and memory [J]. Nature Protocols, 2006,1(2):848-58. |
| [9] | Kee N J, Preston E, Wojtowicz J M. Enhanced neurogenesis after transient global ischemia in the dentate gyrus of the rat [J].Exp Brain Res, 2001,136(3):313-20. |
| [10] | Gould E, Reeves A J, Fallah M, et al. Hippocampal neurogenesis in adult Old World primates [J]. Proc Natl Acad Sci USA, 1999,96(9):5263-7. |
| [11] | Fuchs E, Tumbar T, Guasch G. Socializing with the neighbors:stem cells and their niche [J]. Cell, 2004, 116(6):769-78. |
| [12] | Graciarena M, Depino A M, Pitossi F J. Prenatal inflammation impairs adult neurogenesis and memory related behavior through persistent hippocampal TGFβ1 downregulation [J]. Brain Behav Immun, 2010, 24(8):1301-9. |
| [13] | Das S, Dutta K, Kumawat K L, et al. Abrogated inflammatory response promotes neurogenesis in a murine model of Japanese encephalitis [J]. PLoS One, 2011,6(3):e17225 |
| [14] | Bastos G N, Moriya T, Inui F, et al. Involvement of cyclooxygenase-2 in lipopolysaccharide induced impairment of the newborn cell survival in the adult mouse dentate gyrus [J]. Neuroscience, 2008, 155(2):454-62. |
| [15] | Miller M W, Nowakowski R S. Use of bromodeoxyuidine-immunohistochemistry to examine the proliferation and time of origin of cells in the central nervous system [J].Brain Res,1988,457(1):44-52. |