2. 安徽医科大学附属省立医院, 安徽 合肥 230001
魏伟(1960-),男,博士,教授,博士生导师,研究方向:抗炎免疫药理学,通讯作者,E-mail:wwei@ahmu.edu.cn
2. Affiliated Anhui Provincial Hospital, Anhui Medical University, Hefei 230001, China
糖尿病肾病 (diabetic nephropathy,DN)是糖尿病最常见、最严重的微血管并发症之一,也是造成终末期肾病 (ESRD) 的最常见原因之一,约有20%-40%的糖尿病患者最终会发展到糖尿病肾病阶段[1]。早期DN以肾小球高滤过和尿微量白蛋白为特征,随着疾病发展逐渐产生肾小球萎缩、肾小球和肾小管基底膜增厚、细胞外基质堆积和系膜肿胀变形等,最终导致慢性肾功能不全,直接影响糖尿病患者的生活质量及威胁其生命[2]。早期以微量白蛋白尿为特征,此期如采取措施、积极防治,可延缓或阻止其进入临床蛋白尿期。而一旦出现临床蛋白尿,则肾功能损害的速度将加快,所以探讨糖尿病肾病的早期防治方法则显得尤为重要[3]。血管内皮生长因子 (vascular endothelial growth factor,VEGF) 是一种内皮细胞特异性的丝裂原,已发现VEGF与DN的发生发展密切相关。有研究表明,系膜区VEGF表达增加可促进系膜区蛋白外渗,血管外基质增加而导致系膜区体积增大。另外,VEGF也可引起内皮细胞形态改变,通过影响细胞信号转导及细胞间转运来调节蛋白尿的形成[4]。给与VEGF单克隆抗体或血管生成抑制剂可缓解实验性糖尿病鼠肾高滤过、肾脏萎缩、肾重和白蛋白排泄,提示VEGF与糖尿病肾病阶段的血管结构改变,血管新生有关[5]。因此,抑制VEGF的过表达对延缓DN的发生、发展和转归有着重要的理论意义和临床价值。
小檗碱 (berberine,BBR) 是从毛茛科植物黄干燥根状茎及黄柏皮中提取的一种异喹啉生物碱类。研究表明,BBR具有降低血糖、降脂及内皮依赖性舒张血管等作用。本课题组前期的实验和相关的研究表明,BBR可改善DN大鼠肾功能,减少蛋白尿的产生,这表明BBR可以减轻DN大鼠肾损害,但该作用的确切机制并不明确[6]。本研究在前期模型诱导实验的基础上加以改进,建立了更为合适的DN大鼠模型,观察BBR对DN大鼠肾脏中VEGF表达的影响[7]。
1 材料与方法 1.1 材料清洁级♂ SD大鼠,体质量(180±20)g (安徽医科大学实验动物中心,合格证号:皖医动第028号);普通饲料及高糖高脂饲料(安徽医科大学实验动物中心,其中高糖高脂饲料配方为:基础饲料64.0%,猪油8.0%,蛋黄粉10.0%,蔗糖18.0%,胆酸钠1.0%);STZ(美国Sigma公司);小檗碱(安徽省立医院药剂科提供,含量大于96.5%)。兔抗VEGF多克隆抗体(bs-1313R,北京博奥森生物技术有限公司),DAB显色试剂盒(批号:K145619C,北京中山金桥生物技术有限公司);SP9000通用性SP检测试剂盒(批号:WK141515,北京中山金桥生物技术有限公司);超敏ECL化学发光显色试剂盒(34094,Thermo scientific)。
1.2 实验性SD大鼠模型的制备及分组♂SD大鼠60只,适应性喂养1周后,改用高糖高脂饲料喂养6周,诱发产生胰岛素抵抗。禁食不禁水12 h后,测定血糖作为基础血糖,然后按35 mg·kg-1 剂量腹腔注射STZ诱导建立DN大鼠模型,72 h后尾静脉检测空腹血糖。造模成功大鼠随机分为:DN组,BBR(50 mg·kg-1)、BBR(100 mg·kg-1) 和BBR(200 mg·kg-1) 治疗组,每组12只,继续喂以高糖高脂饲料8周。另设正常对照组,喂以基础饲料。各治疗组均灌胃给药相应浓度小檗碱,正常组和对照组以等量溶媒(0.5% CMC-Na) 灌胃,每日1次,连续8周。
1.3 指标观察及方法 1.3.1 生化指标检测采用爱乐芬血糖仪配套试纸测定大鼠空腹血糖(FBG)水平,记录各组大鼠的血糖变化。给药8周后,同时测定各组大鼠血肌酐和尿素氮的含量。给药8周结束后,将大鼠放入代谢笼中,收集24h尿液,取上清,测定尿总蛋白(UTP)含量。取部分肾脏,10%甲醛溶液固定后切片,待做PAS染色和免疫组化分析。
1.3.2 肾脏病理学检查取实验大鼠肾脏组织,置于冰台用 PBS冲洗干净,除去包膜,滤纸吸干,取左肾沿冠状面剖开,投入10%甲醛中性缓冲溶液固定,石蜡包埋,3μm切片,常规用二甲苯脱蜡至水,加入0.5%~1%高碘酸氧化,Schiff液避光染色,0.5%偏重亚硫酸钠(钾)浸洗,苏木精染色,1%盐酸酒精分化,1%氨水返蓝,常规脱水,二甲苯透明,中性树胶封固。显微镜下观察组织病理学改变情况。
1.3.3 肾脏VEGF免疫组织化学分析按照通用型过氧化物酶标记的链霉卵白素检测试剂盒的相关要求检测VEGF蛋白的表达。取大鼠的肾脏组织,置于体积分数为10%甲醛溶液中固定,常规石蜡包埋、3 μm切片,常规脱蜡、水化、组织抗原修复后,滴加正常山羊血清封闭,室温20 min;滴加一抗(VEGF 兔抗大鼠多克隆抗体),4℃过夜;37℃复温20 min; PBS洗3次;滴加二抗(生物素标记山羊抗兔抗体),37℃孵育 30 min;PBS洗3次;滴加辣根酶标记的链霉素卵白素工作液,37℃孵15 min;PBS洗3次;以DAB显色。苏木精复染、脱水、透明、封片、镜检。阳性物质呈棕色或褐色颗粒状,以PBS代替一抗进行阴性对照实验。采集高倍视野(×200倍)图像,Image-Pro Plus分别对切片免疫组化染色的阳性表达进行半定量分析,测定组织中蛋白染色平均光密度值并分析。
1.3.4 肾脏VEGF蛋白表达分析常规裂解肾皮质(RIPA ∶ PMSF=99 ∶ 1),提取总蛋白。蛋白定量采用考马斯亮蓝法。取20 μL样品蛋白上样,SDS/PAGE凝胶电泳分离蛋白,电转移至PVDF膜,牛奶/TPBS封闭液室温封闭2 h。放入稀释度为1 ∶ 500的一抗(VEGF多抗)中4℃过夜,次日加入1 ∶ 5万稀释度的辣根过氧化物酶标记的二抗室温孵育2 h。ECL试剂盒显影,结果用Image Quant Las 4000mini 凝胶成像系统扫描存盘,采用Image J软件进行分析。
1.4 统计学处理肾组织免疫组化切片采用Image-Pro Plus软件进行分析,Western blot结果采用Image J软件进行分析,测定平均光密度。 计量资料采用 表示,用单因素方差分析(one-way ANOVA)进行组间比较及方差分析,全部数据采用SPSS 16.0统计软件进行统计分析。
表示,用单因素方差分析(one-way ANOVA)进行组间比较及方差分析,全部数据采用SPSS 16.0统计软件进行统计分析。
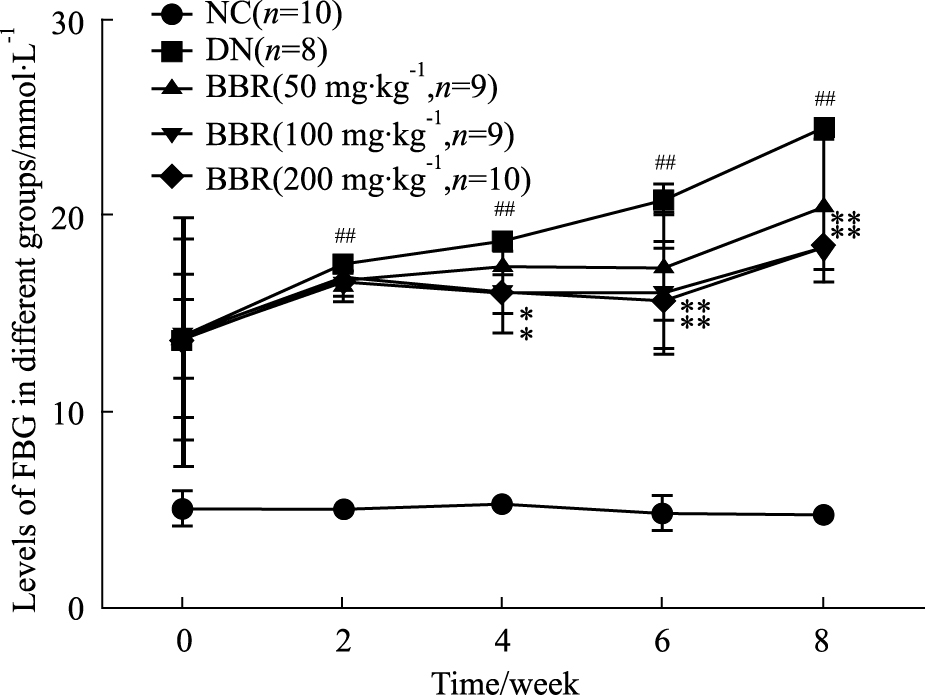
各组大鼠的经STZ造模成功后,每2周检测动物的空腹血糖水平。与正常对照组(NC)比较,模型组动物的血糖水平明显升高,差异具有统计学意义 (P<0.01);BBR中、高剂量组血糖值从4周开始明显降低,差异具有统计学意义。见Fig1。
|
Fig 1
Effect of BBR on FBG in different stage of DN rats ( )
##P<0.01 vs NC group; *P<0.05, **P<0.01 vs DN group )
##P<0.01 vs NC group; *P<0.05, **P<0.01 vs DN group
|
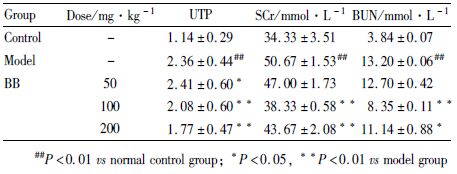
糖尿病肾病模型组血肌酐(SCr)、尿素氮(BUN)水平和尿总蛋白(UTP)量明显高于对照组(P<0.01)。BBR(50 mg·kg-1) 治疗组可以改善增高的UTP水平(P<0.05),而对血肌酐(SCr)和尿素氮(BUN)水平无明显影响;BBR(100 mg·kg-1) 与BBR(200 mg·kg-1)治疗组均可明显改善血肌酐(SCr)(P<0.01)和尿素氮(BUN)(P<0.05)水平以及尿总蛋白(UTP)(P<0.01)。见Tab1。
肾脏病理检查显示对照组肾小球、小管间质、肾血管未见明显异常,而糖尿病组出现明显的肾脏萎缩,系膜基质逐渐增多,肾小管扩张,出现肾小球硬化征象。BBR不同剂量给药后观察发现BBR(50 mg·kg-1) 治疗组并无明显变化;而BBR(100 mg·kg-1) 和BBR(200 mg·kg-1) 治疗组均显示不同程度程的肾脏体积恢复,系膜细胞肿胀减少,有效地改善了肾脏萎缩和纤维化的状态,其中BBR(200 mg·kg-1)较BBR(100 mg·kg-1) 改善作用明显。见Fig2。

|
| Fig 2 Effect of BBR on pathological changes in kidney tissue (×400) A:Normal group; B:Model group; C:BBR (50 mg·kg-1); D:BBR (100 mg·kg-1); E:BBR (200 mg·kg-1) |
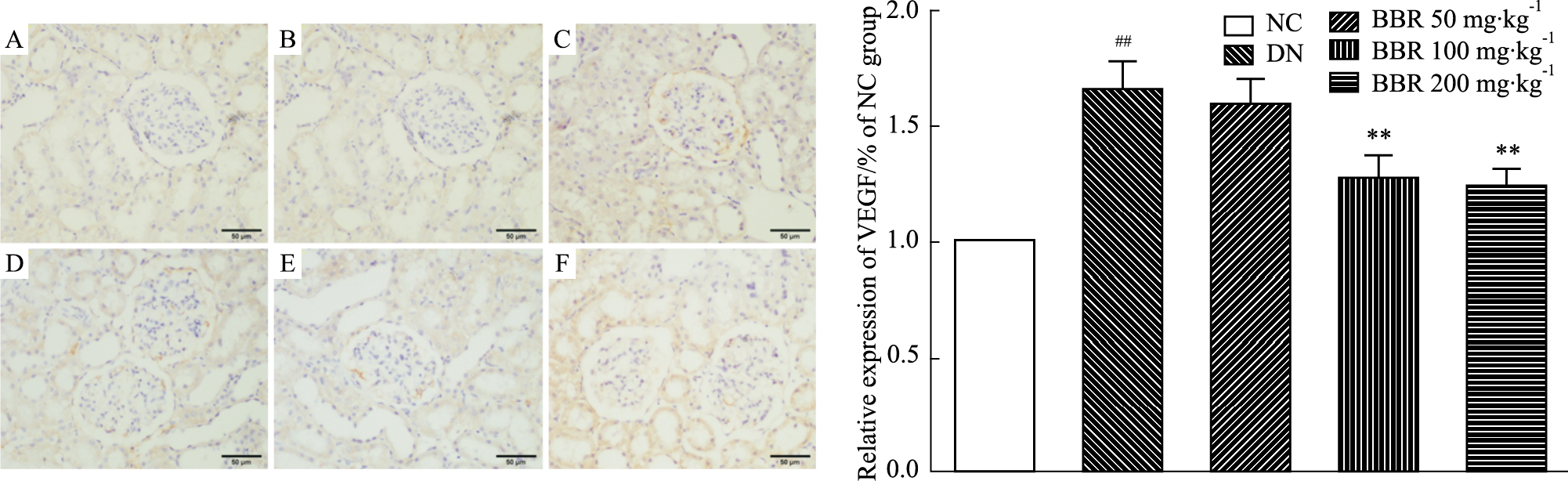
取实验大鼠肾脏进行VEGF免疫组化检查。采集高倍视野(×200倍)图像,采用Image-Pro Plus软件分别对切片免疫组化染色的阳性表达进行半定量分析,测定组织中蛋白染色平均光密度值。肾脏组织免疫组化结果显示:正常对照组大鼠肾组织VEGF的表达呈弱阳性,DN模型大鼠肾组织VEGF呈强阳性表达;BBR(50、100、200 mg·kg-1) 给药对大鼠肾脏上述指标表达有不同程度的降低作用,其中BBR(100、200 mg·kg-1) 作用效果明显,与模型组大鼠差异有显著性(P<0.01)。见Fig3。
|
| Fig 3 Effect of BBR on expression of VEGF in kidney tissue (×200) A:Negative control;B:NC;C:DN;D:BBR (50 mg·kg-1);E:BBR (100 mg·kg-1); F: BBR (200 mg·kg-1). ##P<0.01 vs NC group; **P<0.01 vs DN group |
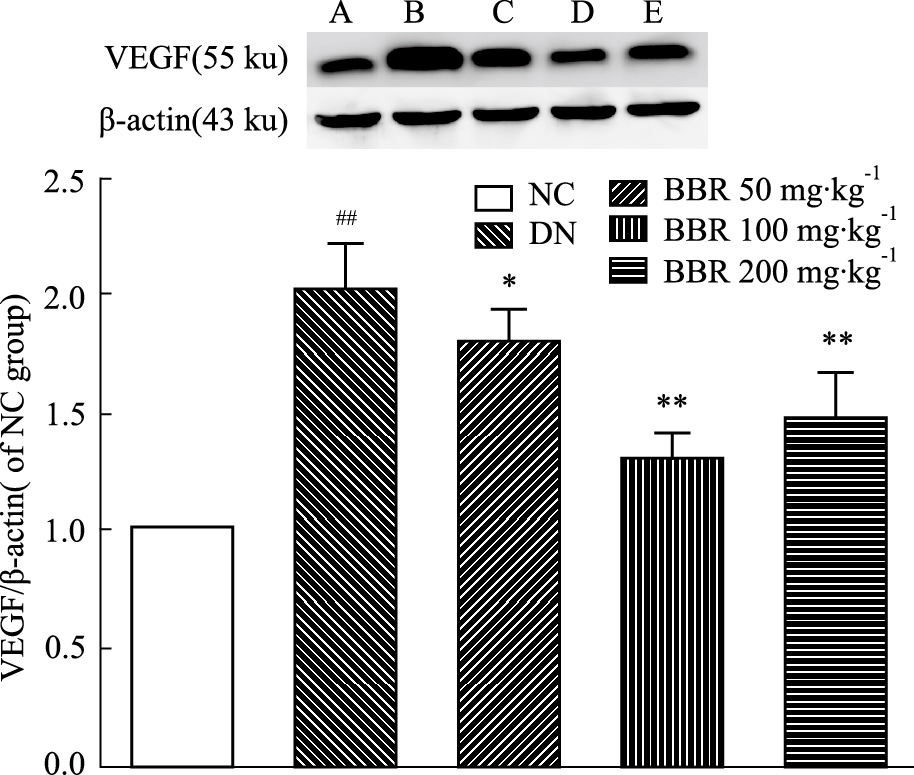
取实验大鼠肾脏进行,分离肾皮质并裂解,提取总蛋白进行VEGF的Western blot检查。采用Image J软件分别对条带进行分析。实验结果显示:DN模型大鼠肾组织VEGF 表达较正常对照组明显增加(P<0.01);BBR(50、100、200 mg·kg-1)给药对大鼠肾脏上述指标表达均产生不同程度的降低肾皮质VEGF的表达的作用,与模型组大鼠差异有显著性(P<0.05;P<0.01)。见Fig4。
|
Fig 4
Effect of BBR on the expression of VEGF in kidney tissue ( , n=4)
A:Normal group; B:Model group; C:BBR (50 mg·kg-1); D:BBR (100 mg·kg-1); E:BBR (200 mg·kg-1).##P<0.01 vs NC group; *P<0.05, **P<0.01 vs DN group , n=4)
A:Normal group; B:Model group; C:BBR (50 mg·kg-1); D:BBR (100 mg·kg-1); E:BBR (200 mg·kg-1).##P<0.01 vs NC group; *P<0.05, **P<0.01 vs DN group
|
糖尿病是一种常见的内分泌代谢障碍疾病,而糖尿病肾病(DN)是糖尿病的较为严重的并发症之一,最终可能导致慢性肾功能不全和终末期肾衰竭,直接影响患者的生活质量并严重威胁其生命[8]。DN除表现为血糖异常升高外,还常常伴有蛋白质和脂肪等的代谢紊乱和肾脏等组织病变损伤[9]。实验显示BBR可明显降低糖尿病及其并发症的血糖。另外,BBR还被证明能够降低高脂饮食动物的血清TC、TG、LDL-C、VLDL-C水平。最近,有研究证实BBR对糖尿病大鼠肾脏具有保护作用[10]。课题组前期研究发现,在糖尿病早期用BBR治疗能够明显延缓DN的发生,BBR通过抑制肾脏炎症因子的释放,减轻糖尿病时肾脏的炎症反应,从而发挥肾脏保护作用,其机制部分取决于对PGE2-EP受体相关信号通路的抑制作用[11];Domitrovic等[12]研究发现BBR对由顺铂(cisplatin,CP)诱导的肾脏损伤大鼠具有一定的肾脏保护作用,其机制可能由于BBR通过减少CYP2E1的表达以及对NF-κB通路的抑制作用所引起的,此实验中BBR发挥肾脏保护作用具有剂量依赖性。本课题组研究还发现糖尿病状态下TGF-β1的表达明显增加,不仅促进炎症因子的释放产生炎症作用,同时促进细胞外基质的主要蛋白成分如:Fibronectin和Ⅳ型胶原的合成,促进细胞外基质的堆积,引起肾小球硬化和糖尿病肾脏纤维化,而BBR治疗可以改善上述病理变化,提示BBR具有较好的保护糖尿病肾病时肾脏的作用[13]。
VEGF是一种促进血管内皮细胞生长和蛋白渗透作用的分子,参与了微血管的生理和病理过程,正常人血浆和各组织中VEGF水平较低,仅维持正常生理功能。生理状态下,肾脏组织VEGF主要表达于肾小球脏层上皮细胞(足细胞),但体外培养的肾组织固有细胞如肾小球内皮细胞和系膜细胞也存在VEGF基因,可合成和分泌一定量的VEGF蛋白[14]。目前VEGF在DN中的作用研究较少,对于VEGF在DN中的作用机制尚不清楚[15]。目前研究认为导致2 型糖尿病患者VEGF升高的机制可能在于疾病状态下的高血糖作用。血糖的异常升高一方面直接激活蛋白激酶C (PKC),使特定的转录因子磷酸化进而增加VEGF基因的转录,促进肾小球足细胞和系膜细胞中VEGF的表达;同时,高糖环境也可以促进血管紧张素转化酶基因的表达,使血液中血管紧张素II (ATII)水平明显升高。而ATII的高表达又会通过激活二酰基甘油水平活化蛋白激酶的β亚型,促进VEGF基因表达,从而刺激肾小球足细胞和系膜细胞合成并分泌VEGF[16]。也有研究认为缺氧会引起VEGF表达的增多,但其具体机制目前还不清楚。糖尿病肾病发生时患者上皮细胞损伤会产生大量VEGF,致使VEGF异常增多,引起肾小球内皮细胞与系膜细胞功能异常改变,增加肾小球通透性和肾小球滤过率从而促进蛋白外渗,血管外基质增加而导致肾小球病变,进而引起肾小球硬化和肾脏纤维化,随后引起肾脏萎缩,加重糖尿病肾病[17]。
本实验结果显示:在糖尿病肾病状态下,DN大鼠血糖水平、血肌酐、尿素氮以及尿总蛋白量等生化指标较正常对照组大鼠明显升高,同时伴有肾脏组织VEGF的表达明显增多,BBR给药可以明显降低DN大鼠肾组织VEGF的异常表达,改善了VEGF异常增多引起的肾小球功能的紊乱,降低了VEGF异常升高所引起的肾小球高滤过和尿总蛋白堆积,从而减轻VEGF对肾小球和肾间质的损伤,提示对VEGF蛋白水平的影响可能是BBR发挥肾脏保护作用和治疗DN大鼠的机制之一。同时BBR发挥治疗作用提示我们中药小檗碱在糖尿病及其并发症的治疗上具有重要的研究价值。
(致谢:本实验完成于安徽医科大学临床药理研究所实验室,实验过程中得到临床药理研究所全体老师和同学的帮助。实验中所涉及的病理技术得到安徽省立医院病理科胡闻老师的技术支持,在此表示感谢。)
| [1] | Sidaway P. Diabetic nephropathy:Heparanase mediates renal injury [J]. Nat Rev Nephrol, 2014, 10(9):483. |
| [2] | Ni W J, Tang L Q, Wei W. Research progress in signalling pathway in diabetic nephropathy [J]. Diabetes Metab Res Rev, 2015,31(3):221-33. |
| [3] | 汪建云, 王栋栋, 陆昭磊, 等.四氢生物蝶呤在2型糖尿病肾病小鼠肾脏NO生成中的作用 [J].中国药理学通报, 2014,30(4):514-9. Wang J Y, Wang D D, Lu Z L, et al. Effects of tetrahydrobiopterin on NO production in the kidney of type 2 diabetic nephropathy mice [J]. Chin Pharmacol Bull, 2014,30(4):514-9. |
| [4] | Senthil D, Choudhury GG, McLaurin C, et al. Vascular endothelial growth factor induces protein synthesis in renal epithelial cells:a potential role in diabetic nephropathy [J]. Kidney Int, 2003, 64(2):468-9. |
| [5] | de Vriese A S, Tilton R G, Elger M, et al. Antibodies against vascular endothelial growth factor improve early renal dysfunction in experimental diabetes [J]. J Am Soc Nephrol, 2001, 12(5):993-1000. |
| [6] | Yang Y, Ni W, Cai M, et al. The renoprotective effects of berberine via the EP4-Galphas-cAMP signaling pathway in different stages of diabetes in rats [J]. J Recept Signal Transduct Res, 2014:1-11. |
| [7] | 杨 洋, 唐丽琴, 倪伟建, 等. 小檗碱对糖尿病肾病大鼠病程中肾脏转化生长因子-β1与白细胞介素-18表达的影响 [J]. 中国药学杂志, 2014,49(17):1513-8. Yang Y, Tang L Q, Ni W J, et al. Effect of berberine on renal expression of transforming growth factor-β1 and interleukin-18 in different stages of diabetic nephropathy rats [J]. Chin Pharm J, 2014,49(17):1513-8. |
| [8] | 曹延萍, 刘青娟, 任韫卓, 等. 氯沙坦抑制转录因子GADDl53/CHOP的激活在糖尿病大鼠肾脏中的保护作用 [J]. 中国药理学通报, 2011,27(5):617-22. Cao Y P, Liu Q J, Ren Y Z, et al. Losartan provides protection on the kidney of diabetic rats by inhibiting the expression of GADDl53/CHOP [J]. Chin Pharmacol Bull, 2011,27(5):617-22. |
| [9] | Tang L Q, Liu S, Zhang S T, et al. Berberine regulates the expression of E-prostanoid receptors in diabetic rats with nephropathy [J]. Mol Biol Rep, 2014, 41(5):3339-47. |
| [10] | Zhang Y, Li X, Zou D, et al. Treatment of type 2 diabetes and dyslipidemia with the natural plant alkaloid berberine [J]. J Clin Endocrinol Metab, 2008, 93(7):2559-65. |
| [11] | Tang L Q, Wang F L, Zhu L N, et al. Berberine ameliorates renal injury by regulating G proteins-AC-cAMP signaling in diabetic rats with nephropathy [J]. Mol Biol Rep, 2013, 40(6):3913-23. |
| [12] | Domitrovic R, Cvijanovic O, Pernjak-Pugel E, et al. Berberine exerts nephroprotective effect against cisplatin-induced kidney damage through inhibition of oxidative/nitrosative stress, inflammation, autophagy and apoptosis [J]. Food Chem Toxicol, 2013, 62:397-406. |
| [13] | Wang F L, Tang L Q, Yang F, et al. Renoprotective effects of berberine and its possible molecular mechanisms in combination of high-fat diet and low-dose streptozotocin-induced diabetic rats [J]. Mol Biol Rep, 2013, 40(3):2405-18. |
| [14] | 魏倩萍, 邓华聪, 赵 劼. p38MAPK信号通路在大鼠肾小球系膜细胞表达VEGF中的作用 [J]. 重庆医学, 2005, 34(1):16-8. Wei Q P, Deng H C, Zhao J. A role of p38 mitogen-activated protein kinase (P38MAPK) for expression of VEGF in rat mesangial cells [J]. Chongqing Yi xue, 2005, 34(1):16-8. |
| [15] | 乔 进, 窦志华, 吴 锋, 等. 灵芝多糖联合二甲双胍预防糖尿病大鼠主动脉病变及对VEGF表达的影响 [J]. 中国药理学通报, 2014, 30(8):1079-84. Qiao J, Dou Z H, Wu F, et al. Effect of combination of ganoderma lucidum polysaccharide and metformin on aortic lesions and expression of VEGF in type 2 diabetic rats [J]. Chin Pharmacol Bull, 2014, 30(8):1079-84. |
| [16] | Tsuzuki Y, Fukumura D, Oosthuyse B, et al. Vascular endothelial growth factor (VEGF) modulation by targeting hypoxia-inducible factor-1alpha - -> hypoxia response element - -> VEGF cascade differentially regulates vascular response and growth rate in tumors [J]. Cancer Res, 2000, 60(22):6248-52. |
| [17] | Yang K S, Lim J H, Kim T W, et al. Vascular endothelial growth factor-receptor 1 inhibition aggravates diabetic nephropathy through eNOS signaling pathway in db/db mice [J]. PLoS One, 2014, 9(4):e94540. |