2. 蚌埠医学院安徽省感染与免疫重点实验室, 安徽 蚌埠 233030
潘治宇(1983-),女,硕士生,研究方向:免疫性疾病的发病机制,共同第一作者,E-mail:panzhiyu969@sohu.com
2. Dept of Infection and Immunity Key Laboratory of Anhui Province, Bengbu Medical College, Bengbu Anhui 230030, China
树突状细胞(dendritic cells,DC)由美国学者Steinman于1973年发现,因其在成熟时伸出许多树突状或伪足状突起而得名[1],是迄今所知的抗原提呈能力最强大的抗原提呈细胞(antigen presenting cell,APC)[2]。目前研究证实在一些自身免疫性疾病的发生、发展中DC发挥了一定的作用。DC可以通过分泌各种具有功能效应的细胞因子,并诱导T细胞激活和分化。DC的微生物识别功能主要依赖于表达在其表面I型跨膜蛋白Toll样受体(TLR)。TLRs可识别多种多样的微生物分子结构,如细胞壁成分、核酸以及微生物合成的化合物[3]。表达在DC表面的TLRs,在调节DC的分化成熟、分泌各种免疫调节细胞因子、激活初始型T细胞,以及启动免疫应答等方面起着重要的作用[4]。因此,调控DCs表面TLR的表达就可以调节DC的成熟状态和免疫功能,进而影响机体的免疫反应和免疫耐受。
内吗啡肽 (endomorphins,EMs)于1997 年由美国神经生物学家 Zadina 等首次报道,并根据结构不同,分为1型(endomorphin-1,EM-1)和2型(endomorphin-2,EM-2)。EMs对Mu阿片受体亲和力和选择性远远高于其它生物活性肽,被认为是Mu阿片受体的内源性配体[5]。EM显著的作用是其镇痛作用,但目前大量证据表明其亦参与机体的免疫调节[6]。有研究报道,EM-1影响DC的免疫功能和成熟,本实验旨在观察EM-1对DC的影响作用是否与DC表面的TLR2和TLR4有关。
1 材料与方法 1.1 材料 1.1.1 实验标本DC培养所用健康人血样取自本校学生志愿者,年龄18~23岁(平均20岁)。每份标本的采集均征得本人书面同意。
1.1.2 药品与试剂DNA MarkerⅠ和总RNA提取试剂(TRIzol) 均购于北京天根公司;焦炭酸二乙酯(DEPC)原液,购于美国Sigma公司;FITC 标记的抗人CD11 抗体购于美国Caltag公司;TLR2、TLR4、β-actin内参引物,购于南京金凯瑞生物科技公司;RNA抽提试剂盒,购于立陶宛Fermentas公司;DNA聚合酶,购于日本TaKaRa公司;琼脂糖、溴化乙锭(EB)购于美国Sigma公司。
1.2 方法 1.2.1 人外周血DC诱导培养抽取健康志愿者的外周静脉血20 mL,肝素钠抗凝。PBS等比稀释,将稀释后血样移入淋巴细胞分离液中,进行密度离心(20℃,2 000 r·min-1,20 min),取界面的白膜细胞,用PBS悬浮细胞,离心洗涤2次,再用RPMI 1640液体培养基悬浮细胞,调整细胞浓度为1×1010·L-1,加入24孔板中[7],37℃、5% CO2孵箱贴壁培养3 h后,弃上清,用RPMI 1640轻洗2遍,贴壁细胞即为单核细胞。悬浮细胞多为淋巴细胞。贴壁的单核细胞加入RPMI 1640完全培养基,采用rhGM-CSF和rhIL-4联合刺激(终浓度均为106 U·L-1),37℃、5%CO2的孵箱中培养3 d后,轻轻吸弃未贴壁细胞,补充等量细胞因子和新的培养基继续培养至6 d,分组加入脂多糖(LPS,100 μg·L-1)或EM-1(1×10-6 mol·L-1)刺激,刺激48 h后,收集细胞即为正常人外周血来源的DC。
1.2.2 实验分组在细胞培养d 6,将细胞分成4组,BLA组:空白对照组,培养过程中不加LPS及EM-1;EM-1组:培养d 6加入EM-1;LPS组:LPS实验对照组(培养d 6加入LPS);LPS+EM-1组:培养d 6加入LPS和EM-1。在实验中LPS的用量均为100 μg·L-1,EM-1的用量均为1×10-6 mmol·L-1。
DC的鉴定:①形态:在细胞培养过程中,采用倒置显微镜观察细胞的形态和结构变化。②流式细胞术:将收集的悬浮细胞,调整细胞浓度为1×109·L-1,加入流式管中,再分别加入FITC 标记的抗人CD11 抗体以及同型对照FITC 标记的IgG1,避光染色30 min 后,PBS 洗涤3 次,加入300 μL浓度 20 g·L-1 多聚甲醛,运用流式细胞术检测DC成熟表型,Cellsquest 软件获取并分析数据。
1.2.3 流式细胞术检测EM-1对DC表面TLR2、TLR4表达的影响收集d 8各组细胞,并用抗CD11c FITC、抗TLR2 PE、抗TLR4 PE荧光标记抗体染色,留取空白管和同型对照管。FACS Calibur流式细胞仪(BD公司)上机检测,CellQuest软件和Flow Jo软件分析数据。
1.2.4 RT-PCR法检测EM-1对DC中TLR2﹑TLR4 mRNA表达的影响将相同组的DC细胞加2 mL TRIzol,氯仿混匀,加异丙醇离心,加75%的乙醇(预冷)洗涤RNA沉淀后离心。再加DEPC水溶解,60℃下孵育10 min助溶。取出2 μL原液置于核酸蛋白测定计算器上,紫外光度仪检测OD260/OD280值和RNA的浓度。取总RNA移入EP管,加入oligo(dT)18 primer,去离子水至12 μL。进行以下反应:65 ℃孵育5 min后置于冰上。依次加入Reaction Buffer、RiboLock RNase inhibitor、10 M Dntp mix。37℃孵育5 min后置于冰上。然后加M-MLV逆转录酶 1 μL ,至20 μL,混匀后离心;42℃孵育60 min,最后 70℃、10 min以终止反应。即获得cDNA,立即进行PCR。引物使用Primer Premier 5.0软件设计,PubMed BLAST验证。南京金凯瑞公司生物科技公司合成。各因子及内参照引物序列、产物长度如Tab1所示。
应用琼脂糖凝胶电泳对扩增产物进行电泳分析。将凝胶电泳图像输入凝胶分析系统,结果以条带灰度值表示,并选择β-actin作为内参,在同样条件下扩增,其表达与细胞总RNA呈正比,以电泳图中各组TLR2、TLR4分别与β-actin的条带灰度值比值作为目的基因表达相对水平,计算目的条带与内参条带灰度值之比。
1.3 统计学分析采用单因素方差分析对结果进行统计分析,用SPPS 17.0软件完成。
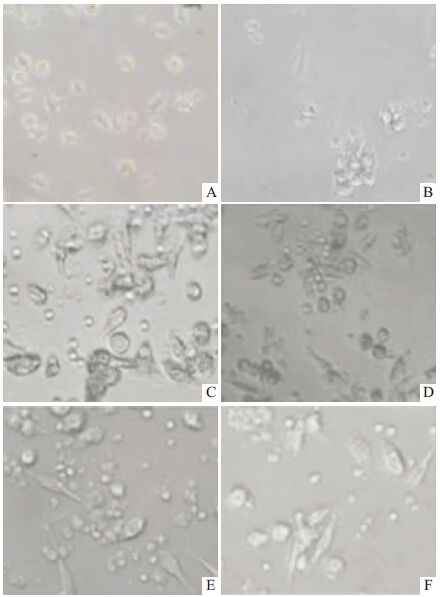
2 结果 2.1 细胞形态学观察人外周血分离的单核细胞在rhGM-CSF和rhIL-4的联合刺激下可分化成未成熟DC,在此过程中,细胞形态会发生变化。倒置相差显微镜下观察可见,培养d 3细胞出现毛刺状突起,随着培养时间延长,DC体积逐渐增大,在d 6突起数量减少,突起增长,呈长梭形,呈贴壁集落式生长。加入LPS约48 h后,部分细胞呈长梭形、条索状,部分细胞形态趋向恢复球形,基本已呈悬浮状生长。但是与对照组相比,EM-1干预后DC形态学变化不明显(Fig1)。
|
| Fig 1 Morphological changes of DC in the induced differentiation process A:imDC in day 3(400×);B: imDC in day 6(200×);C:BLA group DC in day 8(200×);D:EM-1 group DC in day 8(200×);E: LPS group DC in day 8(200×);F: LPS+EM-1 group DC in day 8(200×). Seen under the microscope, with the increased incubation time, the volume of DC increased, the number of projections reduced in the day 6, the length of projections increased. After added LPS approximately 48 h, some cells expressed as fusiform, cords, partially restored cell morphology. However, compared with the control group, the DC morphology did not change significantly in EM-1 group. |
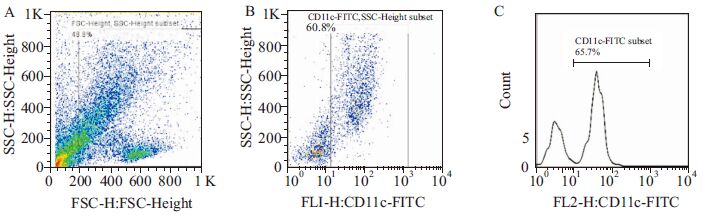
流式细胞术检测培养d 8 DC的表型分子CD11c+细胞率,结果显示DC纯度可高达70%,同时镜下观察DC细胞形态典型,进一步证实了本实验外周血来源DC体系建立(Fig2)。
|
| Fig 2 Purity of DC detected by flow cytometry A: Dot plot of DC; B: Dot plot of CD11c+ DC; C: Histogram of CD11c+ DC |
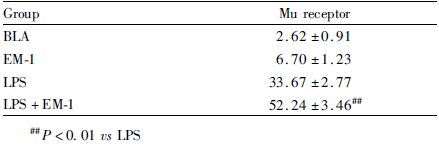
流式细胞术检测证实,Mu受体在DC中均有表达,Mu受体在imDC表达较低,并且EM-1干预可引起imDC上的Mu受体表达数目上调,但差异无统计学意义(P>0.05),在致炎因子LPS作用下,EM-1干预后DC的Mu阿片受体的数目上调明显(P<0.01)(Tab2、Fig3)。

|
| Fig 3 Expression of Mu receptor on DC surface A: BLA group;B: EM-1 group;C: LPS group;D: LPS+EM-1 group |
结果显示,TLR2、TLR 4在imDC表面表达较高,随着DC成熟表达下降。与BLA组相比,EM-1组DC上的TLR2、TLR4表达下调(P<0.05);与LPS组相比,LPS+EM-1组DC表面TLR2、TLR4受体均明显下调(P<0.01),见Tab3。
RT-PCR结果显示,与BLA组相比,EM-1干预后引起DC TLR2 mRNA表达明显降低(P<0.01),TLR4 mRNA的变化差异无统计学意义(P>0.05);与LPS组相比,LPS+EM-1组 DC上TLR2 mRNA、TLR4 mRNA均有所下调(P<0.05),见Fig4。

|
| Fig 4 Expressions of TLR2 mRNA (A) and TLR4 mRNA (B) in DC 0: Marker; 1: BLA group; 2: EM-1 group; 3: LPS group; 4: LPS+EM-1 group. In Fig 4A, β-actin (upper), TLR2 mRNA (lower). In Fig 4B, β-actin (upper), TLR4 mRNA (lower). |
DC是免疫系统中功能最强的抗原提呈细胞,可以激活初始T细胞,具有激发免疫应答和诱导免疫耐受的双重作用[8, 9]。DC在成熟过程中分为前体、未成熟、成熟3个阶段,不同阶段抗原提呈能力有所不同。未成熟阶段具有强大抗原摄取能力,但因细胞表面协同刺激因子低表达,诱导T细胞能力较弱。成熟DC表面MHC-Ⅱ分子和协同刺激分子表达增加,抗原提呈能力增强,对T细胞的诱导能力亦明显增加,启动免疫应答。
有研究表明,μ阿片受体(μ-opioid receptor,MOR)在多种免疫细胞表面表达,可以介导阿片肽 对免疫细胞的作用。DC作为功能最强大的APC,亦有MOR的表达[10]。本实验研究证实,Mu受体在DC中均有表达,在致炎因子LPS作用下,EM-1干预后DC的Mu阿片受体的数目上调明显(P<0.01),与相关研究结果相符[11]。EM-1对Mu阿片受体亲和力和选择性远高于其它生物活性肽,不仅参与炎症反应,还可通过改变细胞因子的产生对APC进行调控,这种调控方式可能通过抑制DC的趋化性进而抑制DC对T淋巴细胞的激活作用[12]。另有文献显示,在大鼠诱发性关节炎模型中,炎症爪局部组织和淋巴结及分泌的滑液中,均发现 EMs的水平有所升高,同时伴有MOR的高表达[13, 14]。本研究中心前期相关研究证实,经LPS及EM-1刺激后小鼠DC表面MHC表达增加[12],那么EM-1是否还可以通过其他途径来调控DC的免疫作用呢?本实验针对研究较多的DC表面的TLR进行研究。TLR是DC和其他免疫细胞识别病原微生物特征的传感器,能够与病毒DNA或细菌细胞壁成分(如LPS)等结合,激活免疫系统的第一道防线,即先天性免疫应答,引起炎症;由TLR途径产生的先天性免疫信号经由DC继而引发以T和B淋巴细胞反应为主的获得性免疫应答,其在启动和调节天然免疫及诱导获得性免疫中起到重要作用[15, 16]。本文结果显示,TLR2、TLR4在imDC表面表达较高,随着DC的成熟其表达下降。并且与BLA组(imDC组)相比,EM-1干预可引起DC上的TLR2、 TLR4表达下调;EM-1和LPS共培养,使DC表面TLR2、TLR4受体明显下调。RT-PCR结果显示,与Blank组相比,EM-1的干预可引起DC表面 TLR2 mRNA表达降低,而TLR4 mRNA的变化差异无统计学意义;与LPS组相比,LPS+EM-1组 DC上的TLR2 mRNA、TLR4 mRNA均有所下调,提示EM-1能下调DC 表面TLR2、TLR4的表达。TLRs是天然免疫和获得性免疫的桥梁,可激活机体的天然免疫和获得性免疫。表达于DC表面上的TLR2和TLR4参与了DC分化成熟的调节,TLR2和TLR4活化后可经过信号转导途径促进DC的分化成熟,并释放细胞因子调节T细胞的分化。因此,抑制DC表达TLR2和TLR4可能会在一定程度上阻断或减少它们对DC的活化作用,从而达到抑制DC的抗原提呈作用。
| [1] | Steinman R M,Cohn Z A. Identification of novel cell type in peripheral lymphoid organs of mice:morphology, quantification,tissue distribution[J]. J Exp Med, 1973, 137(5):1142-62. |
| [2] | Ibrahim M A, Chain B M, Katz D R. The injured cell:the role of the dendritic cell system as a sentinel receptor pathway[J]. Immunol Today, 1995, 16(4):181-6. |
| [3] | Sandor F,Buc M.Toll-like receptors.I.Structure,function and their ligands[J]. Folia Biol(Praha),2005,51(5):148-57. |
| [4] | Akira S,Takeda K,Kaisho T. Toll-like receptors:critical proteins linking innate and acquired immunity[J]. Nat Immunol, 2001,2(8):675-80. |
| [5] | 李小莉,牛 乐,吕伯昌,等.大鼠内吗啡肽2和μ阿片受体参与内脏感觉和运动调控的形态学证据[J].神经解剖学杂志,2010,26(3):233-8. Li X L,Niu L,Lü B C,et al. Morphological evidence for endomorphine 2 and μ opioid receptor involved in modulation of visceral sensation and movement in the rat[J].Chin J Neuroanat, 2010, 26(3):233-8. |
| [6] | Borner C, Stumm R, Hollt V, et al. Comparative analysis of mu-opioid receptor expression in immune and neuronal cells[J]. J Neuroimmunol, 2007, 188(1-2):56-63. |
| [7] | 王 婧,苏良香,朱天峰. 子痫前期患者外周血树突状细胞对Th1/Th17 细胞分化的影响[J]. 细胞与分子免疫学杂志,2013,29(7):744-7. Wang J,Su L X,Zhu T F. Effect of dendritic cells on the differentiation of Th1/Th17 in peripheral blood from preeclampsia patients[J].Chin J Cell Mol Immunol, 2013,29(7):744-7. |
| [8] | Soncin F,Mattot V,Lionnetong F, et al.VE-statin,an endothelial repressor of smooth muscles cell migration[J]. EMBO J,2003,22(21):5700-11. |
| [9] | Park L H,Schmidt M,Jin S W, et al.The endothelial-cell-derived secreted factor EGFL7 regulates vescular tube formation[J]. Natrue, 2004,428(6984):754-8. |
| [10] | Makarenkova V P, Esche C, Kost N V, et al. Identification of delta-and mu-type opioid receptors on human and murine dendritic cells[J]. J Neuroimmunol, 2001,117(1-2):68-77. |
| [11] | Kraus J,Borner C,Giannini E,et al. The role of nuclear factor kappaB in tumor necrosis factor-regulated transcription of the human mu-opiod receptor gene[J]. Mol Pharmacol,2003,64(4):876-84. |
| [12] | 李正红,于 影,杨 锐,等.内吗啡肽对小鼠树突状细胞免疫功能的影响[J].中国药理学通报,2011,27(7):939-43. Li Z H,Yu Y,Yang R, et al. Effect of endomorphins on immunologic function of mouse bone marrow-derived dendritic cells[J].Chin Pharmacol Bull, 2011,27(7):939-43. |
| [13] | Mousa S A, Machelska H, Schafer M, et al. Immunohistochemical localization of endomorphin-1 and endomorphin-2 in immune cells and spinal cord in a model of inflammatory pain[J]. J Neuroimmunol, 2002,126(1-2):5-15. |
| [14] | Jessop D S, Richards L J, Harbuz M S. Opioid peptides endomorphin-1 and endomorphin-2 in the immune system in humans and in a rodent model of inflammation[J]. Ann NY Acad Sci, 2002, 966:456-63. |
| [15] | Thornton C A, Morgan G. Innate and adaptive immune pathways to tolerance[J].Nestle Nutr Workshop Ser Pediatr Program,2009, 64:45-57. |
| [16] | Takeda K, Kaisho T, Akira S. Toll-like receptors[J].Annu Rev Immunol,2003,21(4):335-76. |



 ,n=6)
,n=6)