


刘叔文(1972-),男,博士,教授,博士生导师,研究方向:抗病毒与免疫学,E-mail:liusw@smu.edu.cn
自2008年以来,乳腺癌每年在世界范围内的发病率和死亡率分别为20%和14%,是妇女最常见的癌死亡病因[1]。恶性肿瘤的发生不仅仅是肿瘤细胞自身的问题,而且与其间质关系密切[2, 3]。间质是肿瘤生长的微环境,由正常细胞和肿瘤细胞分泌的细胞外蛋白和非转化的宿主细胞组成。间质变化以细胞外基质蛋白和细胞组分的改变为特征,其在乳腺发育、哺乳和乳腺癌过程中发生。通常肿瘤乳腺间质和正常乳腺间质不同,肿瘤乳腺硬度增长是细胞外基质蛋白数量和质量改变的结果,并导致导管上皮内信号通路组分改变,促进了肿瘤的发生、生长和转移[2, 3]。目前的研究比较了间质样品间的基因或蛋白表达差异、乳腺上皮细胞间的基因或蛋白表达差异、不同来源的组织(如福尔马林石蜡包埋、冰冻样品、或者实验不同的平台)间蛋白表达差异[2, 3, 4, 5, 6, 7, 8, 9, 10]。尽管这些研究解决了各种上皮间、间质间的蛋白/基因表达差异,但是却不知道间质和上皮细胞间的蛋白表达差异;也有研究用包括了细胞类型混合物的手术解剖样品比较肿瘤组织和正常组织间的蛋白或基因表达差异,但由于上皮细胞的蛋白或基因表达数据被附近间质组分的数据稀释,导致结果模糊,很难解释[11]。因此,肿瘤组织内蛋白表达差异的真正评估需要细胞特异性比较。
在本研究中,激光捕获显微切割技术(LCM)和质谱被用于比较浸润性导管内原位癌间质和乳腺上皮细胞间的蛋白表达差异。该蛋白组学研究结果鉴定了侵润性导管内原位癌间质和上皮细胞中表达丰富的蛋白,确定以前被认为表达已经改变的蛋白和基因是否真实存在和突出了乳腺癌瘤诊断和预后标志蛋白的具体定位。本研究为乳腺癌蛋白质组学研究提供了重要的信息和资料,将有助于理解乳腺癌内发生作用的细胞信号通路,乳腺肿瘤细胞侵入和转移的机制,有助于鉴定与肿瘤诊断和预后密切相关的蛋白。
1 材料与方法 1.1 材料 1.1.1 试剂与设备苏木精、伊红、无水乙醇、二甲苯、尿素、福尔马林等均为国产分析纯。石蜡包埋剂、带PEN膜的载片、LCM专用Eppendorf管、CM1900冰冻切片制作仪、激光捕获显微切割仪系德国Leica公司产品。NanoDrop 2000、-86℃超低温冰箱和带电子转移裂解源的离子阱-轨道阱组合型高分辨质谱仪美国Thermo公司产品;Liquid Tissue MS Protein Prep试剂来自美国Expression Pathology公司。
1.1.2 材料和样品准备手术切除的侵润性导管内原位癌组织样品先置液氮中速冻,后置于-80℃冰箱保存备用,整个样品采集过程耗时控制于30 min内。组织样品从-80℃低温冰箱取出后,迅速进行福尔马林固定、石蜡包埋过程,然后用切片机切成8 μm厚,进行HE染色。方法如下:苏木精10~15 s,捞片置于冰水冲洗10~15 s,伊红15 s,用体积分数为0.85、0.95乙醇各20 s,2次无水乙醇15 s梯度脱水,2次二甲苯1 min透明,室温完全干燥。上述染色过程在冰盒中进行,染液温度控制于(4~10)℃,总时间控制在10 min内。完毕后进行激光捕获。
1.1.3 激光捕获将染色完好切片置于Leica AS显微激光切割系统,10×10倍目镜直视观察,重点观察细胞形态和染色情况。找到细胞密集、形态较好、染色满意区域,安置收集管;根据视野、放大倍数及目的细胞分布等调整激光束的直径和功率,在合适的倍率下分别选上皮细胞和间质组分进行收集,总捕获时间不超过40 min。
1.1.4 质谱分析将捕获细胞的塑料帽扣在装有组织裂解液的0.5 mL离心管上,在室温下倒置约5 min,4℃裂解1 h,12 000 r·min-1、4℃离心45 min,取上清液为组织细胞总蛋白,NanoDrop 2000测定总蛋白含量。然后按照说明书用Liquid Tissue MS Protein Prep处理后进行质谱分析。质谱时,1 μg处理好的样品被注入C18反相柱,洗脱用乙晴/0.1 mol·L-1醋酸,在浓度梯度体积分数为0.02~0.8,流速为0.5 μL·min-1洗脱90 min。洗脱下的样品,通过2.5 kV离子源电喷雾源直接进入质谱仪。质谱仪被设定为获得完全扫描质谱以分析肽分子量,然后以20离子扫描谱以鉴定洗脱肽氨基酸序列。Orbitrap XL质谱的参数设定为:毛细管温度为265℃;FT AGC为9E5,1 uscan;FT最大离子时间为500 ms;IT AGC为8E3;IT最大离子时间为100 ms;ms/ms trigger为1 000 counts;隔离宽度为3;以常态化碰撞能量为35;活化时间为10 ms;重复点数为1;重复周期30 s;排除列表为200;排除周期为60 s。质谱产生的数据用Proteome Discoverer 1.4.1搜索Uniprot人类蛋白组数据库,搜索结果通过如下数据过滤处理后载入Scaffold V 4.3.4:唯一肽≥2、肽Prophet积分> 60%、蛋白Prophet积分> 95%、Xcorr> 1.8 (+1),2.2 (+2),2.5 (+3) 和3.5 (+4或更大)。双尾Fisher精确检验测定P值。
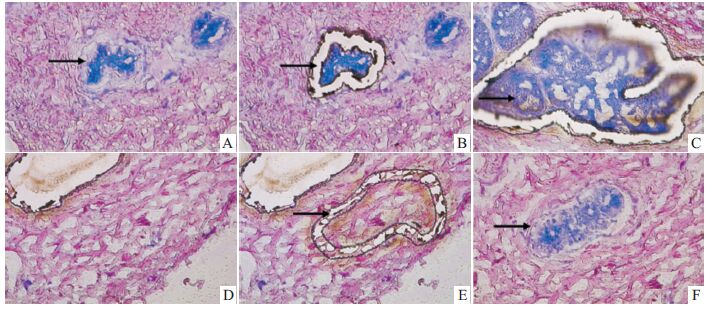
2 结果 2.1 激光捕获显微切割的上皮细胞和间质从Fig1来看,切片用HE方法染色后能获得细胞形态完整、对比度好、肿瘤细胞和间质可清楚区分的合格切片,能够用激光显微切割分离细胞和间质。切割下来的细胞和间质经裂解和NanoDrop 2000测定后总蛋白含量分别为45.1 μg和52.4 μg。Fig1A为切割如下上皮细胞前的图片;Fig1B切割下来的乳腺癌上皮细胞;Fig1C为切割下来的乳腺上皮细胞(10×40);Fig1D切割间质前的图片;Fig1E切割乳腺癌患者间质后的图片;Fig1F间质和癌乳腺上皮切割前的图片。
|
| Fig 1 Laser microdissection of breast stroma and epithelial cells A: Epithelial cells before microdissection; B: Epithelial cells after microdissection; C: Epithelial cells after microdissection oberserved with 40× magnification; D: Stroma before microdissection; E: Stroma after microdissection; F: Stroma and epithelial cells before microdissection |
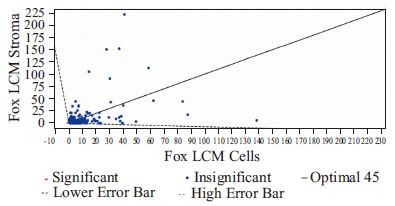
从质谱的Q-Q散布曲线上的散点图看,整个图呈现较为集中的趋势,绝大多数共同表达蛋白位于45度角平分线附近,而差异表达蛋白发生偏离,可清晰、明显的反映样本之间的变化,可以比较两个样品组间的相互关系和蛋白分布的大体轮廓(Fig2)。因此数据的可重现性好,对比的变异程度突出,质谱结论能用于生物学解释。
|
| Fig 2 Q-Q scatterplot of stroma/epithelial cells |
从Fig3可以看出,质谱总共检测了431种蛋白,上皮细胞和间质中分别检测到384和298种蛋白,在两中样品间共同表达的蛋白有251种。Tab1列出了间质和上皮细胞中被鉴定含量最高的50种蛋白对。两组样品蛋白表达进行详细分析发现,仅在间质内表达的蛋白包括Complement C3 (Fragment)、Collagen type V alpha 1、Forkhead box protein F1、Isoform 1 of USH1C-binding protein 1、Isoform 1 of receptor-type tyrosine-protein phosphatase H、ASPN protein、Histone H2A type 1-B/E、Elongation factor 1-alpha 2、Hemoglobin subunit delta、Isoform 1 of Filamin-C、Histone deacetylase 1、Transforming growth factor-beta-induced protein ig-h3、Serotransferrin、Isoform 2 of Trinucleotide repeat-containing gene 6A protein、Putative uncharacterized protein HSPG2、Conserved hypothetical protein等,而仅在上皮细胞中表达的蛋白有Keratin type II cytoskeletal 5、Keratin type I cytoskeletal 19、Keratin type I cytoskeletal 10、Keratin type II cytoskeletal 2 epidermal、Keratin type I cytoskeletal 15、Keratin type I cytoskeletal 16、keratin 7、Fructose-bisphosphate aldolase A、Heat shock protein beta (Fragment)、Alpha-actinin-4、Polymeric immunoglobulin receptor、Heat shock 70 kDa protein 1、Keratin,type I cytoskeletal 17、Basement membrane-specific heparan sulfate proteoglycan core protein、Carbonic anhydrase 2等。在二者共同表达的251种蛋白中,他们的含量在两种样品中不同,69种间质蛋白的含量比在上皮细胞中高,60种比在上皮细胞中低。
 |

|
| Fig 3 Venn diagram of protein spectrum |
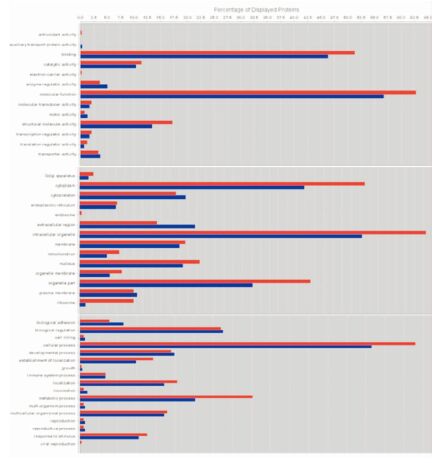
为了充分分析上皮细胞和间质间差异表达蛋白的类型,用基因本体(GO)比较分析了上皮细胞和间质表达蛋白的功能。从Fig4可以看出:在上皮细胞表达的细胞组分蛋白中,除细胞骨架蛋白和细胞外区蛋白比间质含量低外,其他如细胞器、细胞质、内质网相关的蛋白等都比间质含量高;在生物学过程 相关的蛋白中,生物学吸附和调节,细胞增殖、繁殖、移动、发育过程的蛋白的含量在细胞中要低于在间质中,而细胞过程、定位确立、定位、代谢和对刺激反应过程的蛋白在细胞中含量明显要高于在间质中。在上皮细胞表达的分子功能蛋白中除附属运输蛋白活性、酶调节活性和运输活性的蛋白比间质含量低外,其他蛋白都比间质中高。
|
| Fig 4 The GO of proteins from stoma and epithelial cells The red columns are the GO of epithelial cells and the blue ones represent that of the stroma |
乳腺间质组分的改变被认为是宿主对肿瘤发生和进展反应的结果,并会引起肿瘤上皮细胞蛋白表达谱产生相应的改变,因此肿瘤和间质间的相互反应对于肿瘤的发生和进展很重要。涉及肿瘤和间质间反应的蛋白可能是研究诊断方法、治疗手段和预后判断的靶点。为了理解间质和细胞间的反应,有必要细化上皮细胞和间质间蛋白表达的异同,找到标志性蛋白。Ma等[5]发现乳腺癌患者的上皮细胞和间质的基因表达在局部侵袭发生前都明显改变,在导管原位癌和侵袭性导管原位癌转变过程中没有变化发生。但是二者在蛋白表达水平上的差异却没有被验证。在本研究中,激光捕获显微切割技术和质谱分析鉴定的蛋白绝大部分都在癌症研究的文献中被报道过。并且它们的出现位置以及表达水平和它们在肿瘤发生、发展过程中的作用一致。因此质谱和显微切割技术是分析肿瘤细胞和间质蛋白间表达差异的有效方法,能对一些作为诊断和预后判断的分子标志蛋白进行细胞定位。
间质蛋白主要由细胞外间质蛋白和细胞组分如,成纤维为细胞、巨噬细胞、内皮细胞、白细胞等的蛋白构成。胶原是比较大的细胞外间质蛋白,其在肿瘤内形成纤维和网络,对肿瘤的生长和转移有重要影响,能作为预后标志。在目前的研究中,Ⅴ型胶原的alpha 1和2链仅在间质中被检测到,Ⅵ型胶原的alpha-1、alpha-2、alpha-3和Ⅰ型胶原alpha-1、alpha-2链以及Ⅲ型和XIV 型胶原的alpha-1链异位体1在两种样品中都被检测到,但是他们在间质中的含量要远远高于在上皮细胞中。此外,与胶原密切相关蛋白如lamini、periostin、vitronectin等也在间质中检测到。所有这些蛋白均在癌症中有重要作用,如Ⅰ型胶原alpha-1前体和Ⅻ型胶原alpha-1都是预后标志;在间质中检测到的多域蛋白periostin能和Ⅰ型胶原反应,改变periostin的结构将猛烈改变细胞外间质蛋白的结构[12];小亮氨酸重复蛋白家族成员mimecan在间质和上皮细胞中都有表达,但是其在间质中的含量明显高于在上皮细胞中。mimecan能与胶原反应,使胶原免受蛋白酶切割。因此,mimecan是肿瘤侵入标志[13]。与间质蛋白的反应类似,宿主乳腺上皮细胞发生转化后,其蛋白表达谱明显改变,并能作为肿瘤密预后标志。角蛋白是上皮细胞的主要结构蛋白,构成细胞质中间丝。他们的表达结构和潜在的生物学密切相关[14, 15]。keratins 5/6、7/8和13-19因在肿瘤生长和转移过程有重要作用而可以作为预后标志和新生学分类标志[14, 15]。在目前的研究中,18种角蛋白和其相关蛋白在侵润性原位癌的乳腺上皮细胞内被鉴定。该事实进一步证实这些分子可以作为预后的标志。
目前对许多可以作为乳腺癌诊断和预后标志的蛋白的细胞和间质定位不清楚。在目前的研究中,除胶原和Keratin外,许多其他功能明确的蛋白的细胞和间质定位也被确定。例如,仅间质中被检测到的蛋白中,Galectin-1能为肿瘤提供免疫抑制环境并促进肿瘤免疫逃逸[16];CD44肿瘤转移中有作用,可以作为预后不良的标志[17];RpS3是真核细胞40S核糖体亚单位的主要组分,在核酸内切酶破坏中有重要作用[17];叉头蛋白F1的过表达与间叶细胞表型密切相关,能促进肿瘤侵入和转移[18];ASPN蛋白在乳腺导管癌的局部侵入中有重要作用;补体C3是乳腺癌检测和判断的生物标志[19]。而仅在上皮细胞中被检测到的蛋白中,碳酸酐酶IX是乳腺癌诊断后预后判断的生物标志[20];ACTN4是乳腺癌发生的多用途启动子[21];Peroxiredoxin-1和5是雌激素受体阳性乳腺癌的生物标志。而癌症病人的预后标志线粒体ATP合酶亚beta单位;与疾病进展密切相关Tubulin beta-1链[22];表达升高促进了药物抗性和转移的热激蛋白5和90;在乳腺癌的起始和形成中有重要作用的Clusterin和gelsolind的异位体1[23];乳腺癌新辅助化疗的代谢反应标志L-乳酸脱氢酶B等尽管也在间质中被检测到[24],但是它们在上皮细胞中的含量显然更高。不同的是,与乳腺癌细胞启动子甲基化下调密切相联的聚合酶1和转录释放因子在间质中的含量更高。
在目前的研究中,一些和以往研究报道不同的有趣现象存在。首先,一些蛋白的表达定位发生改变,例如,参与上皮细胞迁移的细胞骨架蛋白vimentin是间叶细胞的标志,其过表达加速肿瘤生长、侵袭和差预后。组织学检查乳腺癌样品发现vimentin主要在低雌激素的导管癌上皮细胞内表达[25]。此外,miRNAs表达调节的核蛋白nucleolin和乳腺癌预后的重要因子HDAC1也通常只在乳腺肿瘤上皮细胞内过表达[26, 27]。但目前在间质中都检测到这3种蛋白,并且上皮细胞中检测不到HDAC1,vimentin在间质中的含量要远高于上皮细胞中。其次,个别蛋白的表达谱发生改变,例如,在目前的研究中,除检测到与肿瘤密切相联系的Myosin 2、9、10外,Myosin light chain 6B、Myosin regulatory light chain 12B也被发现,且他们在细胞中含量比间质中高;而过表达与肿瘤密切相关的peptidyl-prolyl cis-trans isomerase FKBP4没有被检测到,但却检测到Peptidyl-prolyl cis-trans isomerase-like 6。最后,在目前的研究中,一些在乳腺癌中没有报道的癌症预后标志被检测到,如卵巢癌症的预后标志Apolipoprotein A-I,前列腺癌的预后判断标志prolargin,甲状腺癌细胞的候选标志ALDH9A1等。这些与以往研究不同的现象可能源于研究材料来源不同和蛋白表达存在种群差异,另外,这也可能与基因分析结果和蛋白表达不一致有关。因为目前对肿瘤标志蛋白的表达定位,表达谱大部分是基于基因表达谱分析,而我们的结果是基于蛋白组学研究。因此不同不可避免存在。
总之,许多差异表达的蛋白在两个样品中被观察到,在二者间不同的蛋白可能突出了他们在肿瘤进展过程中有重要作用。这些不同的蛋白组分可能作为乳腺组织肿瘤发生的标志。可用于鉴定乳腺癌的筛选、诊断、预后和治疗方法检测候选标志。
| [1] | Gaudin N, Terrasse V. Latest world cancer statistics. Global cancer burden rises to 14.1 million new cases in 2012:Marked increase in breast cancers must be addressed[R]. World Health Organization. International Agency for Research on Cancer, Franch Lyon, 2013,12:1-3. |
| [2] | Polyak K, Kalluri R. The role of the microenvironment in mammary gland development and cancer[J]. Cold Spring Harb Perspect Biol, 2010, 2:a003244. |
| [3] | Criscitiello C, Esposito A, Curigliano G. Tumor-stroma crosstalk:targeting stroma in breast cancer[J]. Curr Opin Oncol, 2014, 26(6):551-5. |
| [4] | Massagué J. Sorting out breast-cancer gene signatures[J]. N Engl J Med, 2007, 356(3):294-7. |
| [5] | Ma X J, Dahiya S, Richardson E, et al. Gene expression profiling of the tumor microenvironment during breast cancer progression[J]. Breast Cancer Res, 2009, 11(1):R7. |
| [6] | Kass L, Erler J T, Dembo M, et al. Mammary epithelial cell:influence of extracellular matrix composition and organization during development and tumorigenesis[J]. Int J Biochem Cell Biol, 2007, 39(11):1987-94. |
| [7] | 刘莉萍,白 君,魏 亚,等. 基底细胞样乳腺癌临床病理特征及免疫组织化学分析[J]. 中华病理学杂志,2013,42(2):101-5. Liu L P, Bai J, Wei Y, et al. Clinicopathologic features and immunohistochemistry of the basal-like subtype of invasive breast carcinoma[J]. Chin J Pathol, 2013,42(2):101-5 |
| [8] | Rower C, Koy C, Hecker M. et al. Mass spectrometric characterization of protein structure details refines the proteome signature for invasive ductal breast carcinoma[J]. J Am Soc Mass Spec, 2011, 22:440-56. |
| [9] | Naba A, Clauser K R, Hoersch S, et al. The matrisome:insilico definition and in vivo characterization by proteomics of normal and tumor extracellular matrices[J]. Mol Cell Proteomics, 2012, 11:M111.014647. |
| [10] | Allinen M, Beroukhim R, Cai L, et al. Molecular characterization of the tumor microenvironment in breast cancer[J]. Cancer Cell, 2004, 6:17-32. |
| [11] | Posadas E M, Simpkins F, Liotta L A, et al. Proteomic analysis for the early detection and rational treatment of cancer-realistic hope[J]. Ann Oncol, 2005, 16:16-22. |
| [12] | Wang X, Liu J, Wang Z, et al. Periostin contributes to the acquisition of multipotent stem cell-like properties in human mammary epithelial cells and breast cancer cells[J]. PLoS One, 2013, 8(8):e72962. |
| [13] | R wer C, Ziems B, Radtke A, et al. Toponostics of invasive ductal breast carcinoma:combination of spatial protein expression imaging and quantitative proteome signature analysis[J].Int J Clin Exp Pathol, 2011, 4(5):454-67. |
| [14] | Magin T M, Vijayaraj P, Leube R E. Structural and regulatory functions of keratins[J]. Exp Cell Res, 2007, 313:2021-32. |
| [15] | Gusterson B A, Ross D T, Heath V J, et al. Basal cytokeratins and their relationship to the cellular origin and functional classification of breast cancer[J]. Breast Cancer Res, 2005, 7:143-8. |
| [16] | Dalotto-Moreno T, Croci D O, Cerliani J P, et al. Targeting galectin-1 overcomes breast cancer-associated immunosuppression and prevents metastatic disease[J]. Cancer Res, 2013, 73(3):1107-17. |
| [17] | Fan Y, Wang J, Yang Y, et al. Detection and identification of potential biomarkers of breast cancer[J]. J Cancer Res Clin Oncol, 2010, 136(8):1243-54. |
| [18] | Nilsson J, Helou K, Kovács A, et al. Nuclear Janus-activated kinase 2/nuclear factor 1-C2 suppresses tumorigenesis and epithelial-to-mesenchymal transition by repressing Forkhead box F1[J]. Cancer Res, 2010, 70(5):2020-9. |
| [19] | Profumo A, Mangerini R, Rubagotti A, et al. Complement C3f serum levels may predict breast cancer risk in women with gross cystic disease of the breast[J]. J Proteomics, 2013, 85:44-52. |
| [20] | Furjelová M, Kovalská M, Jurková K, et al. Carbonic anhydrase IX:a promising diagnostic and prognostic biomarker in breast carcinoma[J]. Acta Histochem, 2014, 116(1):89-93. |
| [21] | Hsu K S, Kao H Y. Alpha-actinin 4 and tumorigenesis of breast cancer[J]. Vitam Horm, 2013, 93:323-51. |
| [22] | Dozier J H, Hiser L, Davis J A, et al. Beta class Ⅱ tubulin predominates in normal and tumor breast tissues[J]. Breast Cancer Res, 2003, 5(5):R157-69 |
| [23] | Cohen A, Wang E, Chisholm K A, et al. A mass spectrometry-based plasma protein panel targeting the tumor microenvironment in patients with breast cancer[J]. J Proteomics, 2013, 81:135-47. |
| [24] | Dennison J B, Molina J R, Mitra S, et al. Lactate dehydrogenase B:a metabolic marker of response to neoadjuvant chemotherapy in breast cancer[J]. Clin Cancer Res, 2013, 19(13):3703-13. |
| [25] | Satelli A, Li S. Vimentin in cancer and its potential as a molecular target for cancer therapy[J]. Cell Mol Life Sci, 2011, 68(18):3033-46. |
| [26] | Pichiorri F, Palmieri D, De Luca L, et al. In vivo NCL targeting affects breast cancer aggressiveness through miRNA regulation[J]. J Exp Med, 2013, 210(5):951-68. |
| [27] | Eom M, Han A, Lee M J, et al. Expressional Difference of RHEB, HDAC1, and WEE1 Proteins in the stromal tumors of the breast and their significance in tumorigenesis[J].Korean J Pathol, 2012, 46(4):324-30. |
