


类风湿关节炎(rheumatoid arthritis,RA) 是一种慢性、系统性不明病因的自身免疫性疾病,严重威胁着人类的健康,其中关节软骨和骨组织破坏是其致残的根本原因[1]。软骨细胞作为关节软骨内唯一存在的细胞类型,其在软骨细胞外基质 (extracellar matrix,ECM) 的合成及修复中发挥着关键作用。在RA等一些病理条件下,软骨细胞代谢异常可以直接导致关节软骨结构和功能的改变。自噬(autophagy)是一种细胞依赖溶酶体的自我代谢过程,通过更新和降解一些长寿命、错误折叠的蛋白质和受损的细胞器等来维持细胞内环境的稳态[2]。众多学者研究发现,自噬活化不仅可以为细胞提供能量抵御代谢应激等保护作用,同时亦发现其与多种疾病的发生发展有关,受到广泛关注[3]。且有研究证实,在RA进程中存在着自噬的活化,但是软骨细胞自噬的活化在RA进程中具体的保护或破坏作用目前仍然存在着争议[4]。
BAPTA-AM [1,2-bis ( 2-aminophenoxy) ethane-N,N,N′N′-tetraacetic acid]是一种高选择性高效的钙络合剂,广泛被用于控制细胞内钙水平,能有效降低细胞内钙离子浓度,是一种公认的科研工具药物[5]。研究发现,细胞内游离钙离子与细胞自噬有着密切的关系,游离钙离子既可以诱导自噬的活化,亦可抑制自噬的发生,其具体的作用尚不明确[6]。
本课题组前期研究结果表明,胞外酸化(pH 6.0)可以明显诱导大鼠关节软骨细胞自噬的发生,但机制不明[7]。本研究以大鼠关节软骨细胞为实验对象,胞外酸化诱导细胞自噬活化,探究 BAPTA-AM 对软骨细胞自噬作用的影响及其可能机制,揭示胞外酸化诱导软骨细胞自噬过程细胞内游离钙离子浓度[Ca2+]i与细胞自噬的可能关系。
1 材料与方法 1.1 实验动物SPF 级 Sprague-Dawley(SD)大鼠,♂,体质量180~200 g,购自安徽医科大学实验动物中心,合格证号:皖动准字 01 号。
1.2 药物与试剂BAPTA-AM 购自日本 Dojindo 公司(C34H40N2O18,分子量764.68);抗 LC3 抗体购自 Cell Signaling Technology 公司;抗 AMPKa1 抗体、抗 p-AMPKa1 抗体和抗 CaMKKβ 抗体购自 Biosynthesis 公司;抗 β-actin 抗体、抗 mTOR 抗体和抗 p-mTOR 抗体购自 Santa Cruz 公司;胎牛血清购自Gibco 公司;Ⅱ型胶原酶购自 Sigma 公司;高糖 DMEM 液体培养基购自 Hyclone 公司;辣根酶标记山羊抗兔 IgG 为北京中杉金桥公司产品;胰蛋白酶消化液、D-Hanks 液购自碧云天公司; TRIzol 试剂购自 Invitrogen 公司;逆转录试剂盒、PCR 扩增试剂盒和 SYBR Green 染料购自 Fermentas 公司;ECL 显色试剂盒购自 Thermo Scientific 公司。
1.3 大鼠关节软骨细胞分离、培养按本实验室常规方法进行大鼠关节软骨细胞的分离[8],接种入细胞培养瓶中。置于 37℃、5 % CO2孵育箱中培养 48 h 后首次换液。每隔 2~3 d更换培养液 1 次,倒置显微镜下观察细胞。当培养的软骨细胞铺满培养瓶底 70%~90 %时,即可开始实验。
1.4 软骨细胞自噬诱导及药物处理软骨细胞分组如下:pH 7.4 正常组、 pH 6.0 酸化组、 pH 7.4 + BAPTA-AM (10 μmol·L-1)组、pH6.0 + BAPTA-AM(10 μmol·L-1) 组。细胞给予相应处理后,酸化处理组加入 pH 6.0 的培养基培养 3 h,收集细胞,检测 BAPTA-AM 对酸化诱导的软骨细胞自噬的影响。
1.5 激光共聚焦检测大鼠关节软骨细胞内 Ca2+ 浓度将软骨细胞接种于激光共聚焦专用细胞培养皿中,药物处理后,用 Hanks 液冲洗 2 遍,将10 μmol·L-1 Fluo-3/AM 和 0.02% F-127 的 100 μL 混合工作液滴于平皿中央,37℃、5 % CO2培养箱中避光孵育 30 min,再用 Hanks 液冲洗盖玻片 3 遍,保留少许 Hanks 液于皿内平衡细胞 10 min,于10 min 内检测细胞内 Ca2+ 浓度。激光共聚焦显微镜下动态扫描细胞 20 s,用微量加样器将 pH 6.0 的细胞外液滴注到平皿中,动态观察胞内 Ca2+ 的荧光强度变化。激发光波长为 488 nm、发射光波长 525 nm。
1.6 软骨细胞自噬水平检测 1.6.1 实时荧光定量 PCR检测软骨细胞 Beclin-1 、ULK1 mRNA 表达实验分组同“1.4”。相应药物处理后,按 TRIzol 三步法提取细胞总 RNA,按照逆转录试剂盒说明书和引物反应条件进行逆转录和目的基因扩增,GAPDH 为内标。引物序列详见 Tab1。反应体系为 10 μL,其中 SYBR Green Mix (2×) 5 μL,cDNA 0.5 μL,引物各 0.3 μL,用无酶水补足。反应条件为:Step1:95℃,10 min; Step2:95℃,15 s; 60 ℃,30 s;72℃,30 s; 45 cycles。
实验分组同“ 1.4”。相应药物处理后,弃培养液,用预冷 PBS 洗涤 3 遍,每瓶加入 400 μL RIPA 裂解液(含 10 % PMSF)裂解 30 min,细胞转移到 1.5 mL EP 管中,离心取上清,使用 BCA 蛋白定量试剂盒进行蛋白定量。将上清与上样缓冲液按 4 ∶ 1的比例进行分装,100℃煮10 min 变性,-80℃保存待用。等量的蛋白样品进行 SDS-PAGE 胶分离后转移至PVDF 膜。TBST 洗脱 10 min。室温下用含 5 % 脱脂奶粉(TBST 溶解)封闭 3 h。随后加入一抗(1 ∶ 500)4℃孵育过夜。TBST 洗脱 3 次,加入相应的二抗,孵育 1 h,漂洗 3 次。将 PVDF 膜用化学发光剂 ECL 染色,曝光拍照。结果采用 Image-Pro Plus 图像分析管理系统分析。
1.6.3 吖啶橙(acridine orange,AO)染色分析酸性自噬囊泡实验分组同“1.4”。相应处理后,PBS 洗涤2次,用AO染液进行染色(最终浓度为 2 mg·L-1),室温避光 15 min,然后用 PBS 洗涤 2 次,荧光显微镜观察酸性囊泡自噬体。
1.7 Western blot 法检测CaMKKβ、AMPKa1、p-AMPKa1、mTOR、p-mTOR蛋白的表达实验分组同“1.4”。试验步骤同“1.6.2”。
1.8 统计学分析实验结果均以 表示,所有统计分析均采用 SPSS 16.0 软件完成。各组数据运用单因素方差分析进行统计检验。
表示,所有统计分析均采用 SPSS 16.0 软件完成。各组数据运用单因素方差分析进行统计检验。
Western blot 结果如Fig1所示,与 pH 7.4 正常组相比,酸化刺激组 ( pH 6.0 ) 软骨细胞 LC3Ⅱ 蛋白表达明显增加,且差异具有显著性(P<0.01)。与酸化组比较,BAPTA-AM 处理组可明显下调LC3Ⅱ 蛋白水平(P<0.01),但是 BAPTA-AM对正常组细胞的 LC3Ⅱ 蛋白表达无明显影响。

|
| Fig 1 Effects of BAPTA-AM on expressions of LC3 in acid-induced articular chondrocytes[WTBZ][STBZ](n=3) **P<0.01 vs pH 7.4 normal group; ##P<0.01 vs pH 6.0 group |
如Fig2 所示,酸化刺激组 (pH 6.0) 大鼠关节软骨细胞 Beclin-1、ULK1 mRNA 表达与正常组相比较明显增加(P<0.01)。与酸化组比较,BAPTA-AM 处理组可明显降低 pH 6.0 组细胞 Beclin-1、ULK1 mRNA 表达(P<0.01)。

|
| Fig 2 Effects of BAPTA-AM on expressions of Beclin-1 and ULK1 in acid-induced articular chondrocytes(n=3) **P<0.01 vs pH 7.4 normal group;##P<0.01 vs pH 6.0 group |
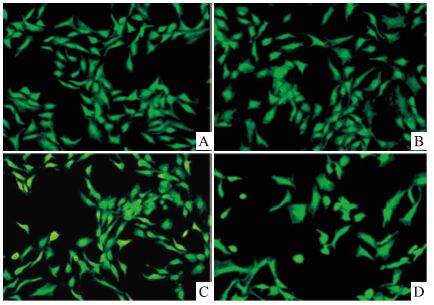
AO染色观 察自噬关键的形态学特征酸性自噬溶酶体的形成,结果如 Fig3 所示,与正常组(Fig3A)相比,pH 6.0酸化刺激能明显增加酸性自噬溶酶体的形成(Fig3C);BAPTA-AM 能够明显减少酸性自噬溶酶体的形成(Fig3D)。
|
| Fig 3 Effects of BAPTA-AM on acid-induced acidic vesicle formation of autophagic vacuoles of articular chondrocytes A: pH 7.4 normal group; B: pH 7.4+ BAPTA-AM group; C: pH 6.0 group; D: pH 6.0+BAPTA-AM group |
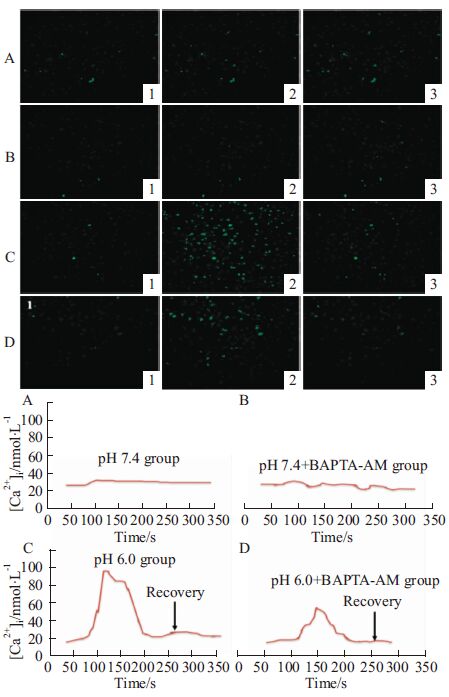
激光共聚焦结果显示,pH 7.4 正常组软骨细胞,前、中、后各时段大鼠关节软骨细胞荧光强度基本没有变化(Fig4A);给予 BAPTA-AM 后对细胞胞质 Ca2+ 浓度无明显影响(Fig4B)。pH 6.0 酸化刺激组软骨细胞,酸化刺激前细胞胞质 Ca2+ 浓度无明显变化,酸化刺激导致细胞 Ca2+ 明显增强,随后荧光开始减弱(Fig4C);在给予 BAPTA-AM 后,酸化刺激对细胞胞质 Ca2+ 影响较小(Fig4D);数据分析后结果显示,正常组细胞荧光变化曲线接近平坦,酸化诱导的关节软骨细胞中荧光曲线先明显升高后降低,BAPTA-AM 处理后软骨细胞中荧光曲线较酸化组平坦。
|
| Fig 4 Effects of BAPTA-AM on acid-induced elevation of [Ca2+]i in articular chondrocytes 1: Before exposure to acid solution; 2: Increased Ca2+ intensity when pH was decreased to 6.0; 3: A few minutes after exposure to the acid solution. A: pH 7.4 normal group; B: pH 7.4+BAPTA-AM group; C: pH 6.0 group; D: pH 6.0+BAPTA-AM group |
Western blot结果如Fig5所示,与 pH 7.4正常组比较,酸化刺激组大鼠关节软骨细胞 CaMKKβ、p-AMPK 蛋白表达均明显增加,p-mTOR 蛋白表达明显降低,且差异有统计学意义(P<0.01)。与酸化组相比,BAPTA-AM组可明显抑制CaMKKβ、p-AMPK蛋白表达,升高 p-mTOR 蛋白表达(P<0.01)。

|
| Fig 5 Effects of BAPTA-AM on expressions of CaMKKβ,AMPK and mTOR in articular chondrocytes[WTBZ][STBZ](n=3) **P<0.01 vs pH 7.4 normal group;#P<0.05, ##P<0.01 vs pH 6.0 group |
自噬是一种溶酶体依赖的细胞降解过程,通过将自噬小体中的细胞“货物”转移至溶酶体,自噬小体与溶酶体融合形成自噬溶酶体,随后自噬溶酶体的“货物”开始降解,这种细胞内的“货物”可以是一些错误折叠的大分子蛋白、脂类以及完整的细胞器等[9]。基础水平的自噬可以维持细胞的稳态和自身代谢[10]。同时自噬可在一些应激条件下被激活,如低氧、营养缺失、热休克、微生物感染、酸化等[11, 12]。这些情况下,自噬可以为细胞提供构建成分,并纳入一些新合成的大分子为细胞抗应激反应和能源生产所需,确保细胞的生存。近年来大量研究表明,自噬与多种疾病的发生发展有关,如炎症、神经退行性疾病、肿瘤等[3]。在RA中,也存在着自噬的活化,但具体机制尚不明确[4]。RA 关节局部组织酸化导致的关节软骨和骨质的破坏是其致残的主要原因[8]。本课题组前期研究表明,pH 6.0 酸化条件能明显激活软骨细胞自噬,自噬标志性蛋白 LC3Ⅱ 表达明显升高,但具体机制尚不明确[7]。同时也有研究表明,钙离子在细胞自噬过程中发挥重要作用,但是具体诱导自噬或抑制自噬目前尚存在着争议[6]。
本文以大鼠关节软骨细胞为实验对象,pH 6.0 胞外酸化为诱导自噬活化条件,使用 Ca2+ 络合剂 BAPTA-AM,探讨 Ca2+ 在胞外酸化诱导软骨细胞自噬中的作用。实验结果显示,胞外酸化大鼠关节软骨细胞可以诱导自噬活化,酸化刺激组加入 BAPTA-AM 后,胞内游离钙离子水平下降,并且自噬标志物 LC3Ⅱ、Beclin-1、ULK1 表达水平明显降低,提示 Ca2+ 可能参与胞外酸化诱导的软骨细胞自噬,同时,BAPTA-AM 处理后正常组自噬水平并无明显改变,这与 Furuta等[5]研究结果相一致。
Ca2+ 作为细胞内重要的第二信使,与细胞内一些重要的生理病理过程具有密切的联系,其微小的改变都可以影响到细胞的正常生理功能。Ca2+ 的信号通路有很多组件,这些组件可以相互连接来创建一个广泛的空间和时间信号[13]。研究表明,升高的细胞质Ca2+ 及一系列信号通路在自噬中发挥着重要作用[14],同时有研究表明,mTOR作为一个细胞的重要信使,在自噬激活中起负性调控作用[15],并且其上游的调节因子如 AMPK 和 CaMKKα/β 参与Ca2+ 调控自噬的过程[16]。我们的研究结果表明,与 pH 7.4 正常组相比,pH 6.0 酸化刺激组 CaMKKβ蛋白水平增加,p-AMPK 水平升高,p-mTOR 表达下调,证实 CaMKKβ、AMPK和mTOR可能参与胞外酸化诱导软骨细胞自噬的过程,同时,酸化刺激组加入BAPTA-AM处理后,CaMKKβ、p-AMPK表达下调,p-mTOR表达上调,表明CaMKKβ、AMPK和mTOR可能作为Ca2+ 下游信号分子参与调控胞外酸化诱导的大鼠关节软骨细胞自噬过程。这一研究结果与文献报道相一致[16]。
综上所述,本研究证实胞外酸化刺激激活关节软骨细胞自噬,钙离子络合剂BAPTA-AM 可明显抑制酸化刺激诱导的软骨细胞自噬,其机制可能与阻断细胞内 Ca2+ 水平,调控 CaMKKβ、AMPK 和 mTOR 表达有关。这为研究RA的发病机制提供了新的视角。
| [1] | Scott D L,Wolfe F,Huizinga T W J. Rheumatoid arthritis[J]. Lancet, 2010, 376(9746):1094-108. |
| [2] | Jesús M B, Carlos L L. Autophagy and self-defense[J]. Adv Exp Med Biol, 2012, 738(3):169-84. |
| [3] | Levine B, Kroemer G. Autophagy in the pathogenesis of disease[J]. Cell, 2008, 132(1):27-42. |
| [4] | Buckland J. Rheumatoid arthritis:autophagy:a dual role in the life and death of RASFs[J]. Nat Rev Rheumatol, 2013, 9(11):637. |
| [5] | Furuta A,Tanaka M,Omata W, et al. Microtubule disruption with BAPTA and dimethyl BAPTA by a calcium chelation-independent mechanism in 3T3-L1 adipocytes[J]. Endocr J, 2009, 56(2):235-43. |
| [6] | Decuypere J P, Bultynck G, Parys J B. A dual role for Ca2+ in autophagy regulation[J]. Cell Calcium, 2011, 50(3):242-50. |
| [7] | 张晨晨,唐 杰,陈飞虎, 等. 酸敏感离子通道1a 在酸诱导的大鼠关节软骨细胞自噬的作用及其机制研究[J]. 中国药理学通报, 2013, 29(8):1092-8. Zhang C C,Tang J,Chen F H, et al. Effects of acid-sensing ion channel 1a on acid-induced autophagy of articular chondrocytes and its possible mechanisms[J].Chin Pharmacol Bull, 2013, 29(8):1092-8. |
| [8] | Rong C, Chen F H, Jiang S, et al. Inhibition of acid-sensing ion channels by amiloride protects rat articular chondrocytes from acid-induced apoptosis via a mitochondrial-mediated pathway[J]. Cell Biol Int, 2012, 36(7):635-41. |
| [9] | Ravikumar B, Sarkar S, Davies J E, et al. Regulation of mammalian autophagy in physiology and pathophysiology[J]. Physiol Rev, 2010, 90(4):1383-435. |
| [10] | Marino G, Madeo F, Kroemer G. Autophagy for tissue homeostasis and neuroprotection[J]. Curr Opin Cell Biol, 2011, 23(2):198-206. |
| [11] | Wojtkowiak J W, Gillies R J. Autophagy on acid[J]. Autophagy, 2012, 8(11):1688-9. |
| [12] | Mizushima N, Klionsky D J. Protein turnover via autophagy:implications for metabolism[J]. Annu Rev Nutr, 2007, 27(2):19-40. |
| [13] | Berridge M J, Lipp P, Bootman M D. The versatility and universality of calcium signalling[J]. Nat Rev Mol Cell Biol, 2000, 1(1):11-21. |
| [14] | Wang S H, Shih Y L, Ko W C, et al. Cadmium-induced autophagy and apoptosis are mediated by a calcium signaling pathway[J]. Cell Mol Life Sci, 2008, 65(22):3640-52. |
| [15] | Jung C H, Ro S H, Cao J, et al. mTOR regulation of autophagy[J]. FEBS Lett, 2010, 584(7):1287-95. |
| [16] | Hoyer H M, Bastholm L, Szyniarowski P, et al. Control of macroautophagy by calcium, calmodulin-dependent kinase kinase-beta, and Bcl-2[J]. Mol Cell, 2007, 25(2):193-205. |


