


Toll样受体 (toll like receptor,TLR)是Ⅰ型跨膜受体,能够识别外来微生物侵入,激活免疫应答反应。TLR为模式识别受体,在天然免疫免疫应答反应中起关键作用[1]。近来研究表明,TLR不仅能够识别外来的病原体 [2],在糖尿病并发症、心血管疾病过程中也发挥重要作用[3, 4, 5]。TLR家族包含13个成员,TLR4是目前研究最广泛的TLR家族成员之一,且与糖尿病并发症发生密切相关。临床研究表明,糖尿病患者的TLR4表达水平增高[6, 7],但分子机制尚不完全清楚。
银杏内酯B是银杏叶提取物,是天然的血小板活化因子受体(platelet activating factor receptor,PAFR)拮抗剂,它通过与PAF受体竞争性结合抑制PAF介导的血小板活化[8]。大量研究显示,银杏内酯B对内皮细胞、神经细胞均有较好的保护作用 [9, 10]。然而,银杏内酯B是否能够对高糖诱导的内皮细胞损伤有保护作用尚不清楚。PAF受体是一类G蛋白偶联受体,介导炎症细胞、血小板的活化过程,在多种细胞中都有表达,包括内皮细胞[11]。内皮细胞损伤及功能障碍是糖尿病血管病变中的早期表现,本研究旨在探讨银杏内酯B对高糖诱导内皮细胞TLR4、炎症蛋白表达的影响以及相关的分子机制。
1 材料与方法 1.1 药品与试剂银杏内酯B 购自江苏大观园商贸公司,纯度为95% ( 批号: BAT2007115)。Ⅰ型胶原酶、明胶购自Sigma 公司; 胰蛋白酶、特级胎牛血清购自Hyclone公司;Medium 199 培养基购自Gibco (Invitrogen 公司);葡萄糖购自Amresco公司;抗TLR4 抗体购自Abcam 公司;抗PAF Receptor 抗体购自Cayman Chemical公司;抗ICAM-1、VCAM-1、β-actin 抗体购自Santa Cruz 公司; 抗NF-κB p65抗体、抗Akt 和phospho-Akt 抗体购自Cell Signaling 公司;辣根过氧化酶标记的山羊抗兔IgG、山羊抗小鼠IgG、兔抗山羊IgG购自北京中杉金桥公司;Dylight-549标记的山羊抗兔IgG购自 Earthox 公司。
1.2 人脐静脉内皮细胞的分离与培养取新鲜脐带,用Ⅰ型胶原酶(1 g·L-1)灌注到脐静脉20 min,收集灌注液、离心。将分离的内皮细胞于M199培养基中培养,含20%的特级胎牛血清,1%青霉素和链霉素,在含5% CO2的37℃培养箱中培养,细胞传至第3代用于实验。
1.3 Western blot 方法检测蛋白表达用葡萄糖(30 mmol·L-1) 刺激内皮细胞 8 h。去除培养基后,用细胞裂解液RIPA(购自碧云天生物技术公司)裂解细胞,收集蛋白。采用BCA法测定蛋白浓度。取15 μg 蛋白样品,经SDS-PAGE 电泳、转膜。用5%的牛血清白蛋白溶液封闭1 h。分别加入特异性的抗体(TLR4、PAFR、ICAM-1、VCAM-1、phospho-Akt、Akt),4℃孵育过夜。用TBST 洗膜3 次,每次5 min,加入对应二抗,室温孵育1 h。洗膜3次,每次5 min。加入ECL 发光液,用VILBER LOURMAT凝胶成像仪成像。
1.4 免疫荧光检测NF-κB 的核转位将灭菌玻片置于24孔板中,接种人脐静脉内皮细胞。待细胞铺满玻片时用于实验。加入0.6 g·L-1银杏内酯B 孵育1 h,再加入30 mmol·L-1葡萄糖刺激细胞8 h。用PBS洗3次,用4%多聚甲醛固定细胞20 min。用PBS洗3次,用5%牛血清白蛋白封闭2 h,加入抗NF-κB抗体(1 ∶ 50)孵育,4℃过夜。PBS洗3次,加入Dylight-549标记的二抗(1 ∶ 100),室温下避光孵育1 h,加入DAPI (1 ∶ 1 000) 孵育10 min,用于细胞核染色。用50%甘油封片。使用Olympus BX60荧光显微镜观察细胞,用尼康CCD成像系统采集图像。
1.5 统计学方法蛋白表达的分析数据以 表示,采用单因素方差分析及student t检验。
表示,采用单因素方差分析及student t检验。
为了探明高糖对内皮细胞TLR4与PAF 受体表达的影响,我们首先观察了不同浓度(0、5、10、20、30 mmol·L-1)葡萄糖刺激内皮细胞TLR4和PAF 受体表达的变化。结果显示,TLR4表达、PAF 受体表达均随着葡萄糖浓度的升高而增加,呈剂量依赖关系,30 mmol·L-1葡萄糖刺激细胞时TLR4表达、PAF 受体均达到较高的水平(Fig1A)。进而,我们观察了葡萄糖刺激内皮细胞TLR4、PAF 受体表达随时间变化的过程。结果显示,高糖刺激内皮细胞4 h和8 h时,TLR4和PAF 受体表达均达到高峰,16 h后表达逐渐降低,二者出现了相同的变化趋势(Fig1B)。

|
| Fig 1 TLR4 and PAF receptor expression induced by glucose A: TLR4 and PAF receptor expression induced by various concentrations of glucose; B: TLR4 and PAF receptor expression induced by glucose at different time. |
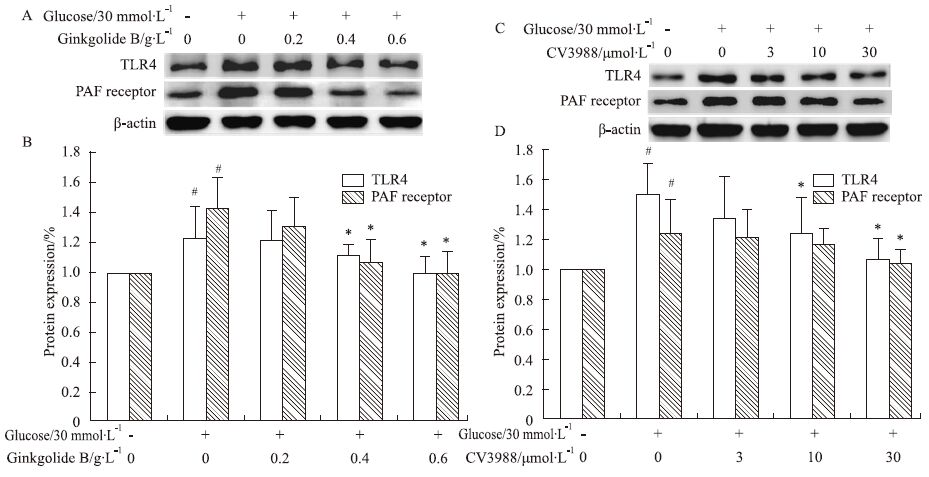
为了探讨PAF受体抑制剂是否对TLR4及PAF受体表达有抑制作用,我们观察了银杏内酯B对高糖刺激内皮细胞TLR4 及PAF受体表达的影响。使用不同浓度的银杏内酯B(0.2、0.4、0.6 g·L-1)处理细胞,观察对TLR4及PAF受体表达的影响。结果表明,葡萄糖刺激内皮细胞8 h后,TLR4表达增加了23%,PAF受体表达增加了41%,银杏内酯B以剂量依赖性的方式抑制了高糖诱导的TLR4及PAF受体表达 (Fig2A、B)。然后,我们使用了另一个PAF 受体抑制剂CV3988,观察其对内皮细胞TLR4及PAF受体表达的影响,CV3988同样以剂量依赖性的方式抑制了高糖刺激的TLR4及PAF受体表达(Fig2C、D)。
|
| Fig 2 Effects of ginkgolide B and CV3988 on TLR4 and PAF receptor expression in glucose-treated HUVECs A, B: Ginkgolide B inhibited the expression of TLR4 and PAF receptor in high dose of glucose-treated HUVECs. C, D: CV3988 inhibited the expression of TLR4 and PAF receptor in high dose of glucose-treated HUVECs. Data are representatives of four independent experiments. #P<0.05 compared with cells without glucose treatment; *P<0.05 compared with cells treated with glucose alone. |
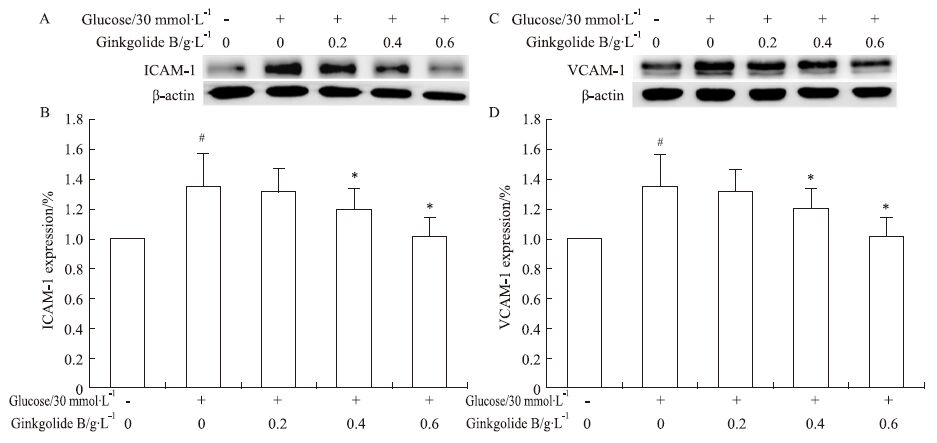
高糖能够导致内皮细胞损伤,表现为内皮细胞的炎症蛋白表达增高。本研究评价了银杏内酯B对高糖刺激内皮细胞黏附蛋白(intercellular cell adhesion molecule-1,ICAM-1)、血管细胞黏附分子(vascular cell adhesion molecule 1,VCAM-1)表达的影响。结果显示,高糖刺激8 h内皮细胞ICAM-1 增加了35%,VCAM-1表达增长了42%。银杏内酯B(0.6 g·L-1)几乎完全抑制了ICAM-1、VCAM-1的表达 (Fig3)。
|
| Fig 3 Effect of ginkgolide B on ICAM-1 and VCAM-1 expression in glucose-treated HUVECs A, B: Ginkgolide B inhibited the expression of ICAM-1 in high glucose-treated HUVECs. C, D: Ginkgolide B inhibited the expression of VCAM-1 in high glucose-treated HUVECs. Data are representatives of four independent experiments. #P<0.05 compared with cells without glucose treatment; *P<0.05 compared with cells treated with glucose alone. |
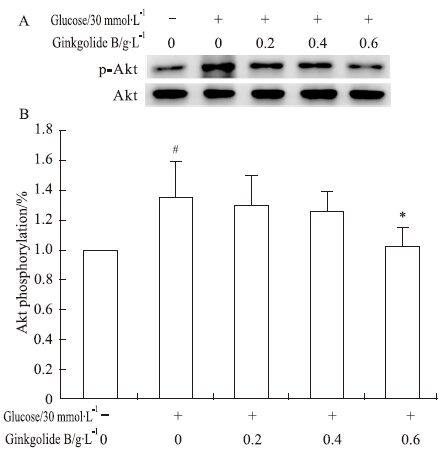
PI3K/Akt通路参与细胞的多种活化反应,本研究观察了高糖刺激内皮细胞对Akt磷酸化的影响。结果表明,高浓度葡萄糖(30 mmol·L-1)刺激后,内皮细胞信号分子Akt磷酸化水平增加了34%,银杏内酯B以剂量依赖的方式抑制了Akt磷酸化(Fig4)。
|
| Fig 4 Effect of ginkgolide B on Akt phosphorylation in glucose-treated HUVECs A: Western blot analysis of Akt phosphorylation; B: Densitometry analysis of Akt phosphorylation. Data are representatives of four independent experiments. #P<0.05 compared with cells without glucose treatment; *P<0.05 compared with cells treated with glucose alone. |
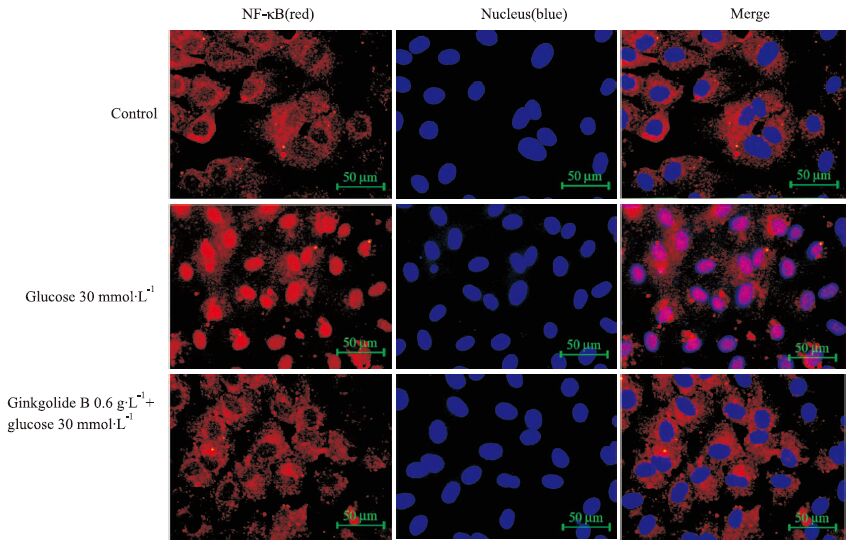
研究已经表明,炎症状态下核转录因子NF-κB 的亚基p65移位到细胞核,与靶基因结合,启动炎症蛋白表达。本研究利用免疫荧光的方法观察了高糖刺激内皮细胞的NF-κB p65核转位。结果显示,未用高糖处理的细胞NF-κB p65主要在细胞质表达,当30 mmol·L-1葡萄糖刺激内皮细胞8 h,NF-κB p65在细胞质中表达减少,而在细胞核表达明显增多,提示NF-κB p65发生核转位 。银杏内酯B(0.6 g·L-1)处理的细胞,NF-κB p65的核转位现象被完全抑制(Fig5)。
|
| Fig 5 Effect of ginkgolide B on NF-κB p65 nuclear translocation in glucose-treated HUVECs The red fluorescence represents NF-κB p65. The blue fluorescence represents nucleus. |
近来研究表明,糖尿病过程中伴有机体免疫功能失调,然而,其机制尚不完全清楚[12]。TLR4是一类进化上非常保守的受体,主要识别革兰阴性杆菌内毒素脂多糖(LPS),在脂肪组织、骨骼肌、内皮细胞中均有表达[13, 14, 15]。TLR4介导的信号能激活转录因子NF-κB活化,从而诱导炎症蛋白的合成,如ICAM-1、VCAM-1[16]。近年来有研究发现,糖尿病中胰岛素抵抗诱导的炎症反应与TLR4有关[17]。同样的现象也存在于糖尿病伴有的动脉粥样硬化。动物实验研究表明TLR4基因缺失有助于减轻动脉粥样硬化病变程度[18]。
PAF是一个强有力的炎症介质,通过与PAF受体结合参与机体多种炎症反应[19]。本研究我们发现,高糖刺激增加内皮细胞TLR4表达,同时PAF受体表达也明显增高。这一现象提示PAF受体参与了高糖诱导的TLR4活化反应。我们提出的问题是,抑制PAF受体介导的信号通路是否能够同时抑制TLR4介导的炎症反应。因此,我们使用了PAF受体抑制剂银杏内酯B,观察其对高糖诱导的内皮细胞TLR4及PAF受体表达,以及相关的炎症反应的影响。本研究的结果提示,银杏内酯B能够降低高糖诱导的TLR4及PAF受体高表达。我们使用另一个PAF受体抑制剂CV3988处理细胞获得了同样的结果。本研究还发现,高糖刺激TLR4表达增高后,ICAM-1、VCAM-1表达随之增高,而银杏内酯B同样抑制了这些炎症蛋白的表达。此外,我们发现银杏内酯B抑制了高糖诱导NF-κB p65核转位,表明银杏内酯B能够抑制高糖刺激的NF-κB通路活化。先前我们的研究发现,银杏内酯B能够抑制ox-LDL刺激内皮细胞的Akt磷酸化[20]。本研究发现,高糖能够增高内皮细胞Akt磷酸化水平,而银杏内酯B有效地抑制高糖刺激的Akt磷酸化。
综上所述,银杏内酯B能够降低高糖刺激内皮细胞TLR4及PAF受体表达,并抑制内皮细胞的炎症反应。银杏内酯B的药理作用可能不仅与其拮抗PAF受体相关,而是通过影响多个信号分子发挥作用的。这些结果为今后糖尿病动脉粥样硬化的防治研究提出了一个新的实验依据,具有重要的科学意义。
| [1] | Takeda K, Kaisho T, Akira S. Toll-like receptors[J]. Annu Rev Immunol, 2003, 21:335-76. |
| [2] | Pichlmair A, Reis e Sousa C. Innate recognition of viruses[J]. Immunity, 2007, 27(3):370-83. |
| [3] | Edfeldt K, Swedenborg J, Hansson G K, et al. Expression of toll-like receptors in human atherosclerotic lesions:a possible pathway for plaque activation[J]. Circulation, 2002, 105(10):1158-61. |
| [4] | Tsukumo D M,Carvalho-Filho M A,Carvalheira J B,et al. Loss-of-function mutation in Toll-like receptor 4 prevents diet-induced obesity and insulin resistance[J]. Diabetes, 2007, 56(8):1986-98. |
| [5] | Erridge C. The roles of Toll-like receptors in atherosclerosis[J]. J Innate Immun, 2009, 1(4):340-9. |
| [6] | Johnstone M T, Creager S J, Scales K M, et al. Impaired endothelium-dependent vasodilation in patients with insulin-dependent diabetes mellitus[J]. Circulation, 1993, 88(6):2510-6. |
| [7] | Roberts A C, Karen E. Cellular and molecular mechanisms of endothelial dysfunction in diabetes[J]. Diab Vasc Dis Res, 2013, 10(6):472-82. |
| [8] | Braquet P. Proof of involvement of PAF-acether in various immune disorder using BN52021(ginkgolide B):a powerful PAF-acether antagonist isolated from Ginkgo billoba L[J]. Adv Prostaglandin Thromboxane Leukot Res, 1986, 16:179-98. |
| [9] | 马丽娜,陈北冬,赵艳阳,等.银杏内酯B对内皮细胞的保护作用及分子机制研究[J].中国药理学通报,2013,29(2):189-93. Ma L N, Chen B D, Zhao Y Y, et al. Protective effect of ginkgolide B on ox-LDL stimulated endothelial cells[J]. Chin Pharmacol Bull, 2013, 29(2):189-93. |
| [10] | Oberpichler H, Sauer D, Rossberg C, et al. PAF antagonist ginkgolide B reduces postischemic neuronal damage in rat brain hippocampus[J]. J Cereb Blood Flow Metab, 1990, 10(1):133-5. |
| [11] | Hourton D, Delerive P, Stankova J, et al. Oxidized low-density lipoprotein and peroxisome-proliferator-activated receptor alpha down-regulate platelet-activating-factor receptor expression in human macrophages[J]. Biochem J, 2001, 354(Pt 1):225-32. |
| [12] | Lee M S. Role of innate immunity in the pathogenesis of type 1 and type 2 diabetes[J]. J Korean Med Sci, 2014, 29(8):1038-41. |
| [13] | Vitseva O I, Tanriverdi K, Tchkonia T T, et al. Inducible Toll-like receptor and NF-kappaB regulatory pathway expression in human adipose tissue[J]. Obesity (Silver Spring), 2008, 16(5):932-7. |
| [14] | Reyna S M, Ghosh S, Tantiwong P, et al. Elevated toll-like receptor 4 expression and signaling in muscle from insulin-resistant subjects[J]. Diabetes, 2008, 57(10):2595-602. |
| [15] | Nagyoszi P, Wilhelm I, Farkas A E, et al. Expression and regulation of toll-like receptors in cerebral endothelial cells[J]. Neurochem Int, 2010, 57(5):556-64. |
| [16] | Gorina R, Font-Nieves M, Márquez-Kisinousky L, et al. Astrocyte TLR4 activation induces proinflammatory environment through the interplay between MyD88-dependent NF-κB signaling, MAPK, and Jak1/Stat1 pathways[J]. Glia, 2011, 59(2):242-55. |
| [17] | Shi H, Kokoeva M V, Inouye K, et al. TLR4 links innate immunity and fatty acid-induced insulin resistance[J]. J Clin Invest, 2006, 116(11):3015-25. |
| [18] | Pasterkamp G, Van Keulen J K, De Kleijn D P. Role of Toll-like receptor4 in the initiation and progression of atherosclerotic disease[J]. Eur J Clin Invest, 2004, 34(5):328-334. |
| [19] | Montrucchio G, Alloatti G, Camussi G. Role of platelet-activating factor in cardiovascular pathophysiology[J]. Physiol Rev, 2000, 80(4):1669-99. |
| [20] | Liu X, Zhao G, Yan Y, et al. Ginkgolide B reduces atherogenesis and vascular inflammation in ApoE (-/-) mice[J]. PLoS One, 2012, 7(5):e36237. |

