


2. 陕西中医学院第一临床医学院, 陕西 咸阳 712046
2. the First Clinical Medical College, Shanxi University of Chinese Medicine, Xianyang Shanxi 712046, China
盐敏感性是高血压最重要的中间表现型之一。已有研究证实,交感神经系统调节缺陷是盐敏感者的关键病理生理特点,如盐负荷后的血浆去甲肾上腺素水平升高、心率变异性中的夜间低频成分增多和血压的应激反应增强等[1]。长期高盐摄入可在盐敏感者中形成交感中枢的抑制紊乱和相继外周交感神经张力增加,继而通过影响肾脏的血流动力学、肾小管对钠和水的处理,产生血压的盐敏感性[2, 3]。然而,在盐敏感性高血压形成中,交感神经活动增强的发生机制目前尚不清楚。发现盐敏感性形成的关键机制是高血压研究面临的重要问题。
Apelin是由同一基因编码的具有不同分子结构的一组内源性活性肽,该类肽通过作用于7次跨膜的G蛋白偶联受体APJ而参与心血管功能、体液平衡、神经系统功能等的调节。形态学研究表明,脑内Apelin和APJ主要分布于下丘脑、脑干和丘脑,包括室旁核(PVN)、视上核(SON)、延髓头端腹外侧核(RVLM)和孤束核(NTS)等心血管调节中枢[4, 5]。我们课题组近来的研究发现,延髓的头端腹外侧核和PVN的Apelin和APJ参与自发性高血压大鼠的交感神经异常活动的形成[5, 6]。然而,Apelin和APJ系统是否参与脑内盐敏感性的形成,以及是否具有调控效应,目前尚未见报道。因此,本实验采用腹主动脉缩窄方法建立压力负荷性高血压模型,观察高盐对压力超负荷大鼠的交感神经活性和脑内Apelin和APJ系统的影响,以明确APJ受体在脑内盐敏感性形成中的调节作用。
1 材料与方法 1.1 试剂与仪器ML221、benzamil和戊巴比妥钠为Sigma产品;兔抗APJ抗体为美国Santa Cruz生物技术公司产品;Power Lab数据分析处理系统为澳大利亚AD instrument公司产品;Qiagen RNeasy Mini Kit试剂盒为Qiagen公司产品;ABI Prism 7000 荧光定量PCR仪为美国ABI公司产品;去甲肾上腺素(norepinephrine,NE)酶联免疫试剂盒由美国Rocky Mountain Diagnostics公司提供;Apelin酶联免疫试剂盒由美国DRG国际有限公司提供。
1.2 实验动物和分组实验选用♂SD大鼠,体质量180~200 g,适应性喂养1周后,随机分成6组:假手术组(sham)、假手术+常规盐组(sham+R),假手术+高盐组(sham+H)、主动脉缩窄组(AB)、主动脉缩窄+常规盐组(AB+R)和主动脉缩窄+高盐组(AB+H)。实验动物由西安交通大学实验动物研究中心提供,合格证:SCXK(陕)2007-001。
1.3 主动脉缩窄大鼠模型大鼠2%戊巴比妥钠腹腔麻醉后,腹部正中线偏左0.5 cm处行纵切口,暴露腹主动脉,在肾动脉分支上1cm处游离腹主动脉,平行放置7号针头(直径0.7 mm),用0号缝合线将动脉与针头一并结扎后,抽去针头,形成约70% 管腔狭窄。假手术组不作主动脉结扎,其余步骤与手术组相同。术后4周,sham+H 和AB+H 组大鼠给予含8% NaCl 的高盐饲料,而sham+R和AB+R组大鼠给予含0.3% NaCl的常规饲料。大鼠在温度 22℃,湿度 30%~40%的环境中饲养,自由饮水和摄食。
1.4 动脉血压和心功能记录参照我们以前的方法[7],在实验的第5周末,各组大鼠给予2%异氟烷(isoflurane)吸入麻醉,分离右侧颈总动脉,将充有肝素生理盐水的自制导管插入颈动脉以及逆行插入左心室,经压力传感器与桥式放大器相连,经Power Lab数据分析处理系统记录各组大鼠的平均动脉血压(MAP)、心率(HR),以及左室收缩末期压(left ventricular end-systolic pressure,LVESP)、左室舒张末期压(left ventricular end-diastole pressure,LVEDP)及心室收缩时室内压最大上升速率(+dP/dt)。
1.5 酶联免疫法(ELISA)检测NE水平收集各组大鼠24 h尿液,使用ELISA分析尿NE水平。严格按照说明书进行操作,选择相应的波长,用酶标仪测定样品的吸光值,并用样品浓度进行标化。试剂盒的敏感性为1.5 μg·L-1。
1.6 Real-time PCR参照我们以前的方法[6, 7],用TRIzol一步法抽提细胞总RNA,经Qiagen RNeasy Mini Kit试剂盒提纯,并测定A260/280值,鉴定RNA浓度与纯度。APJ的引物探针由Invitrogen公司提供。取5 μg RNA用ABI逆转录试剂盒逆转录RNA合成cDNA,使用ABI公司7000型荧光定量PCR仪检测RNA表达,10 μL的反应体系中包括:1 μL cDNA、3.5 μL无核酸酶纯水、0.5 μL引物、5 μL TaqMan Mastermix。
1.7 Western blot参照我们以前的方法[6, 7],各组样品在细胞裂解液中提取蛋白后,按Bradford 法测定蛋白含量,用SDS-PAGE 凝胶电泳分离蛋白。电泳结束后,将蛋白从聚丙酰胺凝胶转移到硝酸纤维素膜上,并在室温下5% 的脱脂奶粉封闭液封闭1 h。加入兔抗APJ一抗(1 ∶ 400),4℃ 孵育过夜,漂洗3 次后,加入标记辣根过氧化物酶的抗兔的IgG二抗,室温下孵育1 h。膜在漂洗3次后,加入ECL 显色液,显色2 min,在暗室里曝光1~2 min,蛋白印迹结果采用图像分析系统进行分析。
1.8 侧脑室药物慢性灌流参照我们以前的方法[5],取主动脉缩窄模型建立4周后的大鼠,经2%戊巴比妥钠腹腔麻醉后,大鼠头部固定于脑立体定位仪,参照Paxinos和Watson大鼠脑图谱,无菌状态下将不锈钢套管(外径0.7 mm,内径0.4 mm,长11 mm)放入右侧侧脑室(前囟后1.0 mm,中线旁开1.4 mm,颅骨表面下4.5 mm),并用牙托粉固定于颅骨。其中内充ML221、benzamil或人工脑脊液(aCSF)的微渗透泵(model 2004,美国Alzet公司) 连接于套管外端进行侧脑室灌流,灌流速度为0.28 μL·h-1,时间为1周,ML221的剂量为50 μg ·kg-1·d-1和200 μg·kg-1·d-1,benzamil的剂量为100 μg·kg-1·d-1。将微渗透泵放置于大鼠背部皮下后,缝合切口,单笼饲养,同时给予含8% NaCl 的高盐饲料,观察记录侧脑室灌流1周后的尿NE水平和心脏指数(HW/BW)的变化。
另一组实验中,♂ SD大鼠,随机分为常规钠组和高钠组,每组6只。参照我们以前的方法,采用无创尾套法测压系统间接测定2组大鼠清醒状态下的血压和心率。在麻醉状态下,分别在右侧侧脑室植入连接微渗透泵的不锈钢套管。其中,高钠组大鼠给予高钠脑脊液(aCSF中Na+浓度为 800 mmol·L-1),常规钠组给予正常脑脊液(aCSF中Na+浓度为 145 mmol·L-1),进行侧脑室灌流,灌流速度为0.28 μL·h-1,时间为1周。实验结束后记录血压、心率、尿NE水平和PVN APJ表达的变化。
1.9 统计学分析实验数据以 表示,组间比较采用单因素方差分析,使用sigmastat 3.0软件处理。
表示,组间比较采用单因素方差分析,使用sigmastat 3.0软件处理。
如Tab1所示,SD大鼠行主动脉缩窄术4周后,与对照sham组比较,MAP、HR和LVESP均明显增加(P<0.01),而LVEDP、+dP/dt和尿NE水平未见明显变化(P>0.05)。压力超负荷大鼠给予高盐饮食1周后,与AB+R组比较,MAP、HR、LVESP和24 h尿NE水平均明显增加 (P<0.05);而sham组大鼠进食高盐饲料后,血流动力学和24 h尿NE水平均未见明显变化(P>0.05)。
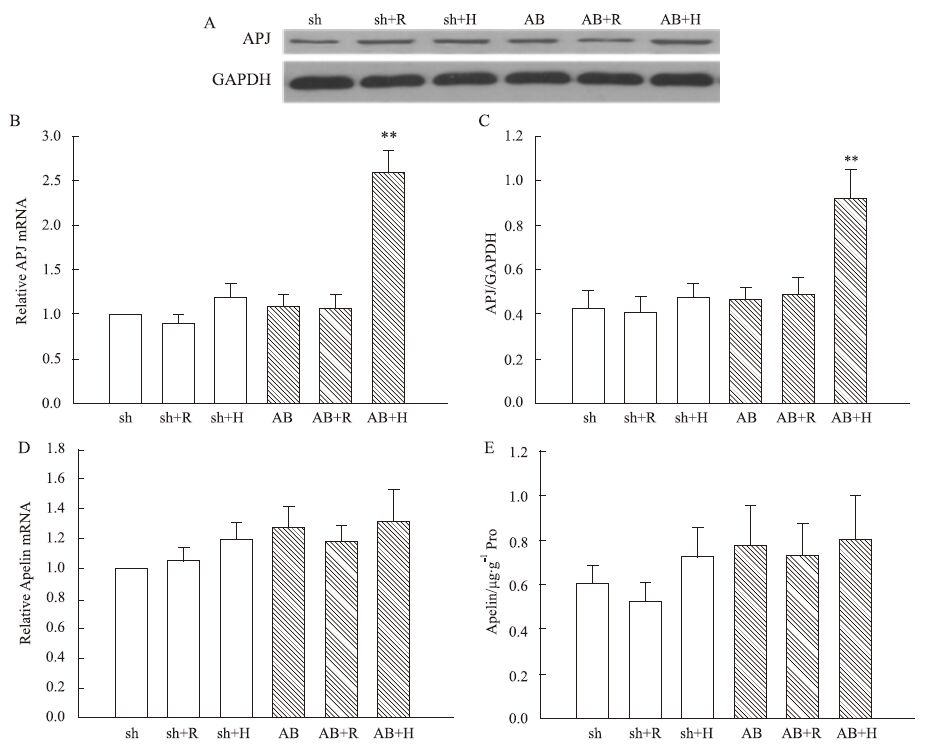
使用real-time PCR方法对各组大鼠下丘脑PVN的APJ mRNA和Apelin mRNA的表达进行分析,如Fig1B所示,AB+H组的APJ mRNA表达较对照组明显增加(P<0.01)。使用Western blot方法分析APJ的蛋白表达,如Fig1C所示,AB+H组PVN的APJ蛋白表达也较对照组明显增加(P<0.01),而各组Apelin的表达未见明显变化(P>0.05)。
|
Fig 1
Changes of Apelin and APJ expression in hypothalamic paraventricular nucleus of rats( , n=7)
A: Representative Western blot demonstrating the change of APJ expression in paraventricular nucleus of rats; B: Graphs showing APJ mRNA expression; C: Graphs showing APJ protein expression; D: Graphs showing Apelin mRNA expression. E: Graphs showing Apelin protein expression. **P<0.01 vs AB+R group. sh:sham; sh+R: sham+regular salt diet; sh+H: sham+high salt diet; AB: Aortic banding; AB+R: Aortic banding+ regular salt diet; AB+H: Aortic banding+ high salt diet. , n=7)
A: Representative Western blot demonstrating the change of APJ expression in paraventricular nucleus of rats; B: Graphs showing APJ mRNA expression; C: Graphs showing APJ protein expression; D: Graphs showing Apelin mRNA expression. E: Graphs showing Apelin protein expression. **P<0.01 vs AB+R group. sh:sham; sh+R: sham+regular salt diet; sh+H: sham+high salt diet; AB: Aortic banding; AB+R: Aortic banding+ regular salt diet; AB+H: Aortic banding+ high salt diet.
|
使用微渗透泵在AB+H组大鼠侧脑室分别灌注APJ拮抗剂ML221(50、200 μg ·kg-1·d-1)或ENaC拮抗剂benzamil(100 μg·kg-1·d-1)1周后,如Fig2所示,24 h尿NE水平和HW/BW比值均明显下调(P<0.05)。

|
Fig 2
Effect of intracerebroventricular infusion of APJ blocker or ENaC blocking on urinary NE levels and HW/BW ratio in AB+H rats( , n=6)
A: The 24 h U-NE in each group after ICV ML221(ABH+M5, ABH+M20) or benzamil(ABH+B)infusion; B: Heart weight to body weight ratio (HW/BW) in each group after ICV ML221(ABH+M5, ABH+M20) or benzamil(ABH+B)infusion. *P<0.05 vs ABH+C group. , n=6)
A: The 24 h U-NE in each group after ICV ML221(ABH+M5, ABH+M20) or benzamil(ABH+B)infusion; B: Heart weight to body weight ratio (HW/BW) in each group after ICV ML221(ABH+M5, ABH+M20) or benzamil(ABH+B)infusion. *P<0.05 vs ABH+C group.
|
使用微渗透泵ICV灌注高Na+脑脊液1周,如Fig3所示,与对照组相比,脑内APJ表达明显上调(P<0.01),同时可见MAP、 HR和24h尿NE水平明显增高(P<0.01)。而对照组大鼠在侧脑室灌流常规脑脊液后,MAP、 HR、24h尿NE和APJ表达水平均未见明显变化(P>0.05)。

|
Fig 3
Effect of intracerebroventricular infusion of Na+-rich aCSF on APJ protein expression in paraventricular nucleus of rats( , n=6)
A-B: Response of arterial pressure and heart rate to ICV high-Na+ aCSF infusion; C: 24 h U-NE excretion after ICV high-Na+ aCSF infusion; D: Western blot demonstrating the expression of APJ in paraventricular nucleus of rats. **P<0.01 vs Regular Na+ aCSF group.1 mmHg=0.133 kPa. , n=6)
A-B: Response of arterial pressure and heart rate to ICV high-Na+ aCSF infusion; C: 24 h U-NE excretion after ICV high-Na+ aCSF infusion; D: Western blot demonstrating the expression of APJ in paraventricular nucleus of rats. **P<0.01 vs Regular Na+ aCSF group.1 mmHg=0.133 kPa.
|
采用腹主动脉缩窄方法建立的压力负荷性高血压模型,是一个较为成熟的研究高血压病理机制的模型。本实验使用0.7 mm针头在右肾动脉上方1 mm处结扎,可形成腹主动脉70%~72%缩窄,术后4周平均动脉压、心率和左室收缩末期压均明显升高,提示该方法可以通过增加压力负荷形成高血压。
盐是高血压形成和病理进展的重要环境因素之一,大量研究发现个体间对盐负荷或限盐却存在敏感性差异。发现盐敏感性形成的关键机制是高血压研究面临的重要问题[2]。本实验发现,主动脉缩窄术4周后,给予含8% NaCl 的高盐饲料喂养1周,可以明显增加MAP、HR、LVESP以及尿NE水平,而对照大鼠的血流动力学和尿NE水平未见变化。该结果表明主动脉缩窄模型的盐敏感性增加,而高盐可通过增加交感神经活性升高血压并降低心功能。已有的研究也证实,高盐负荷作用于中枢神经系统,引起的交感神经活性异常增加,是高血压形成的重要机制[8]。
APJ的内源性配体为Apelin,基因定位于X染色体q25-26.1,编码一个77个氨基酸的前蛋白原。该蛋白原经过蛋白的水解作用断裂产生36、17和13个氨基酸大小的生物活性肽。APJ受体蛋白的30%氨基酸序列与血管紧张素AT1受体相同,而 在跨膜区相同氨基酸序列达54%,但并不与血管紧张素Ⅱ结合[4, 5]。在中枢神经系统内,Apelin/APJ 系统主要分布于下丘脑、脑干和丘脑,包括PVN、SON、RVLM和NTS等心血管调节中枢,其中在下丘脑的PVN和SON表达最高[6]。本研究发现高盐饲料可以明显上调压力超负荷大鼠PVN的APJ mRNA和蛋白的表达,而高盐饮食对正常大鼠的APJ表达无明显影响。该研究结果提示PVN内的APJ受体表达上调可能参与了脑内盐敏感性的形成。为进一步明确脑内APJ受体在盐敏性高血压形成中的作用,我们分别观察了侧脑室慢性灌流APJ受体拮抗剂ML221以及ENaC拮抗剂benzamil对外周交感神经活性的影响,结果发现ML221和benzamil均可降低高盐引起的尿NE水平变化,并下调大鼠的HW/BW比值,表明脑内的APJ受体是压力超负荷大鼠的盐敏感性增加的关键调控分子。
Simchon等[9]研究发现,盐敏感性高血压大鼠静脉给予4 μCi 22NaCl后,脑脊液中的22Na+浓度是盐抵抗性大鼠的5倍,表明盐敏感性大鼠的血脑屏障的通透性是Dahl盐抵抗性大鼠的5倍。PVN是自主性和内分泌性反应的重要整合中枢,且在维持心血管活动的动态平衡中起着关键作用。靠近中线处是小细胞性区域,靠近背侧是大细胞性区域。小细胞性区域的一些神经元细胞与RVLM、NTS和脊髓交感神经节前神经元直接联系,是交感神经活动调控的关键中枢[10]。已有研究发现,损毁Dahl盐敏大鼠的PVN则能阻止高盐诱发的高血压的形成,表明PVN在盐敏性高血压形成中发挥关键作用[8]。本实验使用微渗透泵在正常血压大鼠的侧脑室灌注高Na脑脊液后,PVN内APJ蛋白的表达明显上调,同时大鼠的MAP、HR和尿NE水平均明显增高,表明脑内APJ受体参与了盐敏感性高血压的交感神经异常活动的形成。
综上,本研究发现高盐可以增加压力超负荷大鼠模型的交感神经活性,而该效应与脑内的APJ受体表达上调和Na+敏感性增加密切相关。APJ受体可能是脑内盐敏感性形成的重要调控靶点。
| [1] | 罗怡, 陈明. 盐敏感性高血压研究进展[J].心血管病学进展, 2013,34(5):644-8. Luo Y, Chen M. Research process for salt-sensitive hypertension[J]. Adv Cardiovasc Dis, 2013,34(5):644-8. |
| [2] | Fujita T.Mechanism of salt-sensitive hypertension:focus on adrenal and sympathetic nervous systems[J]. J Am Soc Nephrol, 2014,25(6):1148-55. |
| [3] | Stocker S D, Monahan K D, Browning K N. Neurogenic and sympathoexcitatory actions of NaCl in hypertension[J]. Curr Hypertens Rep, 2013,15(6):538-46. |
| [4] | Yu X H, Tang Z B, Liu L J, et al. Apelin and its receptor APJ in cardiovascular diseases[J].Clin Chim Acta, 2014,428(1):1-8. |
| [5] | 张琪, 谭颖颖. 侧脑室慢性灌流(pyr1)apelin-13对大鼠心血管功能的影响[J].中国药理学通报, 2014,30(1):144-5. Zhang Q, Tan Y Y. Effect of chronic intracerebroventricular infusion of (pyr1) apelin-13 on cardiovascular regulatory actions[J]. Chin Pharmacol Bull, 2014,30(1):144-5. |
| [6] | Zhang Q, Yao F, Raizada M K, et al. Apelin gene transfer into the rostral ventrolateral medulla induces chronic blood pressure elevation in normotensive rats[J]. Circ Res, 2009,104(12):1421-8. |
| [7] | 张琪, 谭颖颖.血管紧张素1-7减弱醋酸去氧皮质酮盐型高血压大鼠的左心室重构[J].中国药理学通报, 2014,30(7):994-9. Zhang Q, Tan Y Y. Angiotensin 1-7 attenuates left ventricular remodeling in deoxycorticosterone acetate salt hypertensive rats[J]. Chin Pharmacol Bull, 2014,30(7):994-9. |
| [8] | Gabor A, Leenen F H.Central neuromodulatory pathways regulating sympathetic activity in hypertension[J]. J Appl Physiol, 2012,113(8):1294-303. |
| [9] | Simchon S, Manger W, Golanov E, et al. Handling 22NaCl by the blood-brain barrier and kidney:its relevance to salt-induced hypertension in dahl rats[J]. Hypertension, 1999,33(1 Pt 2):517-23. |
| [10] | Osborn J W, Olson D M, Guzman P, et al. The neurogenic phase of angiotensin Ⅱ-salt hypertension is prevented by chronic intracerebroventricular administration of benzamil[J]. Physiol Rep, 2014,2(2):e00245. |


