


2. 广东医学院药理学教研室, 广东 湛江 524023;
3. 广东省医学分子诊断重点实验室, 广东 东莞 523808
2. Dept of Pharmacology, Guangdong Medical College, Zhanjiang Guangdong 524023, China;
3. Guangdong Provincial Key Laboratory of Medical Molecular Diagnostics, Dongguan Guangdong 523808, China
血栓栓塞性疾病不仅发病率高,而且致死率和致残率也很高,如由血栓栓塞引起的心肌梗死、脑梗死、肺梗死居各种死亡原因之首。对血栓性疾病的防治药物主要包括抗凝血、抗血小板和溶栓药物。出血是目前临床抗栓药物防治最主要、最常见的并发症。传统的抗凝药物,如华法林、肝素、低分子量肝素(LMWH),以及近年上市的新药,如FXa抑制剂(利伐沙班、阿哌沙班等)和凝血酶抑制剂(达比加群酯、水蛭素等),对减少血栓形成均具有较好效果,但都还面临着共同的不足——可能引起出血并发症。因此,研发具有出血副作用小的抗栓新药具有重要价值。近年来,有关人类FXI缺陷或FXI水平升高的临床资料,以及动物FXI缺陷或被抑制的抗栓实验研究表明,FXI是出血风险小的抗栓防治新靶点。本文综述了相关研究进展,期望为出血风险小的抗栓新药研发提供参考。
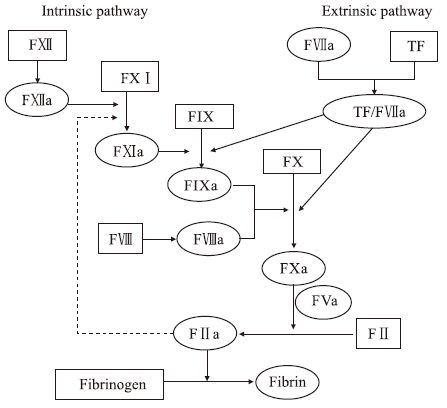
1 FXI在凝血级联反应及血栓形成中的作用凝血级联反应是系列凝血因子相继被激活,最终形成纤维蛋白的过程,见Fig1。凝血级联反应由内源性途径(又称接触激活途径)及外源性途径(又称组织因子途径)启动生成FXa,再经共同途径生成凝血酶(FIIa),最终形成纤维蛋白。FXI是维持内源性途径所必需的,而且在凝血级联反应放大过程中发挥关键作用[1]。在凝血级联反应中,凝血酶可反馈激活FXI,活化的FXI又促使凝血酶的大量产生,从而使凝血级联反应放大。因此,针对FXI靶点的药物可阻断内源性途径并抑制凝血级联反应的放大,从而具有抗血栓形成作用。同时,依赖FXIa生成的大量凝血酶可激活凝血酶激活的纤溶抑制物(TAFI)而下调纤溶系统。
|
| Fig 1 Coagulation cascade |
人类FXI缺陷症(FXI活性<15U/dL)又称C型血友病,该类病人出血表型温和[2]。FVIII缺陷及FIX缺陷病人(即甲型及乙型血友病)易引起自发性出血,常有关节和肌肉内出血,也可见血尿、皮肤瘀伤及手术后出血。FX、FV缺陷病人也有严重的出血表现,而凝血酶原、FVII是人体生理所必需的,如过量减少将会引起大量出血,严重者致死[3]。但FXI缺陷病人很少出现自发性出血,罕见有关节出血和肌肉内出血,出血倾向可发生于创伤或外科手术,尤其是在口腔、鼻和泌尿系统等高纤溶活性部位的创伤或外科手术,而其他外科创伤如整形外科、阑尾切除、包皮环割或皮肤切口等手术极少出现过量出血[2]。20%的严重FXI缺陷妇女生理期月经量过多,但严重FXI缺乏并不影响怀孕与分娩[2]。从FXI缺陷病人出血表型温和的特点来看,FXI被抑制时出血风险较小。
2.2 人类FXI缺陷症与血栓性疾病在FXI缺陷病人中,缺血性脑卒中及深静脉血栓(DVT)的发病率明显降低[4, 5],表明FXI被抑制是有利于减少缺血性脑卒中及深静脉血栓发病风险的。但有关FXI缺陷人群的研究数据还不能支持FXI缺陷对心肌梗死具有保护作用,需要进一步研究。
2.3 人类高水平FXI与血栓性疾病在有患者及对照各474人关于血栓形成倾向的研究中,高FXI水平人群(10%)的DVT发生风险是其他90%人群的2.2倍,表明高水平的FXI是DVT发生的危险因素,且FXI水平与DVT的发生呈正相关[6]。在一项FXI活性水平与脑血管疾病的关系研究中,发现22%的卒中及短暂性脑缺血病人、18%的静脉血栓病人的FXI活性水平高于95百分位的健康人群,即FXI水平升高可明显增加脑卒中及静脉血栓风险[7]。在有初发心肌梗死的560名男性(<70岁)中,FXI水平最高人群的心肌梗死风险是FXI水平最低人群的1.8倍[8]。FXI水平升高明显增加妇女(<50岁)缺血性脑卒中风险,也轻微增加心肌梗死风险[9]。这些研究表明,FXI水平升高可促进血栓性疾病的发生,如能抑制FXI则有可能减少血栓性疾病。
3 FXI基因敲除小鼠的血栓形成能力改变 3.1 FXI基因敲除小鼠与出血FVIII及FIX基因敲除小鼠容易出现自发性出血,FX、凝血酶原、FV及FVII基因敲除小鼠多会因引起出血而导致产前或产期死亡[3],提示在人体中如果因抗栓需要而过度抑制这些凝血因子时,可能产生大量出血乃至危及生命的后果。但FXI基因敲除小鼠却能健康存活,且繁殖力、止血功能与野生小鼠无异,也与FXI缺陷病人一样表现出活化部分凝血活酶时间(aPTT)延长而凝血酶原时间(PT)正常[10]。由此可见,针对FXI靶点的抗栓治疗可能比针对FVIII、FIX、FV、FX、凝血酶及FVII靶点的抗栓治疗具有更好的安全性,在减少出血风险方面具有明显优势。
3.2 FXI基因敲除小鼠的抗栓作用在用不同浓度FeCl3诱导C57BL/6小鼠颈总动脉血栓形成模型中,质量分数为3.5 % 的FeCl3诱导10 min能完全阻断野生型小鼠血管,但在FXI基因敲除小鼠,质量分数为5.0 % 的FeCl3还不能完全阻塞血管,7.5 % 的FeCl3仅能阻塞部分血管[11]。FXI基因敲除小鼠抗栓效果等同于高剂量肝素(1 000 U·kg-1),比阿司匹林(100 mg·kg-1)更有效。在FeCl3诱导下腔静脉血栓形成实验中,结果与上述相似,而且FXI基因敲除小鼠抑制下腔静脉血栓形成能力比高剂量肝素(1 000 U·kg-1)、氯吡格雷(30 mg·kg-1)、阿司匹林(100 mg·kg-1)或阿加曲班(30 mg·kg-1)更有效[12]。FXI基因敲除小鼠也能有效抑制激光损伤、挤压损伤及结扎引起的血栓形成[10, 13]。总的看来,FXI基因敲除小鼠能抑制动脉及静脉血栓形成,而且与几种临床应用的抗栓药物可能会引起小量出血相比较,FXI基因敲除小鼠的尾出血时间与野生型无差异[12],同样表明FXI可能是一个出血副作用小的抗栓防治靶点。
4 FXI抑制剂及其抗栓作用目前已发现的FXI抑制剂还较少,主要包括单克隆抗体、反义寡核苷酸、小分子抑制剂、肽模拟物及肽类抑制剂等。
4.1 单克隆抗体 4.1.1 aXIMabaXIMab是一种鼠抗人FXI A3结构域的单克隆抗体[14]。给予狒狒静脉注射2 mg·kg-1的aXIMab,在10天内几乎能完全抑制血浆FXI活性,并抑制凝血酶的形成和血小板的激活,减少动静脉旁路血栓中血小板沉积和血栓生成,而且不增加出血时间(BT),在抗栓效果及出血时间方面均优于32 mg·kg-1的阿司匹林[14]。
4.1.2 XI-5108XI-5108是一种鼠抗人FXI的单克隆抗体,其作用于FXI/FXIa的轻链而抑制FXa和FXIa的活化[15]。静脉注射3.0 mg·kg-1的XI-5108可明显减少兔髂动脉内膜血栓的形成,而对PT、BT及血小板聚集均没有影响[15]。
4.1.3 14E1114E11是FXI基因敲除Balb/C鼠抗鼠FXI的单克隆抗体,能有效抑制人、猪、家兔、狒狒、猕猴及大鼠等多种哺乳动物血浆FXI活性[16]。14E11与FXI的A2结构域结合后,阻断FXIIa活化FXI,但对FXIa的活性无影响。1.0 mg·kg-1 的14E11可保护小鼠免于质量分数为7.5% 的FeCl3诱导的血管阻塞,不会影响狒狒移植血管表面血小板的沉积,却能降低移植血管0.4的纤维蛋白沉积量[16]。14E11还能降低小鼠败血症引起弥散性血管内凝血(DIC)的发生,提高败血病小鼠的生存率[17]。
前述几种针对FXI靶点的单克隆抗体能抑制鼠、兔和狒狒等动物的血栓形成,也均有出血风险小的优势,但单抗往往价格昂贵,而且这些抗体目前均还处于临床前或候选药物研究阶段。此外,2 mg·kg-1的aXIMab几乎完全抑制血浆FXI活性,因此,aXIMab的抗栓阈值还有待明确。
4.2 反义寡核苷酸(antisense oligonucleotides,ASO)目前已有多种FXI反义寡核苷酸(FXI ASO)的抗栓实验研究。50 mg·kg-1鼠FXI ASO,每周2次,连续3周给药能降低98%鼠肝FXI mRNA及血浆FXI水平;FXI ASO使血浆aPTT延长,但不影响PT;FXI ASO对质量分数为10% 的FeCl3诱导的鼠下腔静脉血栓、肠系膜静脉血栓、降主动脉血栓及狭窄诱导的下腔静脉血栓形成均有很好抑制效果[18]。FXI mRNA减少60%~70%的水平就对FeCl3诱导的鼠下腔静脉血栓有明显抑制效果,而减少90%以上的FXI mRNA水平对鼠尾出血时间及手术出血时间均没有影响[18]。FXI ASO在减少出血副作用方面不但明显优于华法林,而且其与LMWH(enoxaparin)或血小板聚集抑制剂-氯吡格雷(plavix)联合用药时,可增加抗栓效果,也不增加出血风险[18]。鼠FXI ASO能抑制ApoE基因敲除小鼠粥样动脉硬化的血栓形成,并能抑制炎症反应[19]。FXI ASO可使兔颈静脉插入导管内的阻塞性血栓形成时间延长2.3倍[20]。
ISIS 416858是根据人和猕猴FXI 设计的ASO,目前已进入临床试验。连续13周皮下注射不同剂量ISIS 416858,猕猴肝FXI mRNA水平及血浆FXI活性与给药剂量呈依赖关系。每周给予40 mg·kg-1剂量,在第4周时,血浆FXI活性下降80%,延长33% aPTT,连续给药13周,动物BT、PT均正常[21]。FXI ASO使狒狒血浆FXI活性下降50%时,能抑制40%~50%的血栓生成;25 mg·kg-1剂量,每周3次,连续3周可使血浆FXI活性下降约50%,且不增加出血风险[22]。在对ISIS 416858(即ISIS-FXIRx)的临床I期试验中,受试者FXI活性出现持续的、剂量依赖地减少,并伴随着aPTT延长,即使体内FXI降至不能被检测的水平时,也不会出现与药物相关的出血症状[22]。ISIS-FXIRx对受试者心电图、肝功能及肾功能也没有明显影响[22]。在最近的临床II期试验中,观察了ISIS-FXIRx对全膝关节置换病人中VTE的防治及出血的影响(NCT01713361)(2014年8月完成)[23],但结果还没有公开。
从目前的研究看,FXI ASO非常有望发展成为出血副作用小的抗栓新药,但FXI ASO起效较慢,需要数周时间才能形成抗栓效果,在作为防治药物时可能会受到一定限制。
4.3 小分子抑制剂已发现的FXI小分子抑制剂主要包括4-羧基-2-氮杂环丁酮(BMS-262084)、分离自海绵的Clavatadine A和B、以及硫酸五没食子酰葡萄糖苷、单硫酸苯并呋喃、四氢喹啉和芳烃硼酸等的衍生物。BMS-262084抑制FXIa活性很强(IC50=2.8 nmol·L-1),比其他凝血因子选择性高70倍以上;延长正常人和大鼠血浆2倍aPTT时,对PT无影响[24]。BMS-262084能抑制FeCl3诱导的大鼠颈总动脉和深静脉血栓、生理电刺激诱导兔颈动脉血栓、动静脉旁路血栓的生成,但对组织因子引起的血栓无影响;高出2倍有效剂量的BMS-262084不会影响大鼠表皮、肠系膜及肾皮质的出血时间[24]。但BMS-262084对类胰蛋白酶也有较强的抑制作用(IC50=4.0 nmol·L-1),因此,需要进一步提高其抑制FXIa特异性。对其他FXI小分子抑制剂还缺少动物实验研究报道。
4.4 多肽/蛋白类抑制剂蛋白酶连接素 2(PN2)的蛋白酶抑制活性部位 PN2KPI由57个氨基酸残基组成,在人体生理灭活 FXIa 中发挥了重要作用,对 FXIa 有很强的抑制活性(Ki=0.81 nmol·L-1),对其他凝血因子如 FVIIa、FIXa 及纤溶酶等抑制活性很弱(Ki>400 nmol·L-1),但对胰蛋白酶有很强的抑制活性(Ki=0.03 nmol·L-1)[25]。利用FeCl3诱发小鼠颈动脉血栓和小鼠大脑中动脉血栓(MCAO)模型,证实了PN2KPI能有效防止血栓的形成且不引起出血[26]。PN2KPI作为人体生理性多肽,可能具有较好的人体安全性,但也可能被人体组织内的中胰蛋白酶降解而失活,其对胰蛋白酶具有更强的抑制活性是否会限制其在人体应用也还需要研究。
最近,从吸血生物-钩虫、蜱及吸血蝙蝠(desmodus rotundus) [27]中也分别分离到对 FXIa 具有较好抑制作用的多肽/蛋白,但他们同时还能抑制其他凝血因子或蛋白酶。我们课题组报道了钩虫抗凝肽 AduNAP4及AcaNAP10 对FXIa有较强抑制作用[28],并对AcaNAP10进行结构改造获得了FXIa的特异性抑制剂,目前正作为I类新药在进行临床前研究。
4.5 肽模拟物Lin等[29]研发了基于酮精氨酸的系列FXIa肽模拟物(peptidomimetics)抑制剂,其最有效的抑制剂的IC50约为6 nmol·L-1,延长2倍aPTT约需2.4 μmol·L-1,对小鼠静脉血栓形成抑制效果较好,但无有关后续报道。
4.6 其他抑制剂除PN2外,人体内还存在其他一些生理性FXIa抑制物,包括α1抗胰蛋白酶(α1-AT)、抗凝血酶Ⅲ(AT-Ⅲ)、C1 抑制物(C1-Inh)、α2 抗纤溶酶(α2-AP)及PN1等[30],但他们均是广谱的丝氨酸蛋白酶抑制剂,同时还对体内其它多种凝血因子或蛋白酶具有抑制作用。进一步了解这些抑制剂抑制FXIa的结构和作用机制,或许可为设计新的高效、特异性FXI抑制剂提供参考。
5 结语与展望FXI在凝血级联反应放大过程和内源性途径中发挥关键作用,与血栓性疾病的发生密切相关。高水平血浆FXI人群脑卒中及DVT发生风险增加,FXI缺陷病人DVT及脑卒中发病率降低,FXI基因敲除鼠能抑制多种物理及化学因素导致的血栓形成,表明FXI可以作为抗栓治疗新靶点。而FXI缺陷病人出血温和,FXI基因敲除鼠止血功能正常的特点又意味着抑制FXI靶点出血风险低。目前已研发了单抗、反义寡核苷酸、多肽及化学小分子等FXI抑制剂,但还比较少。单抗、反义寡核苷酸目前还存在着价格昂贵、起效慢、可能不易控制等不足,因此,研发特异性好、活性强的FXI多肽或小分子抑制剂值得期待。虽然已有的FXI抑制剂对小鼠、大鼠、兔及灵长类动物体内的血栓形成有较好的抑制效果,且出血副作用小,但在人体内的抗栓效果及副作用还需要进一步观察。总的看来,FXI是近年来才引起关注的具有出血风险小的抗栓防治新靶点,针对该靶点的新药可能能弥补目前临床抗凝抗栓药物易出现出血并发症的不足,将可能产生具有重大影响的重磅新药。
| [1] | Vine A K. Recent advances in haemostasis and thrombosis[J]. Retina, 2009,29 (1):1-7. |
| [2] | Seligsohn U. Factor XI deficiency in humans[J]. J Thromb Haemost, 2009,7 (Suppl 1):84-7. |
| [3] | Emeis J J, Jirouskova M, Muchitsch E M, et al. A guide to murine coagulation factor structure, function, assays, and genetic alterations[J]. J Thromb Haemost, 2007, 5 (4):670-9. |
| [4] | Salomon O, Steinberg D M, Koren-Morag N, et al. Reduced incidence of ischemic stroke in patients with severe factor XI deficiency[J]. Blood, 2008, 111 (8):4113-7. |
| [5] | Salomon O, Steinberg D M, Zucker M, et al. Patients with severe factor XI deficiency have a reduced incidence of deep-vein thrombosis[J]. Thromb Haemost, 2011, 105 (2):269-73. |
| [6] | Meijers J C, Tekelenburg W L, Bouma B N,et al. High levels of coagulation factor XI as a risk factor for venous thrombosis[J]. N Engl J Med, 2000, 342 (10):696-701. |
| [7] | Yang D T, Flanders M M, Kim H, Rodgers G M. Elevated factor XI activity levels are associated with an increased odds ratio for cerebrovascular events[J]. Am J Clin Pathol, 2006, 126 (3):411-5. |
| [8] | Doggen C J, Rosendaal F R, Meijers J C. Levels of intrinsic coagulation factors and the risk of myocardial infarction among men:Opposite and synergistic effects of factors XI and XⅡ[J]. Blood, 2006, 108 (13):4045-51. |
| [9] | Siegerink B, Rosendaal F R, Algra A. Antigen levels of coagulation factor XⅡ, coagulation factor XI and prekallikrein, and the risk of myocardial infarction and ischemic stroke in young women[J]. J Thromb Haemost, 2014,12 (5):606-13. |
| [10] | Renné T, Oschatz C, Seifert S, et al. Factor XI deficiency in animal models[J]. J Thromb Haemost, 2009, 7 (Suppl 1):79-83. |
| [11] | Wang X, Cheng Q, Xu L, et al. Effects of factor IX or factor XI deficiency on ferric chloride-induced carotid artery occlusion in mice[J]. J Thromb Haemost, 2005,3 (4):695-702. |
| [12] | Wang X, Smith P L, Hsu M Y, et al. Effects of factor XI deficiency on ferric chloride-induced vena cava thrombosis in mice[J]. J Thromb Haemost, 2006, 4 (9):1982-8. |
| [13] | Renné T. Safe(r) anticoagulation[J]. Blood, 2010, 116 (22):4390-1 |
| [14] | Tucker E I, Marzec U M, White T C, et al. Prevention of vascular graft occlusion and thrombus-associated thrombin generation by inhibition of factor XI[J]. Blood, 2009, 113 (4):936-44. |
| [15] | Yamashita A, Nishihira K, Kitazawa T, et al. Factor XI contributes to thrombus propagation on injured neointima of the rabbit iliac artery[J]. J Thromb Haemost, 2006, 4 (7):1496-501. |
| [16] | Cheng Q, Tucker E I, Pine M S, et al. A role for factor XⅡa-mediated factor XI activation in thrombus formation in vivo[J]. Blood, 2010, 116 (19):3981-9. |
| [17] | Tucker E I, Verbout N G, Leung P Y, et al. Inhibition of factor XI activation attenuates inflammation and coagulopathy while improving the survival of mouse polymicrobial sepsis[J]. Blood, 2012, 119 (20):4762-8. |
| [18] | Zhang H, L wenberg E C, Crosby J R, et al. Inhibition of the intrinsic coagulation pathway factor XI by antisense oligonucleotides:a novel antithrombotic strategy with lowered bleeding risk[J]. Blood, 2010, 116 (22):4684-92. |
| [19] | van Montfoort M L, Kuijpers M J, Knaup V L, et al. Factor XI regulates pathological thrombus formation on acutely ruptured atherosclerotic plaques[J]. Arterioscler Thromb Vasc Biol, 2014, 34 (8):1668-73. |
| [20] | Yau J W, Liao P, Fredenburgh J C, et al. Selective depletion of factor XI or factor XⅡ with antisense oligonucleotides attenuates catheter thrombosis in rabbits[J]. Blood, 2014, 123 (13):2102-7. |
| [21] | Younis H S, Crosby J, Huh J I, et al. Antisense inhibition of coagulation factor XI prolongs APTT without increased bleeding risk in cynomolgus monkeys[J]. Blood, 2012, 119 (10):2401-8. |
| [22] | Crosby J R, Marzec U, Revenko A S, et al. Antithrombotic effect of antisense factor XI oligonucleotide treatment in primates[J]. Arterioscler Thromb Vasc Biol, 2013,33 (7):1670-8. |
| [23] | Isis Pharmaceuticals. Active comparator-controlled study to assess safety and efficacy of ISIS-FXIRx in total knee arthroplasty[OL]. http://clinicaltrials.gov/show/NCT01713361. |
| [24] | Wong P C, Crain E J, Watson C A, Schumacher W A. A small-molecule factor XIa inhibitor produces antithrombotic efficacy with minimal bleeding time prolongation in rabbits[J]. J Thromb Thrombolysis, 2011,32 (2):129-37. |
| [25] | Navaneetham D, Sinha D, Walsh P N. Mechanisms and specificity of factor XIa and trypsin inhibition by protease nexin 2 and basic pancreatic trypsin inhibitor[J]. J Biochem, 2010, 148 (4):467-79. |
| [26] | Wu W, Li H, Navaneetham D,et al. The kunitz protease inhibitor domain of protease nexin-2 inhibits factor XIa and murine carotid artery and middle cerebral artery thrombosis[J]. Blood, 2012, 120 (3):671-7. |
| [27] | Ma D, Mizurini D M, Assumpão T C, et al. Desmolaris, a novel factor XIa anticoagulant from the salivary gland of the vampire bat (Desmodus rotundus) inhibits inflammation and thrombosis in vivo[J]. Blood, 2013, 122 (25):4094-106. |
| [28] | Li D, He Q, Kang T, et al. Identification of an anticoagulant peptide that inhibits both fXIa and fVⅡa/tissue factor from the blood-feeding nematode ancylostoma caninum[J]. Biochem Biophys Res Commun, 2010, 392 (2):155-9. |
| [29] | Lin J, Deng H, Jin L, et al. Design, synthesis, and biological evaluation of peptidomimetic inhibitors of factor XIa as novel anticoagulants[J]. J Med Chem, 2006, 49 (26):7781-91. |
| [30] | Navaneetham D, Jin L, Pandey P, et al. Structural and mutational analyses of the molecular interactions between the catalytic domain of factor XIa and the Kunitz protease inhibitor domain of protease nexin 2[J]. J Biol Chem, 2005, 280 (43):36165-75. |

