


帕金森病(Parkinson’s disease,PD)是常见的以运动功能障碍为主要特征的神经退行性疾病,临床常以补充左旋多巴为主的治疗,虽然能够改善PD的临床症状,但无法遏制其病理性改变。因此,研制能够延缓病理进展的抗PD创新药物对于提高人口健康水平具有重要意义。
PD缺乏有效治疗药物的主要原因是缺乏能够贴切模拟PD临床与病理变化的模型。因此,针对PD的病因及发病机制建立药物筛选模型,对于抗PD创新药物的研制具有重要意义。PD是多因素综合作用导致的疾病,除了衰老因素外,环境因素和遗传因素共同影响该病的发生与发展[1],而且环境因素可通过影响遗传因素加剧PD的病理过程及病理改变。因此针对PD相关的遗传因素进行抗PD药物研究更具理论和实际意义。导致PD发病的遗传因素与多种基因的突变、异常表达等有关,其中α-突触核蛋白(α-synuclein,α-syn)基因做为常染色体显性基因,其基因多倍体、突变后都能够导致家族性PD的发生[2],但具体的机制仍不清楚。鉴于α-突触核蛋白的异常改变能够影响PD的发生与发展,因此有学者提出“以α-突触核蛋白为靶点治疗PD”的学说[3],该学说已得到许多学者的认同,而且也发现某些具有神经保护功能的化合物能够对抗α-突触核蛋白的毒性作用[4]。因此以α-突触核蛋白损伤为靶点筛选具有抗PD作用的化合物更具特异性。
最初的研究认为α-突触核蛋白主要存在细胞内,近几年的研究发现:α-突触核蛋白可释放到细胞外,而胞外的α-突触核蛋白具有类似朊蛋白的功能,能够在神经细胞之间传递信息[5],促进神经元中路易小体的形成及神经元的死亡[6]。目前,有研究发现外源的α-突触核蛋白刺激神经细胞后,能够对神经细胞构成损伤[7],提示可建立相应的模型进行化合物的筛选,但目前应用这种模型还很少,其主要原因是α-突触核蛋白的来源和获取受到限制。
当前市场上已有商品化的α-突触核蛋白,但其价格昂贵,如果应用商品化的α-突触核蛋白建立模型进行大规模药物筛选将会造成很大的经济负担。本研究旨在通过建立α-突触核蛋白原核表达体系,优化表达和纯化条件并完成其科学鉴定,利用纯化的α-突触核蛋白作用神经细胞,建立以α-突触核蛋白损伤为靶点的细胞筛选模型,用于抗PD创新药物的研究。
NdeI和XhoI限制性内切酶及Taq酶购自TaKaRa,TRIzal购自Invitrogen;异丙基硫代半乳糖苷(isopropyl β-D-1-thiogalactopyranoside,IPTG),咪唑,考马斯亮蓝R250,SDS,丙烯酰胺,N,N′-亚甲基双丙烯酰胺,Agrose购自Amersoco;His TrapTMFF 亲和层析柱购自BD公司;α-突触核蛋白标准品购自Sigma公司;所有细胞培养基购自Gibco公司;胎牛血清购自Invitrogen公司;细胞培养耗材购自Corning, anti-α-synuclein购自Santa Cruz,anti-His购自Clontech,酵母粉、蛋白胨和琼脂购自Oxoid, PVDF膜购自Millipore。化学发光检测试剂购自普利莱公司,其他试剂为国产或进口分析纯试剂。
1.2 仪器ECL检测系统型号-Molecular Device,Lmax, 离心机 Sigma 16KP,基质辅助激光解吸附/飞行时间质谱仪-4800 plus, 美国ABI,酶标仪-Spectra Max190美国 MD,超声破碎仪-美国SONIC VCX 500。
1.3 细胞株和质粒PC12细胞购自医科院基础所细胞中心,载体pET30a来自Novagen。
1.4 目的基因获得与载体的构建根据GenBank中的α-突触核蛋白基因序列[gi:6806897],设计特异性引物,以pEGFP-N1-syn质粒为模板[8],PCR扩增目的基因,将扩增产物用NdeI和XhoI双酶切,回收酶切后的片段,与经过同样双酶切的载体pET30a按3 ∶ 1摩尔比混合,在T4DNA连接酶作用下于16℃连接过夜。过夜连接产物转化大肠杆菌Trans1-T1 Phage Resistant感受态细胞,涂布到含有质量浓度为50 g·L-1卡那霉素的LB平板上,于37℃培养过夜,次日,从LB平板上随机挑取菌落,接种于含有同样浓度卡那霉素的LB液体培养基中,于37℃培养16 h,提取质粒,然后用NdeI/XhoI进行双酶切鉴定,酶切鉴定为阳性的质粒进行测序。
1.5 目的基因在原核系统的表达用测序正确的质粒以及空载体pET30a转化大肠杆菌Trans BL21(DE3) pLysS化学感受态细胞,随机挑取1个菌落,接种于含有质量浓度为50 g·L-1卡那霉素的LB培养基中,于37℃培养过夜,次日按照1 ∶ 100的比例将过夜培养物转接到5 mL含同样浓度卡那霉素的LB液体培养基中,于37℃培养,当培养液OD600值达 到0.2-0.8时,加入不同浓度IPTG,继续培养一段时间,10 000×g离心15 min收集菌体,取适量菌体加入PBS重悬,超声裂解,取上清作为样品,SDS-PAGE电泳分析蛋白表达情况。
1.6 蛋白的纯化将诱导表达的菌体超声破碎,离心收集上清,缓慢加到已用5倍柱体积去离子水及10倍柱体积Binding Buffer (20 mmol·L-1 sodium phosphate,0.5 M NaCl,pH 7.4)平衡的His TrapTMFF 亲和层析柱上,流速控制在0.5~1.0 mL,然后用15倍柱体积的Binding Buffer 冲洗柱子,洗去杂蛋白。再分别用浓度10、20、30、40、50、60、70、80、100、250、500 mmol·L-1咪唑洗脱液竞争性梯度洗脱目的蛋白,并收集洗脱液。上述各个收集液取样处理,SDS-PAGE电泳检测蛋白的纯化情况。将含目的蛋白而不含杂蛋白的洗脱液进行浓缩,并用PBS置换Buffer后,冻存于-80℃。
1.7 SDS-PAGE电泳后染色及Western blot检测蛋白表达BCA试剂盒蛋白定量,样品蛋白加入上样缓冲液煮沸变性。然后经15%的SDS-PAGE分离,电泳结束后加入考马斯亮蓝R250染色液,固定染色1-2 h后脱色,观察蛋白的表达。样品蛋白经SDS-PAGE胶分离后转移到PVDF膜,质量浓度为30 g·L-1的BSA室温封闭2 h,加入一抗4℃过夜,TBS-Tween洗膜后加HRP标记的二抗,室温孵育2 h,加入ECL发光液,进行检测。
1.8 质谱法鉴定表达蛋白配置体积分数为0.3甲醇/0.7乙腈的溶液,用上述溶液配置体积分数为0.001的三氟乙酸,取上述三氟乙酸配置饱和芥子酸溶液为质谱用基质。去离子水配置目的蛋白,浓度为1 g·L-1,将目的蛋白和基质按照1 ∶ 1的体积比混匀,点样,上机检测。
1.9 细胞活力的检测细胞按5×107·L-1浓度接种于96孔版中,每孔100 μL(5 000细胞/孔),培养24 h,加入含有浓度为5、10、20、40 μmol·L-1 α-突触核蛋白的培养基处理,每组设6个复孔。培养24 h后,每孔加入10 μL MTT(质量浓度为50 mg·L-1,细胞孵育箱中培养4 h,弃培养基,加入100 μL DMSO,震荡至晶体颗粒溶解,10 min后在酶标仪上测定570 nm的吸光度(A)值。MTT法检测细胞存活率。细胞存活率/%=(实验组平均A值/对照组平均A值)×100%。
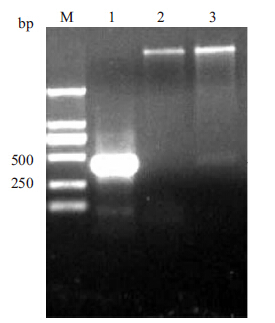
2 结果 2.1 pET-30a-syn融合载体的成功构建PCR扩增获得的目的基因片段经凝胶电泳分离后,在500 bp附近有特异性条带,与α-突触核蛋白基因片段的理论分子量基本一致。连接后获得的转化子提取的质粒,经酶切得到分子量小于500 bp的特异条带,与PCR产物大小一致(Fig 1),表明目的基因已成功克隆至载体。酶切阳性的克隆测序显示序列正确,可进行表达。
|
| Fig 1 The gel picture of α-synuclein cDNA fragment digested by NdeI and XhoI endonucleases M: Molecular weight marker DL2000; 1: cDNA fragment of α-synuclein; 2: pET30a; 3: pET30a-synuclein. |
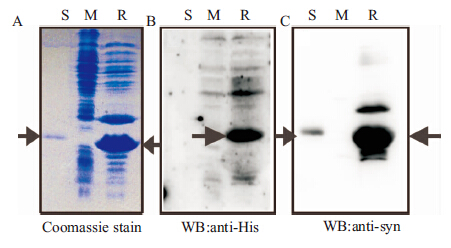
将空载体pET30a与重组载体的菌体裂解提取蛋白,经SDS-PAGE电泳分离后固定、染色及脱色,结果显示与空载体组相比,在分子量约为20 ku时可见特异性蛋白条带,大小与标准品基本一致,如Fig 2A所示。为了进一步验证表达的蛋白是否为目的蛋白,利用pET30a的标签抗体anti-his以及目的蛋白特异性抗体anti-α-synuclein,通过免疫印迹检测发现,在20 ku左右有特异性的条带,如Fig 2B,C。上述结果表明,位于20 ku附近的特异性条带是目的蛋白α-突触核蛋白。
|
| Fig 2 Expression and identification of recombinant α-synuclein A:The recombination protein of α-synuclein expressed in E.Coli. BL21 (DE3) was separated by SDS-PAGE electrophesis and stained by Coomassie brilliant blue; B: The recombination protein of α-synuclein was separated by SDS-PAGE and immblotted with anti-His antibody; C: The recombination protein of α-synuclein was separated by SDS-PAGE and immblotted with anti-synuclein antibody. (S: standard substance obtained from Sigma; M: sample of mock vecter pET30a; R: sample of recombinant vecter pET30a-synuclein.) |
温度、IPTG终浓度、宿主菌的增殖状态(用OD600表示)及不同表达时间能够影响外源蛋白在原核宿主菌的表达。根据不同的培养条件,观察宿主菌中目的蛋白的表达情况。结果(Fig 3)发现:当温度为30℃、培养菌液OD600值为0.2、IPTG终浓度为0.4 mmol·L-1时、诱导时间为7 h、目的蛋白的表达量最多,因此将此优化条件确定为α-突触核蛋白的表达条件。

|
| Fig 3 Optimization of expression condition about recombinant α-synuclein A: Expression of recombinant α-synuclein was induced by different concentrations of IPTG. M: Protein marker,1: Before induction,2: 0,3: 1×10-4 mol·L-1 IPTG; 4: 2×10-4 mol·L-1 IPTG[5: 3×10-4 mol·L-1 IPTG; 6: 4×10-4 mol·L-1 IPTG; 7: 5×10-4 mol·L-1 IPTG; 8: 6×10-4 mol·L-1 IPTG; 9: 7×10-4 mol·L-1; 10: 8×10-4 mol·L-1 IPTG; 11: 9×10-4 mol·L-1; 12: 10×10-4 mol·L-1 IPTG; B: Recombinant α-synuclein was expressed in E.Coli. BL21 (DE3) of different propagating state evaluated by their optical density (OD600). M: Protein marker; 1:before induction; 2: α-synuclein from Sigma 3:OD600=0.1; 4:OD600=0.2; 5:OD600=0.4; 6:OD600=0.6; 7:OD600=0.8; 8:OD600=1.0. C: Recombinant α-synuclein was expressed in E.Coli. BL21 (DE3) at differents temperature induced by 4×10-4 mol·L-1 IPTG. M:Protein marker; 1:before induction; 2:16 ℃;3: 20 ℃;4: 25 ℃;5: 28 ℃;6: 30 ℃;7: 37℃. D: Recombinant α-synuclein was induced by 4×10-4 mol·L-1 IPTG for different times. M: Protein marker; 1:berore induction; 2: 0 h; 3: 1 h; 4: 3 h; 5: 5 h; 6: 7 h; 7: 9 h; 8: 11 h; 9: 20 h. |
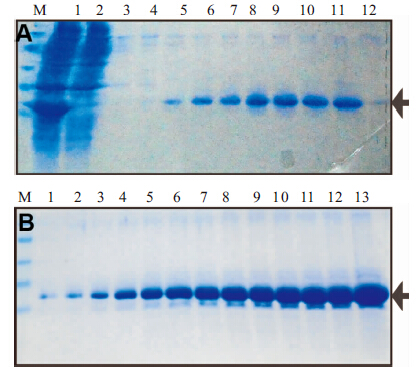
将诱导表达的菌体超声裂解破碎,离心收集上清,加到已用磷酸盐缓冲液平衡的HisTrapTM FF上,让其自然通过柱子,然后用含不同浓度咪唑的磷酸盐缓冲液进行梯度洗脱,收集各洗脱液进行SDS-PAGE检测,如Fig 4 A,采用20及40 mmol·L-1咪唑分阶段洗涤,250 mmol·L-1咪唑洗脱目的蛋白;大量样品经电泳分离后染色,并未发现更多的杂蛋白,如Fig 4 B,图片经灰度扫描后显示,目的蛋白纯度约为86%。
|
| Fig 4 Optimization of purification condition eluting the recombinant α-synuclein with different imidazole by His TrapTM FF column A: The recombinant α-synuclein was eluted from different concentration of imidazole. M: Protein marker; 1: 0; 2: 10 mmol·L-1 3: 20 mmol·L-1 4: 30 mmol·L-1 5: 40 mmol·L-1 6: 50 mmol·L-1 7: 60 mmol·L-1 8: 70 mmol·L-1 9: 80 mmol·L-1 10: 100 mmol·L-1 11: 250 mmol·L-1 12: 500 mmol·L-1. B: The purified α-synuclein was separated by SDS-PAGE gel. M: Protein marker; 1:0.5 μg; 2: 1 μg;3: 2μg; 4: 4μg; 5: 6μg; 6: 8μg; 7: 10 μg; 8:12 μg; 9: 14 μg; 10: 16 μg; 11: 18 μg; 12: 20 μg; 13: 40μg. Arrowhead points to the protein strand of α-synuclein. |
为了进一步明确纯化蛋白是否为α-突触核蛋白,将纯化蛋白进行质谱检测,质谱检测结果Fig 5 A显示商品化标准品的分子量为16.408 ku,Fig 5B显示目的蛋白分子量为15.34 ku,与理论分子质量15.52 ku基本一致,由此表明,该目的蛋白为α-突触核蛋白。

|
| Fig 5 Mass spectrum of α-synuclein A: α-synuclein from Sigma; B: The purified α-synuclein. |
α-突触核蛋白可直接对神经元产生损伤,因此本研究将不同浓度的α-突触核蛋白与PC12细胞或原代神经元共同孵育,通过MTT法检测细胞活力。结果Fig 6A显示,α-突触核蛋白浓度为5 μmol·L-1时,PC12细胞存活率已经开始减弱,浓度为10、20、40 μmol·L-1时,随着浓度的增加,α-突触核蛋白对PC12的损伤也越来越明显,呈一定的剂量依赖性。Fig 6B显示,α-突触核蛋白与原代神经元共孵育时,对原代神经元的损伤也具有剂量依赖性,并具有统计学意义。

|
| Fig 6 Toxic effect of recombinant α-synuclein A: Effects of purified α-synuclein decreased the viability of PC12 cells. B: Effects of purified α-synuclein decreased the viability of primary cells. Results were repeated 3 times. **P<0.01 vs control. |
α-突触核蛋白是由140个氨基酸组成的小分子蛋白,目前生理功能仍不清楚。有研究表明,在生理状态下,α-突触核蛋白能够参与神经递质的释放,并与囊泡的转运有关。研究表明,α-突触核蛋白无论是过表达、突变还是发生异常修饰,都能够造成神经元的损伤或神经退行性改变[9],但具体的作用机制仍需进一步研究。
近来研究发现,细胞外异常的α-突触核蛋白能够影响神经元的功能[6]或毒性作用[10]。研究发现细胞外的α-突触核蛋白不仅能够促进路易小体的形成 [11],同时也能够诱导胶质细胞的激活,促进神经炎症的发生[12],从而进一步加 剧神经元的损伤。胞外的α-突触核蛋白能够通过多种方式 发挥毒性作用,如自身形成离子通道激活钾离子通道;降低胞质膜中胆固醇的含量,改变脂筏中离子通道的分布,从而影响多巴胺的释放[13];其最终的其毒性机制都可能与促进细胞内氧化和硝基化应激有关[14]。
研究证明,胞外的α-突触核蛋白与神经细胞的功能相互影响,在神经元功能紊乱时促进α-突触核蛋白释放到胞外[15],因此胞外的α-突触核蛋白可做为疾病进展的标志物,而研究细胞外α-突触核蛋白的作用能够为阐明PD的发病机制提供更多的理论线索。本研究将α-突触核蛋白与神经细胞共孵育,模拟中枢神经系统细胞外的α-突触核蛋白对神经元的作用模式,在某种程度上可模拟PD发病过程的某一环节,有利于研究胞外的α-突触核蛋白对神经元的毒性机制。基于此建立α-突触核蛋白损伤神经元的细胞模型,可进行抗PD创新药物的研究,对抗帕金森创新药物的筛选以及作用机制的研究具有重要意义。
模型的建立,需要大量的α-突触核蛋白。为了获得大量的人源性α-突触核蛋白,研究中首先通过分子克隆技术成功构建了α-突触核蛋白原核表达载体,鉴定成功后进行诱导表达,并优化表达和纯化条件,可为后续标准操作程序的建立提供依据。获得的蛋白结果通过电泳、蛋白免疫印迹和质谱技术,确认α-突触核蛋白的正确表达并且纯度超过86%,为模型的建立提供了物质保障。目前体外筛选抗PD化合物还主要是通过评价细胞存活率的方法进行筛选,通过将α-突触核蛋白与类神经细胞PC12及原代神经元共孵育,结果发现,α-突触核蛋白能够直接导致上述细胞存活率明显下降,由此可根据细胞存活率的改变筛选到具有抗α-突触核蛋白损伤的活性化合物,这些活性化合物将对治疗PD更具有特异性。
| [1] | Edwards T M, Myers J P. Environmental exposures and gene regulation in disease etiology[J]. Cien Saude colet, 2008, 13(1):269-81. |
| [2] | Pals P, Lincoln S, Manning J, et al. alpha-Synuclein promoter confers susceptibility to Parkinson's disease[J]. Ann Neurol, 2004, 56(4):591-5. |
| [3] | Brundin P, Olsson R. Can alpha-synuclein be targeted in novel therapies for Parkinson's disease?[J]. Expert Rev Neurother, 2011, 11(7):917-9. |
| [4] | 沈 琮,张 兰,李 林.以α-synuclein为靶点的抗帕金森病药物研究进展[J].中国药理学通报,2014,30(2):149-52. |
| [4] | Shen C, Zhang L,Li L.Advance in research on anti-Parkinson's disease drugs targeting α-synuclein[J].Chin Pharmacol Bull,2014,30(2):149-52. |
| [5] | Freundt E C, Maynard N, Clancy E K, et al. Neuron-to-neuron transmission of alpha-synuclein fibrils through axonal transport[J]. Ann Neurol, 2012, 72(4):517-24. |
| [6] | Lee H J, Bae E J, Lee S J. Extracellular alpha-synuclein-a novel and crucial factor in Lewy body diseases[J]. Nat Rev Neurol, 2014, 10(2):92-8. |
| [7] | Volpicelli-Daley L A, Luk K C, Lee V M. Addition of exogenous alpha-synuclein preformed fibrils to primary neuronal cultures to seed recruitment of endogenous alpha-synuclein to Lewy body and Lewy neurite-like aggregates[J]. Nat Protoc, 2014, 9(9):2135-46. |
| [8] | Yuan Y, Jin J, Yang B, et al. Overexpressed alpha-synuclein regulated the nuclear factor-kappaB signal pathway[J]. Cell Mol Neurobiol, 2008, 28(1):21-33. |
| [9] | Cookson M R. alpha-Synuclein and neuronal cell death[J]. Mol Neurodegener, 2009, 4:9. |
| [10] | Gassowska M, Czapski G A, Pajak B, et al. Extracellular alpha-synuclein leads to microtubule destabilization via GSK-3beta-dependent Tau phosphorylation in PC12 cells[J]. PloS one, 2014, 9(4):e94259. |
| [11] | Desplats P, Lee H J, Bae E J, et al. Inclusion formation and neuronal cell death through neuron-to-neuron transmission of alpha-synuclein[J]. Proc Natl Acad Sci USA, 2009, 106(31):13010-5. |
| [12] | Alvarez-Erviti L, Couch Y, Richardson J, et al. Alpha-synuclein release by neurons activates the inflammatory response in a microglial cell line[J]. Neurosci Res, 2011, 69(4):337-42. |
| [13] | Ronzitti G, Bucci G, Emanuele M, et al. Exogenous alpha-synuclein decreases raft partitioning of Cav2.2 channels inducing dopamine release[J].J Neurosci, 2014, 34(32):10603-15. |
| [14] | Wilkaniec A, Strosznajder J B, Adamczyk A. Toxicity of extracellular secreted alpha-synuclein:Its role in nitrosative stress and neurodegeneration[J]. Neurochem Int, 2013, 62(5):776-83. |
| [15] | Lee H J, Cho E D, Lee K W, et al. Autophagic failure promotes the exocytosis and intercellular transfer of alpha-synuclein[J]. Exp Mol Med, 2013, 45:e22. |

