


 , BAO Kai-fan, JIANG Xiao-yan, WEI Xiao, YU Xi, TAO Yu, WANG Xiao-yu, WANG Yan, HONG Min
, BAO Kai-fan, JIANG Xiao-yan, WEI Xiao, YU Xi, TAO Yu, WANG Xiao-yu, WANG Yan, HONG Min

近年来过敏性疾病的发病率不断上升,已知上皮细胞(EC)是过敏性疾病中激发和调节免疫反应的关键参与细胞,其分泌的细胞因子TSLP、IL-33作为关键启动因子可能成为干预过敏性疾病的重要靶点[1, 2]。在皮肤过敏性疾病中,角质形成细胞是上述因子的主要来源[3],故可选择角质形成细胞考察上述关键因子的产生及药物的影响。但对于不同刺激剂和不同培养环境对角质细胞内细胞因子表达的影响依然知之甚少[4]。因此,本实验利用体外培养的HaCaT 细胞,观察不同刺激因素对HaCaT细胞中TSLP、IL-33表达水平的影响,探讨过敏性疾病中TSLP、IL-33的表达的最佳刺激条件,为过敏性疾病病理机制及药物作用的研究提供实验基础。
1 材料与方法 1.1 材料 1.1.1 试剂无血清培养液K-SFM (keratinocyte serum free medium 1X)、牛垂体浸膏(bovine pituitary extract)、rhEGF、Trypsin、山羊血清、胰酶抑制剂,均为Gibco产品;Poly(I:C)、LPS、PMA均为Sigma生产;TNF-α、PeproTech;TSLP(FL-159)、rabbit polyclonal IgG、IL-33(M-266、rabbit polyclonal IgG,Goat anti-rabbit IgG-FITC,为Santa Cruz Biotechnology产品;DAPI(5 g·L-1),抗荧光淬灭封片液,Beyotime Biotechnology产品;TritonX-100,北京鼎国生物技术有限公司生产;BSA,上海惠兴生化试剂有限公司;Human TSLP ELISA Kit,eBioscience公司;Human IL-33 ELISA Kit,RD Systems公司;总蛋白定量试剂盒(BCA法),南京建成生物工程研究所。
1.1.2 仪器净化工作台,苏州净化设备公司,SW-CJ-1F;CO2细胞培养箱,日本三洋公司,MCO-20AIC;倒置荧光显微镜,日本Nikon公司,Nikon Ti;高压灭菌器,日本三洋公司,MLS-3030CH;低速自动平衡离心机,北京医用离心机厂,型号LDZ5-2;多功能酶标仪,型号:SyneRgy HT,美国Bio-Tek。
1.1.3 细胞人角质形成细胞HaCaT由南京大学模式动物研究所馈赠,用角质形成细胞无血清培养液(K-SFM)添加重组人表皮生长因子(rhEGF) 2.5 μg·L-1和牛垂体提取物(BPE)25 mg·L-1体外培养人HaCaT。用胰酶消化,洗涤一次后加入培养液重悬,转移到放置有无菌盖玻片的细胞培养板中,置37 ℃、5% CO2孵箱内培养。
1.2 方法 1.2.1 实验分组及处理单独刺激剂的量效关系考察 实验分为6组(对照组、Poly(I:C)组、TNF-α组、LPS组、PMA组、Trypsin组),每组3个复孔,刺激HaCaT细胞12 h后收取上清液,采用ELISA法和免疫荧光技术检测不同刺激剂组TSLP和IL-33细胞因子表达水平,筛选出表达明显的刺激浓度。Poly(I:C)组采用0.1、1、10、100 mg·L-1不同浓度单独刺激,TNF-α组采用20、100、200 μg·L-1不同浓度单独刺激,LPS组采用5、20、50 mg·L-1不同浓度单独刺激,PMA组采用10、50、100 mg·L-1不同浓度单独刺激,Trypsin组采用10、100、1 000 nmol·L-1不同浓度单独刺激,并加无血清培养液作为对照组。
联合刺激剂的量效关系考察 根据上述实验筛选出的刺激剂,将实验分为4组[对照组、Poly(I:C)组、TNF-α组、Poly(I:C)与TNF-α联合组]进行,每组3个复孔,刺激HaCaT细胞12 h后收取上清液,采用ELISA 法和免疫荧光技术检测不同刺激剂组TSLP和IL-33的表达水平。Poly(I:C)组采用0.1、1、10、100 mg·L-1不同浓度单独刺激,TNF-α组采用20、100、200 μg·L-1不同浓度单独刺激,Poly(I:C)与TNF-α组采用TNF-α 20 μg·L-1分别与Poly(I:C)0.1、1、10、100 mg·L-1 4个浓度联合刺激,并加无血清培养液作为对照组。
联合刺激剂刺激HaCaT细胞的时效关系考察 实验分为4个组,0 h组、6 h组、12 h组和24 h组,每组6个复孔。对HaCaT细胞采用Poly(I:C)100 mg·L-1与TNF-α 20 μg·L-1联合刺激0、6、12和24 h后收取培养上清液,0 h组作为对照组,采用ELISA 法检测不同时间点TSLP和IL-33的表达水平。
1.2.2 TSLP和IL-33的检测免疫荧光检测 将细胞接种到无菌盖玻片上爬片培养24 h,细胞融合80%左右后,按1.2.1方案加入刺激剂处理后取出,4%多聚甲醛固定30 min,1.5%山羊血清封闭60 min,然后加一抗4℃过夜,PBS冲洗后加FITC标记的二抗37 ℃孵育2 h后,DAPI复染核5 min,封片,用荧光显微镜观察细胞中TSLP和IL-33的表达,蓝色代表细胞核,绿色代表TSLP和IL-33的表达。
ELISA检测,收集各组细胞培养上清液,保存在-20 ℃冰箱中,采用Human- TSLP、IL-33 ELISA试剂盒中推荐的步骤,检测细胞培养上清液中TSLP和IL-33的表达水平。并通过样本总蛋白定量检测进行样本蛋白校正。
1.2.3 统计学处理数据采用SPSS 12.0软件进行分析,检测数据以x±s表示,多组间数据采用方差分析(one-way ANOVA),组间两两比较采用Student-t检验。
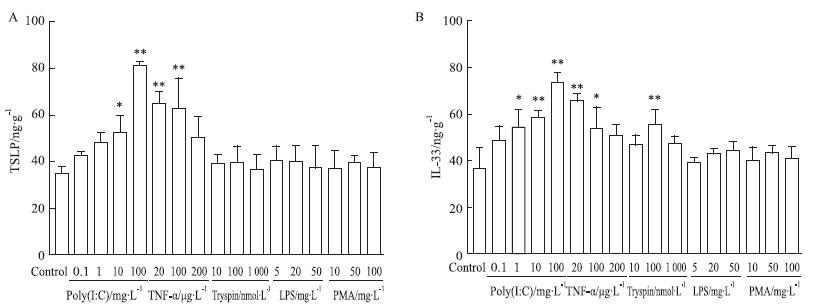
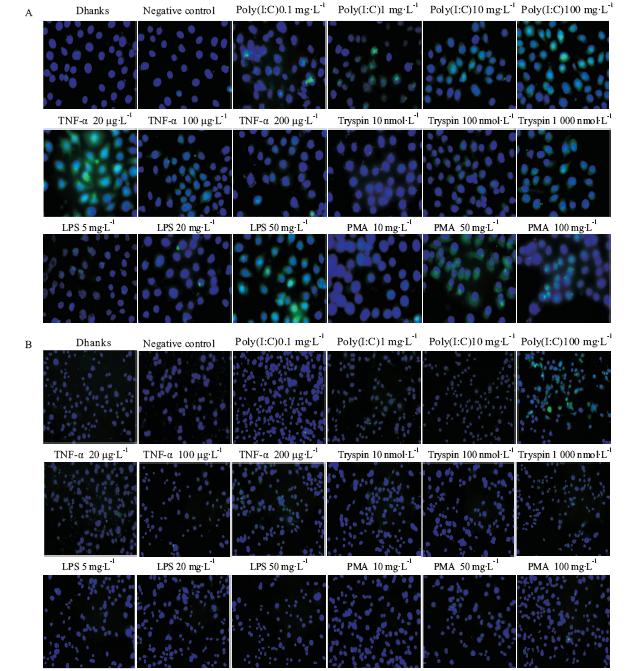
2 结果 2.1 单独刺激剂时HaCaT细胞分泌TSLP和IL-33的量效关系用不同刺激剂刺激HaCaT细胞12 h后收集细胞上清液,ELISA法测定上清液中TSLP(Fig 1A)、IL-33(Fig 1B)的含量,免疫荧光法检测细胞中TSLP(Fig 2A)、IL-33(Fig 2B)的表达。结果表明,Poly(I:C)10、100 mg·L-1与TNF-α 20、100 μg·L-1浓度能明显刺激HaCaT细胞表达TSLP。Poly(I:C)组1、10、100 mg·L-1,TNF-α组20、100 μg·L-1以及Trypsin组100 nmol·L-1浓度能明显刺激HaCaT细胞表达IL-33,其余组别浓度未见明显差异。
|
| Fig 1 TSLP and IL-33 levels in HaCaT cells under different stimulants by ELISA A:TSLP; B:IL-33,*P<0.05,**P<0.01 vs control |
|
| Fig 2 Effects of different stimulants on TSLP(A)and IL-33(B) levels of HaCaT cells in co-culture system (immunofluorescence,A,×630;B,×200) |
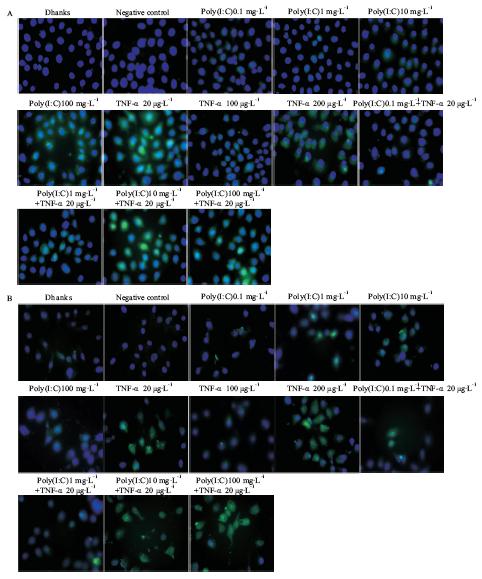
为进一步筛选出刺激HaCaT细胞表达TSLP和IL-33的最佳刺激剂,采用上述实验中表达比较明显的poly(I:C)组和TNF-α组中表达较高的TNF-α 20 μg·L-1联合刺激,并与单独的poly(I:C)组和TNF-α 组进行比较。采用ELISA(Fig 3)和免疫荧光(Fig 4)检测结果显示,Poly(I:C)100 mg·L-1 与TNF-α 20 μg·L-1联合刺激时HaCaT细胞中TSLP(Fig 3A,Fig 4A)和IL-33(Fig 3B,Fig 4B)的表达最为明显。

|
| Fig 3 Changes of TSLP and IL-33 levels in HaCaT cells under combined stimulants by ELISA A:TSLP; B:IL-33;*P<0.05,**P<0.01 vs control |
|
| Fig 4 Effects of combined stimulants on TSLP(A)and IL-33(B) levels of HaCaT cells in co-culture system (immunofluorescence,A,×630;B,×200) |
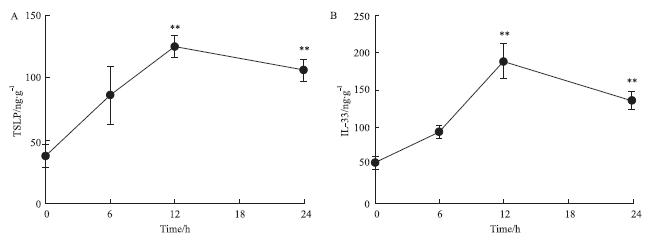
用poly(I:C)100 mg·L-1与TNF-α 20 μg·L-1联合刺激HaCaT,于0、6、12、24 h收集细胞上清,ELISA法测定TSLP和IL-33含量。结果显示与0 h相比:poly(I:C)100 mg·L-1与TNF-α 20 μg·L-1联合刺激12、24 h后,HaCaT细胞中TSLP(Fig 5A)和IL-33(Fig 5B)的表达都明显提高,其中以12 h最为明显,故选择poly(I:C)100 mg·L-1与TNF-α 20 μg·L-1联合刺激HaCaT细胞12 h做为HaCaT细胞表达TSLP和IL-33的最佳时间。
|
| Fig 5 -effect curve of TSLP and IL-33 expression of HaCaT cells in combined stimulants system A:TSLP:B:IL-33;**P<0.01 vs control |
近年来研究表明,角质形成细胞在过敏性疾病的发生和发展过程中起重要作用,其分泌的细胞因子TSLP和IL-33作为关键启动因子可能成为干预过敏性疾病的重要靶点[5, 6]。TSLP主要由上皮细胞和肥大细胞分泌。属 IL-7家族成员,其受体由IL -7 Rα和TSLPR组成。TSLP与受体结合后引起过敏性炎症反应[7]。IL-33是最新发现的IL-1家族成员,是一个组织来源的细胞因子[8]。其受体为ST2,两者结合可以介导Th2免疫反应[9]。本研究通过筛选角质形成细胞中TSLP和IL-33表达的最佳刺激条件来建立适宜的过敏性疾病细胞模型。Toll样受体(TLRs)作为连接天然免疫与特异性免疫的关键元件,在炎症反应、细胞信号转导方面起重要作用[10]。前期研究报道,TLR2、3、4、8、9与上皮细胞分泌TSLP和IL-33联系密切,尤其是TLR3和TLR4[11],它们的配体分别是Poly(I:C)和LPS,能介导过敏性炎症反应。TNF-α也是过敏性疾病中的一种重要免疫调节因子,在炎性免疫反应中调控部分炎性介质并协同刺激T淋巴细胞分泌细胞因子[12]。另有报道蛋白激酶C(PKC)的激活物PMA和Tryspin也被用于过敏性疾病研究中。PKC可激活下游蛋白激酶的磷酸化形成级联反应,引起T细胞活化,促进IL-33及其受体的表达[13, 14]。而细胞结构完整性和通透性的破坏,也会影响细胞膜的免疫应答、细胞分裂与分化等功能,Tryspin可使黏蛋白膜水解,导致上皮细胞间连接蛋白表达减少,继而促进TSLP的表达增多,引发Th2型过敏性反应[15]。
本实验选择Poly(I:C)、TNF-α、LPS、PMA和Trypsin等5种刺激剂对HaCaT细胞进行刺激,观察不同刺激剂和不同培养环境对HaCaT细胞分泌TSLP和L-33 细胞因子的影响,并根据TSLP和IL-33的表达水平进而考察不同刺激条件时的量效关 系和时效关系,筛选出Poly(I:C)100 mg·L-1 与TNF-α 20 μg·L-1联合刺激HaCaT细胞12 h后TSLP和IL-33的表达水平升高最为明显。该实验获得了HaCaT细胞分泌TSLP和IL-33的最佳刺激条件,将此作为过敏性疾病体外细胞模型来模拟过敏性疾病的致病因素和病理过程,为探索药物对过敏性疾病初期的作用及其机制提供了实验依据。
| [1] | Zhu D D, Jiang X D,Zhu X W, Dong Z. Thymic stromal lymphopoietin expression is increased in nasal epithelial cells of patients with mugwort pollen sensitive-seasonal allergic rhinitis[J]. Chin Med J, 2009, 122(19):2303-7. |
| [2] | Nakanishi W, Yamaguchi S, Matsuda A, et al. IL-33, but not IL-25, is crucial for the development of house dust mite antigen-induced allergic rhinitis[J]. PloS One, 2013, 8(10):e78099. |
| [3] | Kim B S,Siracusa M C,Saenz S A, et al. TSLP elicits IL-33-independent innate lymphoid cell responses to promote skin inflammation[J]. Sci Transl Med, 2013, 5(170):1-16. |
| [4] | 周茂华,吴长有.不同刺激剂和培养环境对CD4+、CD8+T细胞内细胞因子表达的影响[J]. 细胞与分子免疫学杂志, 2007, 23(2):168-71. Zhou M H,Wu C Y. Cytokine expression of CD4+and CD8+T cells induced by different stimuli underdifferent culture conditions [J]. Chin J Cell Mol Immunol, 2007, 23(2):168-71. |
| [5] | Kumar S, Khodoun M,Kettleson E M, et al.Glyphosate-rich air samples induce IL-33, TSLP and generate IL-13 dependent airway inflammation[J]. Toxicology, 2014, 325(1):42-51. |
| [6] | Muto T, Fukuoka A,Kabashima K, et al.The role of basophils and proallergic cytokines, TSLP and IL-33, in cutaneouslysensitized food allergy[J]. Int Immunol, 2014, 26(10):539-49. |
| [7] | 桂黎黎,洪 敏,王慧珠,等.基于Th2型过敏性炎症的胸腺基质淋巴细胞生成素产生小鼠模型的建立[J]. 中国药理学通报, 2013, 29 (10):1473-4. Gui L L,Hong M,Wang H Z, et al.A mouse of TSLP production based on Th2 cell-cell-mediated allergic inflammation[J]. Chin Pharmacol Bull, 2013, 29 (10):1473-4. |
| [8] | van de Veerdonk F L,Netea M G. New insights in the immunobiogy of IL-1 family members[J]. Front Immunol, 2013, 8(4):167. |
| [9] | Murakami-Satsutani N,Ito T,Nakanishi T, et al.IL-33 promotes the induction and maintenance of Th2 immune responses by enhancing the function of OX40 ligand[J]. Allergol Int, 2014, 63(3):443-55. |
| [10] | Nakamura N,Tamagawa-Mineoka R,Ueta M, et al.Toll-like receptor 3 increases allergic and irritant contact dermatitis[J]. J Invest Dermatol, 2014, 17(1):402. |
| [11] | Tse K,Horner A A.Defining a role for ambient TLR ligand exposures in the genesis and prevention of allergic diseases[J]. Semin Immunopathol,2008, 30(1):53-62. |
| [12] | Byrne A M,Goleva E,Chouiali F,et al. Induction of GITRL expression in human keratinocytes by Th2 cytokines and TNF-α:implications for atopic dermatitis[J]. Clin Exp Allergy,2012, 42(4):550-9. |
| [13] | Sanada S,Hakuno D,Higgins L J,et al. IL-33 and ST2 comprise a critical biomechanically induced and cardioprotective signaling system[J]. J Clin Invest, 2007, 117(6):1538-49. |
| [14] | Lefrançais E,Roga S,Gautier V, et al. IL-33 is processed into mature bioactive forms by neutrophil elastase and cathepsin G[J]. Proc Natl Acad Sci USA,2012, 109(5):1673-8. |
| [15] | Heijink I H,Kies P M,Kauffman H F, et al. Down-regulation of E-cadherin in human bronchial epithelial cells leads to epidermal growth factor receptor-dependent Th2 cell-promoting activity[J]. J Immunol, 2007, 178(12):7678-85. |