


法尼醇X受体(farnesoid X receptor,FXR)是核激素受体超级家族的一员,它主要分布在肝脏和肠道系统中,参与胆汁酸(bile acid,BA)的合成和代谢[1],也作为一种胆汁酸受体(bile acid receptor,BAR)而被大家所熟知。FXR的缺失将导致胆汁酸内稳态的破坏,致使肝胆固醇和甘油三酯升高[2]。同时,其功能障碍也会导致许多肝脏疾病如胆汁淤积[3]和动脉粥样硬化[4]等。与其他核激素受体不同,在脑毛细血管内皮细胞中无法检测到FXR[5]。同时FXR活性最强的天然配体胆汁酸,即鹅脱氧胆酸(chenodeoxycholic acid,CDCA)也被证明不能通过外界摄取入脑[6]。所有这些证据表明,FXR可能不是分布于中枢神经系统。因此,目前仍不清楚它是否参与调节情感、记忆或运动等神经行为。
研究发现,许多肝病患者同时患有神经功能障碍或脑病,如焦虑[7]、抑郁症[8]、躁狂症[9]和认知功能损害[10]等。由于抑制FXR能有效控制阻塞性胆汁淤积症的发病[3],那么是否敲除FXR基因也可以有效防治精神病或神经功能紊乱呢?为了检验这一假设,我们对FXR基因敲除小鼠的神经行为及神经递质进行了检测,进而探讨了其可能的神经行为学机制,以期对FXR神经行为调节中的作用有更深入的理解。
1 材料与方法 1.1 实验动物FXR基因敲除型(KO)纯合子(-/-)小鼠由美国(马里兰州)国立卫生研究所基础医学部代谢实验室提供,上海中医药大学动物实验中心饲养及繁殖。对照组野生型(WT)纯合子(+/+)为FXR KO小鼠与C57BL / 6小鼠远交繁殖后代。在小鼠4~5个月大时进行行为学测试。每组包含14只♀小鼠,置于室温(25±1)℃下,12-12 h昼夜循环光照,自由进食、饮水。所有实验动物的饲养及操作均符合上海中医药大学实验动物管理饲养条例,并遵循人道原则。
1.2 RT-PCR用TRIzol法从小鼠的肝组织以及不同的脑组织包括海马、前额叶皮质、小脑、嗅球、垂体、脑干、丘脑、纹状体、下丘脑和大脑皮层中提取总RNA,Nanodrop蛋白核酸分析仪测定RNA浓度。取2 μg总RNA,应用反转录试剂盒(Thermo)逆转成cDNA。将上述转录产物cDNA,用ddH2O按1 ∶ 5比例稀释后作为模板,进行常规PCR反应,检测各组织中FXR基因表达,内参基因选用GAPDH,引物序列如Tab 1所示。 PCR反应条件如下:95℃预变性5 min后,进行95℃ 30 s,60℃ 30 s,72℃ 30 s,共35个循环的扩增反应,最后72℃延伸5 min。PCR产物通过2%琼脂糖凝胶电泳进行检测。
| Genes | Forward primer | Reverse primer | Accession number | Amplicon length |
| FXR | TCTCTTTAAGTGATGACGGG | TTCTGCAGGGATGGAAACAT | NM 009108 | 101 bp |
| GAPDH | ATGTGTCCGTCGTGGATCTGA | ATGCCTGCTTCACCACCTTCT | NM_001289726 | 81 bp |
所有行为测试,包括高架十字迷宫,强迫游泳,社交活动及避暗实验均于9 ∶ 00~17 ∶ 00在安静的环境中进行,同时所有的行为观察员均未被告知受试小鼠的基因型以避免主观因素造成的实验偏差。上述试验均在2周内按序进行。为避免老鼠之间的相互影响,实验中均以10%的乙醇清洁设备表面。
1.3.1 强迫游泳实验(forced-swimming test,FST)将小鼠单独放置在直径20 cm,水深20 cm的玻璃圆筒内,水温(23~25) ℃。小鼠入水后计时6 min,记录后4 min内累计不动时间(s)。不动时间定义为小鼠在水中停止挣扎,或呈漂浮状态,仅有细微肢体运动以保持头部浮于水面的累计时间。
1.3.2 高架十字迷宫实验(elevated plus maze test,EPMT)高架十字迷宫(EPM)由两个相对的开放臂(30 cm×5 cm)和两个相对的封闭臂(30 cm×5 cm×15 cm)以及连接4个臂的中央平台(5 cm×5 cm)组成,即开放臂—中央平台—开放臂或封闭臂—中央平台—封闭臂,两者之间互相垂直形成“十”字,四臂底板及中央平台均为黑色。迷宫底板距实验室地面60 cm高。实验时,将小鼠放置在中心平台并将其头转向开放臂。实验在暗室中进行并记录5min内小鼠进入开放臂的次数(open arm entry,OE)及停留在开放臂内的时间(open arm time,OT)。
1.3.3 社交活动测试(social interaction test,SIT)本行为测试根据文献进行简化[11]。将测试鼠与另一只陌生同性小鼠置于同一个测试箱内,记录5min内受试小鼠嗅闻同性小鼠的次数。 FXR KO组和对照组小鼠同时进行实验。小鼠过度活动及攻击行为视为无效结果。但在实际测试中未见明显的攻击行为。
1.3.4 避暗试验(passive avoidance test,PAT)用于PAT的穿梭箱分为明黑暗两室(每室30 cm×30 cm×30 cm),以一不透明的树脂玻璃门隔开。明室上方置一荧光灯(约500勒克司)。箱子的底板是连接到电击发生器的不锈钢网格。在记忆获得训练中,将小鼠背朝暗室放入明室内。小鼠因嗜暗习性而进入暗室,受到0.4 mA电刺激后迅速逃离暗室,训练时,以小鼠在暗室停留时长达300s为合格,并记录被电击次数,作为评价情感记忆获得的指标。24h后将受试小鼠再次放入明室以同样的方法记录5min内小鼠在暗室的潜伏期。实验数据记录采用避暗监测装置进行检测。
1.4 神经递质检测行为测试结束后,将麻醉小鼠断头,立刻在冰台上迅速取出全脑并分离出海马和前额叶皮层,液氮冷冻固化,储存于-80℃直至进行含量测定。运用LC-MS/MS方法测定神经递质含量,包括多巴胺(DA)、5-羟色胺(5-HT)、γ-氨基丁酸(GABA)、谷氨酸(GLU)、去甲肾上腺素(NE)、肾上腺素(EPI)和5-羟基吲哚乙酸(5-HIAA),具体方法学参考本实验室已建立方法[12]。
1.5 统计学分析 所有数据用 表示,并采用Prism Demo 5.0统计软件中t检验进行统计分析。
表示,并采用Prism Demo 5.0统计软件中t检验进行统计分析。
如Fig 1所示,RT-PCR结果显示,FXR基因在正常小鼠海马、前额叶皮质、小脑、嗅球、垂体、脑干、丘脑、纹状体、下丘脑和大脑皮层各脑组织中均没有表达,而在肝组织中表达明显。

|
| Fig 1 FXR mRNA expression pattern in brain of wild-type mouse 1:Liver(positive);2:Hippocampus;3:Prefrontal cortex;4:Cerebellum;5:Olfactory bulb;6:Pituitary gland;7:Brain stem;8:Thalamus;9:Striatum;10:Hypothalamus;11:Cortex |
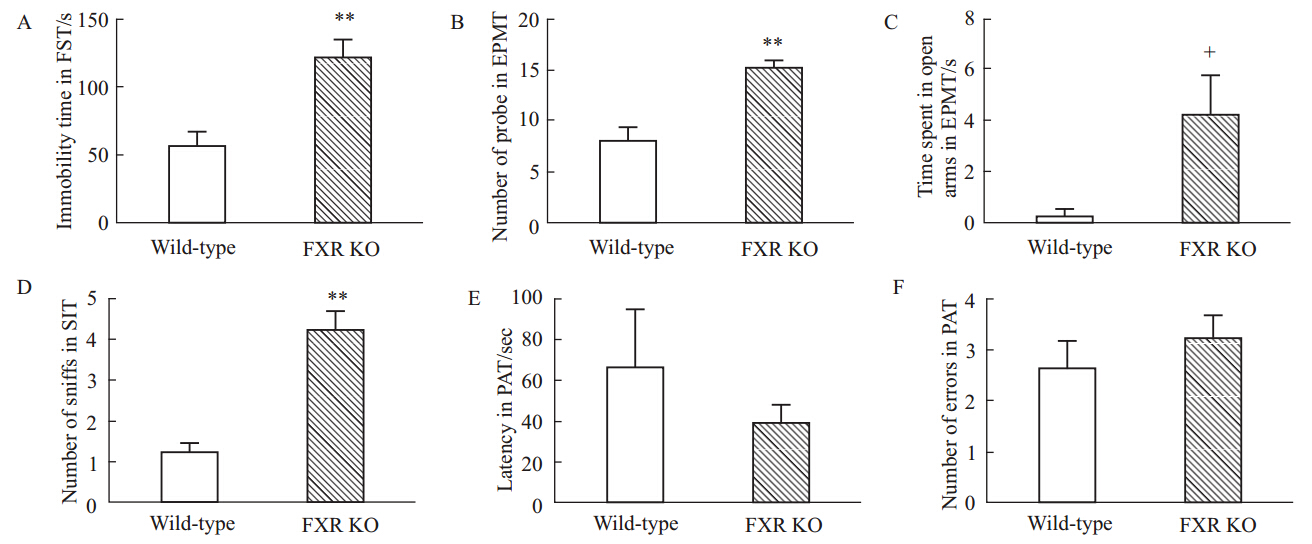
小鼠在强迫游泳模型中出现的不动状态反映了动物的绝望行为,显示出在困境中容易放弃,可模拟人类的抑郁状态。如Fig 2A所示,FXR KO组小鼠较野生对照组小鼠强迫游泳不动时间明显延长(P<0.01),表明FXR基因缺失小鼠在困境中更倾向于放弃,呈现出绝望行为。
2.3 FXR缺失对小鼠高架十字迷宫OE和OT的影响进入开放臂的次数以及在开放臂内停留时间反映了小鼠在非保护区内的探索行为,代表小鼠对陌生环境的好奇探究或因惊恐而寻求逃避,表现为情绪较为兴奋,与焦虑程度有一定的相关性。如Fig 2 B,C所示,实验中,FXR KO组小鼠进入开放臂的次数明显多于野生对照组(P<0.01);同时FXR KO组小鼠停留在开放臂内的时间也略高于野生对照组小鼠,由此表明,FXR基因缺失小鼠在非保护区的探索行为增多,对陌生环境更好奇并显示出更兴奋的情绪。
2.4 FXR缺失对小鼠社交行为的影响对同性小鼠嗅闻的次数反映了小鼠对新事物的好奇探究或对周围环境及事物较为敏感,情绪更为兴奋。如Fig 2 D所示,在社交行为测试实验中,FXR KO组小鼠对同一测试箱内的同性小鼠的嗅闻次数相对野生对照组小鼠有明显提高(P<0.01),表明FXR基因缺失小鼠对新事物更好奇或对新事物更敏感谨慎,情绪较为兴奋。
|
| Fig 2 Influence of FXR deletion on mouse neurobehaviors including depression,anxiety,social interaction and memory (n=14) wild type vs FXR KO,**P<0.01; +P<0.1 |
如Fig 2 E、F所示,在避暗实验中,与野生对照组小鼠比较,FXR KO组小鼠错误进入暗箱潜伏期和错误次数无明显变化。
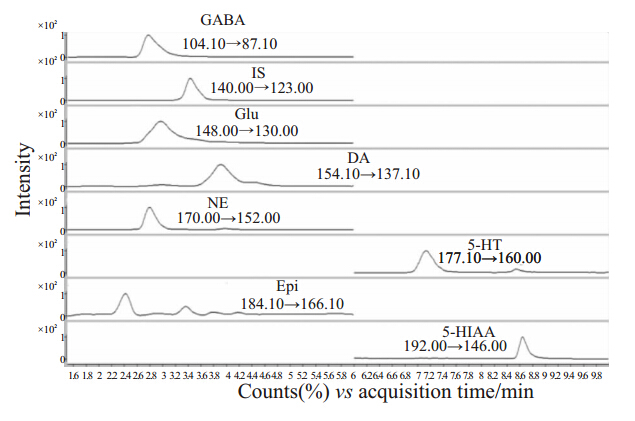
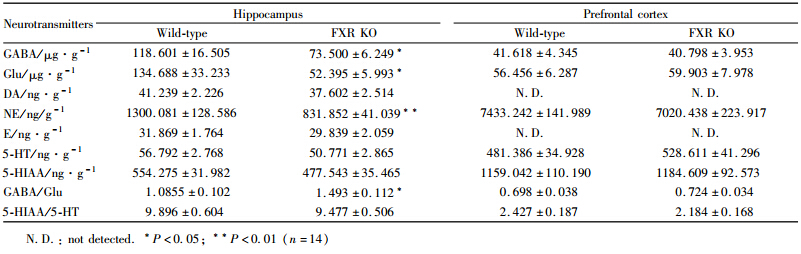
2.6 FXR缺失对脑神经递质的影响许多神经行为,如情绪、记忆和自主行为的信号都是通过中枢神经系统中的神经递质介导的,因此如Fig 3所示,我们运用了LC-MS/MS方法对海马和前额叶皮质中7种常见的神经递质进行检测。结果显示,前额叶皮层中,FXR敲除小鼠的神经递质和野生对照组小鼠没有差异(Tab 2)。而海马中FXR KO小鼠的GABA(P<0.05)、Glu(P<0.05)和NE(P<0.01)相对野生型小鼠均明显下降。而GABA与Glu之比上升(P<0.05)。结果表明,FXR缺失影响不同的脑区的神经递质系统。
|
| Fig 3 Representative LC-MS/MS chromatogram of seven neurotransmitters in mouse hippocampus |
 )
)
 |
FXR参与胆汁酸的合成和代谢,由此维持胆汁酸在体内的动态平衡。如前文所述,肝脏疾病能引起许多心理问题和认知功能障碍[7, 8, 9, 10],并改变运动 协调能力和自主活动[13]。但是FXR对神经系统和神经行为的调节作用鲜为人知。众所周知,基因敲除可导致基因表达和生理活性代偿性的改变,这些改变会直接影响神经行为表现[14]。在本研究中,我们比较了FXR KO组和它们的对照组间的神经行为变化,以评估其不同的神经功能影响。虽然在各脑组织中检测不到FXR基因的表达,但由FXR缺失导致的功能障碍却引起了小鼠行为不同程度的改变。如FXR KO ♀鼠在FST中与它们的对照组相比,表现出更容易放弃的行为,同时,它们又在EMPT和SIT中表现得更为兴奋,从而在一定程度上反映出FXR缺失引起♀小鼠情绪上的变化,使小鼠情绪变得较为不稳定。
神经递质在神经元之间的信号传递中具有举足轻重的作用,它们在某些大脑区域的平衡被破坏会引起严重的神经功能障碍与异常。核磁共振研究显示,重度抑郁症患者脑内GABA能神经元回路和Glu能神经元回路的活性下降[15],而服用抗抑郁药和情绪稳定剂可以增加GABA能活性[16]。GABA是中枢神经系统主要的抑制性神经递质,在抑郁症的发病机制中发挥重要作用[18],本研究中,FXR KO小鼠海马区的GABA相对野生型小鼠明显下降,破坏了GABA与Glu之间的平衡,这也部分印证了FXR KO小鼠在强迫游泳实验中不动时间延长的行为表现。根据1979年Zis等[19]提出的抑郁症NE能假说,NE含量下降或者活性降低均可引起抑郁,在本研究中,FXR KO小鼠海马区的NE相对野生型小鼠明显下降,和FXR KO小鼠在强迫游泳实验中倾向于放弃的行为表现相符。而FXR KO小鼠进入开放臂次数增多并且社交行为更频繁则可能与其Glu降低相关,Glu是一种中枢神经系统最重要的兴奋性氨基酸能神经递质,有报道称抗焦虑药的应用能够增加血浆中Glu的水平[20],这也部分解释了FXR缺失导致小鼠情绪焦虑的现象。这一系列神经行为的变化及神经递质的改变均归因于FXR对中枢神经系统的间接作用。因此,从本研究结果来看,FXR可能参与调控中枢神经系统中神经递质稳态平衡,进而影动物的情感和社交行为。
综上所述,在本研究中,我们首次发现FXR,这种周围器官中的胆汁酸代谢相关核受体,是神经功能和行为的重要调节器之一,参与调控了不同脑区的多种神经递质系统,从而为进一步研究和了解FXR在中枢神经系统中的功能提供了一定借鉴。
| [1] | Maruyama T, Miyamoto Y, Nakamura T, et al. Identification of membrane-type receptor for bile acids (M-BAR)[J]. Biochem Biophys Res Commun, 2002, 298(5):714-9. |
| [2] | Sinal C J, Tohkin M, Miyata M, et al. Targeted disruption of the nuclear receptor FXR/BAR impairs bile acid and lipid homeostasis[J]. Cell, 2000, 102(6):731-44. |
| [3] | Stedman C, Liddle C, Coulter S, et al. Benefit of farnesoid X receptor inhibition in obstructive cholestasis[J]. Proc Natl Acad Sci USA, 2006, 103(30):11323-8. |
| [4] | Guo G L, Santanmarina-Fojo S, Akiyama T E, et al. Effects of FXR in foam-cell formation and atherosclerosis development[J]. Biochim Biophys Acta, 2006, 1761(12):401-9. |
| [5] | Akanuma S, Hori S, Ohtsuk S, et al. Expression of nuclear receptor mRNA and liver X receptor-mediated regulation of ABC transporter A1 at rat blood-brain barrier[J]. Neurochem Int, 2008, 52(4-5):669-74. |
| [6] | Jia L, Jiang D, Hu P, et al. Synthesis and evaluation of (18)F-labeled bile acid compound:a potential PET imaging agent for FXR-related diseases[J]. Nucl Med Biol, 2014, 41(6):495-500. |
| [7] | Tkachenko O V, Kharchenko N V, Korzhenevs'kyi IuL, Lopukh Iia. Anxiety level studies in patients with chronic liver diseases[J]. Lik Sprava, 2013, (5):46-50. |
| [8] | Suh J I, Sakong J K, Lee K, et al. Anxiety and depression propensities in patients with acute toxic liver injury[J]. World J Gastroenterol, 2013, 19(47):9069-76. |
| [9] | Machado A C, Dequti M M, Caixeta L, et al. Mania as the first manifestation of Wilson's disease[J]. Bipolar Disord, 2008, 10(3):447-50. |
| [10] | Monfort P, Erceq S, Piedrafita B, et al. Chronic liver failure in rats impairs glutamatergic synaptic transmission and long-term potentiation in hippocampus and learning ability[J]. Eur J Neurosci, 2007, 25(7):2103-11. |
| [11] | File S E, Seth P. A review of 25 years of the social interaction test[J]. Eur J Pharmacol, 2003, 463(1-3):35-53. |
| [12] | Huang F, Li J, Shi H L, et al. Simultaneous quantification of seven hippocampal neurotransmitters in depression mice by LC-MS/MS[J]. J Neurosci Methods, 2014, 229:8-14. |
| [13] | Caul O, Rodrigo R, Piedrafita B, et al. Neuroinflammation contributes to hypokinesia in rats with hepatic encephalopathy:ibuprofen restores its motor activity[J]. J Neurosci Res, 2009, 87(6):1369-74. |
| [14] | Stiedl O, Meyer M. Cardiac dynamics in corticotropin-releasing factor receptor subtype-2 deficient mice[J]. Neuropeptides, 2003, 37(1):3-16. |
| [15] | Sanacora G, Zarate C A, Krystal J H, Manji H K. Targeting the glutamatergic system to develop novel, improved therapeutics for mood disorders[J]. Nat Rev Drug Discov, 2008, 7(5):426-37. |
| [16] | Brambilla P, Perez J, Barale F, et al. GABAergic dysfunction in mood disorders[J]. Mol Psychiatry, 2003, 8:721-37. |
| [17] | Sevincok L, Erol A. The prolactin resonse to buspirone in post stroke depression a prelininary report[J]. J Affect Disord, 2000, 59(2):169-73. |
| [18] | Petroff O A. GABA and glutamate in the human brain[J]. Neuroscientist, 2002, 8(6):562-73. |
| [19] | Zis A P, Goodwin F K. Novel antidepressants and the biogenic amine hypothesis of depression. The case for iprindole and mianserin[J]. Arch Gen Psychiatry, 1979, 36(10):1097-107. |
| [20] | Hoekstra R, Fekkes D, Loonen A J, et al. Bipolar mania and plasma amino acids:increased levels of glycine[J]. Eur Neuropsychopharmacol, 2006, 16(1):71-7. |
