


2. 重庆医科大学药理学教研室, 重庆 400016
 , WANG Dong-xu1, 2, WU Qiu-xiang1, 2, CHEN Qian-zhao1, 2, LI Yang1, 2, ZENG Yu-hua1, 2, SHAO Ying1, 2, HUANG Jun1, 2, LIU Ying-zi1, 2, HE Bai-cheng1, 2
, WANG Dong-xu1, 2, WU Qiu-xiang1, 2, CHEN Qian-zhao1, 2, LI Yang1, 2, ZENG Yu-hua1, 2, SHAO Ying1, 2, HUANG Jun1, 2, LIU Ying-zi1, 2, HE Bai-cheng1, 2

2. Dept of pharmacology, Pharmacy School of Chongqing Medical University, Chongqing 400016, China
白藜芦醇(resveratrol,Res)又名芪三酚,是一种天然多酚类物质,主要来源于葡萄、虎杖、花生、桑葚等植物[1, 2]。Res作为一种抗氧剂,临床可用于动脉粥样硬化、冠心病、缺血性心脏病和高血脂等疾病的防治[3, 4]。近年研究表明,Res对多种肿瘤细胞具有增殖抑制和促进凋亡作用,如肺癌、肝癌、乳腺癌和结肠癌细胞。但具体机制目前仍不十分清楚。
结肠癌是一种常见的消化系统恶性肿瘤,死亡率仅次于肺癌和肝癌,严重危害人类的健康 [5]。虽然结肠癌的诊断和治疗方法已有较大的发展,但目前结肠癌的治疗效果仍不理想,面临的挑战主要包括传统化疗药物的细胞毒性及结肠癌细胞的转移[6]。Wnt/β-catenin信号异常活化是结肠癌发生的重要原因之一[7]。在结肠癌细胞中,由于β-catenin或APC突变,导致β-catenin不能被降解。结果引起β-catenin在胞质内大量聚积并转位入核,与相应的转录因子(如TCF4/LEF)结合促进下游某些原癌基因表达,导致肿瘤发生[7]。文献报道,Res能抑制结肠癌细胞增殖并促进凋亡,这种作用可能与Res调节Wnt/β-catenin信号转导有关[8],但Res对Wnt/β-catenin信号转导的具体调节机制仍不清楚。
本研究通过检测Res对HCT116细胞增殖和凋亡的影响,并分析Res的这种作用是否与其抑制Wnt/β-catenin信号转导有关;最后分析Res调控Wnt/β-catenin信号转导的可能机制。本研究为将Res作为抗肿瘤药物或辅助抗肿瘤药物治疗结肠癌提供新的理论与实验基础。
1 材料及方法 1.1 试剂及细胞培养人结肠癌细胞HCT116细胞购自American Type Culture Collection(ATCC)。白藜芦醇购自西安昊轩生物科技有限公司。实验所用抗体均购自Santa Cruz Biotechnology公司。 Lipofectamine 购自Invitrogen公司。HCT116细胞采用DMEM培养基(高糖)培养细胞(含10%胎牛血清、105 U·L-1青霉素和0.1 g·L-1链霉素),培养条件为5%的CO2及37 ℃。
1.2 实验设计及分组将HCT116细胞分为对照组和实验组。用DMSO溶解Res,实验组用不同浓度的Res处理(20、40、60、80及100 μmol·L-1),对照组用相同体积DMSO处理。
1.3 结晶紫染检测细胞增殖将细胞铺于24孔板,用不同浓度Res(20、40、60、80、100 μmol·L-1)处理。分别在处理后24、48和72 h进行结晶紫染色[9],检测细胞增殖情况。方法如下:弃培养基,用PBS小心清洗孔板一次。每孔加500 μL结晶紫饱和溶液,在室温下孵育20 min。移去结晶紫染液,用PBS小心清洗3次。室温下将孔板晾干后扫描。每组实验重复3次。
1.4 流式分析检测细胞凋亡将处于指数生长期的细胞铺于6孔板中,待其贴壁后按实验设计加入不同浓度Res(20、40、80 μmol·L-1)。24 h后收集细胞,先用PBS (4 ℃) 清洗,然后分别用Annexin-V EGFP和PI处理细胞(按试剂盒操作说明进行);最后通过流式细胞仪进行凋亡检测。每组实验重复3次。
1.5 萤光素酶报告质粒检测Wnt/β-catenin信号转导活性将处于指数生长状态的细胞铺于T25培养瓶中。待细胞贴壁后,用lipofectamine转染TCF4/LEF报告质粒 (pTOP-Luc) 3 μg,4 h后换液。12 h后将细胞消化并重新种于24孔板中,待细胞贴壁后按实验设计加入不同浓度Res(20、40、80 μmol·L-1)进行处理。24 h后,裂解细胞,收集裂解液,并按照试剂盒操作说明进行萤光素酶活性测定。用BCA法测定裂解液总蛋白浓度(用以校正萤光素酶活性)。每组实验重复3次,结果取平均值。
1.6 Western blot实验将处于指数生长期的细胞种于6孔板中,按实验设计加入不同浓度的Res(20、40、80 μmol·L-1),并于相应时间点提取各组总蛋白。 采用10%的聚丙烯酰胺凝胶进行电泳,按常规操作方法进行Western blot实验。最后采用ECL试剂盒显影并成像。每组实验重复3次。
1.7 RNA提取及RT-PCR实验RT-PCR实验按如下步骤进行:将细胞铺于T25培养瓶中,按实验设计加入不同浓度的Res(20、40、80 μmol·L-1),并用含1%胎牛血清的完全培养基培养细胞。 TRIzol法提取总RNA, 通过逆转录反应制备cDNA,然后进行PCR检测目的基因mRNA表达水平。所用引物如下:GAPDH上游引物 5′-CAACGAATTTGGCTACAGCA-3′,下游引物 5′-AGGGGAGATTCAGTGTG GTG-3′ ;β-catenin上游引物 5′-CTGC AGGGGTCCTCTGTG-3′,下游引物 5′-TGCATATGTCGCCACACC-3 ′。每组实验重复3次。
1.8 统计学分析实验数据以x±s表示,t-test进行组间比较。
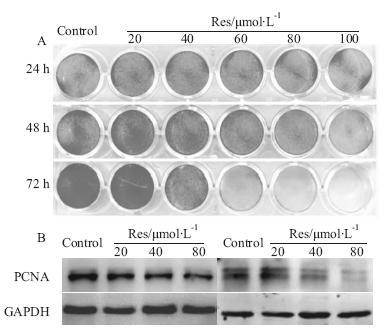
2 结果 2.1 Res对HCT116细胞增殖的影响本研究首先分析Res对HCT116细胞的增殖影响。结晶紫染色分析结果显示(Fig 1A),与对照组相比,Res处理组HCT116细胞的增殖明显呈浓度依赖性抑制,并且这种作用随着药物作用时间延长而增强;Res在40 μmol·L-1时已能明显抑制HCT116细胞生长。 Western blot分析结果显示,Res对增殖细胞核抗原(proliferating cell nuclear antigen,PCNA)表达也具有明显抑制作用(Fig 1B)。以上结果提示,Res能抑制HCT116增殖。
|
| Fig 1 Effect of Res on proliferation in HCT116 cells A: Crystal violet staining results showed the anti-proliferation effect of Res in HCT116 cells; B: Western blot results showed the effect of Res on the protein level of PCNA in HCT116 cells. |
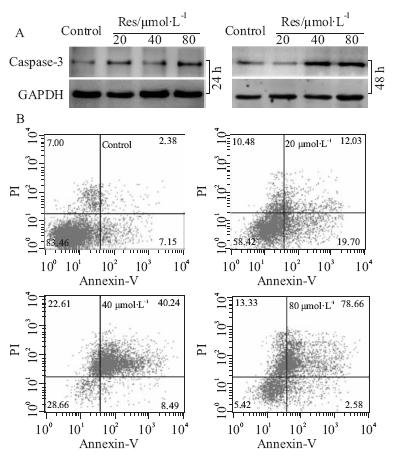
诱导肿瘤细胞凋亡是抗肿瘤药物的重要特点之一。Western blot分析结果显示(Fig 2A),Res不同浓度处理组Caspase-3蛋白水平明显高于对照组,并呈浓度依赖 性增加,Caspase-3蛋白水平在48 h升高更明显。Annexin-V EGFP/PI双染流式分析结果显示(Fig 2B),与对照组相比,Res处理组凋亡细胞比例明显随药物浓度增加而升高。结果提示,Res 对HCT116细胞凋亡具有促进作用。
|
| Fig 2 Effect of Res on apoptosis in HCT116 cells A: Western blot results showed the effect of Res on Caspase-3 in HCT116 cells; B: Flow cytometry analysis results showed the effect of Res on apoptosis in HCT116 cells. |
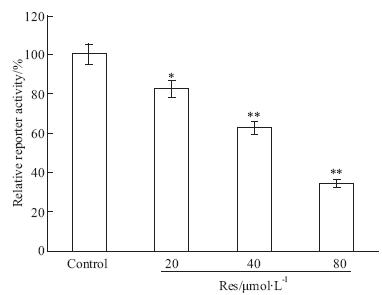
Wnt/β-catenin信号异常激活是结肠癌的重要发病原因之一。因此,抑制Wnt/β-catenin信号是抑制结肠癌细胞生长的重要靶点之一。 萤光素酶报告质粒分析结果显示,与对照组相比,Res对TCF4/LEF报告质粒的转录活性具有明显抑制作用(Fig 3),并且这种抑制作用呈浓度依赖性增加。结果提示,Res对HCT116细胞的Wnt/β-catenin信号转导具有抑制作用。
|
| Fig 3 Effect of Res on Wnt/β-catenin signal transduction in HCT116 cells Luciferase reporter assay results showed the effect of Res on Wnt/β-catenin signal transduction in HCT116 cells. *P<0.05,**P<0.01 vs control |
β-catenin在Wnt/β-catenin信号转导过程中具有重要作用。Western blot分析结果显示,与对照组相比,Res处理组β-catenin蛋白水平明显呈浓度依赖性下降(Fig 4A)。由于HCT116细胞中存在β-catenin突变而无法被降解复合物降解,所以Res对β-catenin蛋白水平的降低可能与β-catenin mRNA表达降低有关。进一步PCR分析结果显示,与对照组相比,Res处理HCT116细胞后能明显降低β-catenin 的mRNA表达水平(Fig 4B)。结果提示,Res对HCT116细胞中Wnt/β-catenin信号转导的抑制作用很可能与其下调β-catenin的mRNA表达有关。

|
| Fig 4 Effect of Res on β-catenin in HCT116 cells A:Western blot results showed the effect of Res on the level of β-catenin in HCT116 cells;B:PCR results showed the effect of Res on the expression of β-catenin in HCT116 cells. |
结肠癌是一种常见的消化系统恶性肿瘤,其发病率和致死率均较高,仅次于肝癌、肺癌及胃癌,对人类健康的危害很大,每年全球约有50万患者死于结肠癌[6]。目前虽然对结肠癌的诊断和治疗水平都有了较大提高,但结肠癌的预后仍不乐观。植物药来源的有效单体成份在各种肿瘤的治疗中发挥 着重要作用[10, 11]。本研究表明,Res对人结肠癌 HCT116细胞的增殖具有明显抑制作用,并能促进凋亡;这种作用可能与Res通过下调β-catenin mRNA表达,抑制Wnt/β-catenin信号转导有关。
研究表明,大部分结肠癌发病与遗传因素无关[12],Wnt信号的异常激活是结肠癌发生的重要原因之一[7]。该信号参与个体胚胎发育及正常生理功能调节,分为经典Wnt信号通路和非经典Wnt信号通路。 在经典Wnt信号通路中,β-catenin对信号转导起着中枢作用;非经典Wnt信号通路包括细胞极性及钙依赖性信号,和经典Wnt信号一样与肿瘤的发生密切相关[7, 13, 14]。在经典Wnt信号通路中,Wnt配体与细胞膜上的卷曲蛋白(Frizzled/FZD,Wnt的受体)结合,使β-catenin降解复合物Axin-APC-GSK3β无法形成,从而使β-catenin降解受到抑制而在胞内聚集,最后转位入核,与相应的转录因子(如T-cell factor 4/lymphoid enhancer factor,TCF4/LEF)结合形成复合物,调节下游靶基因表达。反之,当Wnt 受体未与Wnt配体结合时,胞内β-catenin降解复合物形成,促进β-catenin降解,抑制Wnt信号转导。文献报道,经典Wnt/β-catenin信号异常活化可能与调节β-catenin蛋白水平的重要因子发生突变有关,如APC突变 [7,14]。因此,β-catenin成为治疗结肠癌药物的重要靶点之一。
白藜芦醇(Res)是一种天然多酚类物质,主要来源于葡萄、虎杖、花生、桑葚等植物。近年研究表明,Res能抑制多种肿瘤细胞增殖和促进凋亡,如肺癌、肝癌、乳腺癌和结肠癌等。这种作用可能与Res抑制Wnt/β-catenin信号转导有关,但具体机制仍不十分清楚[8]。本研究通过结晶紫染色发现,Res能够明显抑制人结肠癌细胞的增殖(Fig 1A)。PCNA是细胞增殖启动的重要调节因子,其蛋白水平可以反映细胞的增殖状态。本研究分析表明,Res也能明显降低HCT116细胞中的PCNA蛋白水平(Fig 1B),进一步证实Res能抑制结肠癌细胞增殖。半胱氨酸天冬氨酸蛋白酶(cysteine-aspartic proteases,Caspase)属于半胱氨酸蛋白水解酶类,在细胞的凋亡、坏死及炎症反应中具有重要作用。其中,Caspase-8和Caspase-9被认为是凋亡的启动者,而caspase-3是凋亡的执行者。另外,在凋亡的早期,处于细胞膜内侧的磷脂酰丝氨酸翻向外侧。 Annexin V是一种磷脂结合蛋白,与磷脂酰丝氨酸有高度亲和力,可与细胞外侧暴露的磷脂酰丝氨酸结合,是检测细胞早期凋亡的特异性指标。本研究结果显示,Res能明显增强Caspase-3蛋白水平(Fig 2A),流式分析结果也显示Res处理后Annexin V阳性细胞比例明显增加(Fig 2B)。以上结果表明,Res不仅能抑制HCT116细胞增殖,也能促进HCT116细胞凋亡。
由于经典Wnt/β-catenin信号异常活化是结肠癌的重要发病原因之一[7],所以本研究利用TCF4/LEF萤光素酶报告质粒(pTOP-Luc)分析Res对Wnt/β-catenin信号的影响。实验结果显示,Res能明显抑制TCF4/LEF报告质粒的转录活性(Fig 3)。这一结果提示Res对Wnt/β-catenin信号转导具有抑制作用。进一步分析发现,Res能明显降低HCT116细胞内的β-catenin蛋白水平(Fig 4A)。由于HCT116细胞中β-catenin本身存在突变,已形成 的降解复合物无法加速β-catenin降解。因此,在这些肿瘤细胞中,β-catenin能在胞质内聚积并转位入核,持续激活Wnt/β-catenin信号[15]。由此,我们推测,Res降低β-catenin的蛋白水平可能与抑制β-catenin mRNA表达有关。 PCR分析结果显示,Res对β-catenin mRNA表达具有明显抑制作用(Fig 4B)。以上结果表明,Res能通过下调β-catenin mRNA表达实现对Wnt/β-catenin信号转导的抑制,但Res对β-catenin mRNA表达调控的具体机制仍不清楚。
本研究结果表明,Res能抑制结肠癌细胞增殖,这种作用与抑制Wnt/β-catenin信号转导有关;Res在结肠癌细胞中抑制Wnt/β-catenin信号转导可能通过下调β-catenin mRNA表达实现。但是,Res对β-catenin mRNA表达调控的详细机制还有待进一步研究。课题组将利用其他结肠癌细胞株,进一步确认Res抑制结肠癌细胞生长与Wnt/β-catenin的关系;深入分析Res对β-catenin表达调控的可能机制,为将Res用于对结肠癌的临床治疗提供理论和实验基础。
| [1] | Baur J A, Sinclair D A. Therapeutic potential of resveratrol:the in vivo evidence[J]. Nat Rev Drug Discov, 2006, 5(6):493-506. |
| [2] | Wang K H, Lai Y H, Chang J C, et al. Germination of peanut kernels to enhance resveratrol biosynthesis and prepare sprouts as a functional vegetable[J]. J Agric Food Chem, 2005, 53(2):242-6. |
| [3] | Tamaki N, Cristina Orihuela-Campos R, Inagaki Y, et al. Resveratrol improves oxidative stress and prevents the progression of periodontitis via the activation of the Sirt1/AMPK and the Nrf2/antioxidant defense pathways in a rat periodontitis model[J]. Free Radic Biol Med, 2014,75:222-9. |
| [4] | Tomayko E J, Cachia A J, Chung H R, et al. Resveratrol supplementation reduces aortic atherosclerosis and calcification and attenuates loss of aerobic capacity in a mouse model of uremia[J]. J Med Food, 2014,17(2):278-83. |
| [5] | Tárraga López P J, Albero J S, Rodríguez-Montes J A. Primary and secondary prevention of colorectal cancer[J]. Clin Med Insights Gastroenterol, 2014, 7:33-46. |
| [6] | Merika E, Saif M W, Katz A, et al. Review colon cancer vaccines:an update[J]. In Vivo, 2010, 24(5):607-28. |
| [7] | Saif M W, Chu E. Biology of colorectal cancer[J]. Cancer J, 2010,16(3):196-201. |
| [8] | Chen H J, Hsu L S, Shia Y T, et al. The β-catenin/TCF complex as a novel target of resveratrol in the Wnt/β-catenin signaling pathway[J]. Biochem Pharmacol, 2012, 84(9):1143-53. |
| [9] | 杨秋珺,周龙洋,刘映孜,等. 小檗碱抑制HCT116细胞生长与Wnt/β-catenin信号的关系研究[J]. 中国药理学通报, 2012, 28(09):60-4. Yang Q J, Zhou L Y, Liu Y Z, et al. Study on the correlation between the anti-proliferation effect of berberine on HCT116 cells and Wnt/β-catenin signaling[J]. Chin Pharmacol Bull, 2012, 28(9):60-4. |
| [10] | Wu K, Yang Q J, Mu Y Q, et al. Berberine inhibits the proliferation of colon cancer cells by inactivating Wnt/β-catenin signaling[J]. Int J Oncol, 2012, 41:292-8. |
| [11] | He B C, Gao J L, Luo X J, et al. Ginsenoside Rg3 inhibits colorectal tumor growth through the down-regulation of Wnt/β-catenin signaling[J]. Int J Oncol, 2011, 38:437-45. |
| [12] | Watson A J, Collins P D. Colon cancer:a civilization disorder[J]. Dig Dis, 2011, 29(2):222-8. |
| [13] | Pourreyron C, Reilly L, Proby C, et al. Wnt5a is strongly expressed at the leading edge in non-melanoma skin cancer, forming active gradients, while canonical Wnt signaling is repressed[J]. PloS One, 2012, 7(2):e31827. |
| [14] | Markowitz S D, Bertagnolli M M. Molecular origins of cancer:molecular basis of colorectal cancer[J]. N Engl J Med, 2009, 361(25):2449-60. |
| [15] | Morin P J, Sparks A B, Korinek V, et al. Activation of bet-acatenin-Tcf signaling in colon cancer by mutations in beta-catenin or APC[J]. Sci, 1997, 275:1787-90. |